transizioni termiche e transizioni radiative eccitazione Eb Ea

transizioni termiche e transizioni radiative eccitazione Eb Ea E Ea diseccitazione E Ea+E = Eb Ea= E + Eb Eb Nelle transizioni termiche l’energia E viene scambiata, attraverso gli urti, con le altre particelle del bagno termico. Lo scambio dipende dall’energia E, dalla temperatura (funzione di Boltzmann f. Bz(E, T)) e dagli stati accessibili nello stato finale (degenerazione gfin) Ni=gi e -E/k. T Nelle transizioni radiative l’energia E viene scambiata con il campo elettromagnetico: le leggi che governano lo scambio sono in parte diverse
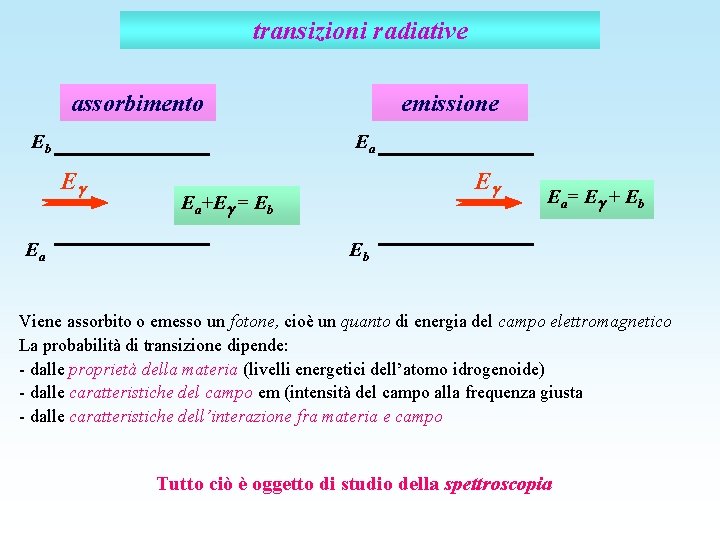
transizioni radiative assorbimento Eb Ea E Ea emissione E Ea+E = Eb Ea= E + Eb Eb Viene assorbito o emesso un fotone, cioè un quanto di energia del campo elettromagnetico La probabilità di transizione dipende: - dalle proprietà della materia (livelli energetici dell’atomo idrogenoide) - dalle caratteristiche del campo em (intensità del campo alla frequenza giusta - dalle caratteristiche dell’interazione fra materia e campo Tutto ciò è oggetto di studio della spettroscopia

sviluppo storico della spettroscopia L’inizio: il problema del “colore” Il colore “è contenuto” nella luce o nei corpi? *1660 Newton studia la rifrazione e scopre gli spettri il colore è “contenuto” nella luce tuttavia … da dove proviene il “colore” delle fiamme? *1752 Melville scopre gli spettri a righe e descrive la riga gialla della fiamma sodio il “colore” è contenuto anche nei corpi? *1800 Herschel scopre l’infrarosso nella radiazione solare e Ritter scopre l’ultravioletto nelle proprietà fotochimiche di Ag Cl

sviluppo storico della spettroscopia dal qualitativo al quantitativo *1801 Young calcola la lunghezza d’onda usando dati di Newton di interferenza da lamine sottili 2 d = differenza di cammino fra il raggio (2) e il raggio (1) si assegna al colore la “lunghezza” = 2 d (1) raggio incidente (2) d *1810 Fraunhofer sviluppa i diffrattometri e misura ben 700 “righe” fra righe “chiare” (di emissione) e righe “scure” (di assorbimento) Herschel, Brewster, Foucault associano righe e sostanze nasce la spettroscopia come tecnica di analisi chimica

sviluppo storico della spettroscopia *1859 Le leggi di Kirchoff • la lunghezza d’onda a cui una sostanza emette dipende unicamente dalla sostanza • una sostanza assorbe alle stesse lunghezze d’onda a cui emette • una sostanza trasparente non emette nel visibile Inoltre Kirchoff spiega: - le righe scure nella corona solare - il puzzle della “riga D” del sodio - predice l’esistenza del rubidio estrapolando le righe di Na e K

verso la fisica dei “quanti” sviluppo storico della spettroscopia * 1885 la serie di Balmer: f 1/n 2 - 1/m 2 * 1901 Planck spiega lo spettro di corpo nero e introduce il “quanto di azione h” * 1905 Einstein spiega l’effetto fotoelettrico e introduce il “quanto di luce (fotone)” di energia E=hf * 1908 Principio di “ricombinazione” di Ritz: “termine spettrale” a cui è associata una frequenza f = R Z 2 1/n 2 (R 3 · 1015 s-1)
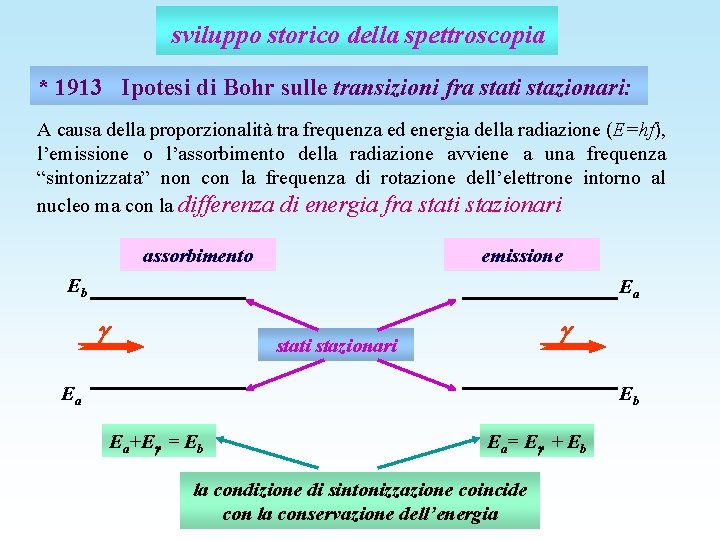
sviluppo storico della spettroscopia * 1913 Ipotesi di Bohr sulle transizioni fra stati stazionari: A causa della proporzionalità tra frequenza ed energia della radiazione (E=hf), l’emissione o l’assorbimento della radiazione avviene a una frequenza “sintonizzata” non con la frequenza di rotazione dell’elettrone intorno al nucleo ma con la differenza di energia fra stati stazionari assorbimento emissione Eb Ea stati stazionari Ea Eb Ea+E = Eb Ea= E + Eb la condizione di sintonizzazione coincide con la conservazione dell’energia
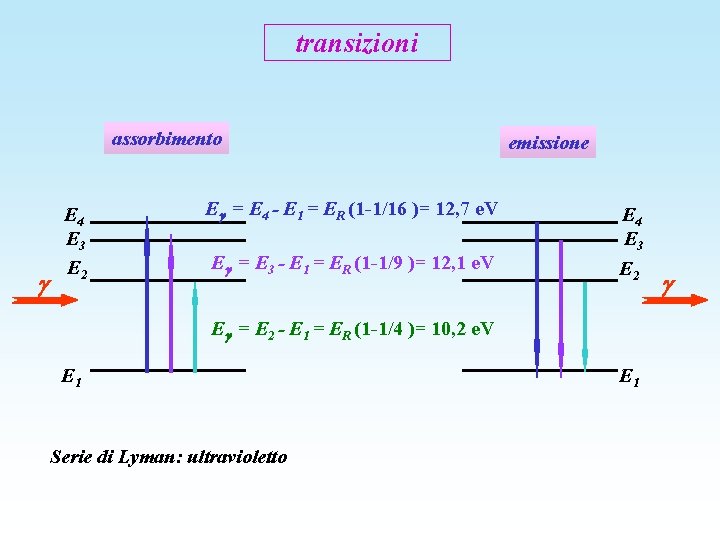
transizioni assorbimento E 4 E 3 E 2 E = E 4 - E 1 = ER (1 -1/16 )= 12, 7 e. V E = E 3 - E 1 = ER (1 -1/9 )= 12, 1 e. V emissione E 4 E 3 E 2 E = E 2 - E 1 = ER (1 -1/4 )= 10, 2 e. V E 1 Serie di Lyman: ultravioletto E 1
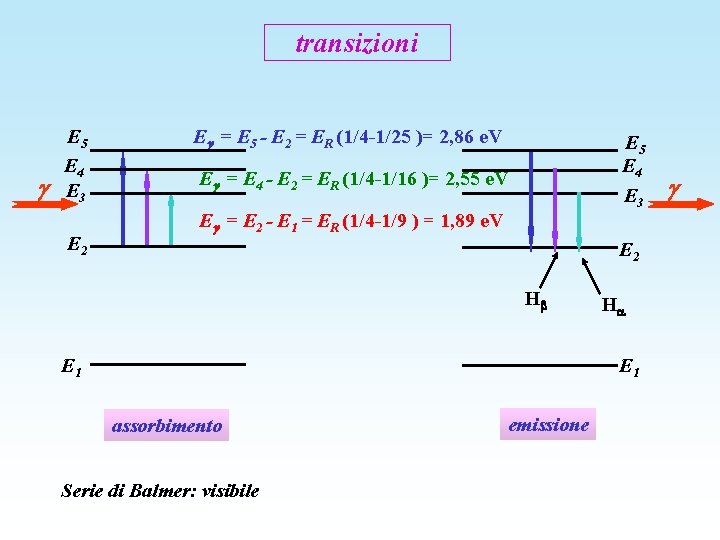
transizioni E 5 E 4 E 3 E 2 E = E 5 - E 2 = ER (1/4 -1/25 )= 2, 86 e. V E 5 E 4 E 3 E = E 4 - E 2 = ER (1/4 -1/16 )= 2, 55 e. V E = E 2 - E 1 = ER (1/4 -1/9 ) = 1, 89 e. V E 2 H E 1 H E 1 assorbimento Serie di Balmer: visibile emissione
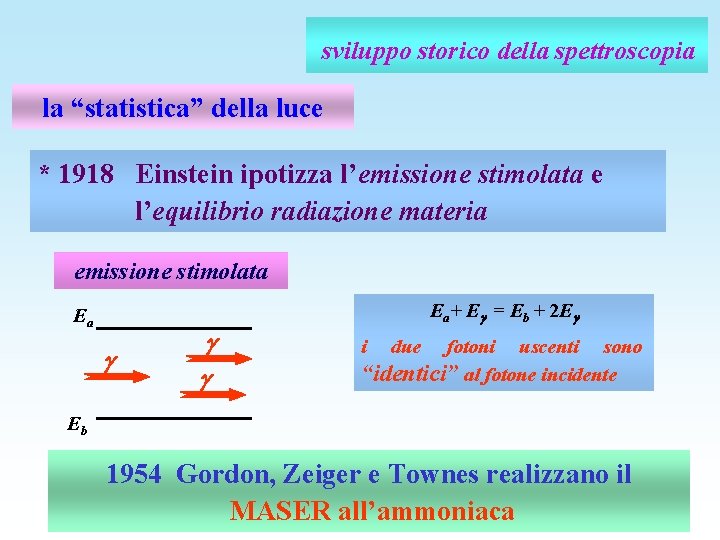
sviluppo storico della spettroscopia la “statistica” della luce * 1918 Einstein ipotizza l’emissione stimolata e l’equilibrio radiazione materia emissione stimolata Ea Ea+ E = Eb + 2 E i due fotoni uscenti sono “identici” al fotone incidente Eb 1954 Gordon, Zeiger e Townes realizzano il MASER all’ammoniaca
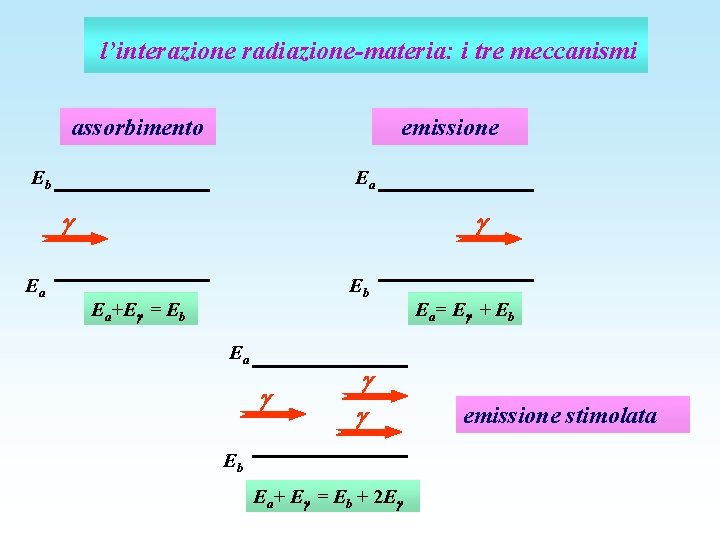
l’interazione radiazione-materia: i tre meccanismi assorbimento emissione Eb Ea+E = Eb Ea Eb Ea+ E = Eb + 2 E Ea= E + Eb emissione stimolata

descrizione degli stati: la funzione d’onda (r, t) risolve l’equazione temporale di Schrödinger (r) è soluzione dell’equazione stazionaria di Schrödinger 5 lm 4 lm 3 lm 2 lm E 5=-0, 54 e. V E =0, 31 e. V IR E =-0, 85 e. V E =0, 75 e. V IR 4 E 3=-1, 6 e. V E =1, 8 e. V rosso E 2=-3, 4 e. V E =10 e. V lontano UV 100 E 1=-13, 6 e. V Es. : per l’atomo idrogenoide
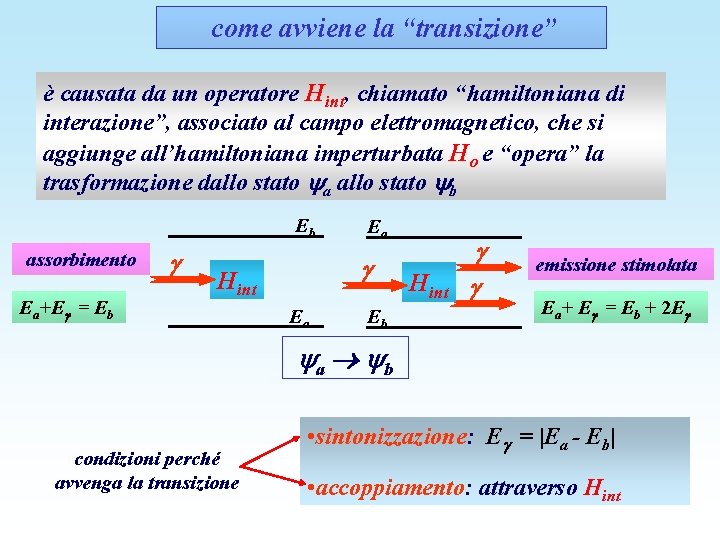
come avviene la “transizione” è causata da un operatore Hint, chiamato “hamiltoniana di interazione”, associato al campo elettromagnetico, che si aggiunge all’hamiltoniana imperturbata Ho e “opera” la trasformazione dallo stato a allo stato b Eb assorbimento Ea+E = Eb Ea Hint Ea Eb Hint emissione stimolata Ea+ E = Eb + 2 E a b condizioni perché avvenga la transizione • sintonizzazione: E = |Ea - Eb| • accoppiamento: attraverso Hint

l’hamiltoniana di interazione • è piccola rispetto ad Ho “perturbazione” • dipende dal tempo, perché deve modificare l’evoluzione temporale di (r, t) dato che l’evoluzione temporale dello stato a ( exp-i a t) è diversa da quella dello stato b ( exp-i b t) • può essere di diversi tipi, la più semplice e importante è l’interazione di “dipolo elettrico” dipolo elettrico perché un accoppiamento di “dipolo elettrico”?
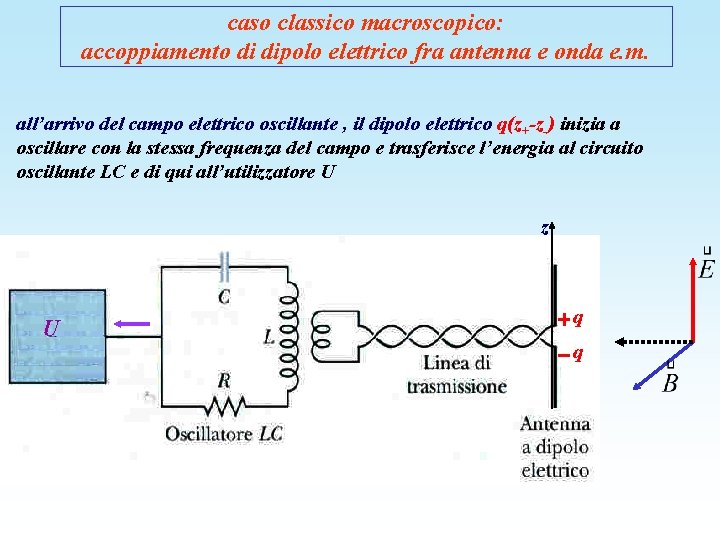
caso classico macroscopico: accoppiamento di dipolo elettrico fra antenna e onda e. m. all’arrivo del campo elettrico oscillante , il dipolo elettrico q(z+-z-) inizia a oscillare con la stessa frequenza del campo e trasferisce l’energia al circuito oscillante LC e di qui all’utilizzatore U z U q q
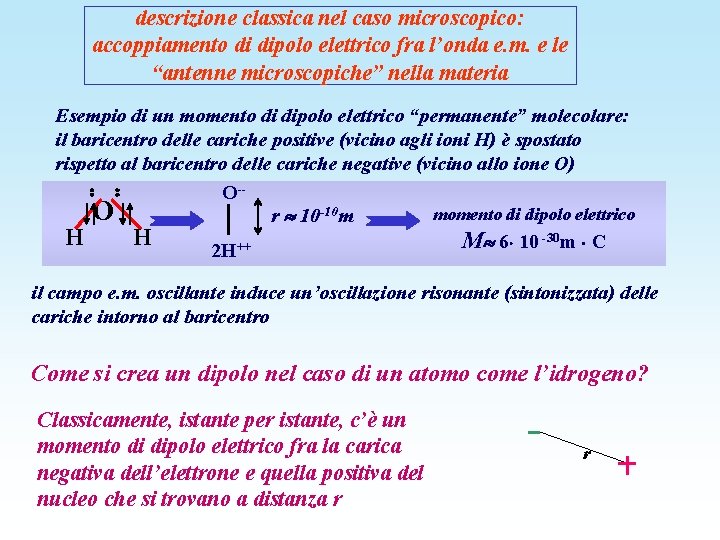
descrizione classica nel caso microscopico: accoppiamento di dipolo elettrico fra l’onda e. m. e le “antenne microscopiche” nella materia Esempio di un momento di dipolo elettrico “permanente” molecolare: il baricentro delle cariche positive (vicino agli ioni H) è spostato rispetto al baricentro delle cariche negative (vicino allo ione O) O-momento di dipolo elettrico O r 10 -10 m -30 m C H H M 6 10 ++ 2 H il campo e. m. oscillante induce un’oscillazione risonante (sintonizzata) delle cariche intorno al baricentro Come si crea un dipolo nel caso di un atomo come l’idrogeno? Classicamente, istante per istante, c’è un momento di dipolo elettrico fra la carica negativa dell’elettrone e quella positiva del nucleo che si trovano a distanza r r

…. nel caso quantistico occorre pensare a una “sovrapposizione di due stati” di diversa energia che evolvono nel tempo con una diversa legge temporale, ad esempio: uno stato “ 1 s” (n=1, l=0) stato a e uno stato “ 2 p” (n=2, l=1) stato b la funzione d’onda (r, t) è in una “sovrapposizione” degli stati a e b che hanno energia diversa, con ampiezze ca e cb: con a , b autofunzioni dell’hamiltoniana Ho: NON è uno stato “stazionario”, perché non ha una energia definita, dato che
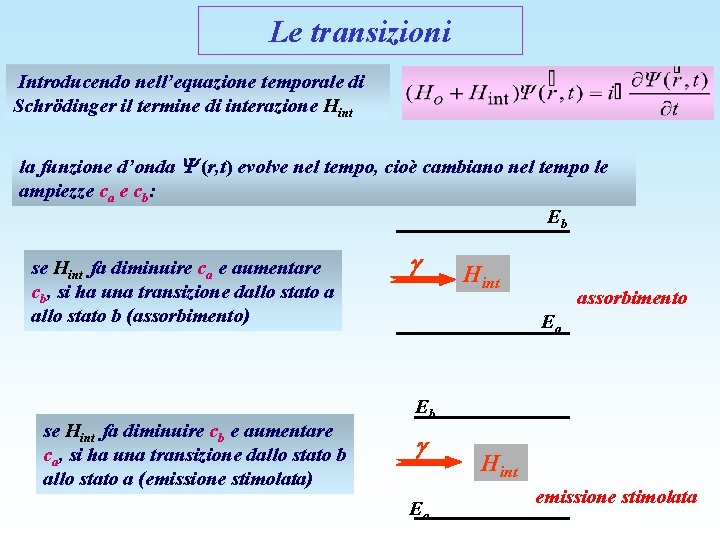
Le transizioni Introducendo nell’equazione temporale di Schrödinger il termine di interazione Hint la funzione d’onda (r, t) evolve nel tempo, cioè cambiano nel tempo le ampiezze ca e cb: Eb se Hint fa diminuire ca e aumentare cb, si ha una transizione dallo stato a allo stato b (assorbimento) se Hint fa diminuire cb e aumentare ca, si ha una transizione dallo stato b allo stato a (emissione stimolata) Hint assorbimento Ea Eb Ea Hint emissione stimolata
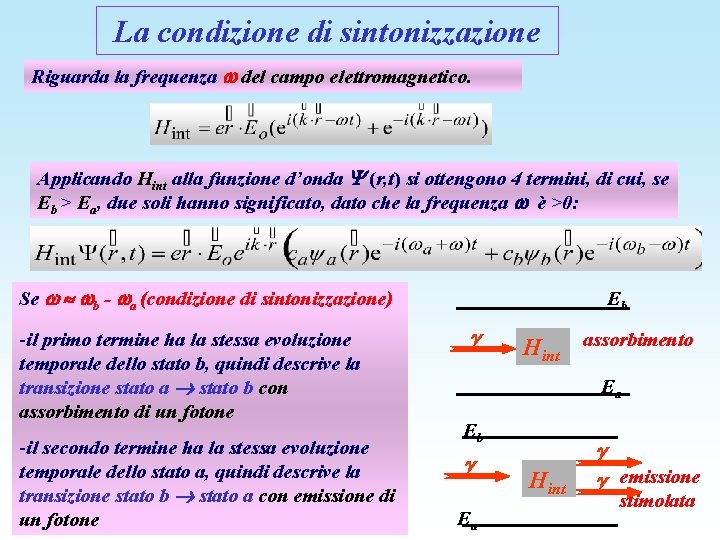
La condizione di sintonizzazione Riguarda la frequenza del campo elettromagnetico. Applicando Hint alla funzione d’onda (r, t) si ottengono 4 termini, di cui, se Eb > Ea, due soli hanno significato, dato che la frequenza è >0: Se b - a (condizione di sintonizzazione) -il primo termine ha la stessa evoluzione temporale dello stato b, quindi descrive la transizione stato a stato b con assorbimento di un fotone -il secondo termine ha la stessa evoluzione temporale dello stato a, quindi descrive la transizione stato b stato a con emissione di un fotone Eb Hint assorbimento Ea Eb Ea Hint emissione stimolata

La condizione di accoppiamento Come evolve nel tempo, ad esempio, cb, cioè la probabilità di trovare il sistema sullo stato b se Eb > Ea? (calcoli dettagliati nella nota 4) Conviene definire l’operatore “dipolo elettrico” e il suo valore Mba fra gli stati b e a: • il valore Mba fra gli stati b e a dell’operatore di dipolo elettrico esprime l’accoppiamento fra gli stati a e b e il campo elettromagnetico • integrando fra t=0 e t=to si ottiene l’ampiezza di probabilità che avvenga la transizione nel tempo to, che è proporzionale a Mba • il modulo al quadrato |cb(to)|2 dà la frequenza delle transizioni nell’intervallo di tempo to
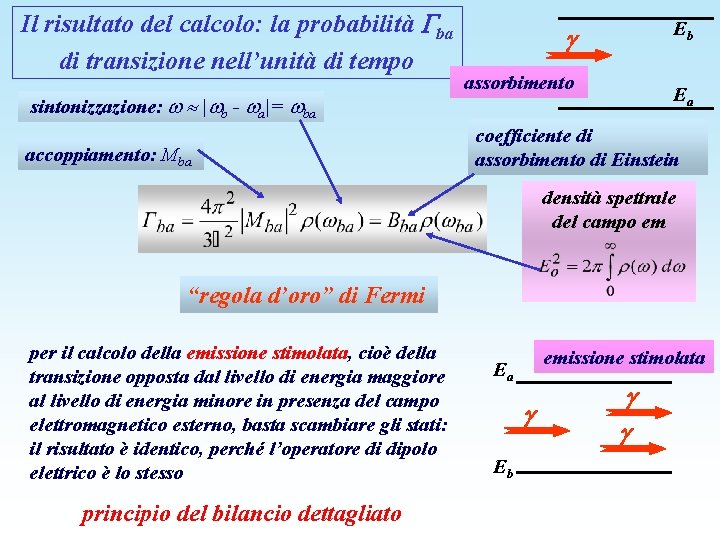
Il risultato del calcolo: la probabilità ba di transizione nell’unità di tempo sintonizzazione: | b - a|= ba accoppiamento: Mba Eb assorbimento Ea coefficiente di assorbimento di Einstein densità spettrale del campo em “regola d’oro” di Fermi per il calcolo della emissione stimolata, cioè della transizione opposta dal livello di energia maggiore al livello di energia minore in presenza del campo elettromagnetico esterno, basta scambiare gli stati: il risultato è identico, perché l’operatore di dipolo elettrico è lo stesso principio del bilancio dettagliato emissione stimolata Ea Eb
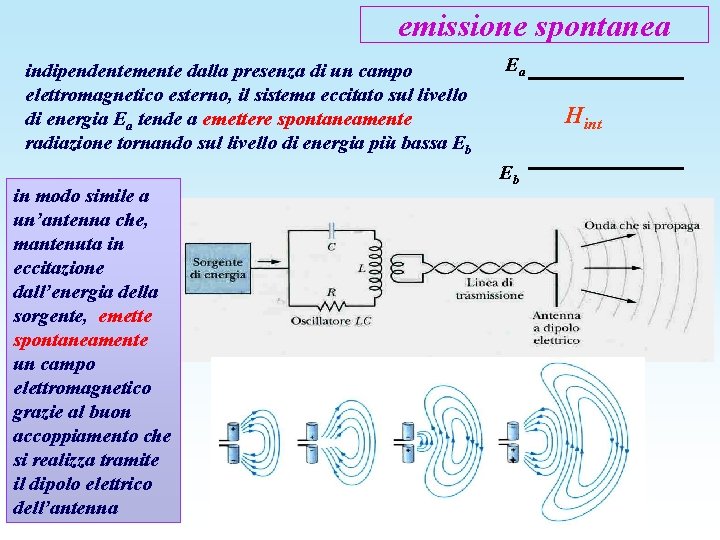
emissione spontanea indipendentemente dalla presenza di un campo elettromagnetico esterno, il sistema eccitato sul livello di energia Ea tende a emettere spontaneamente radiazione tornando sul livello di energia più bassa Eb in modo simile a un’antenna che, mantenuta in eccitazione dall’energia della sorgente, emette spontaneamente un campo elettromagnetico grazie al buon accoppiamento che si realizza tramite il dipolo elettrico dell’antenna Ea Hint Eb

emissione spontanea Ea probabilità di emissione spontanea per dipolo elettrico (dalla teoria delle antenne): Hint Eb è proporzionale al quadrato del momento di dipolo elettrico, come le probabilità di emissione indotta e di assorbimento è proporzionale al cubo della frequenza Esempio: probabilità di transizione spontanea fra i livelli n=2 ed n=1 dell’idrogeno, ipotizzando r 21 1 angstrom E 2 -E 1= -3, 4 -(-13, 6)=10, 2 e. V vita media sul livello n=2: = 1/ 21 0, 3 s
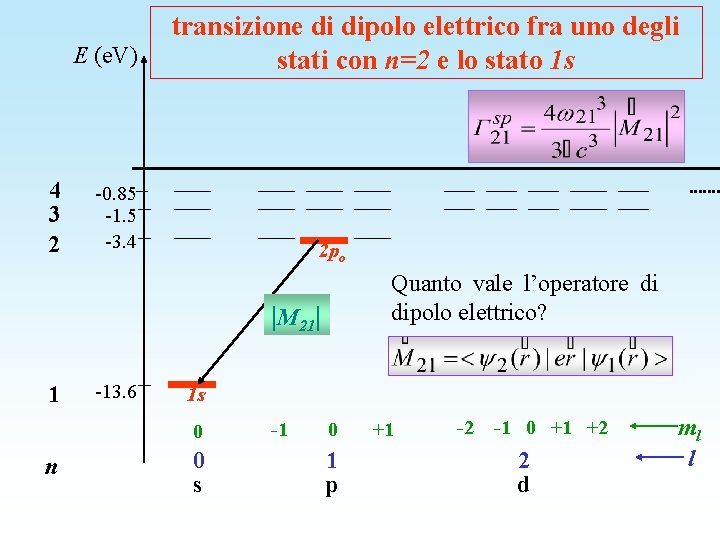
E (e. V) 4 3 2 transizione di dipolo elettrico fra uno degli stati con n=2 e lo stato 1 s -0. 85 -1. 5 -3. 4 2 po Quanto vale l’operatore di dipolo elettrico? |M 21| 1 -13. 6 1 s 0 n 0 s -1 0 1 p +1 -2 -1 0 +1 +2 2 d ml l
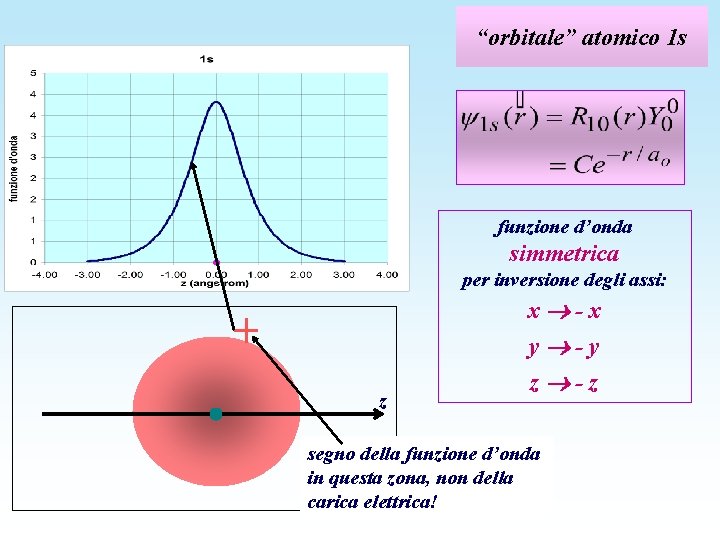
“orbitale” atomico 1 s funzione d’onda simmetrica per inversione degli assi: z x -x y -y z -z segno della funzione d’onda in questa zona, non della carica elettrica!
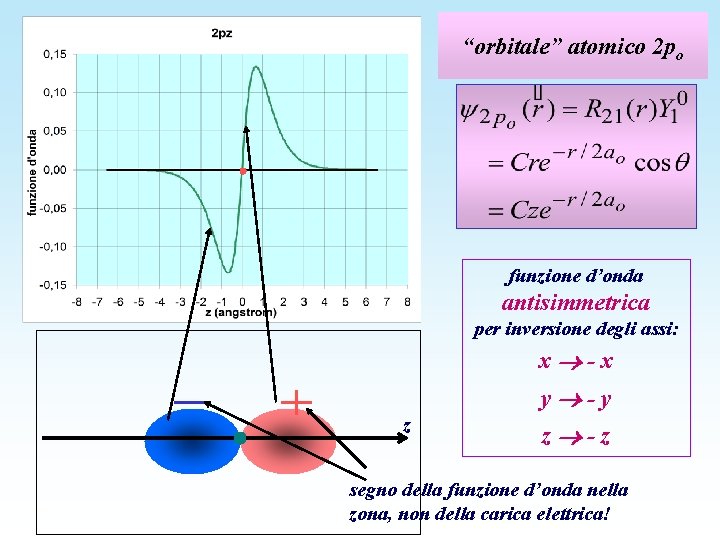
“orbitale” atomico 2 po funzione d’onda antisimmetrica per inversione degli assi: x -x y -y z z -z segno della funzione d’onda nella zona, non della carica elettrica!
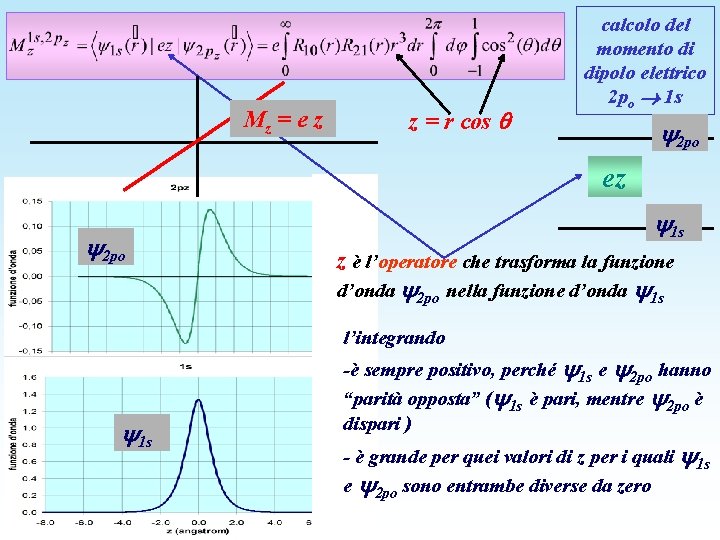
Mz = e z z = r cos calcolo del momento di dipolo elettrico 2 po 1 s 2 po ez 2 po 1 s z è l’operatore che trasforma la funzione d’onda 2 po nella funzione d’onda 1 s l’integrando 1 s -è sempre positivo, perché 1 s e 2 po hanno “parità opposta” ( 1 s è pari, mentre 2 po è dispari ) - è grande per quei valori di z per i quali 1 s e 2 po sono entrambe diverse da zero
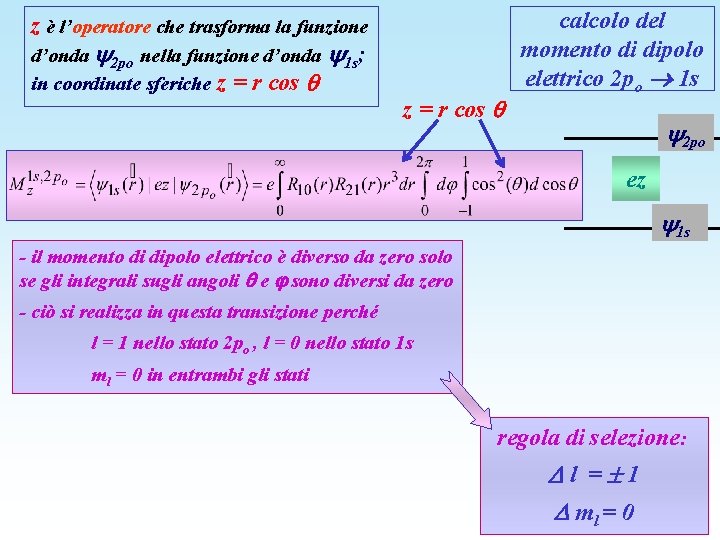
z è l’operatore che trasforma la funzione d’onda 2 po nella funzione d’onda 1 s; in coordinate sferiche z = r cos calcolo del momento di dipolo elettrico 2 po 1 s 2 po ez 1 s - il momento di dipolo elettrico è diverso da zero solo se gli integrali sugli angoli e sono diversi da zero - ciò si realizza in questa transizione perché l = 1 nello stato 2 po , l = 0 nello stato 1 s ml = 0 in entrambi gli stati regola di selezione: l = 1 ml = 0

Transizioni 2 p+ 1 s 2 p- 1 s Per indurre la transizione 2 p+ 1 s oppure 2 p- 1 s occorre un “operatore” che operi anche una trasformazione della dipendenza azimutale della funzione d’onda, dato che la dipendenza è diversa nelle due funzioni d’onda: 2 p- Occorre ricorrere a uno degli altri componenti dell’operatore di dipolo elettrico, perché l’operatore z non opera sull’angolo 1 s M è un “operatore vettoriale” , cioè è composto da 3 operatori: 2 p+
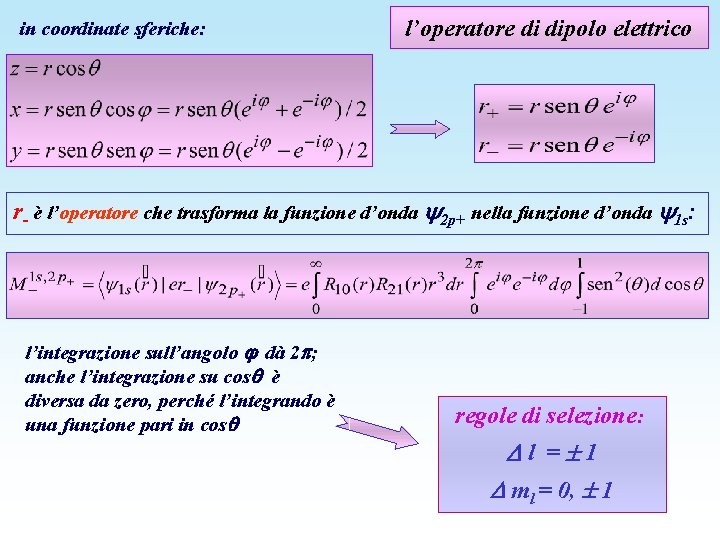
in coordinate sferiche: l’operatore di dipolo elettrico r- è l’operatore che trasforma la funzione d’onda 2 p+ nella funzione d’onda 1 s: l’integrazione sull’angolo dà 2 ; anche l’integrazione su cos è diversa da zero, perché l’integrando è una funzione pari in cos regole di selezione: l = 1 ml = 0, 1
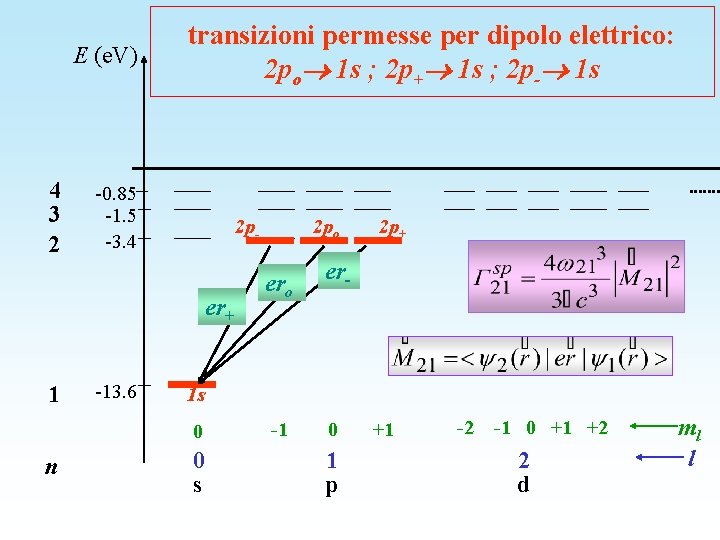
E (e. V) 4 3 2 transizioni permesse per dipolo elettrico: 2 po 1 s ; 2 p+ 1 s ; 2 p- 1 s -0. 85 -1. 5 -3. 4 2 p- er+ 1 -13. 6 ero 2 p+ er- 1 s 0 n 2 po 0 s -1 0 1 p +1 -2 -1 0 +1 +2 2 d ml l
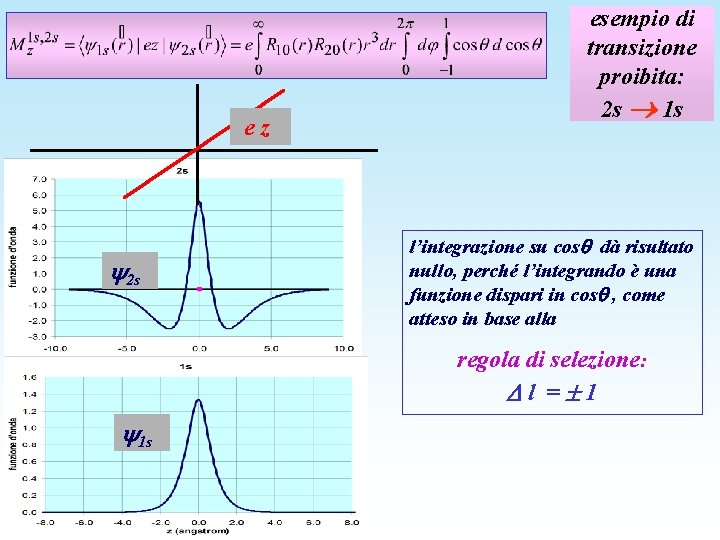
ez 2 s esempio di transizione proibita: 2 s 1 s l’integrazione su cos dà risultato nullo, perché l’integrando è una funzione dispari in cos , come atteso in base alla regola di selezione: l = 1 1 s
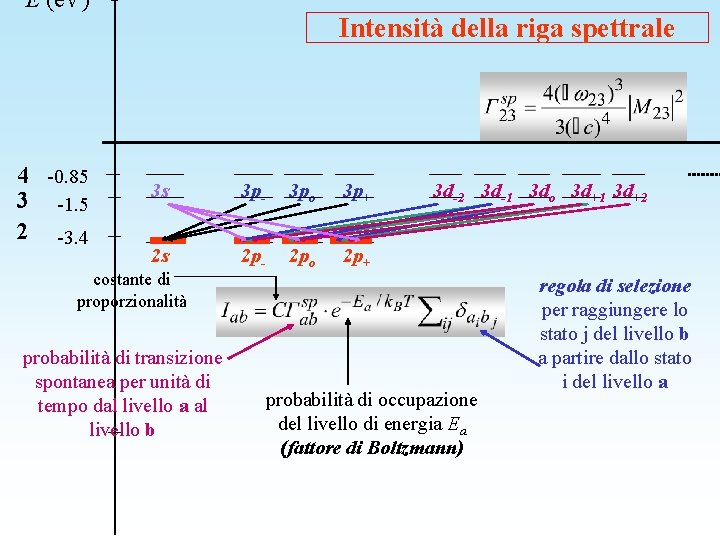
E (e. V) Intensità della riga spettrale 4 -0. 85 3 -1. 5 2 -3. 4 3 s 3 p- 3 po 3 p+ 2 s 2 p- 2 po 2 p+ costante di proporzionalità probabilità di transizione spontanea per unità di tempo dal livello a al livello b 3 d-2 3 d-1 3 do 3 d+1 3 d+2 probabilità di occupazione del livello di energia Ea (fattore di Boltzmann) regola di selezione per raggiungere lo stato j del livello b a partire dallo stato i del livello a
- Slides: 33