Transizioni di stato sublimazione vaporizzazione fusione solido liquido

Transizioni di stato

sublimazione vaporizzazione fusione solido liquido solidificazione brinamento gas condensazione

Trasformazione liquido-gas • Un gas in equilibrio con la sua fase liquida esercita una pressione costante a T costante = pressione del vapore saturo o tensione di vapore P = n/V RT Se si diminuisce V, una certa quantità di gas condensa in modo che n/V sia costante. • In un recipiente aperto, V = infinito, e la pressione non raggiunge mai quella del vapor saturo e si ha quindi evaporazione completa. Equilibrio dinamico

Ebollizione • Avviene alla T alla quale la tensione di vapore è uguale alla pressione che si esercita su di esso. • Temperatura normale di ebollizione = temperatura alla quale la tensione di vapore è 1 atm. • E’ un processo che non coinvolge solo la superficie del liquido.

Transizione solido-liquido • La temperatura a cui avviene la trasformazione solido- liquido alla pressione di 1 atm è detta temperatura normale di fusione.
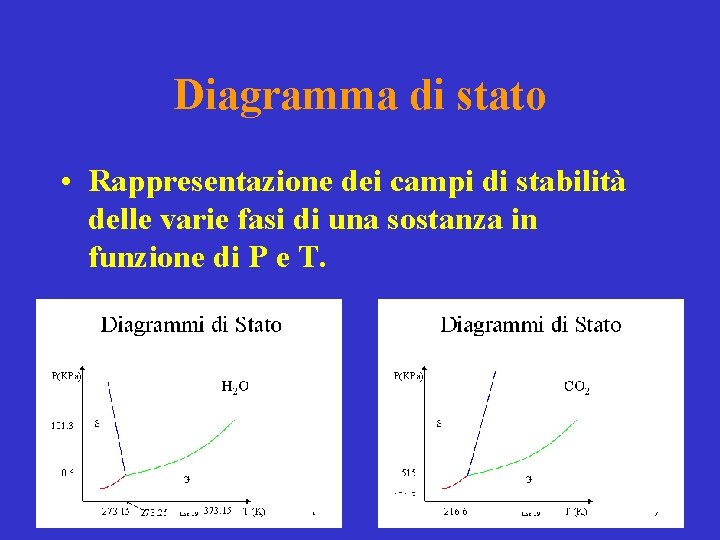
Diagramma di stato • Rappresentazione dei campi di stabilità delle varie fasi di una sostanza in funzione di P e T.

• La curva di equilibrio liquido-gas mostra la dipendenza da T della tensione di vapore. • La curva di equilibrio solido-liquido rappresenta la dipendenza della temperatura di fusione dalla pressione esercitata sul sistema. • La curva di equilibrio solido-gas mostra la dipendenza della tensione di vapore del solido da T. • Punto triplo = esiste un solo punto in cui le tre fasi coesistono.
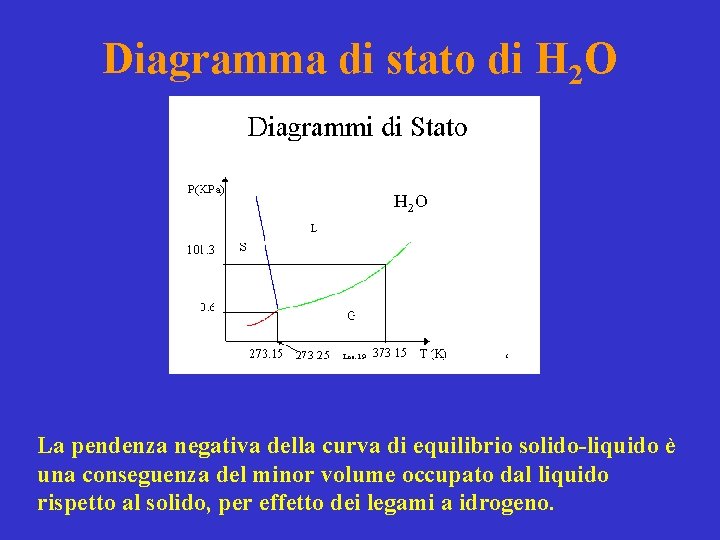
Diagramma di stato di H 2 O La pendenza negativa della curva di equilibrio solido-liquido è una conseguenza del minor volume occupato dal liquido rispetto al solido, per effetto dei legami a idrogeno.
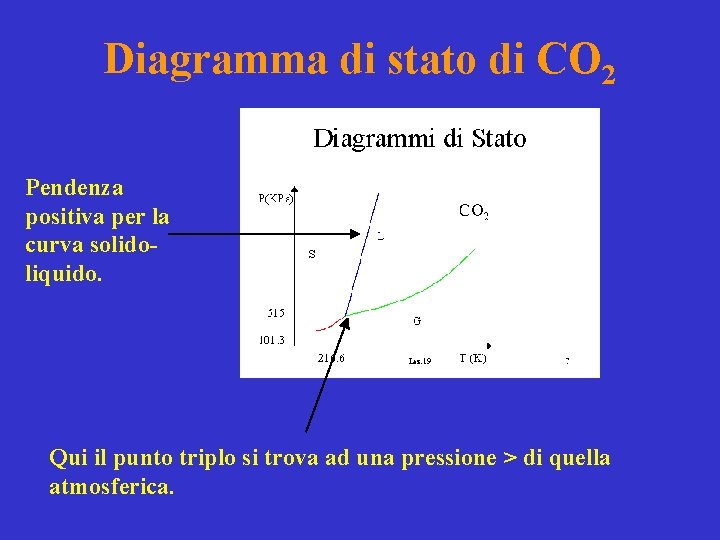
Diagramma di stato di CO 2 Pendenza positiva per la curva solidoliquido. Qui il punto triplo si trova ad una pressione > di quella atmosferica.

Diagramma di stato dell'acqua e di una sua soluzione di un soluto poco volatile DTeb= Keb Cm Innalzamento ebullioscopico e abbassamento crioscopico: non dipendono dalla natura del soluto ma solo dal numero di particelle presenti in una certa massa di solvente. DTcr= Kcr Cm Keb = costante ebullioscopica molale Kcr = costante crioscopica molale

Stati della materia Per alcune sostanze esistono varie forme solide differenti Es. grafite e diamante per il carbonio. Per He esistono addirittura due forme liquide
- Slides: 11