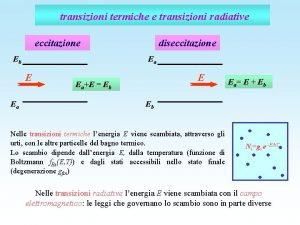
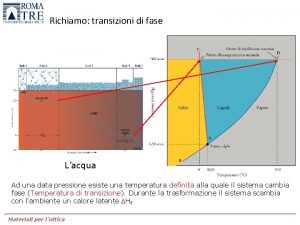
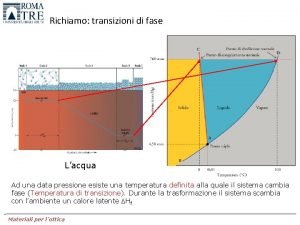
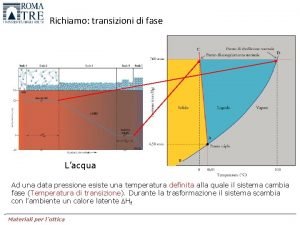
Transizioni di fase Fase Fase di un sistema


























- Slides: 58

Transizioni di fase

Fase • Fase di un sistema è una parte di esso nella quale la composizione (natura e concentrazione delle specie atomiche presenti) e la struttura (distribuzione spaziale delle specie atomiche) sono costanti o variano continuità • Per variazione continua della struttura si intende, ad esempio, la modificazione dei vettori reticolari di un cristallo sotto l’azione di sollecitazioni meccaniche localizzate o sotto l’effetto di un campo di temperature non uniforme. • Una fase risulta separata dal sistema da superfici definite, lungo le quali la composizione e la struttura presentano variazioni discontinue

Definizioni • LEGA: sistema composto da uno o più componenti • COMPONENTE (o costituente): composti presenti nel sistema che vanno a formare le fasi aventi composizione e microstruttura variabile • SOLUZIONE: sistema costituito da una fase omogenea, costituita da due o più componenti in proporzioni variabili (sistema omogeneo) • COMPOSTO: fase omogenea in cui deve essere rispettato un rapporto stechiometrico tra i componenti • MICROSTRUTTURA: numero di fasi presenti, loro proporzioni, il modo in cui sono distribuite (morfologia) • Quando un sistema è costituito da un'unica fase, si dice omogeneo • Quando è costituito da due o più fasi, si definisce eterogeneo. • Un sistema omogeneo non è necessariamente costituito da un'unica sostanza pura

Esempi di fase • I tre stati della materia - gas, liquido e solido - costituiscono gli esempi più semplici di fasi nel caso di sostanze pure. • Tuttavia, una singola fase non necessariamente corrisponde ad uno stato, (polimorfismo del ferro) Temperatura (°C) Struttura cristallina Nome della fase <912 CCC (ferrite) 912 -1394 CFC (austenite) 1394 -1538 CCC (ferrite) >1538 liquido

Parametri fisici • Le transizioni di fase sono governate da un parametro energetico che si chiama potenziale chimico (funzione di pressione e temperatura) • Quando più fasi sono in equilibrio i loro potenziali chimici sono uguali • In generale, una transizione di fase avviene sempre dalla fase a potenziale chimico maggiore alla fase a potenziale chimico minore • Energeticamente, la fase stabile è quella che ha potenziale chimico minore

Equilibrio chimico • Alterando pressione e temperatura si cambiano i potenziali chimici • Quindi pressione e temperatura determinano la fase energeticamente stabile μ p μ 2 • Di fatto, nelle transizioni che coinvolgono fasi liquide e solide l’effetto della pressione si può trascurare • Ciò non vale se si considerano anche trasformazioni che coinvolgono fasi gassose T 0 μ 1 T

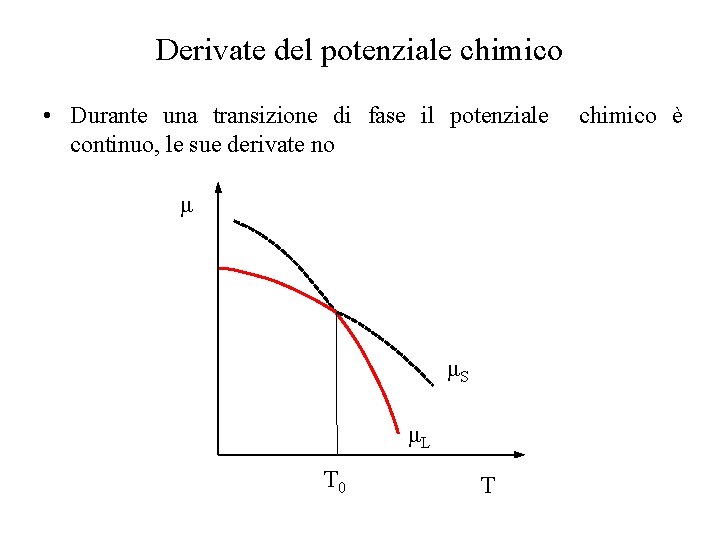
Derivate del potenziale chimico • Durante una transizione di fase il potenziale chimico è continuo, le sue derivate no μ μS μL T 0 T

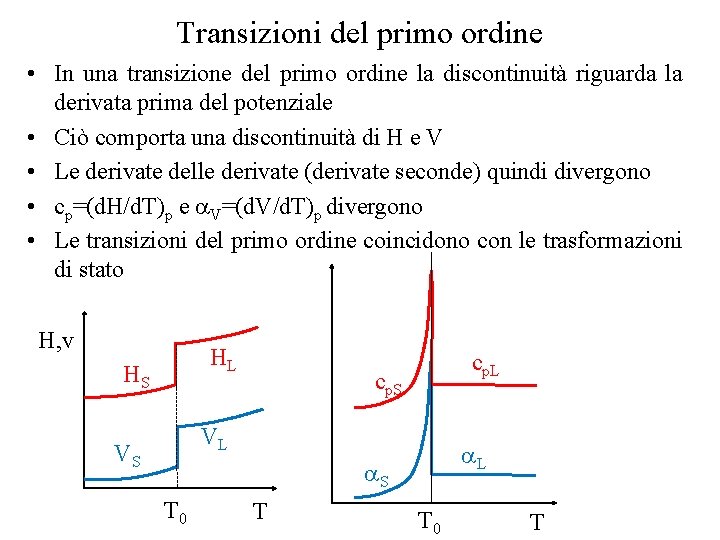
Transizioni del primo ordine • In una transizione del primo ordine la discontinuità riguarda la derivata prima del potenziale • Ciò comporta una discontinuità di H e V • Le derivate delle derivate (derivate seconde) quindi divergono • cp=(d. H/d. T)p e V=(d. V/d. T)p divergono • Le transizioni del primo ordine coincidono con le trasformazioni di stato H, v HL HS cp. L cp. S VL VS L S T 0 T

Transizione di ordine superiore • Una transizione del secondo ordine comporta la discontinuità della derivata seconda del potenziale (derivata prima di V o S) • Transizioni di ordine superiore riguardano discontinuità di derivate successive del potenziale • Transizione vetrosa T 0 T H, v T 0 T cp T 0 T

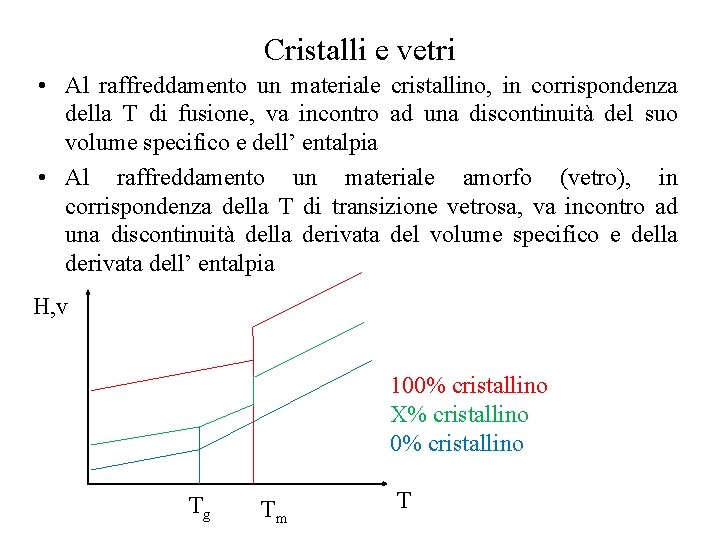
Cristalli e vetri • Al raffreddamento un materiale cristallino, in corrispondenza della T di fusione, va incontro ad una discontinuità del suo volume specifico e dell’ entalpia • Al raffreddamento un materiale amorfo (vetro), in corrispondenza della T di transizione vetrosa, va incontro ad una discontinuità della derivata del volume specifico e della derivata dell’ entalpia H, v 100% cristallino X% cristallino 0% cristallino Tg Tm T

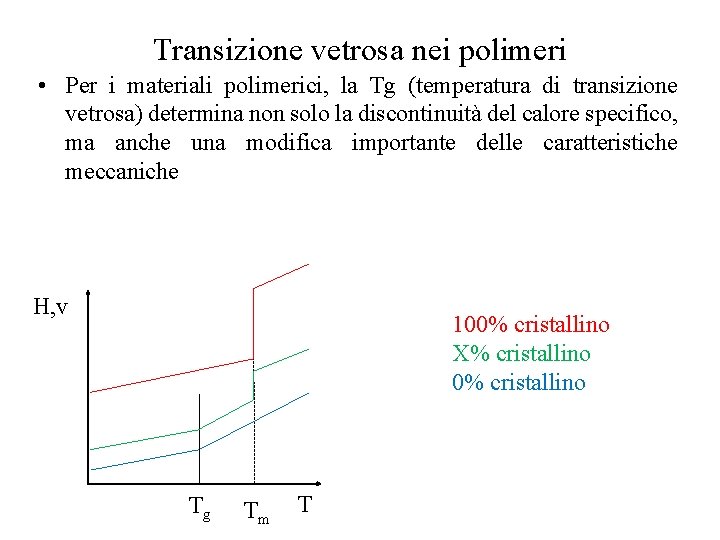
Transizione vetrosa nei polimeri • Per i materiali polimerici, la Tg (temperatura di transizione vetrosa) determina non solo la discontinuità del calore specifico, ma anche una modifica importante delle caratteristiche meccaniche H, v 100% cristallino X% cristallino 0% cristallino Tg Tm T

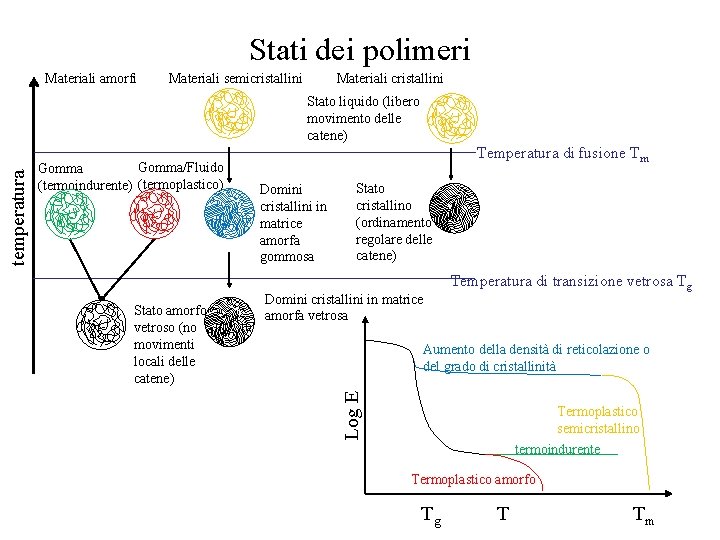
Stati dei polimeri Materiali amorfi Materiali semicristallini Materiali cristallini Gomma/Fluido Gomma (termoindurente) (termoplastico) Stato amorfo vetroso (no movimenti locali delle catene) Temperatura di fusione Tm Domini cristallini in matrice amorfa gommosa Stato cristallino (ordinamento regolare delle catene) Domini cristallini in matrice amorfa vetrosa Temperatura di transizione vetrosa Tg Aumento della densità di reticolazione o del grado di cristallinità Log E temperatura Stato liquido (libero movimento delle catene) Termoplastico semicristallino termoindurente Termoplastico amorfo Tg T Tm

Un polimero allo stato solido può essere: • Completamente amorfo • Parzialmente cristallino – La frazione amorfa di un polimero semicristallino può essere vetrosa o liquida (fuso polimerico). In quest’ultimo caso può avere un comportamento da liquido o da gomma

Stati fisici di un polimero: fuso (o liquido) • Allo stato liquido, è consentita la mobilità rotazionale di almeno 50 -100 segmenti della catena principale intorno ai legami • Le molecole possono facilmente scivolare una sull’altra.

Stati fisici di un polimero: “gomma” • È lo stato fisico di un polimero reticolato o di un termoplastico sopra la Tg • Anche in questo stato è consentita la mobilità rotazionale dei tratti lineari del reticolo intorno ai legami • Le molecole possono scivolare una sull’altra nei limiti permessi dalla reticolazione

Stati fisici di un polimero: vetro • • Assenza di rotazioni intorno ai legami nella catena principale. Le molecole restano intrappolate in uno stato completamente disordinato

Stati fisici di un polimero: cristallo • • Struttura ordinata, con ordine a lungo raggio Le molecole si impacchettano in modo che le forze di attrazione intermolecolari stabilizzino le catene in un reticolo regolare.

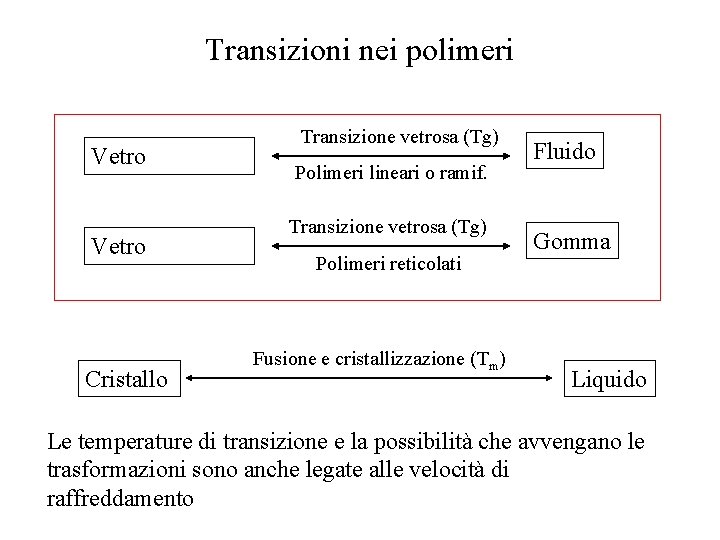
Transizioni nei polimeri Vetro Cristallo Transizione vetrosa (Tg) Polimeri lineari o ramif. Transizione vetrosa (Tg) Polimeri reticolati Fusione e cristallizzazione (Tm) Fluido Gomma Liquido Le temperature di transizione e la possibilità che avvengano le trasformazioni sono anche legate alle velocità di raffreddamento

Termodinamica e cinetica • Lo sviluppo delle fasi all’interno di un sistema (ossia quale microstruttura sarà presente) dipende da due fattori: – termodinamico – cinetico • L’aspetto termodinamico tiene solo conto dello stato al quale il sistema tende in funzione dei valori delle variabili considerate • Questo stato finale, che rappresenta lo stato di equilibrio del sistema, può essere raggiunto molto rapidamente o, al contrario, dopo un tempo infinito. • La cinetica è mooooooolto importante in molti tipi di applicazioni industriali

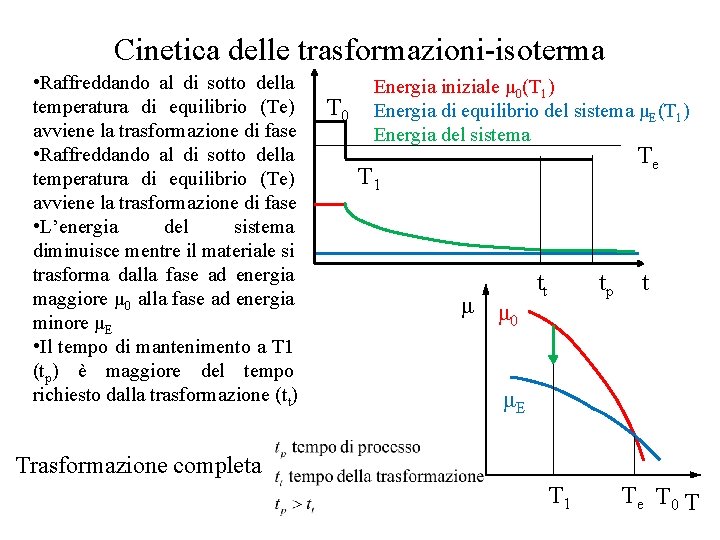
Cinetica delle trasformazioni-isoterma • Raffreddando al di sotto della temperatura di equilibrio (Te) avviene la trasformazione di fase • L’energia del sistema diminuisce mentre il materiale si trasforma dalla fase ad energia maggiore μ 0 alla fase ad energia minore μE • Il tempo di mantenimento a T 1 (tp) è maggiore del tempo richiesto dalla trasformazione (tt) T 0 Energia iniziale μ 0(T 1) Energia di equilibrio del sistema μE(T 1) Energia del sistema Te T 1 μ μ 0 tt tp t μE Trasformazione completa T 1 Te T 0 T

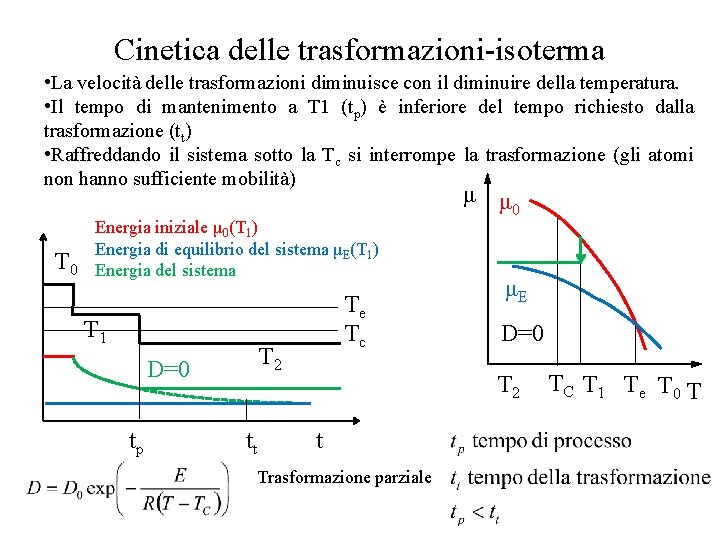
Cinetica delle trasformazioni-isoterma • La velocità delle trasformazioni diminuisce con il diminuire della temperatura. • Il tempo di mantenimento a T 1 (tp) è inferiore del tempo richiesto dalla trasformazione (tt) • Raffreddando il sistema sotto la Tc si interrompe la trasformazione (gli atomi non hanno sufficiente mobilità) Energia iniziale μ 0(T 1) Energia di equilibrio del sistema μE(T 1) T 0 Energia del sistema T 1 T 2 D=0 tp Te Tc tt μ μ 0 μE D=0 T 2 t Trasformazione parziale TC T 1 Te T 0 T

Cinetica delle trasformazioni-isoterma • La velocità delle trasformazioni diminuisce con il diminuire della temperatura. • Raffreddando al di sotto della temperatura di equilibrio (Tc) si inibisce completamente la trasformazione Trasformazione nulla Energia iniziale μ 0(T 1) Energia di equilibrio del sistema μE(T 1) T 0 Energia del sistema Te Tc T 2 D=0 tp tt t

Cinetica delle trasformazioni-non isotermo • x. T frazione di moli trasformate • v. T velocità di trasformazione Velocità di raffreddamento T=T 0 - t

Cinetica delle trasformazioni • La trasformazione avviene in piccola misura se la velocità di raffreddamento è molto maggiore della velocità con cui avviene il processo (integrale) • Quindi, passando ai tempi (reciproci delle velocità), se tr (tempo caratteristico di raffreddamento) è molto minore di tt (tempo caratteristico della trasformazione) • tt>>tr • Processo lento o raffreddamento veloce • La trasformazione avviene completamente se la velocità di raffreddamento è molto minore della velocità con cui avviene il processo (integrale) • Quindi, passando ai tempi (reciproci delle velocità), se tr (tempo caratteristico di raffreddamento) è molto maggiore di tt (tempo caratteristico della trasformazione) • tt<<tr • Processo rapido o raffreddamento lento

Metastabilità • Un sistema si trova allo stato metastabile se la sua energia è maggiore di quanto previsto dalla termodinamica • Il sistema non può evolvere verso lo stato di minore energia perché la temperatura è troppo bassa e la mobilità è ridotta (o annullata) al di sotto di una temperatura Tg • Se il sistema viene riscaldato a T 3>Tg, esso può evolvere verso uno stato di minore energia, trasformandosi in parte o totalmente Energia iniziale μ 0(T 1) Energia di equilibrio del sistema μE(T 1) H T 0 Energia del sistema T 3 T 2 D=0 D>0 Te Tc Energia dello stato metastabile Energia dello stato stabile E D=0 t T 2 D>0 TC T 3 T

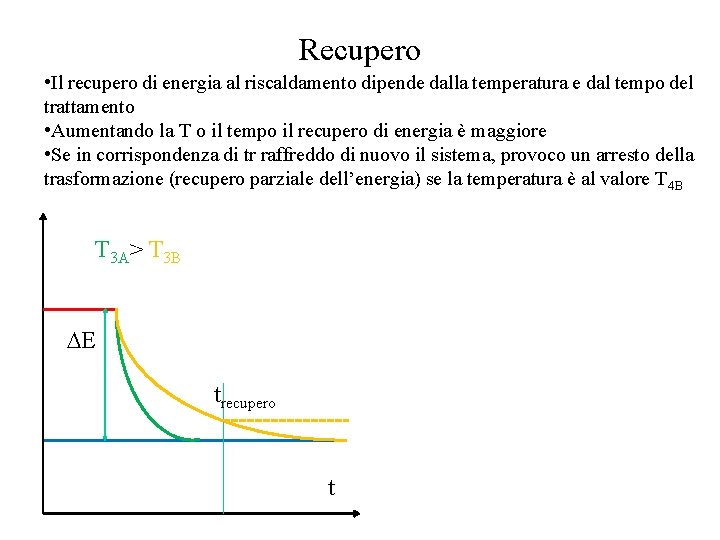
Recupero • Il recupero di energia al riscaldamento dipende dalla temperatura e dal tempo del trattamento • Aumentando la T o il tempo il recupero di energia è maggiore • Se in corrispondenza di tr raffreddo di nuovo il sistema, provoco un arresto della trasformazione (recupero parziale dell’energia) se la temperatura è al valore T 4 B T 3 A> T 3 B E trecupero t

Indurimento per dispersione e trattamento termico- strutture di equilibrio • • Al di sopra di circa 450°C, la lega 96%Al-4%Cu forma una soluzione solida omogenea in cui gli atomi di Cu occupano le posizioni interstiziali della struttura cristallina del Al Raffreddando al di sotto di ca 450°C la lega, si supera il limite di solubilità, per cui gli atomi di Cu vengono espulsi dalla struttura cristallina dell’Al Si formano due fasi, una ricca di Al ( ) ed una ricca di Cu ( , in cui c’è circa il 55% di Cu ed il 45% di Al) La fase è un composto intermetallico, Cu. Al 2, duro e fragile La microstruttura del materiale non è soddisfacente, perché al fase costituisce la fase continua, conseguente infragilimento del materiale 500 Temperatura (°C) • 400 300 200 Raff re lento ddament o Fase stabile 100 tempo (Cu. Al 2) ai bordi di grano

Importanza della diffusione • • La possibilità di formare la fase dipenda dalla capacità degli atomi di Cu di diffondere verso i bordi di grano Ciò richiede del tempo, ed è quindi possibile quando il materiale viene raffreddato lentamente, in modo tale che il tempo del raffreddamento tp sia maggiore del tempo richiesto alla diffusione tt Fase stabile Diffusione del Cu (atomi blu) verso i bordi di grano (Cu. Al 2) ai bordi di grano

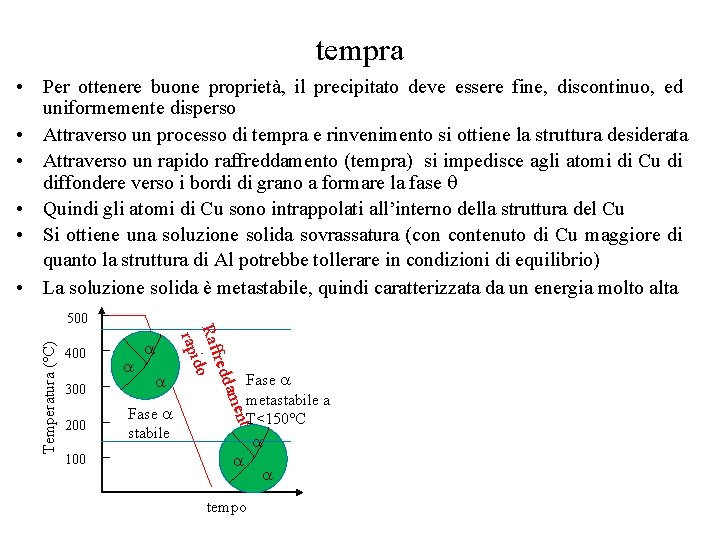
tempra • Per ottenere buone proprietà, il precipitato deve essere fine, discontinuo, ed uniformemente disperso • Attraverso un processo di tempra e rinvenimento si ottiene la struttura desiderata • Attraverso un rapido raffreddamento (tempra) si impedisce agli atomi di Cu di diffondere verso i bordi di grano a formare la fase • Quindi gli atomi di Cu sono intrappolati all’interno della struttura del Cu • Si ottiene una soluzione solida sovrassatura (con contenuto di Cu maggiore di quanto la struttura di Al potrebbe tollerare in condizioni di equilibrio) • La soluzione solida è metastabile, quindi caratterizzata da un energia molto alta 400 300 100 Fase stabile Fase metastabile a T<150°C to 200 en dam fred Raf o d rapi Temperatura (°C) 500 tempo

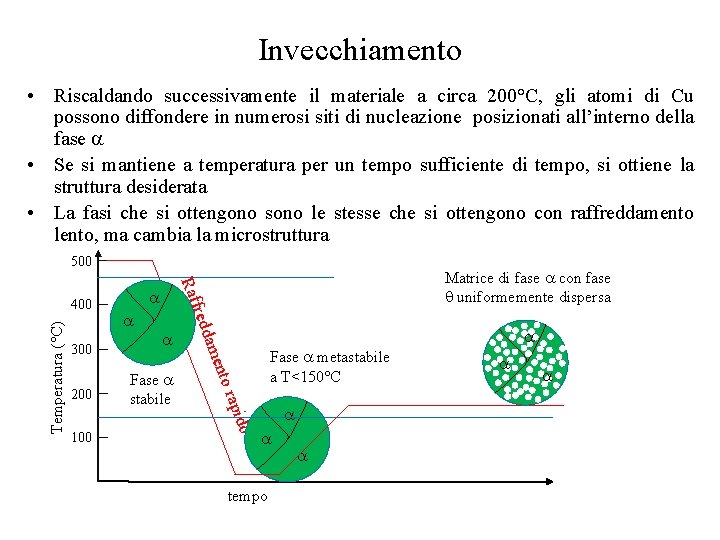
Invecchiamento • Riscaldando successivamente il materiale a circa 200°C, gli atomi di Cu possono diffondere in numerosi siti di nucleazione posizionati all’interno della fase • Se si mantiene a temperatura per un tempo sufficiente di tempo, si ottiene la struttura desiderata • La fasi che si ottengono sono le stesse che si ottengono con raffreddamento lento, ma cambia la microstruttura 500 Fase stabile Fase metastabile a T<150°C ido rap Temperatura (°C) ento 100 dam 200 fred 300 Raf 400 Matrice di fase con fase uniformemente dispersa tempo

Acciaio • Acciaio: lega ferro-carbonio contenuto di carbonio C<2. 11% • Fe puro: • Rm = 180 -290 MPa • Re = 100 -170 MPa • A% = 40 -50% • HB = 45 -55 • E = 210 GPa • Oltre alla fusione, il ferro presenta due trasformazioni di fase allo stato solido, le temperature corrispondenti vengono indicate con A 3 ed A 4 (nelle condizioni di equilibrio). • A 3 (912°C): Fe (CCC) Fe (CFC) • A 4 (1394°C): Fe (CFC) Fe (CCC)

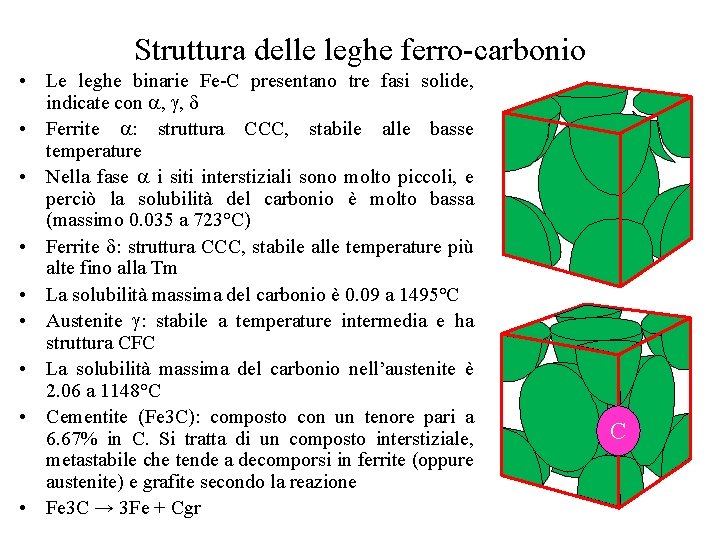
Struttura delle leghe ferro-carbonio • Le leghe binarie Fe-C presentano tre fasi solide, indicate con , , • Ferrite : struttura CCC, stabile alle basse temperature • Nella fase i siti interstiziali sono molto piccoli, e perciò la solubilità del carbonio è molto bassa (massimo 0. 035 a 723°C) • Ferrite : struttura CCC, stabile alle temperature più alte fino alla Tm • La solubilità massima del carbonio è 0. 09 a 1495°C • Austenite : stabile a temperature intermedia e ha struttura CFC • La solubilità massima del carbonio nell’austenite è 2. 06 a 1148°C • Cementite (Fe 3 C): composto con un tenore pari a 6. 67% in C. Si tratta di un composto interstiziale, metastabile che tende a decomporsi in ferrite (oppure austenite) e grafite secondo la reazione • Fe 3 C → 3 Fe + Cgr C

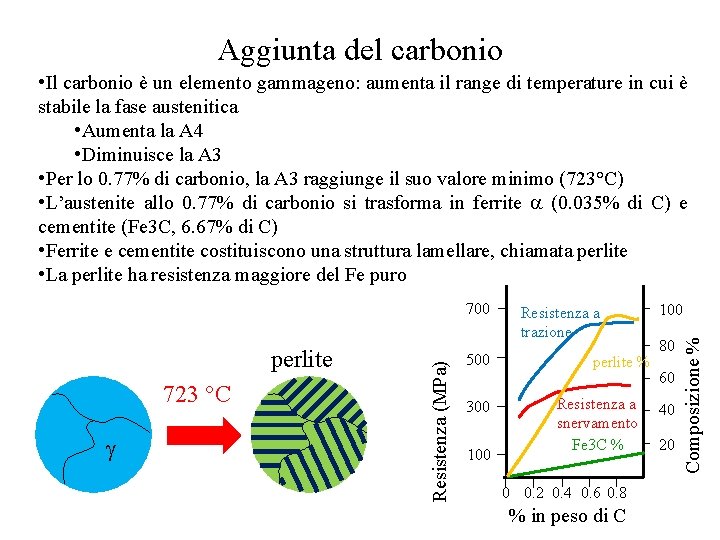
Aggiunta del carbonio • Il carbonio è un elemento gammageno: aumenta il range di temperature in cui è stabile la fase austenitica • Aumenta la A 4 • Diminuisce la A 3 • Per lo 0. 77% di carbonio, la A 3 raggiunge il suo valore minimo (723°C) • L’austenite allo 0. 77% di carbonio si trasforma in ferrite (0. 035% di C) e cementite (Fe 3 C, 6. 67% di C) • Ferrite e cementite costituiscono una struttura lamellare, chiamata perlite • La perlite ha resistenza maggiore del Fe puro 723 °C 500 300 100 Resistenza a trazione perlite % Resistenza a snervamento Fe 3 C % 0 0. 2 0. 4 0. 6 0. 8 % in peso di C 100 80 60 40 20 Composizione % perlite Resistenza (MPa) 700

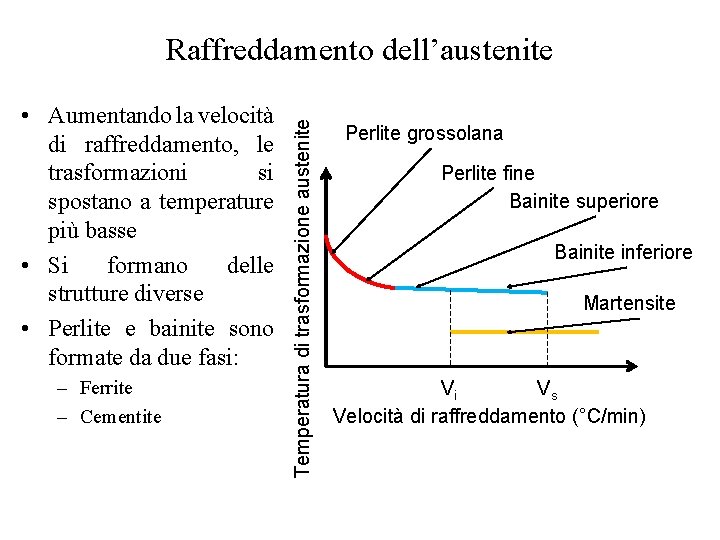
• Aumentando la velocità di raffreddamento, le trasformazioni si spostano a temperature più basse • Si formano delle strutture diverse • Perlite e bainite sono formate da due fasi: – Ferrite – Cementite Temperatura di trasformazione austenite Raffreddamento dell’austenite Perlite grossolana Perlite fine Bainite superiore Bainite inferiore Martensite Vi Vs Velocità di raffreddamento (°C/min)

• La perlite è una struttura lamellare dove ferrite e cementite sono alternate • Quanto la T di trasformazione diminuisce, le lamelle diventano sempre più sottili (per ridurre i tempi di diffusione) • Di conseguenza, nella bainite la struttura più favorevole è una struttura in cui la cementite in particelle discrete è dispersa nella matrice ferritica • Riducendo la T, la bainite diventa sempre più fine • Perlite e bainite sono costituite dalle stesse fasi (perlite e cementite) • Quella che cambia, ed influenza le proprietà del materiale, è la MICROSTRUTTURA (dimensione e distribuzione delle fasi) Cresce la velocità di nucleazione, diminuisce la velocità di crescita Perlite e bainite Fe 3 C Perlite grossolana Perlite fine Bainite superiore Bainite inferiore

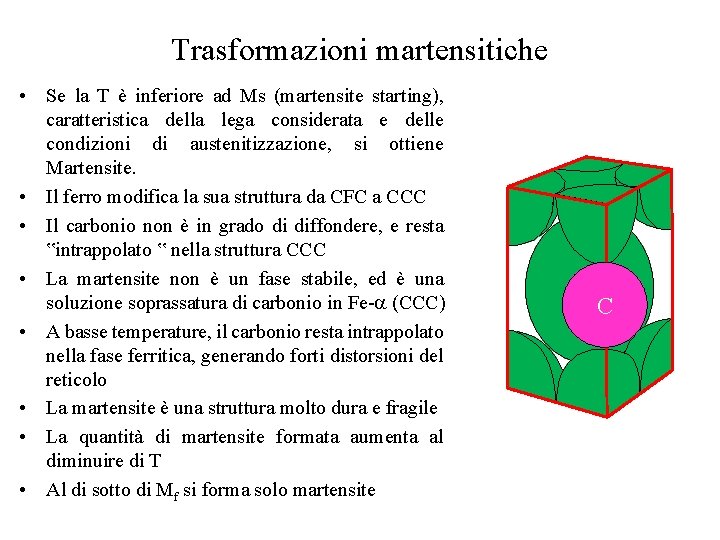
Trasformazioni martensitiche • Se la T è inferiore ad Ms (martensite starting), caratteristica della lega considerata e delle condizioni di austenitizzazione, si ottiene Martensite. • Il ferro modifica la sua struttura da CFC a CCC • Il carbonio non è in grado di diffondere, e resta ‟intrappolato ‟ nella struttura CCC • La martensite non è un fase stabile, ed è una soluzione soprassatura di carbonio in Fe- (CCC) • A basse temperature, il carbonio resta intrappolato nella fase ferritica, generando forti distorsioni del reticolo • La martensite è una struttura molto dura e fragile • La quantità di martensite formata aumenta al diminuire di T • Al di sotto di Mf si forma solo martensite C

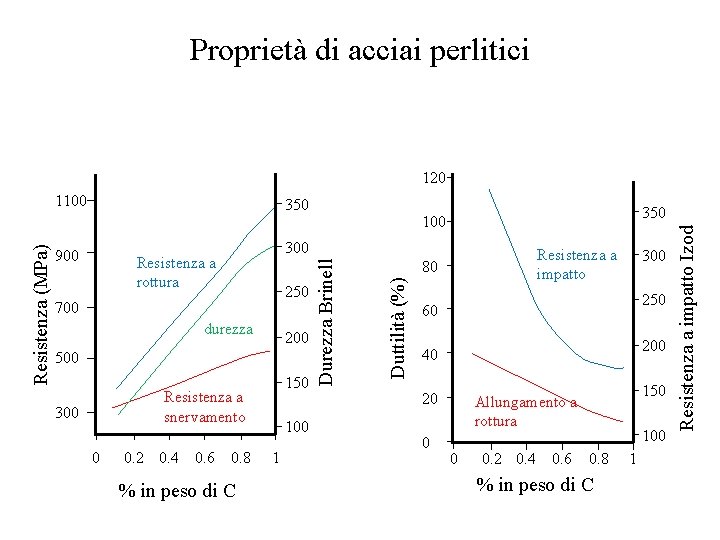
Proprietà di acciai perlitici 120 300 Resistenza a rottura 250 700 durezza 200 500 150 Resistenza a snervamento 300 0 0. 2 0. 4 0. 6 0. 8 % in peso di C 100 1 Resistenza a impatto 80 Duttilità (%) 900 350 100 300 250 60 200 40 20 0 150 Allungamento a rottura 0 0. 2 0. 4 0. 6 100 0. 8 % in peso di C 1 Resistenza a impatto Izod 350 Durezza Brinell Resistenza (MPa) 1100

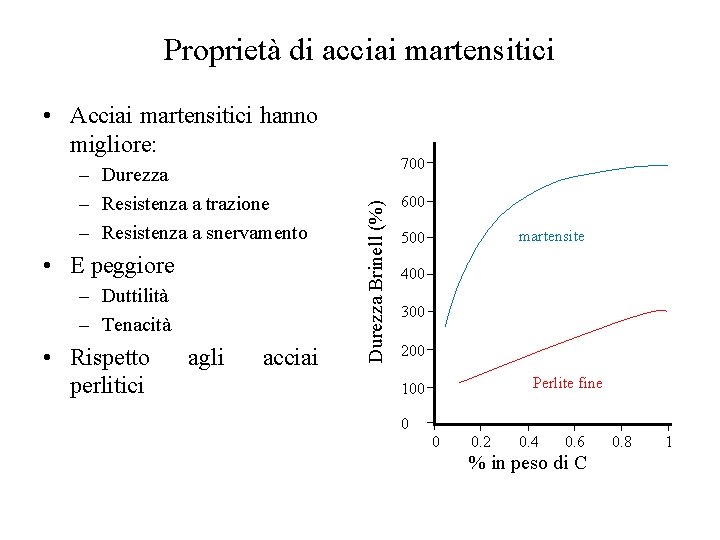
Proprietà di acciai martensitici • Acciai martensitici hanno migliore: • E peggiore – Duttilità – Tenacità • Rispetto perlitici agli acciai 700 Durezza Brinell (%) – Durezza – Resistenza a trazione – Resistenza a snervamento 600 martensite 500 400 300 200 Perlite fine 100 0 0 0. 2 0. 4 0. 6 % in peso di C 0. 8 1

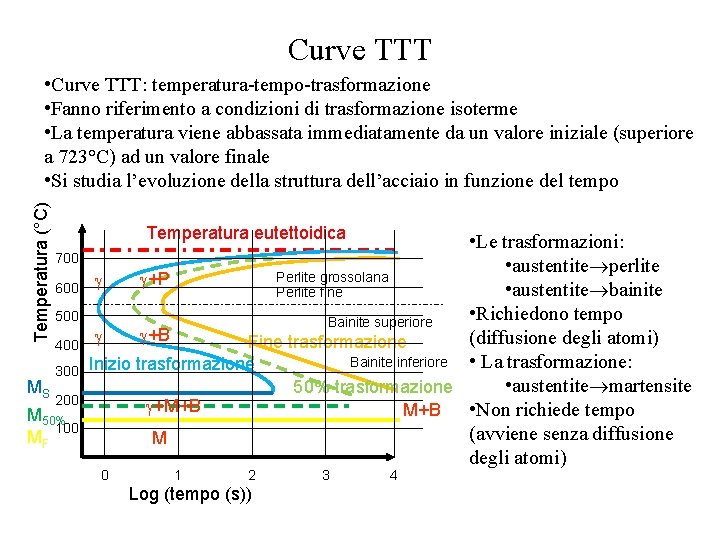
Curve TTT Temperatura (°C) • Curve TTT: temperatura-tempo-trasformazione • Fanno riferimento a condizioni di trasformazione isoterme • La temperatura viene abbassata immediatamente da un valore iniziale (superiore a 723°C) ad un valore finale • Si studia l’evoluzione della struttura dell’acciaio in funzione del tempo MS Temperatura eutettoidica 700 600 500 400 300 200 M 50% 100 MF • Le trasformazioni: • austentite perlite Perlite grossolana +P • austentite bainite Perlite fine • Richiedono tempo Bainite superiore +B (diffusione degli atomi) Fine trasformazione Bainite inferiore • La trasformazione: Inizio trasformazione • austentite martensite 50% trasformazione +M+B • Non richiede tempo M+B (avviene senza diffusione M degli atomi) 0 1 2 Log (tempo (s)) 3 4

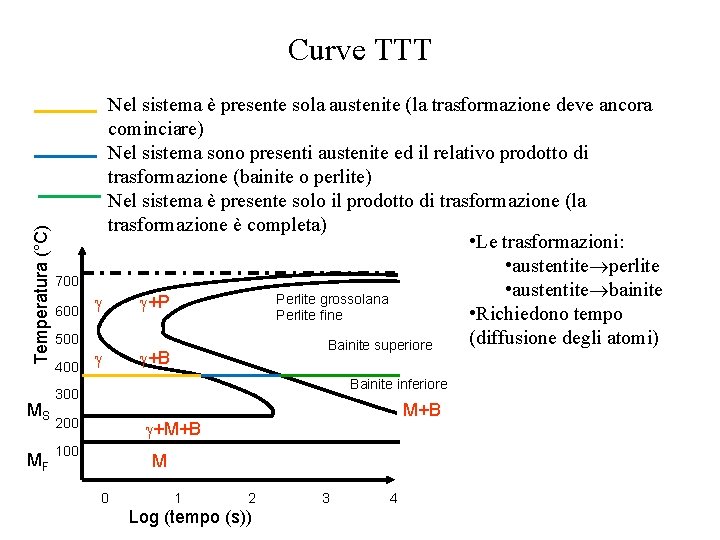
Temperatura (°C) Curve TTT MS MF 700 600 500 400 Nel sistema è presente sola austenite (la trasformazione deve ancora cominciare) Nel sistema sono presenti austenite ed il relativo prodotto di trasformazione (bainite o perlite) Nel sistema è presente solo il prodotto di trasformazione (la trasformazione è completa) • Le trasformazioni: • austentite perlite • austentite bainite Perlite grossolana +P • Richiedono tempo Perlite fine (diffusione degli atomi) Bainite superiore +B Bainite inferiore 300 200 M+B +M+B 100 M 0 1 2 Log (tempo (s)) 3 4

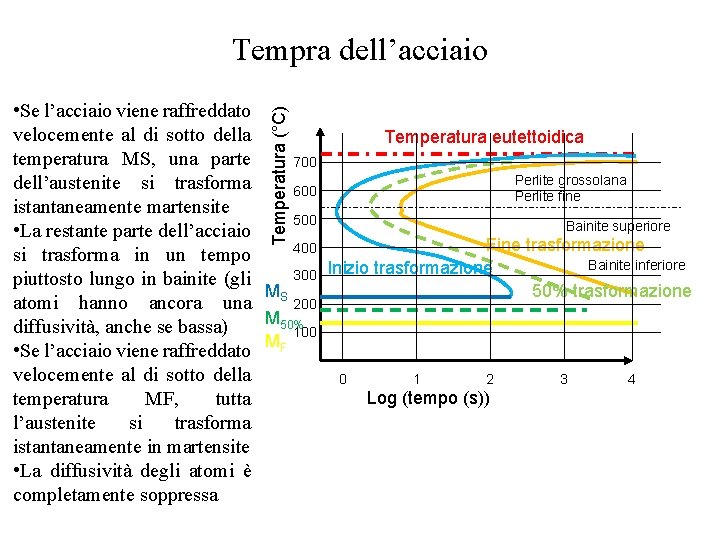
Tempra dell’acciaio Temperatura (°C) • Se l’acciaio viene raffreddato velocemente al di sotto della Temperatura eutettoidica temperatura MS, una parte 700 Perlite grossolana dell’austenite si trasforma 600 Perlite fine istantaneamente martensite 500 Bainite superiore • La restante parte dell’acciaio Fine trasformazione 400 si trasforma in un tempo Bainite inferiore Inizio trasformazione 300 piuttosto lungo in bainite (gli M 50% trasformazione atomi hanno ancora una S 200 M 50% diffusività, anche se bassa) 100 MF • Se l’acciaio viene raffreddato velocemente al di sotto della 0 1 2 3 4 Log (tempo (s)) temperatura MF, tutta l’austenite si trasforma istantaneamente in martensite • La diffusività degli atomi è completamente soppressa

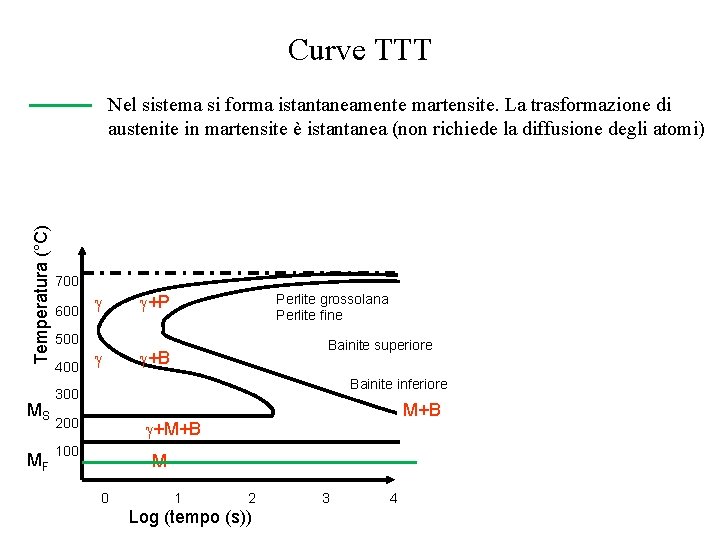
Curve TTT Temperatura (°C) Nel sistema si forma istantaneamente martensite. La trasformazione di austenite in martensite è istantanea (non richiede la diffusione degli atomi) MS MF 700 600 500 400 +P Perlite grossolana Perlite fine Bainite superiore +B Bainite inferiore 300 200 M+B +M+B 100 M 0 1 2 Log (tempo (s)) 3 4

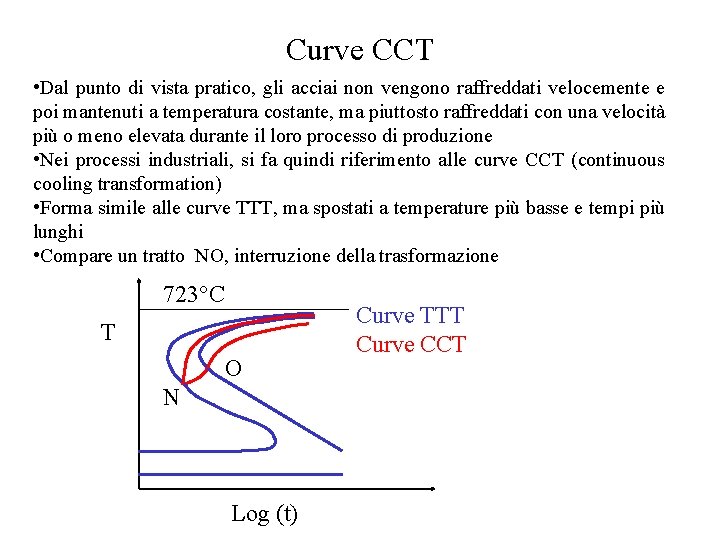
Curve CCT • Dal punto di vista pratico, gli acciai non vengono raffreddati velocemente e poi mantenuti a temperatura costante, ma piuttosto raffreddati con una velocità più o meno elevata durante il loro processo di produzione • Nei processi industriali, si fa quindi riferimento alle curve CCT (continuous cooling transformation) • Forma simile alle curve TTT, ma spostati a temperature più basse e tempi più lunghi • Compare un tratto NO, interruzione della trasformazione 723°C T O N Log (t) Curve TTT Curve CCT

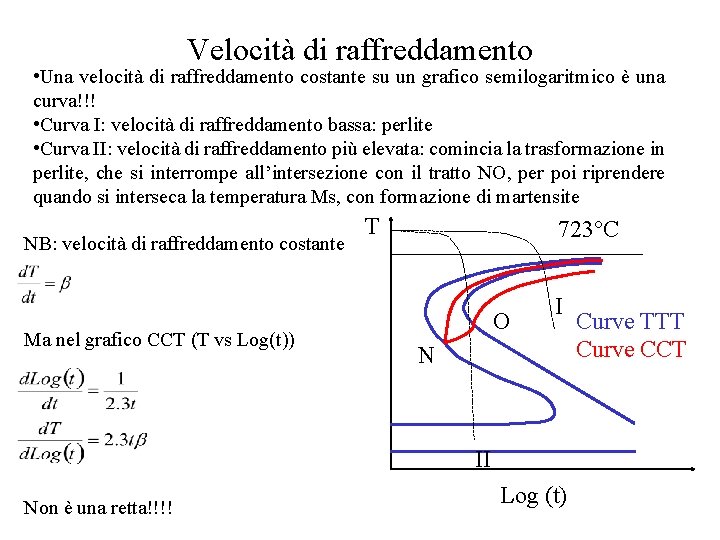
Velocità di raffreddamento • Una velocità di raffreddamento costante su un grafico semilogaritmico è una curva!!! • Curva I: velocità di raffreddamento bassa: perlite • Curva II: velocità di raffreddamento più elevata: comincia la trasformazione in perlite, che si interrompe all’intersezione con il tratto NO, per poi riprendere quando si interseca la temperatura Ms, con formazione di martensite NB: velocità di raffreddamento costante Ma nel grafico CCT (T vs Log(t)) T 723°C O I N II Non è una retta!!!! Log (t) Curve TTT Curve CCT

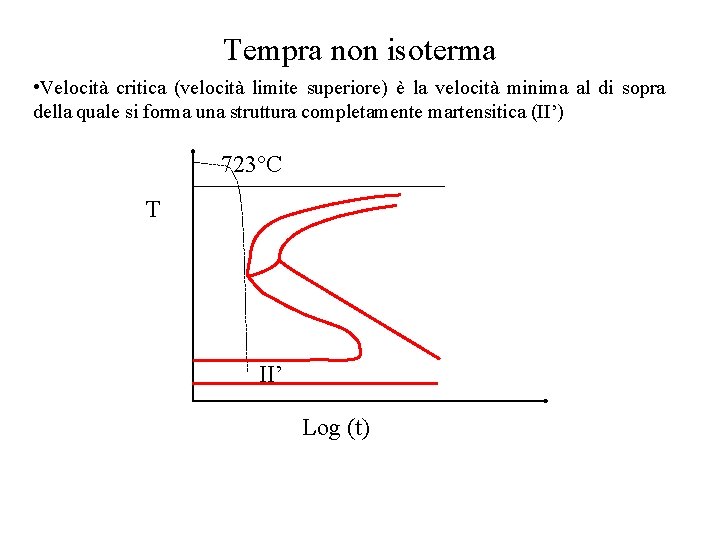
Tempra non isoterma • Velocità critica (velocità limite superiore) è la velocità minima al di sopra della quale si forma una struttura completamente martensitica (II’) 723°C T II’ Log (t)

Raffreddamento • Nella tempra, è necessario avere un rapido raffreddamento • E’ necessario verificare quali sono le condizioni di processo che permettono di ottenere rapidi raffreddamenti • E’ possibile studiare due ipotesi: 1) raffreddamento uniforme (trascuro i gradienti di temperatura) 2) raffreddamento non uniforme

Riscaldamento e raffreddamento uniformi • Lastra di materiale molto sottile • Raffreddata dall’esterno per mezzo di un fluido. La quantità di calore asportato per unità di tempo vale • h: coefficiente di scambio termico convettivo (W/(m 2*K)) (dipende dal fluido), A superficie di contatto del fluido a temperatura Te con il solido a temperatura T • L’effetto della rimozione del calore è una riduzione dell’entalpia del materiale: Te T Te

Riscaldamento e raffreddamento uniformi

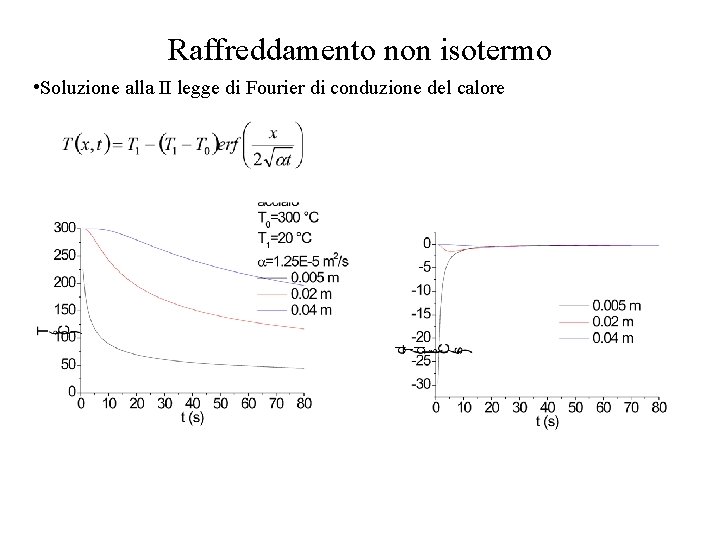
Raffreddamento non isotermo • Soluzione alla II legge di Fourier di conduzione del calore

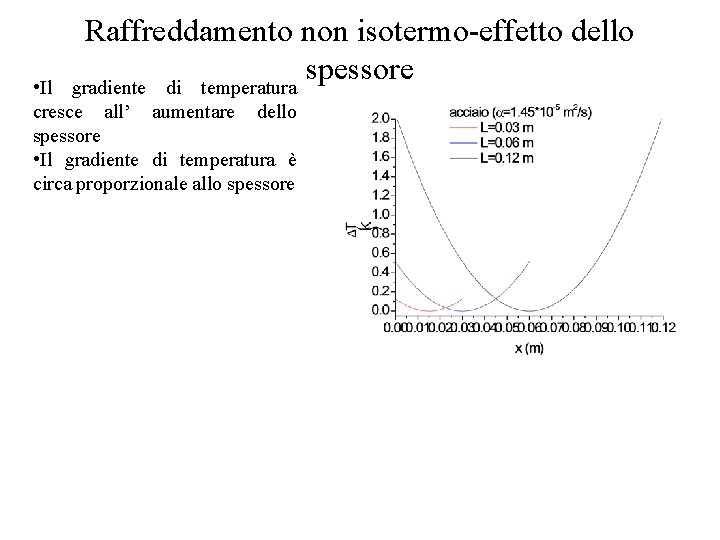
Raffreddamento non isotermo-effetto dello spessore gradiente di temperatura • Il cresce all’ aumentare dello spessore • Il gradiente di temperatura è circa proporzionale allo spessore

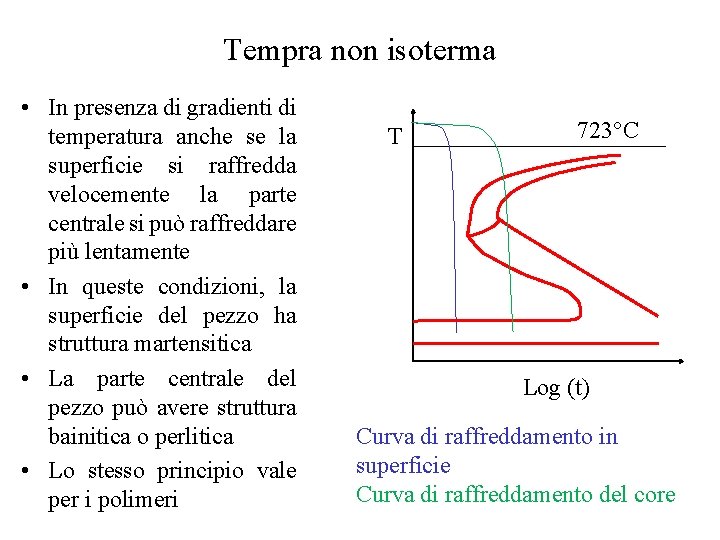
Tempra non isoterma • In presenza di gradienti di temperatura anche se la superficie si raffredda velocemente la parte centrale si può raffreddare più lentamente • In queste condizioni, la superficie del pezzo ha struttura martensitica • La parte centrale del pezzo può avere struttura bainitica o perlitica • Lo stesso principio vale per i polimeri T 723°C Log (t) Curva di raffreddamento in superficie Curva di raffreddamento del core

Prova Jominy • Si utilizza per studiare la temprabilità di un acciaio • Si parte da un provino di acciaio completamente austenitizzato (T>723 °C) Provino di acciaio (dimensioni Zona più calda standardizzate) T>723 °C Getto d’acqua (distanza, getto libero, portata e diametro Zona più fredda ugello standardizzati)

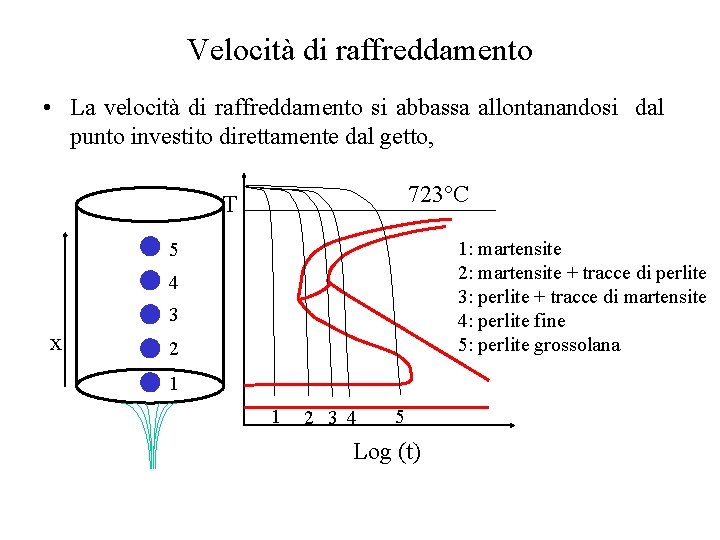
Velocità di raffreddamento • La velocità di raffreddamento si abbassa allontanandosi dal punto investito direttamente dal getto, 723°C T 1: martensite 2: martensite + tracce di perlite 3: perlite + tracce di martensite 4: perlite fine 5: perlite grossolana 5 4 3 x 2 1 1 2 3 4 5 Log (t)

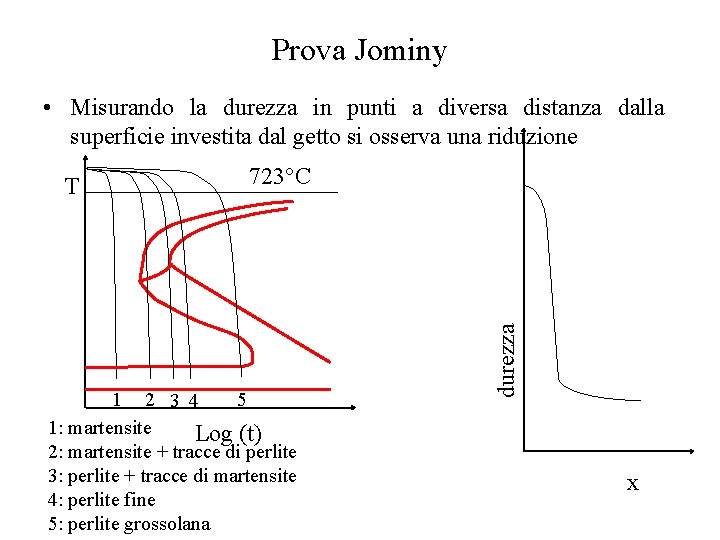
Prova Jominy • Misurando la durezza in punti a diversa distanza dalla superficie investita dal getto si osserva una riduzione 723°C 1 2 3 4 5 1: martensite Log (t) 2: martensite + tracce di perlite 3: perlite + tracce di martensite 4: perlite fine 5: perlite grossolana durezza T x

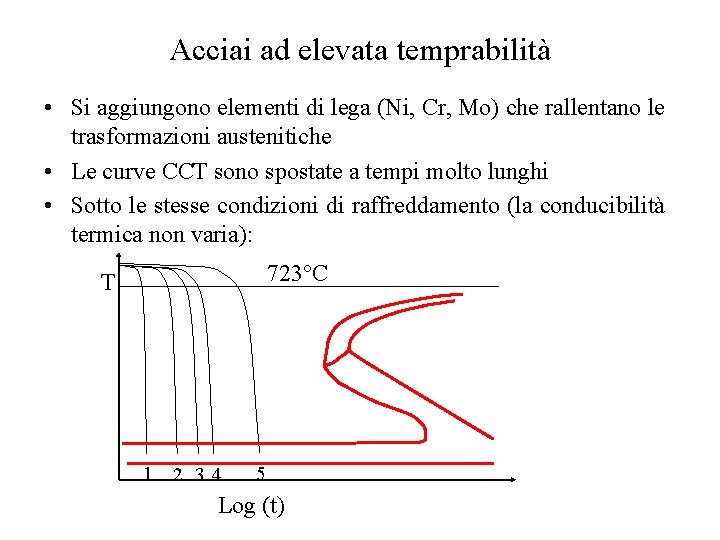
Acciai ad elevata temprabilità • Si aggiungono elementi di lega (Ni, Cr, Mo) che rallentano le trasformazioni austenitiche • Le curve CCT sono spostate a tempi molto lunghi • Sotto le stesse condizioni di raffreddamento (la conducibilità termica non varia): 723°C T 1 2 34 5 Log (t)

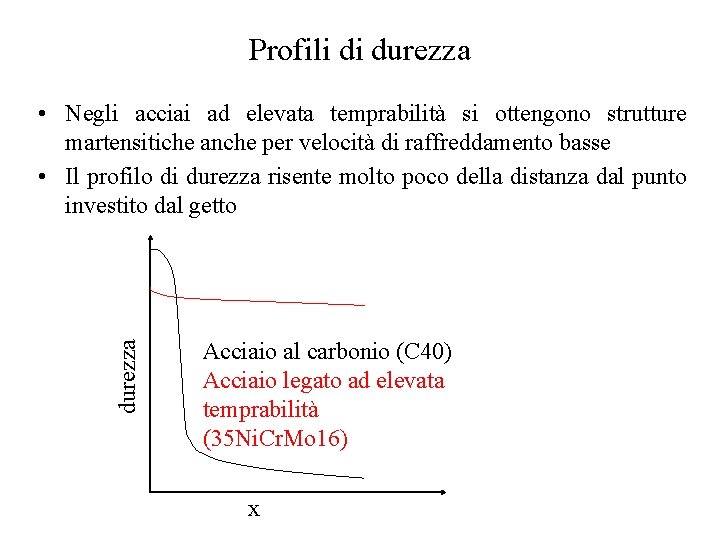
Profili di durezza • Negli acciai ad elevata temprabilità si ottengono strutture martensitiche anche per velocità di raffreddamento basse • Il profilo di durezza risente molto poco della distanza dal punto investito dal getto Acciaio al carbonio (C 40) Acciaio legato ad elevata temprabilità (35 Ni. Cr. Mo 16) x

Rinvenimento • Permette di eliminare tensioni interne derivanti dal rapido raffreddamento e aumentare duttilità e tenacità • Nel rinvenimento, la martensite riscaldata a 250 -650°C si trasforma in ferrite e cementite • La cementite è dispersa sotto forma di particelle piccole disperse uniformemente nella matrice ferritica

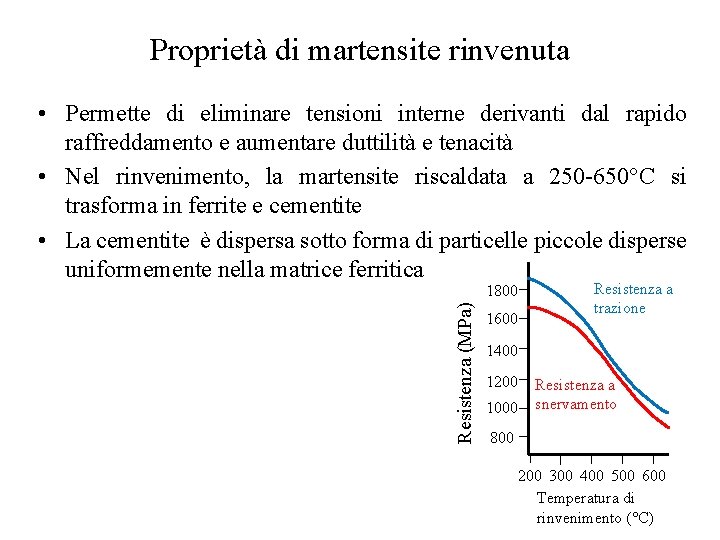
Proprietà di martensite rinvenuta • Permette di eliminare tensioni interne derivanti dal rapido raffreddamento e aumentare duttilità e tenacità • Nel rinvenimento, la martensite riscaldata a 250 -650°C si trasforma in ferrite e cementite • La cementite è dispersa sotto forma di particelle piccole disperse uniformemente nella matrice ferritica Resistenza (MPa) 1800 1600 Resistenza a trazione 1400 1200 1000 Resistenza a snervamento 800 200 300 400 500 600 Temperatura di rinvenimento (°C)
 Transizioni di fase
Transizioni di fase In morte del fratello giovanni
In morte del fratello giovanni Transizioni obs
Transizioni obs Elemen proses pemecahan masalah
Elemen proses pemecahan masalah Leer y transcribir
Leer y transcribir Fase hermeneutica del estado del arte
Fase hermeneutica del estado del arte Fase fase pengambilan keputusan
Fase fase pengambilan keputusan Fase ebb fase flow
Fase ebb fase flow 3 fase naar 1 fase transformator
3 fase naar 1 fase transformator Entnologi
Entnologi Fase fase proses kompilasi
Fase fase proses kompilasi Fase dan beda fase gelombang
Fase dan beda fase gelombang Fase diam
Fase diam Novas abordagens da administração
Novas abordagens da administração Metodo americano y europeo
Metodo americano y europeo Ejemplos de sistemas continuos
Ejemplos de sistemas continuos Sistema semashko o sistema centralizado
Sistema semashko o sistema centralizado Complejo mayor de histocompatibilidad
Complejo mayor de histocompatibilidad A que edad inicia la pubertad
A que edad inicia la pubertad Cracinoma
Cracinoma Sintomas fase aguda doença de chagas
Sintomas fase aguda doença de chagas Fase sefalik
Fase sefalik Benaderingswijzen dementie
Benaderingswijzen dementie Fase developer adalah
Fase developer adalah Fase vascular
Fase vascular Fase folicular
Fase folicular Fase de muerte bacteriana
Fase de muerte bacteriana Hibridación en fase líquida
Hibridación en fase líquida Burbujeo espiratorio
Burbujeo espiratorio Dieta para diverticulitis fase aguda
Dieta para diverticulitis fase aguda Vanni lughi
Vanni lughi Fase formula
Fase formula Juicio ordinario (etapa expositiva)
Juicio ordinario (etapa expositiva) Hplc fase normal
Hplc fase normal Fase luminosa aciclica
Fase luminosa aciclica Agonia definicion
Agonia definicion Fase antillana
Fase antillana Complesso mioelettrico migrante
Complesso mioelettrico migrante Fase eliptica
Fase eliptica Sensomotorische fase
Sensomotorische fase Screening neonatale richiamo
Screening neonatale richiamo Fase pertumbuhan padi
Fase pertumbuhan padi Fase diam kkt yang biasa digunakan adalah
Fase diam kkt yang biasa digunakan adalah Fase tidur rem
Fase tidur rem Stervensfase palliatieve zorg
Stervensfase palliatieve zorg Hplc fase normal
Hplc fase normal Cromatografia de afinidad fase movil
Cromatografia de afinidad fase movil Fase farmacodinamia
Fase farmacodinamia Modulo 22 semana 4
Modulo 22 semana 4 Evolucao de ferida enfermagem
Evolucao de ferida enfermagem Corriente de linea y de fase
Corriente de linea y de fase Palliatieve sedatie nhg
Palliatieve sedatie nhg Fase luminosa fotosintesi zanichelli
Fase luminosa fotosintesi zanichelli Proses menelan makanan
Proses menelan makanan Fase fluida
Fase fluida Fase condensada
Fase condensada Palliatief redeneren voorbeeld
Palliatief redeneren voorbeeld Valores de pcr en artritis reumatoide
Valores de pcr en artritis reumatoide Eritrofago
Eritrofago