TRANSFECCION Transferencia de material gentico Mtodos no virales

















- Slides: 26

TRANSFECCION Transferencia de material genético • Métodos no virales (Mecanismos físicos). – Técnicas no virales con aplicaciones “in vitro” e “in vivo” – Vectores no virales limitados a aplicaciones “in vitro” • Métodos virales. 1

• Técnicas no virales limitadas a aplicaciones “in vitro” • • Transfección compuestos químicos: fosfato cálcico, DEAE-dextrano Microinyección Electroporación Técnicas no virales con aplicaciones “in vitro” e “in vivo” • • Liposomas Inyección de ADN desnudo Inyección balística de ADN Inmunización basada en ADN 2

3

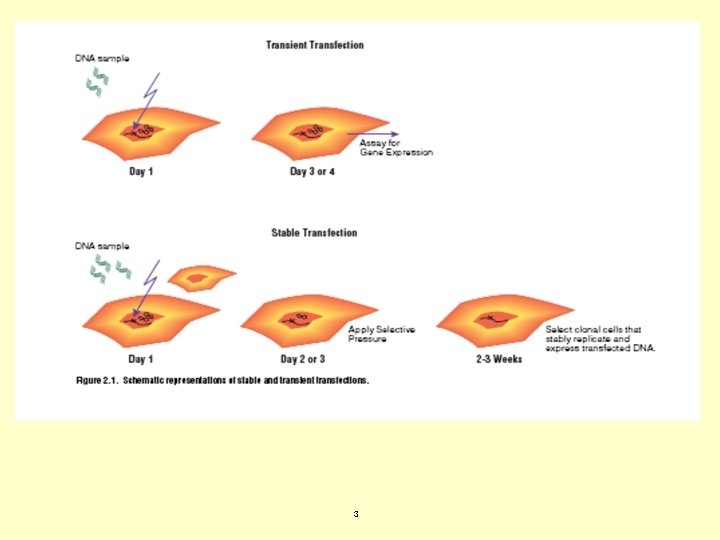
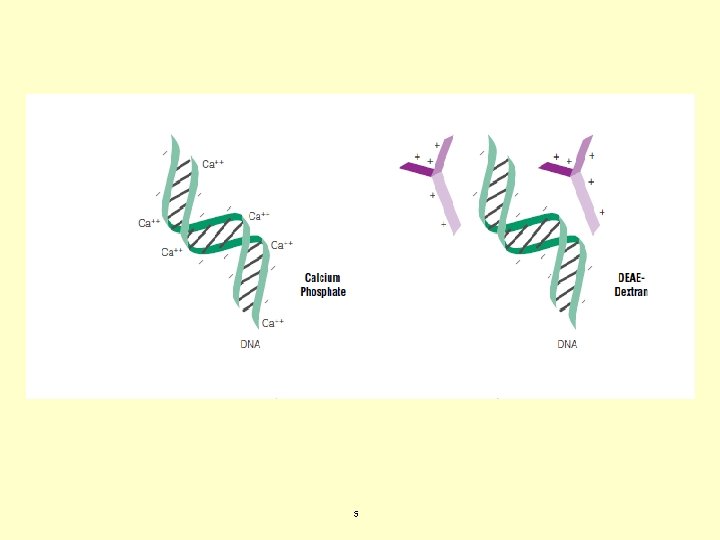
Técnicas no virales limitadas a aplicaciones “in vitro” Transfección con fosfato cálcico. Eficiencia de transfección mayores del 10% en alguna línea celular. En muchos casos menor del 1%. Toxicidad mínima. Mecanismo: endocitosis. Transfección con DEAE-dextrano. Más reproducible. Mecanismo desconocido. Sólo funciona en un número reducido de líneas. 4

5

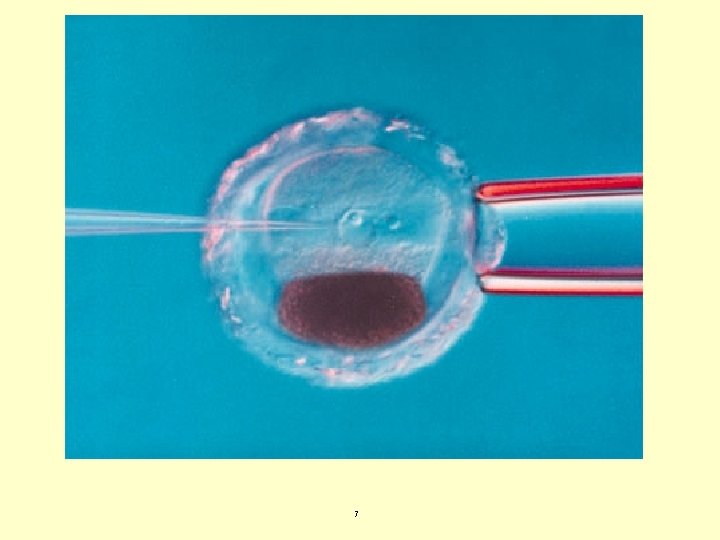
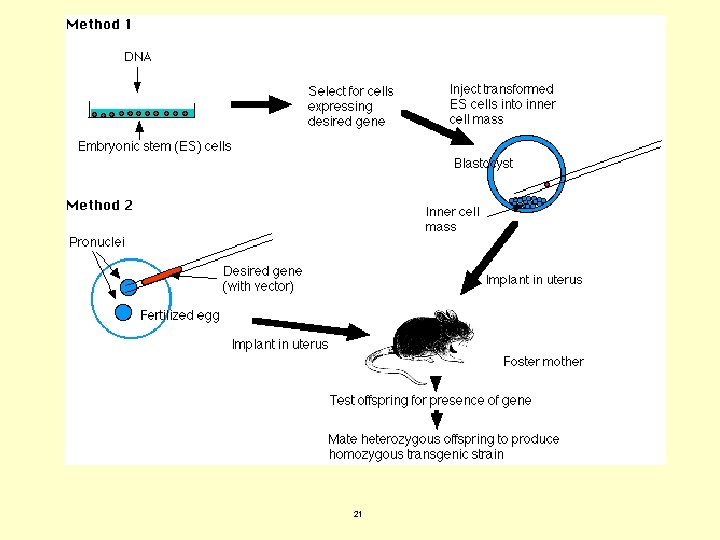
Técnicas no virales limitadas a aplicaciones “in vitro” Microinyección. Se evita la degradación lisosomal y citoplasmática del material. Técnica laboriosa que requiere células bien aisladas. La modificación de la línea germinal permite en mamíferos la producción de transgénicos. 6

7

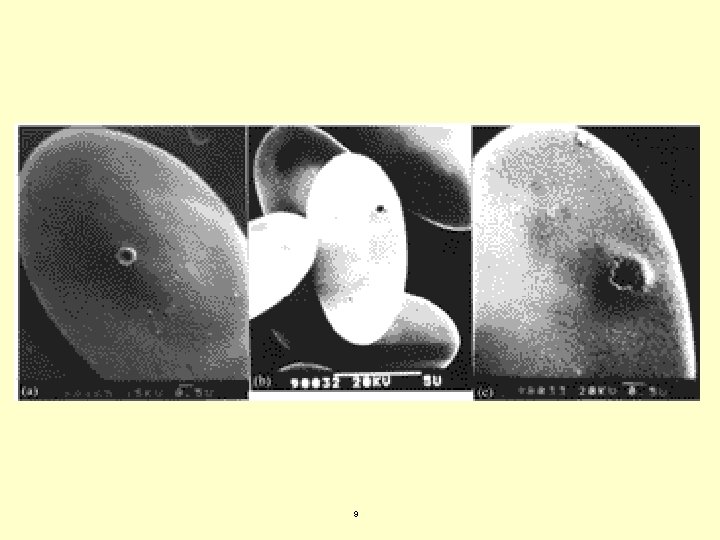
Técnicas no virales limitadas a aplicaciones “in vitro” Electroporación. Aplicación de alto voltaje a una mezcla de ADN y células en suspensión. La eficiencia de la transferencia depende del pulso eléctrico, distancia entre electrodos, fuerza iónica del tampón de suspensión celular y de la naturaleza de las células. Muchas células de mamíferos no sobreviven al pulso eléctrico. 8

9

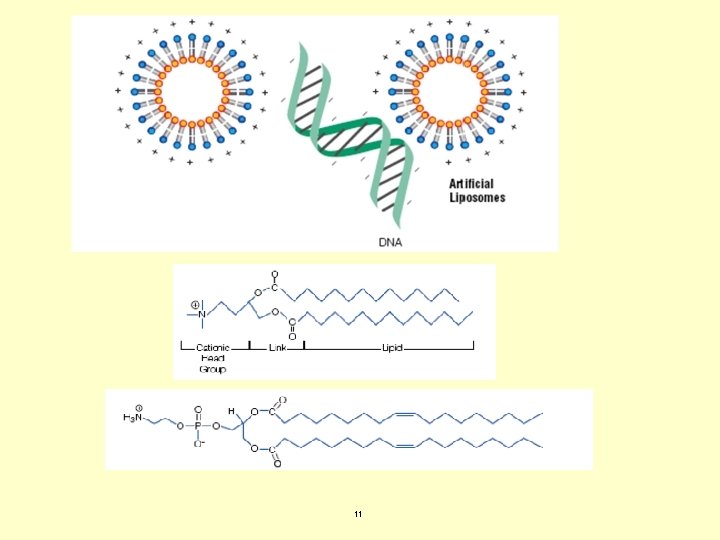
Técnicas no virales con aplicaciones “in vitro” e “in vivo” Liposomas catiónicos. Forman complejos con el ADN. Están formados por un lípido positivamente cargado y un colípido (“lípidos ayudantes”: DOPE, DOPC). Un lípido catiónico ampliamente utilizado es la lipofectina (1987. Mezcla de cloruro de N-[1 -(2, 3 -dioleyiloxy))propil]-N-N-N-trimetil amonio – DOTMA- y DOPE). ADN y lipofectina interaccionan espontáneamente formando complejos con una eficiencia del 100%. Inmediatamente después de la administración intravenosa de estos complejos tanto pulmón como hígado muestran una afinidad marcada por su incorporación y la expresión del transgen. Liposomas sensible a p. H (liposomas negativamente cargados). No forman complejos. ADN queda atrapado en la fase acuosa interior del liposoma. Aplicaciones: 1. - Pueden transferir moléculas negativa- o positivamente cargadas. 2. - Ofrecen un grado de protección al ADN de procesos degradativos. 3. - Pueden llevar trozos grandes de ADN. 4. - Pueden ser dirigidos específicamente a tejidos u órganos. 10

11

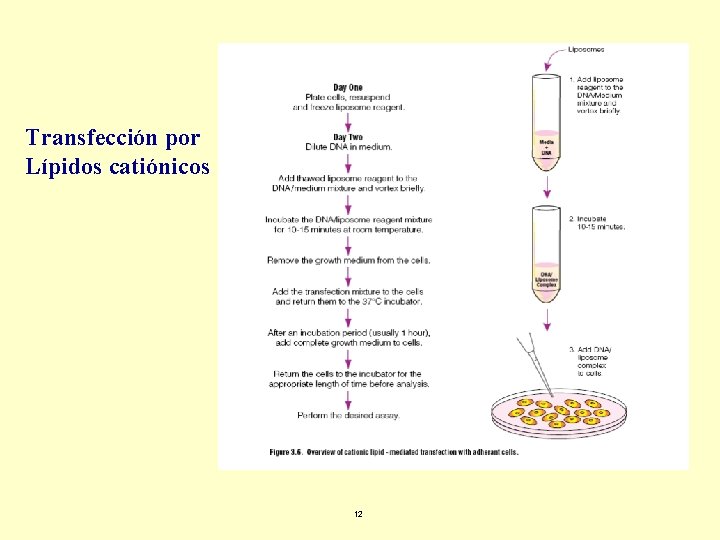
Transfección por Lípidos catiónicos 12

Técnicas no virales con aplicaciones “in vitro” e “in vivo” Inyección de ADN plasmídico desnudo Fácil de realizar. Los tejidos que muestran expresión del transgen después de inyección de ADN plasmídico incluyen timo, piel, músculo cardíaco y esquelético. El ADN plasmídico no sufre cambios en el patrón de metilación sugiriendo que no se ha replicado después de la inyección y tampoco se integra en el genoma. La preinyección de soluciones de sacarosa en el músculo incrementa algo los niveles de expresión del transgen. El músculo de primates parece ser menos eficiente en la incorporación del ADN que el músculo de roedores. Tamaño del ADN: 2 -19 kilobases. 13

Técnicas no virales con aplicaciones “in vitro” e “in vivo” Inyección balística de ADN Bombardeo de partículas, transferencia génica por microproyectiles o “gene-gun”. El ADN plasmídico del gen recubre micropartículas de oro o tungsteno de 1 -3 micras de diámetro. Estas se colocan en una lámina soporte y se descargan sobre el blanco. Libera dosis controladas de ADN. Produce daño en la célula. Inmunización basada en ADN. Inmunización contra HIV, hepatitis B y C, papiloma, Helicobacter pylori, malaria, etc. 14

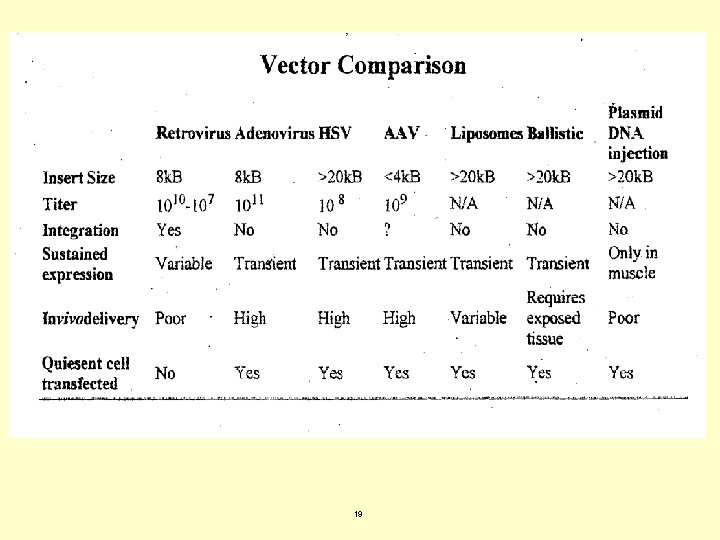
Vectores virales Retrovirus • Son virus ARN que tienen capacidad para integrar genes terapéuticos relativamente grandes (un máximo de 8 Kb). Necesitan de células empaquetadoras para su obtención. Se transfiere el DNA del virus mediante la técnica del fosfato de calcio a las células empaquetadoras. Posteriormente se realiza una segunda transducción en la cual introducimos la construcción génica de interés. • Los virus inyectados en el huésped integran su DNA en el genoma del huésped expresando así el gen que le hemos añadido. Como las proteínas del virus no son expresadas por el huésped, no tenemos una respuesta inmunitaria. Tienen una alta eficacia de transducción y también de expresión, siendo un sistema bien estudiado. • Sin embargo, únicamente sirven para infectar células del huésped que se encuentran en división. Además los títulos de virus obtenidos hasta ahora son bajos y la integración en el genoma es al azar. • Existen también vectores basados en el virus del SIDA (HIV), cuyo genoma es más complejo pero con un funcionamiento similar al que hemos visto. Son los denominados lentivirus. 15

Vectores virales Adenovirus • Son una familia de virus ADN que causan infecciones en el tracto respiratorio humano. Se pueden llegar a insertar en ellos hasta 7. 5 Kb. de DNA exógeno. Normalmente en terapia génica se utiliza el serotipo 5, aunque existen hasta 42 serotipos diferentes que infectan a humanos. • En este caso no se necesita la integración del material hereditario del virus en el del huésped para su replicación, por lo tanto tampoco el transgén será introducido en el genoma de la célula. Y por tanto tampoco necesitan que las células infectadas estén dividiéndose para su replicación. • La gran ventaja de usar un adenovirus como vector es la alta eficacia de transducción, al igual que la expresión de la construcción génica introducida, sin embargo ésta es transitoria (pocas semanas). Esto último obligaría a tratamientos periódicos lo cual es un inconveniente ya que los adenovirus producen respuesta inmune celular e inflamatoria. 16

Vectores virales Virus adenoasociados (VAA) • Son parvovirus, contienen ADN como material genético, y requieren la coinfección con un adenovirus para multiplicarse. Son vectores que combinan las ventajas de los retrovirales y los adenovirales. Su capacidad de integrar DNA exógeno es pequeña, sólo de 5 Kb. • Las principales ventajas son que los virus adenoasociados integran su ADN en la célula durante la replicación, por lo que la transducción (la cual es altamente eficaz) es estable en la célula diana. Además pueden infectar tanto a células en división como a las que no lo están (de gran importancia para la terapia génica "in vivo"). Los vectores AAV no están implicados en ningún tipo de enfermedad humana. Además el riesgo de una respuesta inmune está minimizado ya que no produce proteínas víricas. • Sin embargo existen también una serie de inconvenientes como que este tipo de vectores todavía no ha sido tan bien estudiado como los retrovirus y los adenovirus. 17

Vectores virales Herpesvirus • Son virus DNA cuyas células diana son las neuronas. Su complejidad y lo poco que todavía conocemos de esta familia de virus dificulta su utilización. • La gran ventaja es el gran tamaño de su ADN, que les permite aceptar varios genes terapéuticos, incluso podrían ir con sus propias regiones reguladoras. • Uno de los inconvenientes es que habría que eliminar las secuencias que codifican para las proteínas líticas del virus que causan la muerte de las células a las que infectan. 18

19

20

21

Nivel de intervención Estrategia de tratamiento Gen mutante Modificación del genotipo somático (trasplante: terapia por transferencia génica) m. RNA mutante Modulación farmacológica de la expresión génica Proteína mutante Reemplazo de la proteína. Estimulación de la función residual de la proteína Disfunción metabólica Compensación en la dieta o farmacológica o bioquímica en pacientes seleccionados Fenotipo clínico Intervención médica o quirúrgica Familia Consejo genético; “screening”; diagnóstico presintomático 22

Tratamiento por manipulación metabólica Intervención metabólica Sustancia o técnica Ejemplo Bioquímico Anulación Fármacos antimalaria Deficiencia G 6 PD Restricción dieta Fenilalanina, Galactosa PKU, Galactosemia Reemplazo Tiroxina, Biotina Hipotiroidismo, Deficiencia biotinasa Desvío Benzoato sódico Desórdenes ciclo de la urea Inhibición Lovastatina Hipercolesterolemia familiar Agotamiento Terapia de cambio de plasma Hipercolesterolemia familiar 23

Tratamiento al nivel de la proteína mutante Estrategia Ejemplo . Incremento de la función proteína mutante Administración cofactor para Homocistinuria con respuesta a incrementar la actividad del enzima piridoxina Incremento de la función proteína mutante Reemplazo de una proteína extracelular Factor VIII en hemofilia A Deficiencia en alfa-1 -antitripsina Reemplazo extracelular de una Deficiencia en adenosina deaminasa proteína intracelular (ADA modificada con PEG) Reemplazo de una proteína intracelular Glucocerebrosidasa modificada por “cell targeting” en la enfermedad de Gaucher 24

Modificación del genoma o su expresión Tipo de modificación Ejemplo . Modificación farmacológica Hidroxiurea para estimular la síntesis de Hb F (anemias y talasemias) INF-γ (enfermedad granulomatosa) Modificación del genotipo somático Por transplante Trasplante de médula ósea (Talasemias y enfermedades lisosomales) Trasplante de hígado (deficiencia en alfa-1 -antitripsina) Por transferencia de ADN Adenosina deaminasa (deficiencia ADA) Factor de crecimiento endotelial vascular (isquemia de miocardio) p 53 (cáncer de pulmón) BRCA 1 (cáncer de ovario) E 1 A (cáncer de ovario) CFTR (Fibrosis quística) Bcl-2 antisentido (linfoma non-Hodgkin) 25

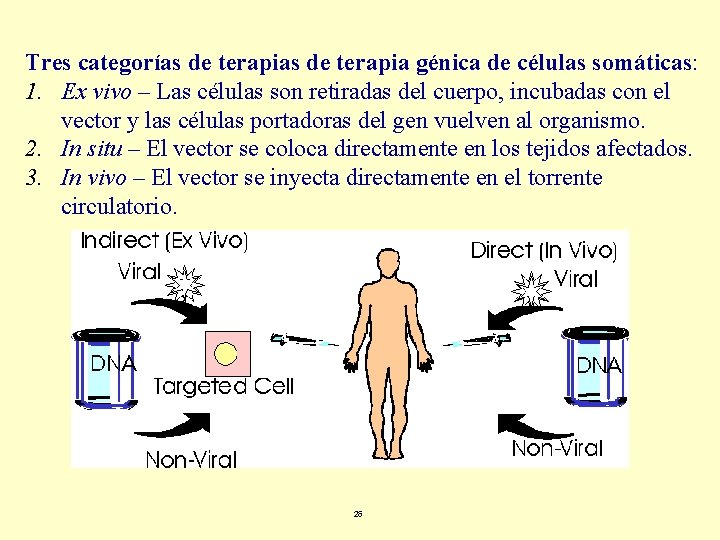
Tres categorías de terapia génica de células somáticas: 1. Ex vivo – Las células son retiradas del cuerpo, incubadas con el vector y las células portadoras del gen vuelven al organismo. 2. In situ – El vector se coloca directamente en los tejidos afectados. 3. In vivo – El vector se inyecta directamente en el torrente circulatorio. 26