Traitement des NMOSD une explosion des possibles Le

Traitement des NMOSD : une explosion des possibles ! • Le traitement préventif des poussées de NMOSD est en train de vivre une véritable révolution • Les immunosuppresseurs « à spectre d’action large » (utilisés hors AMM) sont généralement efficaces, alors que les traitements proposés dans la SEP sont généralement inefficaces • En plus des produits actuellement utilisés, notre arsenal devrait s’enrichir de 3 traitements dont les études de phase III montrent des résultats très favorables – Inebilizumab – Satralizumab – Eculizumab La Lettre du Neurologue ECTRIMS 2019 - D’après Free Communication 1: New treatment options in NMO, actualisé

Inebilizumab (Cree, Free communications 1) • Anti-CD 19 – CD 19 = antigène de surface des lymphocytes B, exprimé un peu plus longtemps que le CD 20 dans le développement des cellules B (plus précocement et plus tardivement, mais qui comme le CD 20 n’est généralement plus présent sur les plasmocytes) • N-Momentum study (multicentrique, 25 pays, 99 centres) – Phase III, monothérapie, randomisée contre placebo en double aveugle, sur 197 jours (puis extension en ouvert) – Inebilizumab 300 mg J 1 et J 15, puis 300 mg tous les 6 mois – Randomisation 3/1 : n = 174 (inebilizumab) et n = 56 (placebo) – Critère principal de jugement : délai à la 1 re poussée – Diminution risque de 1 re nouvelle poussée de 77, 3 % (phase en double aveugle contre placebo) • 88, 8 % des patients sous inebilizumab sans poussée, maintien des résultats dans la phase d’extension Patients sans poussées (%) 86, 7 59, 9 84, 7 50, 1 Inebilizumab Placebo – Moins de réactions à la perfusion que dans le groupe placebo • Réactions + fréquentes lors de la 1 re dose La Lettre du Neurologue Jours ECTRIMS 2019 - D’après Cree BA et al. , abstr. 139, actualisé
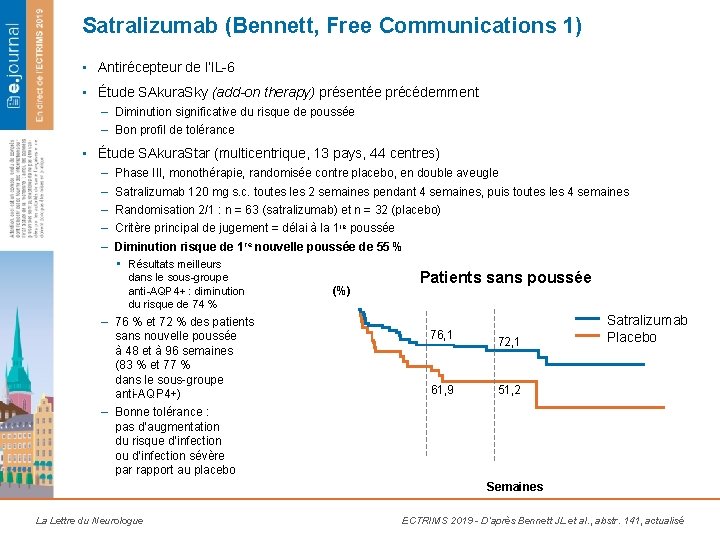
Satralizumab (Bennett, Free Communications 1) • Antirécepteur de l’IL-6 • Étude SAkura. Sky (add-on therapy) présentée précédemment – Diminution significative du risque de poussée – Bon profil de tolérance • Étude SAkura. Star (multicentrique, 13 pays, 44 centres) – – – Phase III, monothérapie, randomisée contre placebo, en double aveugle Satralizumab 120 mg s. c. toutes les 2 semaines pendant 4 semaines, puis toutes les 4 semaines Randomisation 2/1 : n = 63 (satralizumab) et n = 32 (placebo) Critère principal de jugement = délai à la 1 re poussée Diminution risque de 1 re nouvelle poussée de 55 % • Résultats meilleurs dans le sous-groupe anti-AQP 4+ : diminution du risque de 74 % – 76 % et 72 % des patients sans nouvelle poussée à 48 et à 96 semaines (83 % et 77 % dans le sous-groupe anti-AQP 4+) – Bonne tolérance : pas d’augmentation du risque d’infection ou d’infection sévère par rapport au placebo (%) Patients sans poussée 76, 1 61, 9 72, 1 Satralizumab Placebo 51, 2 Semaines La Lettre du Neurologue ECTRIMS 2019 - D’après Bennett JL et al. , abstr. 141, actualisé

Eculizumab (Wingerchuk, Free Communications 1) • Anti-C 5 – C 5 = protéine terminale de la voie du complément • Étude PREVENT (multicentrique, 18 pays, 70 sites) – – – Population uniquement anti-AQP 4+ Phase III, add-on therapy, randomisée contre placebo Eculizumab 900 mg toutes les semaines pendant 4 semaines, puis 1 200 mg toutes les 2 semaines Randomisation 2/1 : n = 96 (eculizumab) et n = 47 (placebo) Résultats déjà présentés précédemment : diminution de 94 % du risque de poussée Présentation ici des données de l’extension en ouvert (n = 119) • Maintien efficacité : estimation de 93, 9 % de patients sans nouvelle poussée à 192 semaines • Pas d’alerte sur la sécurité par rapport aux éléments déjà notés durant la phase contrôlée Patients sans poussées (%) 96, 8 93, 9 Eculizumab Semaines La Lettre du Neurologue ECTRIMS 2019 - D’après Wingerchuk DM et al. , abstr. 142, actualisé
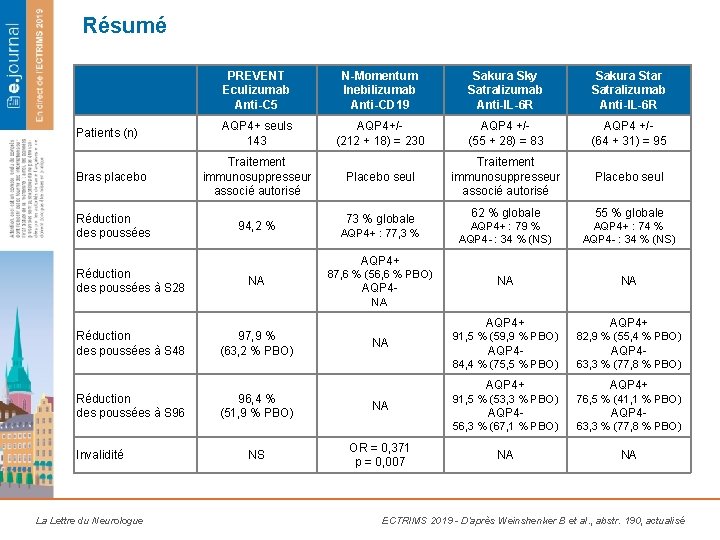
Résumé Patients (n) PREVENT Eculizumab Anti-C 5 N-Momentum Inebilizumab Anti-CD 19 Sakura Sky Satralizumab Anti-IL-6 R Sakura Star Satralizumab Anti-IL-6 R AQP 4+ seuls 143 AQP 4+/(212 + 18) = 230 AQP 4 +/(55 + 28) = 83 AQP 4 +/(64 + 31) = 95 Placebo seul Traitement immunosuppresseur associé autorisé Placebo seul Bras placebo Traitement immunosuppresseur associé autorisé Réduction des poussées 94, 2 % Réduction des poussées à S 28 73 % globale AQP 4+ : 77, 3 % 62 % globale 55 % globale AQP 4+ : 79 % AQP 4 - : 34 % (NS) AQP 4+ : 74 % AQP 4 - : 34 % (NS) NA NA AQP 4+ 91, 5 % (59, 9 % PBO) 82, 9 % (55, 4 % PBO) AQP 4 - 84, 4 % (75, 5 % PBO) 63, 3 % (77, 8 % PBO) AQP 4+ NA 87, 6 % (56, 6 % PBO) AQP 4 NA Réduction des poussées à S 48 Réduction des poussées à S 96 Invalidité La Lettre du Neurologue 97, 9 % (63, 2 % PBO) 96, 4 % (51, 9 % PBO) NS NA NA OR = 0, 371 p = 0, 007 AQP 4+ 91, 5 % (53, 3 % PBO) 76, 5 % (41, 1 % PBO) AQP 4 - 56, 3 % (67, 1 % PBO) 63, 3 % (77, 8 % PBO) NA NA ECTRIMS 2019 - D’après Weinshenker B et al. , abstr. 190, actualisé
- Slides: 5