Traitement de la leucmie mylode chronique LMC par
















- Slides: 27

Traitement de la leucémie myéloïde chronique (LMC) par Cemivil: Etude Tunisienne multicentrique à propos de 215 patients Pr Ag R Ben Lakhal Pour le groupe d’étude Tunisien de la LMC Le congres Maghrébin, Alger 26 -28, Mai 2016

INTRODUCTION �Les inhibiteurs de la tyrosine kinase (ITK): avancée thérapeutique de la LMC �Trois ITK sont disponibles en Tunisie �Depuis janvier 2015: Générique de l’Imatinib Le Cemivil

Les objectifs de notre étude �Evaluer la tolérance et la toxicité du Cemivil chez les patients traités pour une LMC

Patients et Méthodes � 215 patients: 176 patients traités initialement par le Glivec: 2002 -2014 39 patients traités initialement par le Cemivil: 2015 �Etude multicentrique �Etude prospective et observationnelle �Un recueil des données à partir d’une fiche établie en janvier 2015 évaluant la toxicité et la réponse au Cemivil



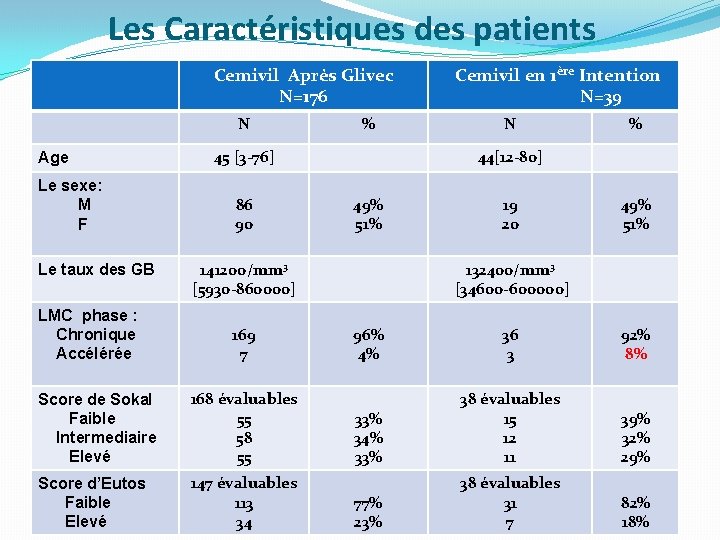
Les Caractéristiques des patients Cemivil Après Glivec N=176 N Age Le sexe: M F Le taux des GB LMC phase : Chronique Accélérée % 45 [3 -76] 86 90 Score de Sokal Faible Intermediaire Elevé 168 évaluables 55 58 55 Score d’Eutos Faible Elevé 147 évaluables 113 34 N % 44[12 -80] 49% 51% 141200/mm 3 [5930 -860000] 169 7 Cemivil en 1ère Intention N=39 19 20 49% 51% 132400/mm 3 [34600 -600000] 96% 4% 36 3 92% 8% 33% 34% 33% 38 évaluables 15 12 11 39% 32% 29% 77% 23% 38 évaluables 31 7 82% 18%

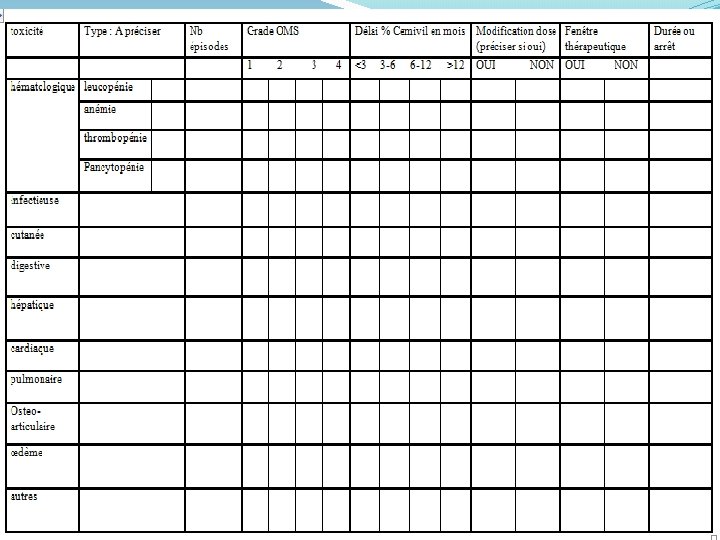
Toxicité au cemivil (22, 4%) �Étudiée chez les 215 patients: Cémivil en première intention: 19 patients parmi les 39: une toxicité au cours de la première année de traitement: 48, 7%. Délai médian: 30 jours[15 -180] Un seul épisode : 74% des cas Grade 3 -4: 6 patients/19 (32%) Une modification des doses chez un seul patient Une fenêtre thérapeutique chez 10 patients: médiane 15 jours [7 -30] Cémivil après Glivec: 29 patients parmi les 176 ont présenté une toxicité: 16%

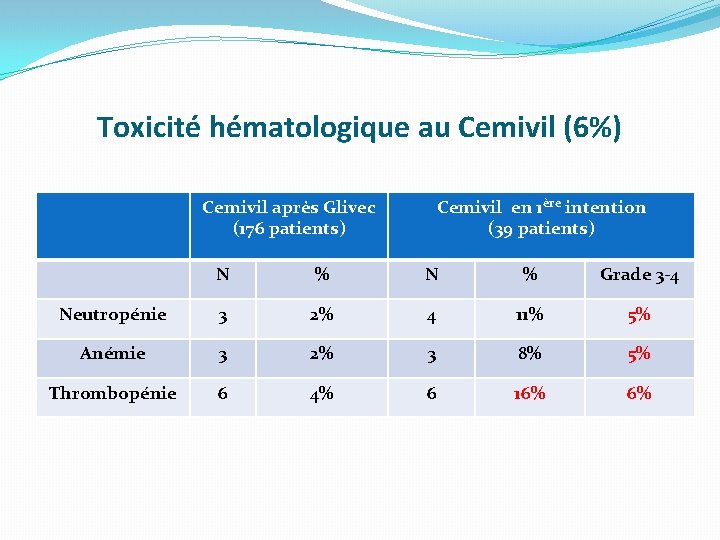
Toxicité hématologique au Cemivil (6%) Cemivil après Glivec (176 patients) Cemivil en 1ère intention (39 patients) N % Grade 3 -4 Neutropénie 3 2% 4 11% 5% Anémie 3 2% 3 8% 5% Thrombopénie 6 4% 6 16% 6%

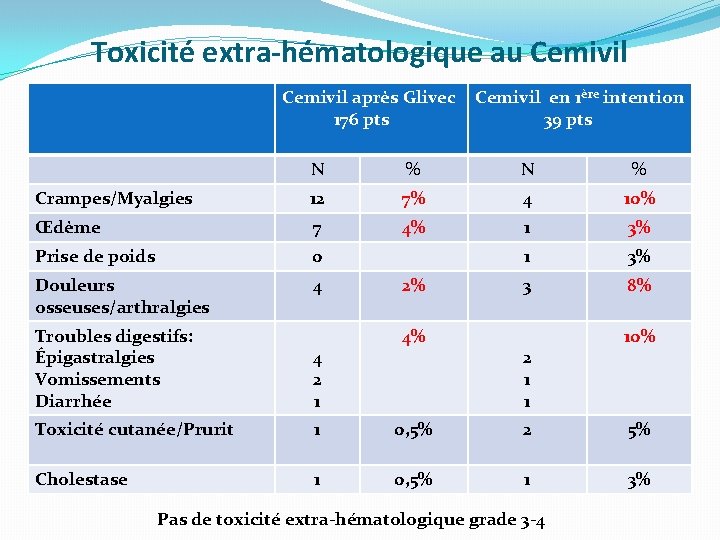
Toxicité extra-hématologique au Cemivil après Glivec Cemivil en 1ère intention 176 pts 39 pts N % Crampes/Myalgies 12 7% 4 10% Œdème 7 4% 1 3% Prise de poids 0 1 3% Douleurs osseuses/arthralgies 4 3 8% 2% Troubles digestifs: Épigastralgies Vomissements Diarrhée 4% 4 2 1 Toxicité cutanée/Prurit 1 0, 5% 2 5% Cholestase 1 0, 5% 1 3% 2 1 1 Pas de toxicité extra-hématologique grade 3 -4 10%

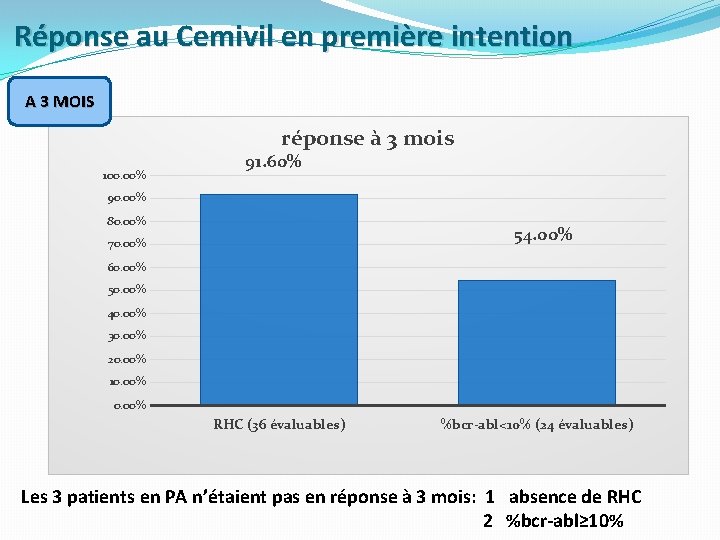
Réponse au Cemivil en première intention A 3 MOIS réponse à 3 mois 100. 00% 91. 60% 90. 00% 80. 00% 54. 00% 70. 00% 60. 00% 50. 00% 40. 00% 30. 00% 20. 00% 10. 00% RHC (36 évaluables) %bcr-abl<10% (24 évaluables) Les 3 patients en PA n’étaient pas en réponse à 3 mois: 1 absence de RHC 2 %bcr-abl≥ 10%

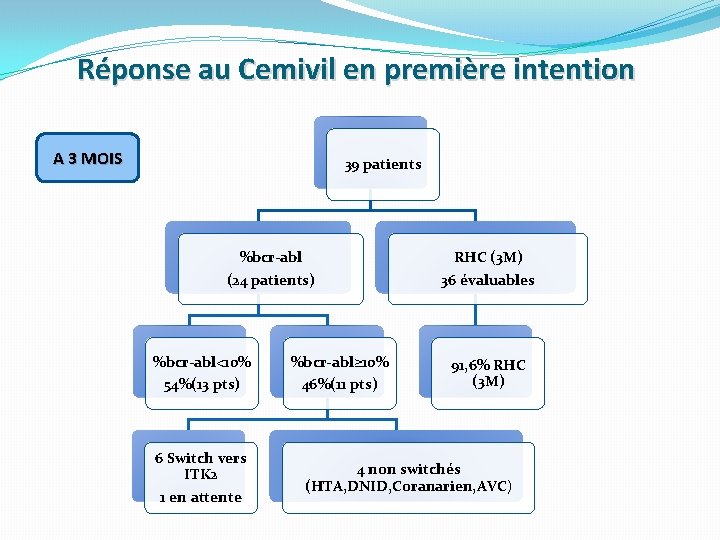
Réponse au Cemivil en première intention A 3 MOIS 39 patients %bcr-abl (24 patients) %bcr-abl<10% %bcr-abl≥ 10% 54%(13 pts) 46%(11 pts) 6 Switch vers ITK 2 1 en attente RHC (3 M) 36 évaluables 91, 6% RHC (3 M) 4 non switchés (HTA, DNID, Coranarien, AVC)

Réponse au Cemivil en première intention A 3 MOIS �Profil des 11 patients avec %bcr-abl≥ 10%: - 2/11 en phase accélérée - Score de SOKAL: 60% RI/HR -Score d’EUTOS: 20%HR - 6 patients parmi les 11 ont présenté au moins un épisode toxique -5 patients ont présenté une toxicité hématologique grade 3 -4 ayant indiqué un arrêt de traitement de 15 jours.

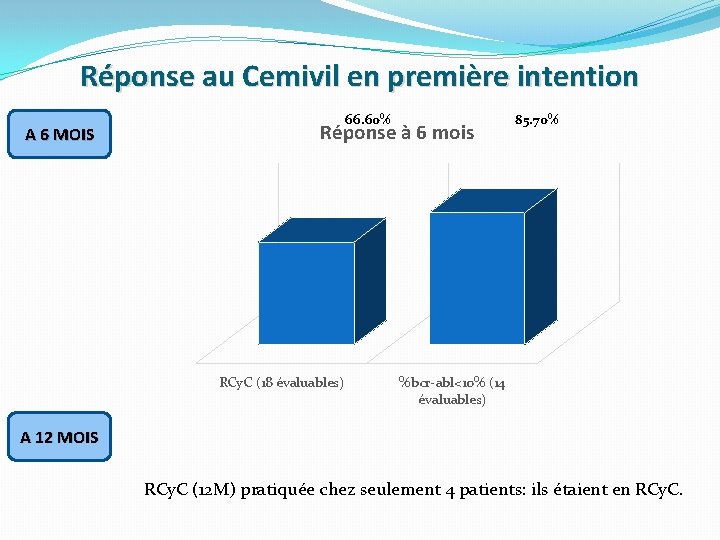
Réponse au Cemivil en première intention A 6 MOIS 66. 60% Réponse à 6 mois RCy. C (18 évaluables) 85. 70% %bcr-abl<10% (14 évaluables) A 12 MOIS RCy. C (12 M) pratiquée chez seulement 4 patients: ils étaient en RCy. C.

Réponse au Cemivil en première intention Nbre de patients évaluables % de réponse Délai médian RCy. C 18 66, 6% 6 mois RMM 13 76, 9% 6 mois

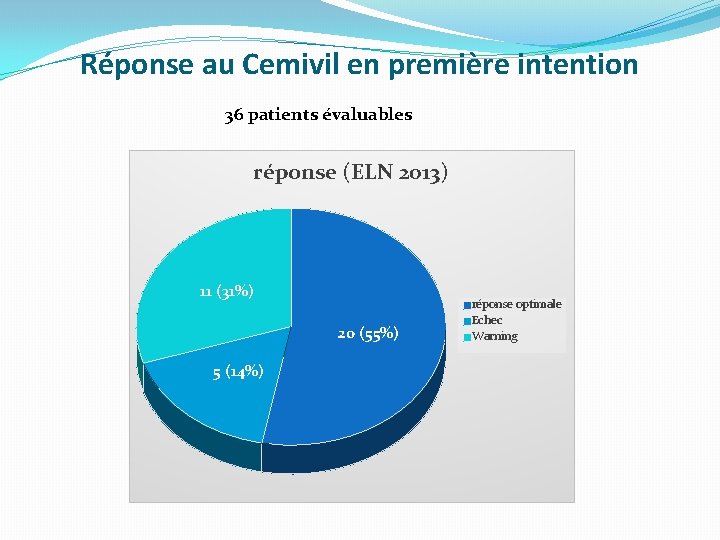
Réponse au Cemivil en première intention 36 patients évaluables réponse (ELN 2013) 11 (31%) 20 (55%) 5 (14%) réponse optimale Echec Warning

Réponse au Cemivil en première intention �Après un recul médian de 8 mois [2 -13], aucun événement n’a été noté; 8 patients ont été « switchés » vers une ITK 2. �Indications: 6 patients: %bcr-abl≥ 10% à 3 M 1 patient: Absence de RCy. C (6 M) 1 patient: Toxicité digestive à type de diarrhée et vomissement. � 2 patients en réponse optimale sous ITK 2 et 6 non encore évaluables

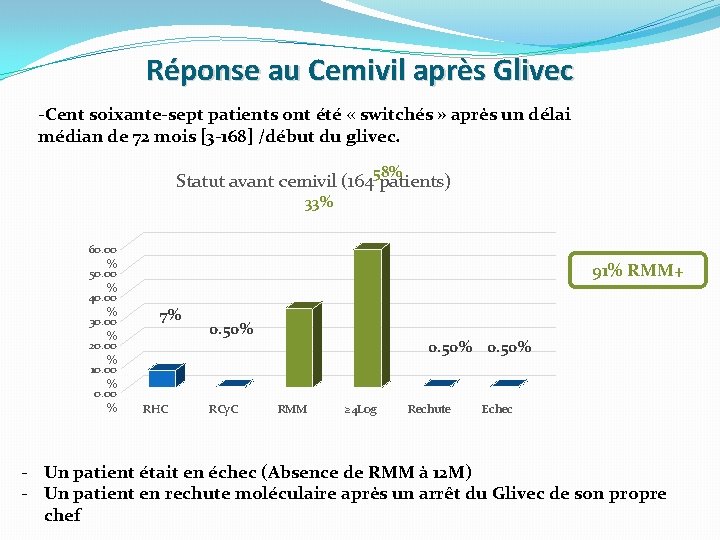
Réponse au Cemivil après Glivec -Cent soixante-sept patients ont été « switchés » après un délai médian de 72 mois [3 -168] /début du glivec. 58% Statut avant cemivil (164 patients) 33% 60. 00 % 50. 00 % 40. 00 % 30. 00 % 20. 00 % 10. 00 % 91% RMM+ 7% RHC 0. 50% RCy. C 0. 50% RMM ≥ 4 Log Rechute Echec - Un patient était en échec (Absence de RMM à 12 M) - Un patient en rechute moléculaire après un arrêt du Glivec de son propre chef

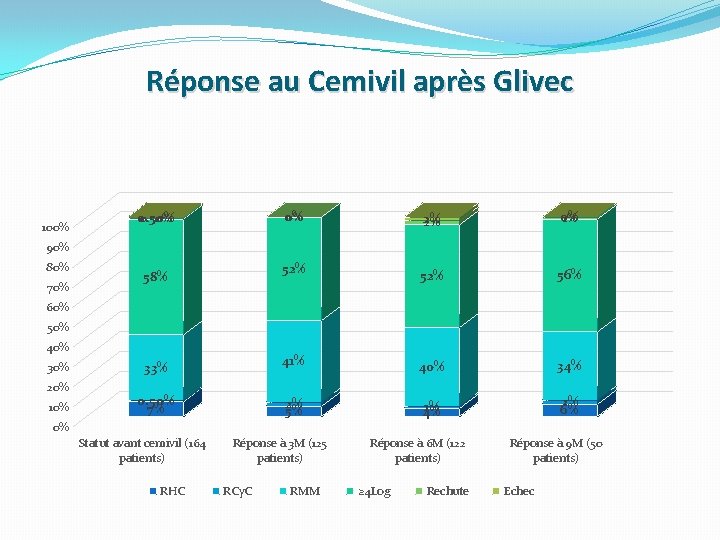
Réponse au Cemivil après Glivec 100% 0% 0% 2% 2% 0% 1% 52% 56% 33% 41% 40% 34% 0. 50% 7% 2% 5% 1% 4% 2% 6% 0. 50% 90% 80% 70% 58% 60% 50% 40% 30% 20% 10% 0% Statut avant cemivil (164 patients) RHC Réponse à 3 M (125 patients) RCy. C RMM Réponse à 6 M (122 patients) ≥ 4 Log Rechute Réponse à 9 M (50 patients) Echec

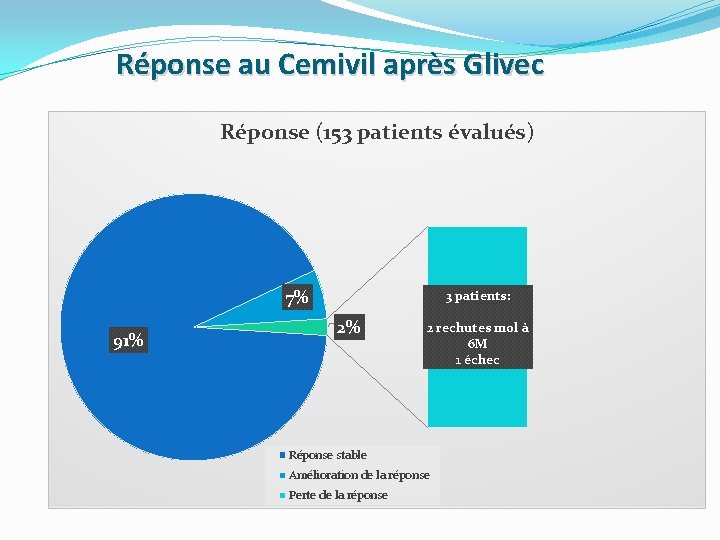
Réponse au Cemivil après Glivec Réponse (153 patients évalués) 7% 91% 3 patients: 2% 2 rechutes mol à 6 M 1 échec Réponse stable Amélioration de la réponse Perte de la réponse

Réponse au Cemivil après Glivec �Le recul médian est de 7 mois �Durant la période de traitement par Cemivil: - Aucun décès ni progression n’ont été notés -Deux évènements (chez 2 patients SOKAL HR/RI): 2 rechutes moléculaires à 6 M sont survenues chez des patients en RMM et en RM 4, 5 avant le début du Cemivil. Ils n’ont pas présenté de toxicité au Cemivil. La durée du traitement par Glivec était respectivement de 9 et 34 mois. - Un patient est resté en échec sous Cémivil.

DISCUSSION � La problématique des génériques: un équilibre Sécurité et efficacité / réduction du cout � Les particularités pour l’Imatinib: Un traitement anti-néoplasique innovant efficace et bien toléré Un traitement au long court: impact sur la qualité de vie Un traitement très couteux : l’utilisation du générique aura un Impact économique important et permettra une utilisation plus large dans le monde

DISCUSSION En Tunisie: Impact économique certain Glivec depuis 2002: un cout 2100 euro/mois (25200/An) Cemivil depuis 2015: 611 euro/mois (7332 euro/An) Pour les 215 pts sous Imatinib: une économie de 3 841 620 (70% de réduction) Aux EU: Une réduction du prix de 70 à 90% Une diminution de 30% des dépenses pharmaceutiques en rapport avec les ITK

DISCUSSION �En Tunisie: Sécurité du Cemivil? Toxicité acceptable et gérable De première intention > après Glivec �En Tunisie: Efficacité du Cemivil? Monitoring non respecté pour les 215 patients 24/39 pts traités de 1ère intention ont eu un BCR/ABL à 3 mois: 13/24( 54%)ont un taux < 10% Monitoring moléculaire tous les 03 mois non respecté chez les 176 pts traités en 2ème intention Uniquement 2 pertes de réponse moléculaire sous Cémivil

DISCUSSION �Quelle stratégie thérapeutique de la LMC en 2016? � Le générique Imatinib ou ITK 2 de première intention? �Stratification pronostique indispensable au diagnostic Imatinib pour les LMC faible risque ITK 2 pour les LMC risque intermédiaire et haut risque

CONCLUSION Le Cemivil en Tunisie: v Impact économique avec une baisse du cout du traitement de 70% v Toxicité surtout la première année du traitement v Efficacité comparable au Glivec Mais absence de recul : évaluation préliminaire

MERCI Le groupe Tunisien d’étude de la LMC R Ben Lakhal H Ghedira H Bellaaj A Laatiri Y Ben Youssef Z Medini Manai A Lakhal S Menif Pr Bechir Zouari