TRABAJO Y ENERGA ENERGA La energa es una

TRABAJO Y ENERGÍA

ENERGÍA La energía es una cualidad de los cuerpos que permite que se puedan producir cambios en ellos mismos y en otros Formas de presentarse la energía: Energía química: la energía de los alimentos y de la gasolina Energía eléctrica: como la suministrada por la batería de un coche Energía de movimiento debida a la velocidad del móvil Energía de posición debida a la altura sobre el suelo en la que se encuentra el móvil Energía luminosa como aquella que radia una bombilla Otras (como la calorífica, eólica, térmica, atómica, . . . ) La energía se presenta en formas diversas y se puede transformar de una en otra La energía se conserva en los cambios, aunque se degrada al pasar de formas más útiles a menos útiles
Energía mecánica Energía cinética Energía potencial

ENERGÍA CINÉTICA Es la energía que posee un cuerpo en virtud de su estado en movimiento Todo cuerpo en movimiento tiene capacidad de realizar un trabajo, el cual se pone de manifiesto cuando el objeto se detiene bruscamente (estrellándose por ejemplo). Dicha energía se invierte en un trabajo de destrozo. Es directamente proporcional al producto de la masa del cuerpo por el cuadrado de su velocidad. La bala tiene mucha energía cinética por salir con velocidad muy elevada El tren tiene mucha energía cinética por tener una gran masa
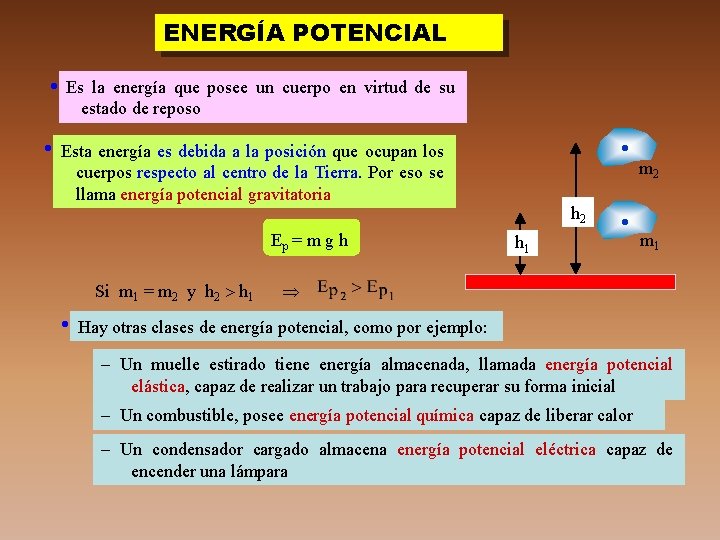
ENERGÍA POTENCIAL Es la energía que posee un cuerpo en virtud de su estado de reposo Esta energía es debida a la posición que ocupan los m 2 cuerpos respecto al centro de la Tierra. Por eso se llama energía potencial gravitatoria Ep = m g h Si m 1 = m 2 y h 2 h 1 h 2 h 1 m 1 Hay otras clases de energía potencial, como por ejemplo: - Un muelle estirado tiene energía almacenada, llamada energía potencial elástica, capaz de realizar un trabajo para recuperar su forma inicial - Un combustible, posee energía potencial química capaz de liberar calor - Un condensador cargado almacena energía potencial eléctrica capaz de encender una lámpara

CALOR Y TEMPERATURA: INTERCAMBIO DEL CALOR COMO FORMA DE TRANSFERENCIA DE ENERGÍA • • Pese a que los cambios que pueden producirse en los sistemas son muy variados, el modo en que los sistemas intercambian energía solo se produce de dos formas: mediante el calor y el trabajo. Mediante el calor. El Intercambio térmico se produce, entre dos sistemas que se encuentren en desequilibrio térmico; esto es a diferente temperatura. Pasa del de mayor temperatura a menor. Dos sistemas a igual temperatura se encuentran en equilibrio térmico. Mediante trabajo. El intercambio mecánico se da cuando las fuerzas actúan sobre los cuerpos y se desplazan, deforman o modifican de algún modo su movimiento. Es el tipo de intercambio energético que se produce en las máquinas: un coche, una grúa, una lavadora. El calor y el trabajo son dos magnitudes físicas. Al ser formas de transferencia de energía, el calor y el trbajo se miden en las mismas unidades que la energía: en julios (j) o kilojulios (. 1 Kj = 1000 j)
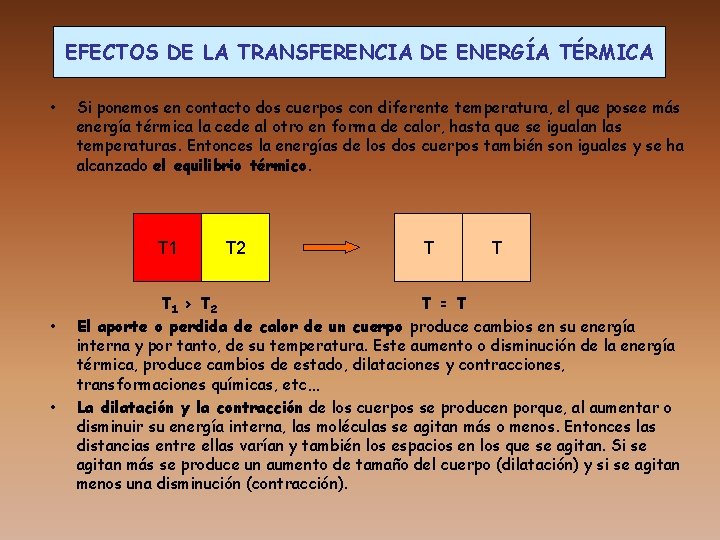
EFECTOS DE LA TRANSFERENCIA DE ENERGÍA TÉRMICA • Si ponemos en contacto dos cuerpos con diferente temperatura, el que posee más energía térmica la cede al otro en forma de calor, hasta que se igualan las temperaturas. Entonces la energías de los dos cuerpos también son iguales y se ha alcanzado el equilibrio térmico. T 1 • • T 2 T T T 1 > T 2 T = T El aporte o perdida de calor de un cuerpo produce cambios en su energía interna y por tanto, de su temperatura. Este aumento o disminución de la energía térmica, produce cambios de estado, dilataciones y contracciones, transformaciones químicas, etc… La dilatación y la contracción de los cuerpos se producen porque, al aumentar o disminuir su energía interna, las moléculas se agitan más o menos. Entonces las distancias entre ellas varían y también los espacios en los que se agitan. Si se agitan más se produce un aumento de tamaño del cuerpo (dilatación) y si se agitan menos una disminución (contracción).

ENERGÍA TÉRMICA Agua fría Agua templada Agua caliente Cuando dos cuerpos a distinta temperatura, se ponen en contacto, al cabo de cierto tiempo se acaban igualando sus temperaturas. Se dice que se ha logrado el equilibrio térmico Se define temperatura como la propiedad común a los cuerpos que se encuentran en equilibrio térmico La temperatura se mide con los termómetros El termómetro alcanza el equilibrio térmico con la muestra y nos indica la temperatura de la misma 8

TERMÓMETROS • Un termómetro es un instrumento que permite medir la temperatura de un sistema. • Una forma usual de construirlo es utilizando una sustancia que tenga un coeficiente de dilatación que permanezca aproximadamente constante, como el mercurio (Hg). • Dicha sustancia se dispone dentro de un tubo de vidrio graduado, de manera que las variaciones de temperatura conllevan una variación de longitud que se visualiza a lo largo de la escala. • Tipos: – MERCURIO – ALCOHOL – ELECTRICO




CALOR, TEMPERATURA Y EQUILIBRIO TÉRMICO Calor y temperatura son conceptos diferente. El calor es energía en movimiento, es decir energía térmica transferida de un sistema que está a mayor temperatura, a otro que está a menor. La temperatura es la magnitud física que mide la cantidad de energía térmica que tiene un cuerpo o un sistema. Las moléculas que forman todos los cuerpos están siempre en movimiento. La temperatura nos informa del grado de agitación de las partículas de un cuerpo y equivale al valor promedio de la energía de todas sus partículas. La unidad de temperatura en el S. I. es el grado Kelvin (K) de la escala absoluta. Pero la escala que se utiliza normalmente es la escala Centígrada, en la que la unidad es el grado centígrado (ºC) es la temperatura de fusión del hielo; y el valor de 100ºC, es la temperatura de ebullición del agua. Equivalencia: entre grados centígrados y grados Kelvin es: 0ºC = 273 K 0 K = - 273º C

Escalas termométricas Escala Celsius (ºC) Establecido por Anders Celsius en 1741 Utiliza dos temperaturas de referencia que se llaman puntos fijos Se divide el intervalo en 100 partes siendo cada una de ellas 1 ºC 100 ºC Hielo fundente (0 ºC) Agua hirviendo (100 ºC) Escala Fahrenheit (ºF) Utilizada en el mundo anglosajón y emplea los mismos puntos fijos que la escala centígrada pero los marca con los números 32 (fusión) y 212 (ebullición), dividiendo el intervalo en 180 partes, siendo cada una, un grado Fahrenheit (1 ºF) Escala Kelvin (ºK) Propuesta por Lord Kelvin en 1854. Es la llamada escala de temperaturas absolutas Sitúa el 0 ºK en la temperatura a la que las moléculas de un cuerpo, no poseen energía cinética (-273, 16 ºC) T (ºK) = T (ºC) + 273, 16

EL CONCEPTO DE TEMPERATURA T 1 T 2 > T 1 Las partículas del gas son muy pequeñas comparadas con la distancia que las separa Las partículas están en continuo movimiento, chocando entre sí y contra las paredes Se mueven en todas direcciones, con velocidades distintas en módulo El número de partículas cuya velocidad tiene el mismo módulo, presenta un máximo para cada temperatura, el cual crece con la temperatura del gas La teoría cinética explica la presión del gas como consecuencia de los choques, así como la temperatura, que es directamente proporcional a la energía cinética media de translación por partícula / k es la cte de Boltzmann cuyo valor es k = 1, 38 10 -23 J/molécula

PROPAGACION DEL CALOR • • • El calor se propaga por conducción, por convección y por radiación. La conducción del calor se produce preferentemente cuando la energía se transmite a través de cuerpos sólidos. Por ejemplo, al calentar el extremo de una varilla metálica, las partículas se agitan mas y transmiten esas vibraciones a las partículas que tienen a su lado, y la temperatura va aumentando hacia el otro extremo. Unas sustancias conducen el calor mejor que otras, esto permite clasificarlas en conductoras y aislantes del calor. Por ejemplo, los metales son muy buenos conductores del calor, sin embargo la madera, el plástico o el aire no son buenos conductores, son aislantes. La convección del calor se produce en los líquidos y en los gases porque sus moléculas se mueven con cierta libertad. La zona que se calienta, se dilata y al adquirir menor densidad asciende. Su lugar es ocupado por las partículas de las zonas mas frías. Así se producen unas corrientes de gas o de líquido que ascienden y otras bajan, son las corrientes de convección, importantes para explicar los fenómenos atmosféricos, como calienta la calefacción el interior de una vivienda, las corrientes marinas, como se calienta en la cocina el líquido de un recipiente, etc… La radiación del calor la producen todos los cuerpos por el hecho de tener temperatura, y es mayor cuanto mas temperatura tiene el cuerpo. El calor se propaga igual que la luz, las ondas de radio y de TV, las microondas, etc. , se puede propagar incluso por el vacío, como ocurre en el Universo, con el calor que irradian las estrellas.

TEMPERATURA : Es la manifestación externa del estado de movimiento de las partículas de un cuerpo. Nos informa sobre la energía interna de dicho cuerpo. Q T 1 T 2 El sistema se encuentra a temperatura T 1 El sistema recibe una cantidad de calor Q La temperatura final del sistema es T 2 > T 1 Cantidad de calor es la energía que intercambian dos sistemas a distinta temperatura hasta alcanzar el equilibrio térmico La cantidad de calor Q aportada al sistema es Q = C (T 2 - T 1) La constante de proporcionalidad es la capacidad calorífica del cuerpo (J/grado) El calor específico de la sustancia es la capacidad calorífica por unidad de masa: Se mide en J/kg. K, o bien J/kg. ºC En consecuencia diremos que: Q = m ce (T 2 - T 1)
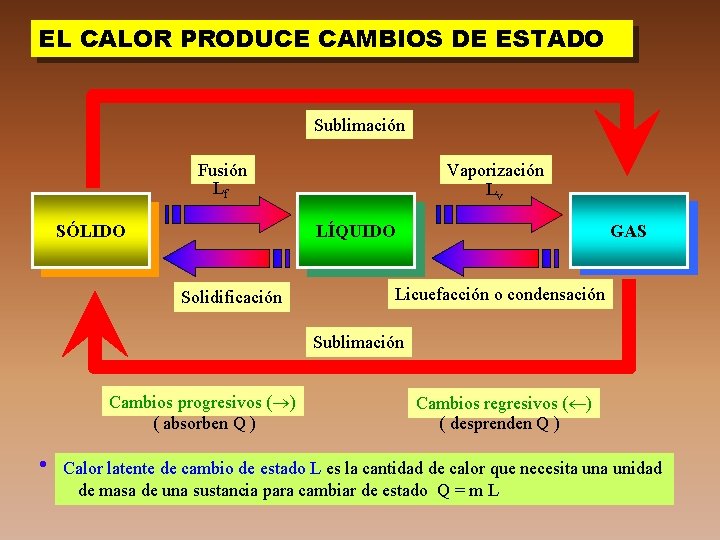
EL CALOR PRODUCE CAMBIOS DE ESTADO Sublimación Fusión Lf SÓLIDO Vaporización Lv LÍQUIDO Solidificación GAS Licuefacción o condensación Sublimación Cambios progresivos ( ) ( absorben Q ) Cambios regresivos ( ) ( desprenden Q ) Calor latente de cambio de estado L es la cantidad de calor que necesita unidad de masa de una sustancia para cambiar de estado Q = m L
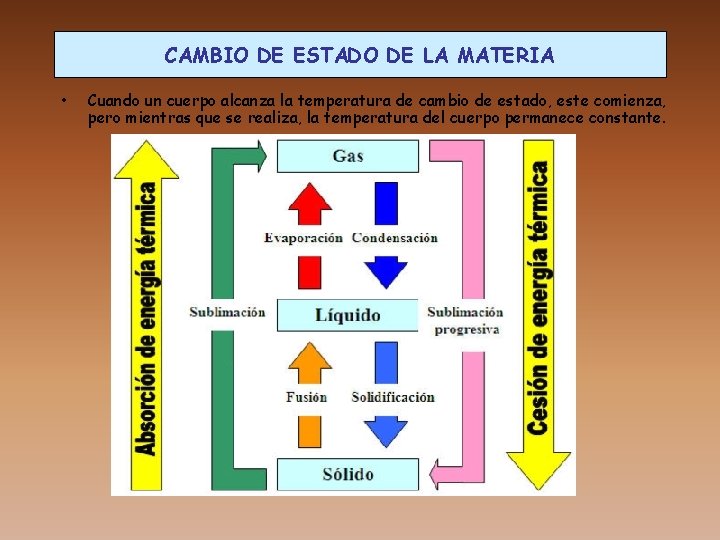
CAMBIO DE ESTADO DE LA MATERIA • Cuando un cuerpo alcanza la temperatura de cambio de estado, este comienza, pero mientras que se realiza, la temperatura del cuerpo permanece constante.
- Slides: 19