TOXIKUS FMEK KRNYEZETKMIA S TECHNOLGIA Vegyszmrnk B Sc

TOXIKUS FÉMEK KÖRNYEZETKÉMIA ÉS TECHNOLÓGIA Vegyészmérnök B. Sc. hallgatók részére KÖRNYEZETI KÉMIA Környezetmérnök B. Sc. hallgatók részére Biomérnök M. Sc. hallgatók részére HAGYOMÁNYOS ÉS MEGÚJULÓ ENERGIAFORRÁSOK KÖRNYEZETI HATÁSAI Műszaki menedzser B. Sc. hallgatók részére Dr. Bajnóczy Gábor egyetemi docens Kémiai és Környezeti Folyamatmérnöki Tanszék Vegyész- és Biomérnöki Kar Budapesti Műszaki Egyetem 2012

AZ ELŐADÁS ANYAGA, KÉPEK, RAJZOK KIZÁRÓLAG OKTATÁSI CÉLRA, KORLÁTOZOTT HOZZÁFÉRÉSSEL HASZNÁLHATÓK ! INTERNETRE KORLÁTLAN HOZZÁFÉRÉSSEL FELTENNI TILOS !

Toxikus fémek bekerülése a környezetünkbe Az egyes környezeti elemekbe az emberi tevékenységtől függetlenül is nem toxikus és toxikus fémek kerülnek be és távoznak. Jelentős különbség: eltérően a többi környezet károsító anyagoktól a fémek nem bomlanak le. Veszély helyzet: emberi emisszió >> természetes emisszió Elem vegyjele Emberi és természetes emisszió aránya As 28 Cd 19 Cr 1, 6 Co 0, 6 Cu 14 Pb 340 Hg 275 Ni 2, 5

Toxikus fémek Bizonyos élő szervezetekre megadható toxicitási sorrend Nieboer és Ricardson 1980 Élő szervezet Fémek ionjainak toxicitási sorrendje Algák Hg > Cu > Cd > Fe > Cr > Zn > Ni > Co > Mn Gombák Halak Patkány, nyúl Ag > Hg > Cu > Cd > Cr > Ni > Pb > Co > Zn > Fe > Ca Ag > Hg > Cu > Pb > Cd > Au > Al > Zn > Ni > Cr > Co > Mn Ag, Hg, Tl, Cd > Cu, Pb, Co, Sn, Mn, Zn, Ni, Fe, Cr > Al

ÉRCBÁNYÁSZAT → kitermelésből

ÉRCBÁNYÁSZAT → melléktermékek tárolása Vörösiszap katasztrófa

Azért másutt is történt ilyen Szénsalak tározó átszakadása (USA)

Hulladék égetés Elektronikai ipar Hg Ag Au Széntüzelésű erőművek Hg Hg Pb Cd As Ni
Higany - elektronikai ipar energiatakarékos világító testek (5 mg Hg) (beltérben max 35μg Hg /m 3) elemek, akkumulátorok cinnabarit (Hg. S) - klór-alkáli ipar - csávázó szer fenil-higany acetát a 70 -es évek végéig minden csávázott vetőmag piros színű !!!

Higany előfordulása a természetben Elemi állapotban: gőz formában Vegyületként: metil-higany CH 3 Hg+ vízoldható ! dimetil-higany (CH 3)2 Hg gőz higany-szulfid (Hg. S) Az elemi higany bakteriális úton (metilezés) vízoldható metil-higannyá (felhalmozódás veszély) és gőz halmazállapotú dimetil-higannyá alakítható. A dimetil-higany napsütés hatására elemi higannyá bomlik.
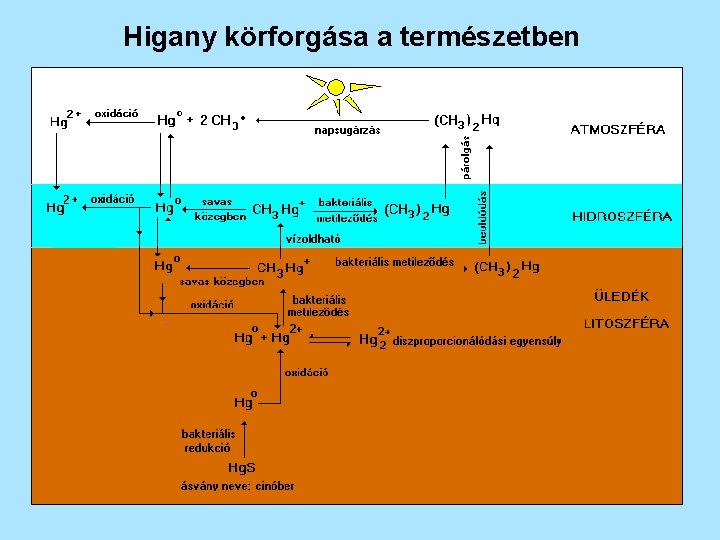
Higany körforgása a természetben
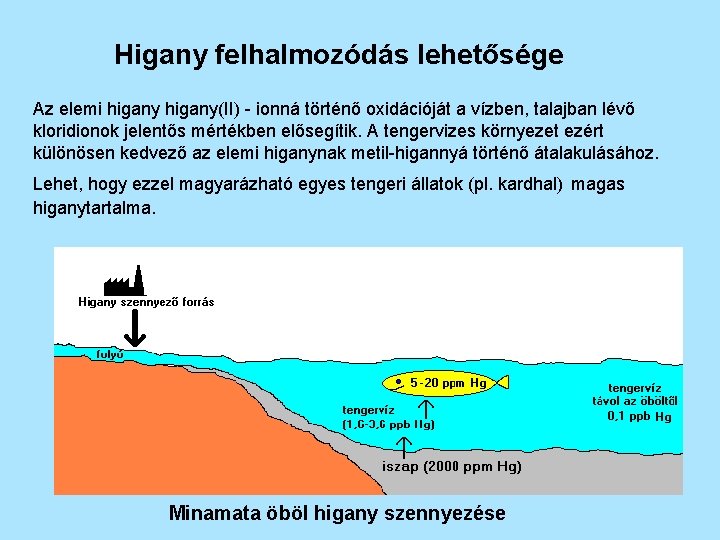
Higany felhalmozódás lehetősége Az elemi higany(II) - ionná történő oxidációját a vízben, talajban lévő kloridionok jelentős mértékben elősegítik. A tengervizes környezet ezért különösen kedvező az elemi higanynak metil-higannyá történő átalakulásához. Lehet, hogy ezzel magyarázható egyes tengeri állatok (pl. kardhal) magas higanytartalma. Minamata öböl higany szennyezése

Higany kibocsátás korlátozása (hulladékégetők, ritkán széntüzelésű erőművek) Füstgázban 90% higany Higanytartalmú hulladék ÉGETŐ Salakban 10% higany A füstgáz higanytartalma : 1. elemi higany gőz (a higany forráspontja: 357 °C ), 2. higany(II)-klorid (az elemi higany sósav és klór jelenlétében 300 -400 o. C-on higany(II)-kloriddá oxidálódik), Hg + 4 HCl + O 2 = 2 Hg. Cl 2 + 2 H 2 O Hg + Cl 2 = Hg. Cl 2 A higany(II)-klorid könnyen szublimál, így gőz halmazállapotban lesz jelen. 3. részecskéhez kötött higany.
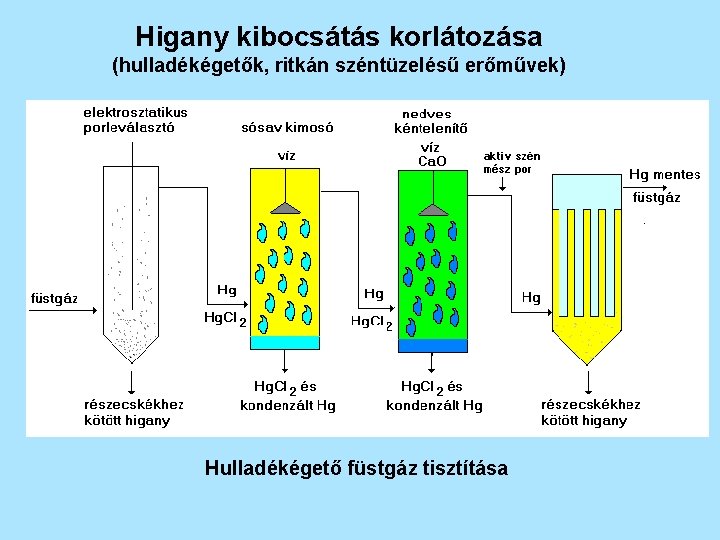
Higany kibocsátás korlátozása (hulladékégetők, ritkán széntüzelésű erőművek) Hulladékégető füstgáz tisztítása

Ólom A környezetünket az ólom szennyezi legrégebben, mivel a rómaiak egy főre jutó éves ólomfelhasználása kb. 4 kg, közelítőleg megegyezik a fejlett ipari államok felhasználásával. Ismeretek hiányából adódó felhasználások: - ólomcukor (ólom-acetát) édesítőszer - ólomfehér (ólom-szulfát) szobafesték - mínium (vörös ólom-oxid) korrózióvédő festék - ólomtartalmú nyomdafesték - ólommázas edények - oktánszám növelő (ólom-tetrametil) repülőgép motoroknál maradt Jelenlegi felhasználások: - ólom akkumulátorok (a teljes felhasználás 80 %-ka) - lőszer gyártás - forraszanyag gyártás - sugárvédelmi eszközök

Ólom egészségkárosító hatása Szervetlen ólomvegyületek bejutása: emésztő rendszeren keresztül Szerves ólomvegyületek bejutása: légző rendszeren keresztül A higany biológiai felezési ideje az emberi testben kb. 70 nap addig az ólomé 2 -3 év. Az ólommérgezés tünete: vérszegénység, agy működés károsodás Lerakódás a csontokban, lázas állapot esetén gyors mobilizálódás Az ólom bakteriális metilezhetősége nem bizonyított.
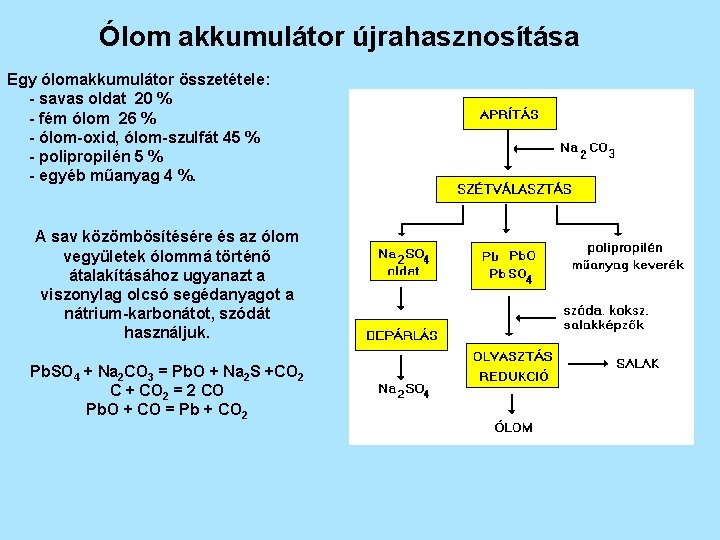
Ólom akkumulátor újrahasznosítása Egy ólomakkumulátor összetétele: - savas oldat 20 % - fém ólom 26 % - ólom-oxid, ólom-szulfát 45 % - polipropilén 5 % - egyéb műanyag 4 %. A sav közömbösítésére és az ólom vegyületek ólommá történő átalakításához ugyanazt a viszonylag olcsó segédanyagot a nátrium-karbonátot, szódát használjuk. Pb. SO 4 + Na 2 CO 3 = Pb. O + Na 2 S +CO 2 C + CO 2 = 2 CO Pb. O + CO = Pb + CO 2

Kadmium Önálló előfordulása rendkívül ritka, cink kohászat melléktermékeként állítják elő Nagyon hasonló a cinkhez, helyettesíteni tudja az élő szervezetben. Növények toxikus fémeket nem szívják fel, kivéve a kadmiumot a cinkhez való hasonlósága miatt (különösen savas talajoknál). A növények kadmium tartalma a foszfáttartalmú műtrágyázásból származik. A foszfát műtrágyák kadmium tartalma elérheti a 170 mg/kg-ot Észak-Afrikai apatit: sok kadmium tartalom, Kóla félszigeti apatit: kevés kadmium Biomassza égetés → hamu → nem használható talajerő utánpótlásra a Cd tartalom miatt Hasonló a helyzet a lakossági szennyvíz iszapnál a foszfáttartalmú vízlágyítók miatt.
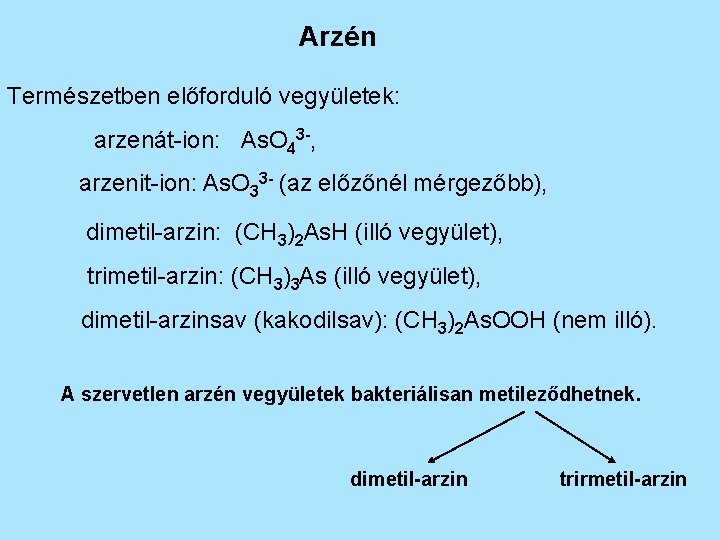
Arzén Természetben előforduló vegyületek: arzenát-ion: As. O 43 -, arzenit-ion: As. O 33 - (az előzőnél mérgezőbb), dimetil-arzin: (CH 3)2 As. H (illó vegyület), trimetil-arzin: (CH 3)3 As (illó vegyület), dimetil-arzinsav (kakodilsav): (CH 3)2 As. OOH (nem illó). A szervetlen arzén vegyületek bakteriálisan metileződhetnek. dimetil-arzin trirmetil-arzin
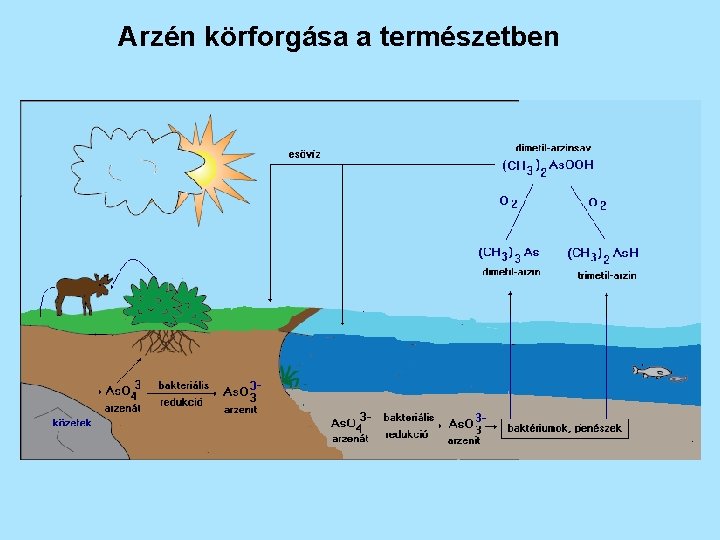
Arzén körforgása a természetben

Arzén szennyezés veszélye A legtöbb légköri emisszió a réz kohászatból és a széntüzelés pernyéjéből származik. A talajba kerülő arzén legnagyobb problémája, hogy az arzenát-ion As. O 43 szerkezetileg megfelel a foszfát-ionnak PO 43 -, így beépülése a növényekbe, egyéb élőlényekbe különösebb nehézség nélkül végbe megy. A beépült arzén mennyiségtől függő toxikus hatást fejt ki. Legnagyobb gond az arzéntartalmú ivóvíz. nem környezet szennyezés, hanem kőzet beoldódás eredménye
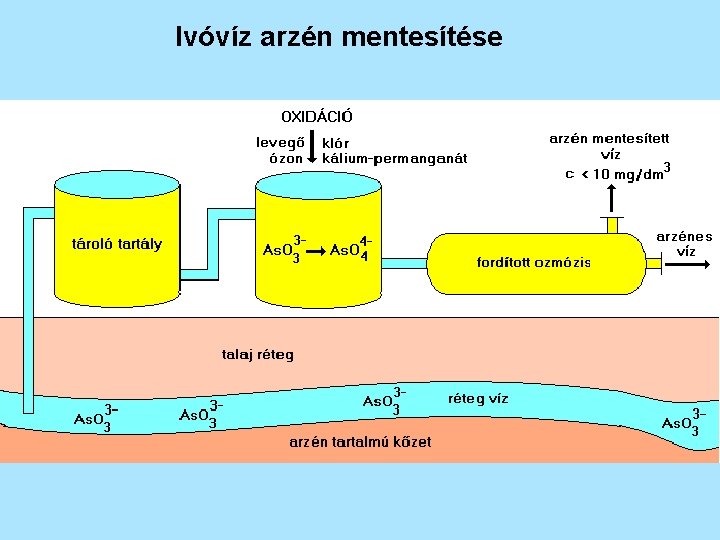
Ivóvíz arzén mentesítése
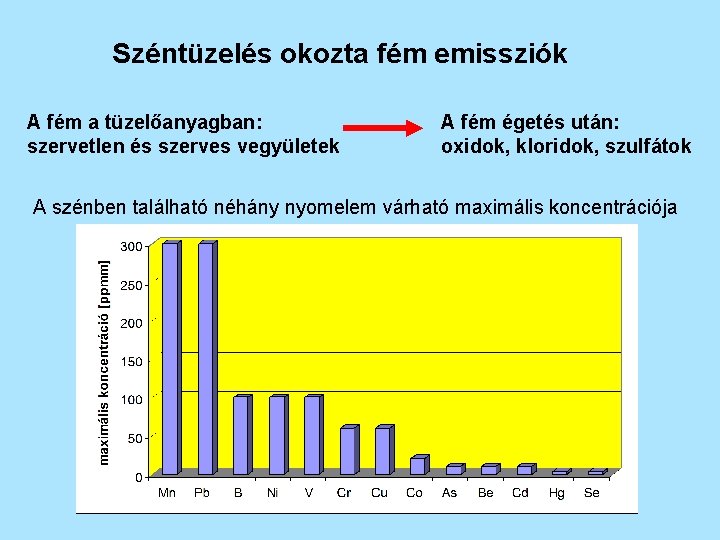
Széntüzelés okozta fém emissziók A fém a tüzelőanyagban: szervetlen és szerves vegyületek A fém égetés után: oxidok, kloridok, szulfátok A szénben található néhány nyomelem várható maximális koncentrációja
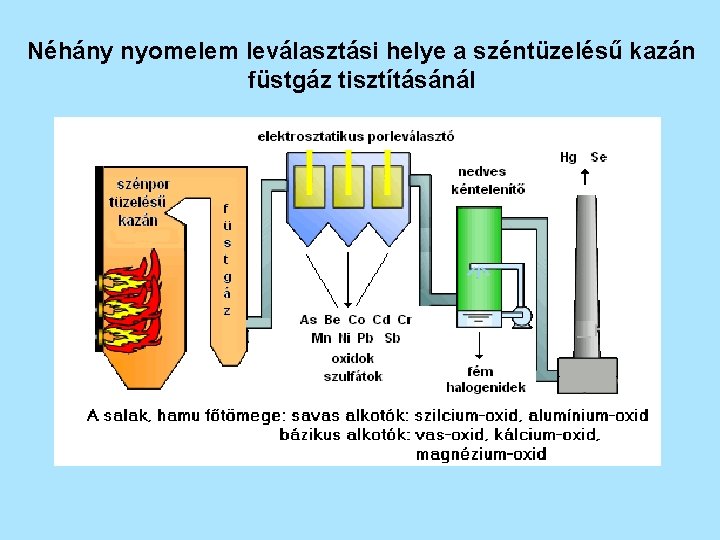
Néhány nyomelem leválasztási helye a széntüzelésű kazán füstgáz tisztításánál

Szénsalakból történő kioldódás As. O 43 - As. O 33 - A jelentős kalcium-oxid tartalom miatt az áthaladó esővíz lúgos lesz, így a toxikus fémek közül elsősorban az arzenátok kioldódására lehet számítani.

Hulladék égetés és fém emisszió Hasonló a helyzet, mint a széntüzelésnél csak egyes fémek kiugróan nagy koncentrációban jelentkezhetnek. - Műanyagokban (színező anyagok, katalizátor maradványok) Cr, Pb, Sb, Cd, As - A PVC-ben lévő klórtartalom növeli a füstgáz illó fém-klorid tartalmát. - Gomb akkumulátorok: Ni, Hg A hulladék égetés salakja lakossági hulladéklerakóba kerülhet takaró földként. A toxikus fémek kimosódása a csurgalék víz kezelésével valósul meg.

Szénszűrős tálcás adszorber Alkalmas: higany, szénhidrogének, szagok megkötésére, ha nincs más megoldás Hátrány: drága, vízgőzt is megköti, ketonok adszorpciójakor begyullad !!!!

Bányavíz okozta környezetszennyezés Minden olyan bányában, ahol szulfidos ércek fordulnak elő. A meleg, levegővel érintkező, nedves bányafalon a kénbaktériumok az oldhatatlan fém szulfidokat vízoldható szulfátokká oxidálhatják. A szén kísérő ásványa a pirit: 2 Fe. S 2 + 7 O 2 + 2 H 2 O kénbaktérium 4 SO 42 - + 2 Fe 2+ + 4 H+ Szénbányászatnál a kiszivattyúzott bányavíz savas. O 2 Fe. SO 4 Fe 2(SO 4)3 + 6 H 2 O = 2 Fe(OH)3 + 3 H 2 SO 4 A bauxit bányából szivattyúzott víz jó minőségű is lehet (nincs jelen szulfidos érc)

Bányavíz okozta környezetszennyezés Acid mine drainage, as experienced in Mpumalanga, causes serious environmental and health implications Radio active acid mine drainage mine sludge pours into the Crocodile Limpopo River in June 2010. pic censorbugbear

Bányavíz okozta környezetszennyezés Gyöngyösoroszi elhagyott tárnából kifolyó savas bányavíz.
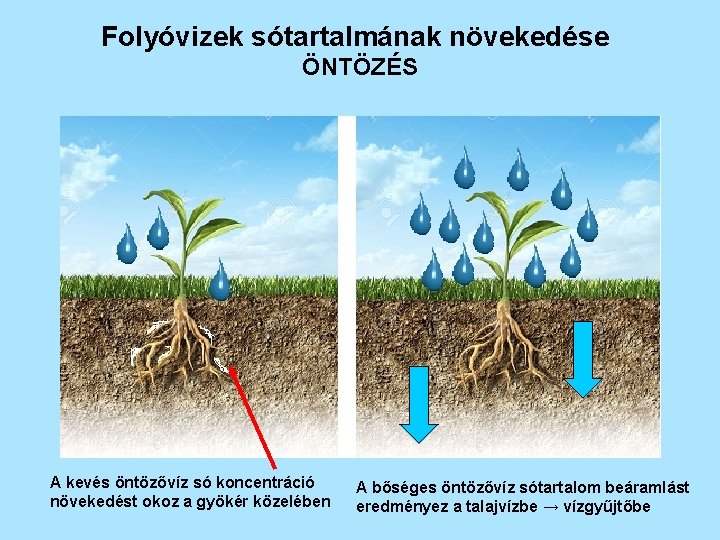
Folyóvizek sótartalmának növekedése ÖNTÖZÉS A kevés öntözővíz só koncentráció növekedést okoz a gyökér közelében A bőséges öntözővíz sótartalom beáramlást eredményez a talajvízbe → vízgyűjtőbe
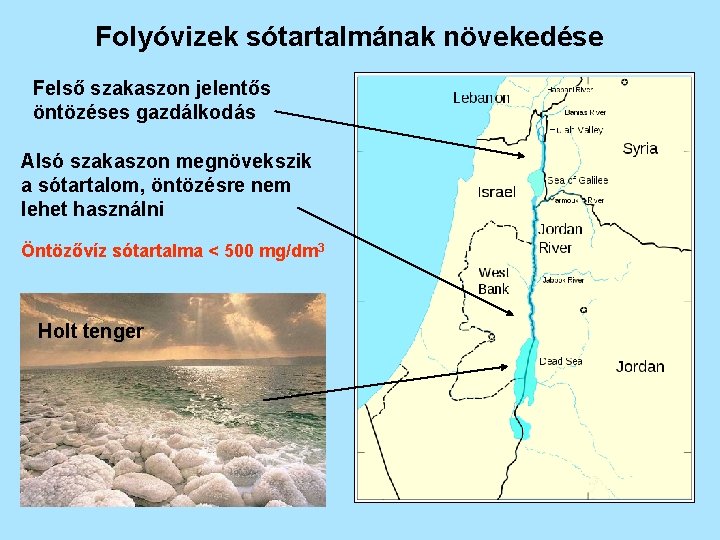
Folyóvizek sótartalmának növekedése Felső szakaszon jelentős öntözéses gazdálkodás Alsó szakaszon megnövekszik a sótartalom, öntözésre nem lehet használni Öntözővíz sótartalma < 500 mg/dm 3 Holt tenger
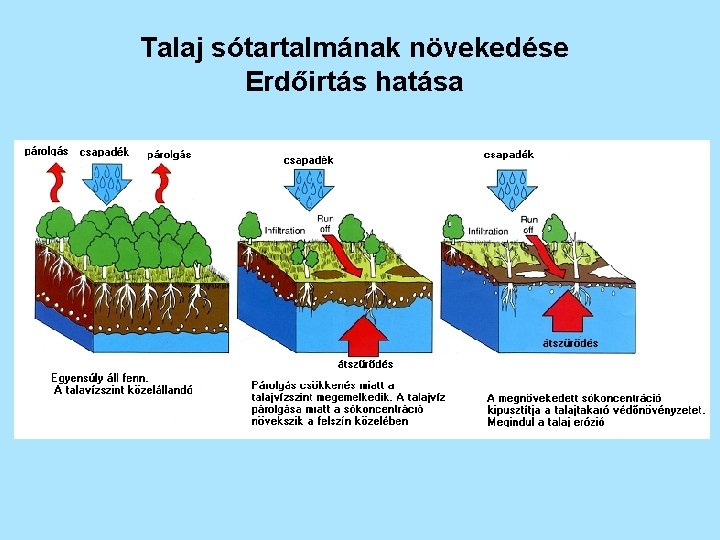
Talaj sótartalmának növekedése Erdőirtás hatása

Síkosság mentesítés A fagyáspont csökkenés függ a vízben oldható részecske számtól, de korrózió veszély az ionokra történő disszociációkor. A klorid ion különösen korrózió veszélyes. Nátrium-klorid: Na. Cl → Na+ + Cl- 1 mól nátrium-kloridból 2 mól ion, korrózió veszély, káros a növényekre, tönkreteszi az áteresztő képességet, de a legolcsóbb. Kálium-klorid: KCl → K+ + Cl- 1 mól kálium-kloridból 2 mól ion, korrózió veszély, hasznos a növényeknek, (műtrágya), drágább, mint a nátrium-klorid Kalcium-klorid: Ca. Cl 2 → Ca++ + 2 Cl- 1 mól kalcium-kloridból 3 mól ion, korrózió veszély, növények jobban tűrik, drágább az előző kettőnél Magnézium-klorid: Mg. Cl 2 → Mg++ + 2 Cl- 1 mól magnézium-kloridból 3 mól ion, korrózió veszély, nem káros a növényekre, jóval drágább az előző háromnál A klorid lecserélhető acetátra → kisebb korrózió veszély!

Síkosság mentesítés Karbamid: Karbamid → nem disszociál 1 mól karbamidból 1 mól oldott részecske, nincs korrózió veszély, nem káros a növényekre (műtrágya), drága Glikolok: etilén-, propilén-glikol Glikolok→ nem disszociál 1 mól glikolból 1 mól oldott részecske, nincs korrózió veszély, drága, repülőgépeknél ezt használják Érdesítők: homok, zeolit Városban problémás lehet, mivel a kiszórt szilárd anyag végül a csatornában köthet ki. Leülepedve szűkíti az átáramlási keresztmetszetet.

Elhasznált termálvizek Termálvíz: 30 o. C-nál melegebb felszín alatti víz Gyógyvíz: amelyet valamilyen szempontból gyógyhatásúnak minősítenek, nem feltétlenül meleg, de ásványvíz. Ásványvíz: az oldott összes szilárd ásványianyag-tartalma 500 -1000 mg/l között van, és tartalmazza az alább felsorolt aktív biológiai anyagok valamelyikét: Lítium-ion legalább 5 mg/l, Szulfid-ion vagy titrálható kén legalább 1 mg/l, Metakovasav legalább 50 mg/l, Nátrium-ion kevesebb 200 mg/l-nél, Magnézium-ion legalább 20 mg/l, Kalcium-ion legalább 60 mg/l, Bromid-ion legalább 5 mg/l, Jodid-ion legalább 1 mg/l, Fluorid-ion 0, 8 -1, 2 mg/l, Radonaktivitás legalább 37 Bq/l, Szabad szén-dioxid legalább 1000 mg/l ivóvíz: 500 mg/dm 3 ásványi anyagtartalom alatt
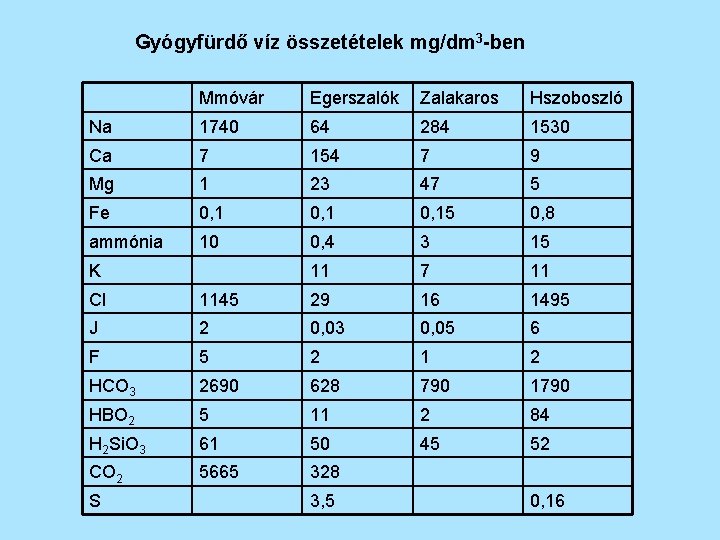
Gyógyfürdő víz összetételek mg/dm 3 -ben Mmóvár Egerszalók Zalakaros Hszoboszló Na 1740 64 284 1530 Ca 7 154 7 9 Mg 1 23 47 5 Fe 0, 15 0, 8 ammónia 10 0, 4 3 15 11 7 11 K Cl 1145 29 16 1495 J 2 0, 03 0, 05 6 F 5 2 1 2 HCO 3 2690 628 790 1790 HBO 2 5 11 2 84 H 2 Si. O 3 61 50 45 52 CO 2 5665 328 S 3, 5 0, 16

Elhasznált termálvizek Az elhasznált termálvizek a csak a hőtartalom hasznosítása céljából felszínre hozott vizekkel ellentétben nem sajtolhatók vissza, így növelik a befogadó vízfolyások sótartalmát. Közcsatornába: 1. 5 -3. 0 g/dm 3 Felszíni vízfolyásba: 1. 0 – 2 g/dm 3 sótartalom, területi kategóriától függően Nátrium egyenérték % < 45 Na eé Nátrium egyenérték % = –––––––––––––––––– Na eé + K eé + Ca eé + Mg eé Na eé: Na mg/dm 3 / 23 K eé: K mg/dm 3 / 39, 1 Ca eé: Ca mg/dm 3 / 20 Mg eé: Mg mg/dm 3 / 12 Lehetséges megoldás: puffer tározó építése, szakaszos leengedés nagy vízhozamnál.

Hőszennyezés Elhasznált termálvizek közvetlen beengedése vízfolyásokba. Geotermikus energiahasznosítás üzemzavara. Felszíni vízfolyások használata hűtővízként (pl. : atomerőmű, fosszilis erőművek) Hatás: szerves anyag termelés növekedése, oxigén koncentráció csökkenése, anaerob folyamatok gyorsulása, ammónium ion koncentráció növekedése, vízi ökoszisztéma változása. Védekezés: felszíni vízfolyásokba csak 40 °C-nál kisebb hőmérsékleten, hűtőtavak és vésztározók kiépítése.
- Slides: 39