TOXICIDAD NIVOLUMAB EXPERIENCIA H U DONOSTIA M ngeles

TOXICIDAD NIVOLUMAB: EXPERIENCIA H. U. DONOSTIA Mª Ángeles Díaz Gallego 1; Jenifer Gómez Mediavilla 2; María Otaño Ariño 1; Ana Landa Magdalena 1; Beatriz Sánchez Casi 1; Cristina Sarasqueta 4, María Aranzazu Bujedo Martínez 1; Ibone De Elejoste Echebarria 1; Naiara Sagastibeltza Mariñelarena 1; Alfredo Paredes Lario 1; Garbiñe Lizeaga Cundin 3, Mª del Coro Andueza Granados 3, Laura Basterrechea Badiola 1. 1 Médico del departamento de Oncología Médica del H. U. Donostia. 2 Médico del departamento de Oncología Médica del I. Onkologikoa (Donostia). 3 Farmacéutico del departamento de Farmacia Hospitalaria del H. U. Donostia. 4 Instituto Biodonostia. #SEOM 2018

INTRODUCCIÓN Y OBJETIVOS INTRODUCCIÓN: q. Nivolumab: anticuerpo monoclonal humano de tipo Ig G 4 q. Mecanismo de acción q. Espectro particular de toxicidad (mediada inmunológicamente) y afectación a múltiples órganos. OBJETIVO: q. Experiencia del H. U. Donostia de las reacciones adversas producidas por el uso de Nivolumab para el tratamiento de tumores sólidos. #SEOM 2018

MATERIALES Y MÉTODOS q. Base de datos anonimizada de los pacientes tratados con Nivolumab (Datos obtenidos desde la Farmacia Hospitalaria). q. Análisis retrospectivo. q. N= 101 pacientes. q 1 de Junio de 2015 al 30 de Abril de 2017. q. Los datos se recogen en el programa informático Access 2007 -2010 y el programa estadístico elegido para el análisis es el SPSS versión 23. #SEOM 2018
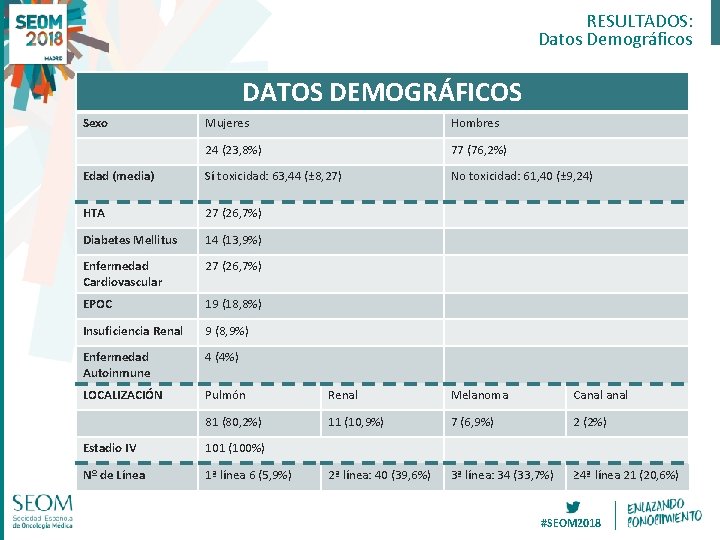
RESULTADOS: Datos Demográficos DATOS DEMOGRÁFICOS Sexo Mujeres Hombres 24 (23, 8%) 77 (76, 2%) Edad (media) Sí toxicidad: 63, 44 (± 8, 27) No toxicidad: 61, 40 (± 9, 24) HTA 27 (26, 7%) Diabetes Mellitus 14 (13, 9%) Enfermedad Cardiovascular 27 (26, 7%) EPOC 19 (18, 8%) Insuficiencia Renal 9 (8, 9%) Enfermedad Autoinmune 4 (4%) LOCALIZACIÓN Pulmón Renal Melanoma Canal 81 (80, 2%) 11 (10, 9%) 7 (6, 9%) 2 (2%) 2ª línea: 40 (39, 6%) 3ª línea: 34 (33, 7%) ≥ 4ª línea 21 (20, 6%) Estadio IV 101 (100%) Nº de Línea 1ª línea 6 (5, 9%) #SEOM 2018
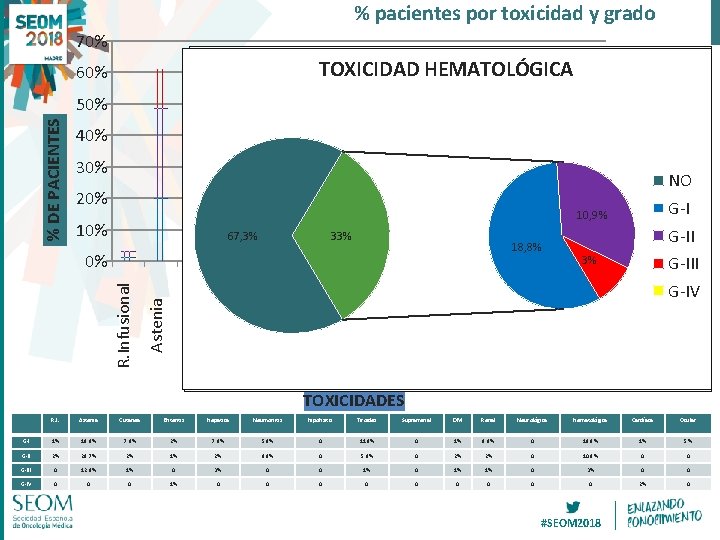
% pacientes por toxicidad y grado 70% ASTENIA TOXICIDAD TOXICIDAD NEUMONITIS ENDOCRINA HEMATOLÓGICA HEPÁTICA CUTÁNEA RENAL (TIROIDES) 60% 40% 30% 20% 10% 2% 8, 9% 28, 7% 2% 5, 9% 10, 9% 2% 3% 1% 1% 19, 8% 18, 8% 9, 9% 1% 7, 9% 11, 9% 3% 7, 9% 6%12, 9% 33% 15% 19% 11% 61% 38, 6% 67, 3% 87, 1% 85, 1% 81, 2% 89, 1% GRADO NO 4 GRADO G-I 3 GRADO G-II 2 Tiroides Suprarrenal DM Renal Neurológica Hematológica Cardíaca Ocular G-I 1% 19. 8% 7. 9% 2% 7. 9% 5. 9% 0 11. 9% 0 1% 9. 9% 0 18. 8% 1% 5% Tiroidea Hepática Astenia Ocular Hipofisitis Cardíaca Neurológica Neumonitis Suprarrenal Hepática Hipofisitis Enteritis Neumonitis Cutánea Enteritis Astenia Cutánea R. Infusional Renal GRADO G-III 1 G-IV DM 0% Hematológica % DE PACIENTES 50% TOXICIDADES G-II 2% 28. 7% 2% 1% 2% 8. 9% 0 5. 9% 0 2% 2% 0 10. 9% 0 0 G-III 0 12. 9% 1% 0 3% 0 0 1% 1% 0 3% 0 0 G-IV 0 0 0 1% 0 0 0 0 0 2% 0 #SEOM 2018
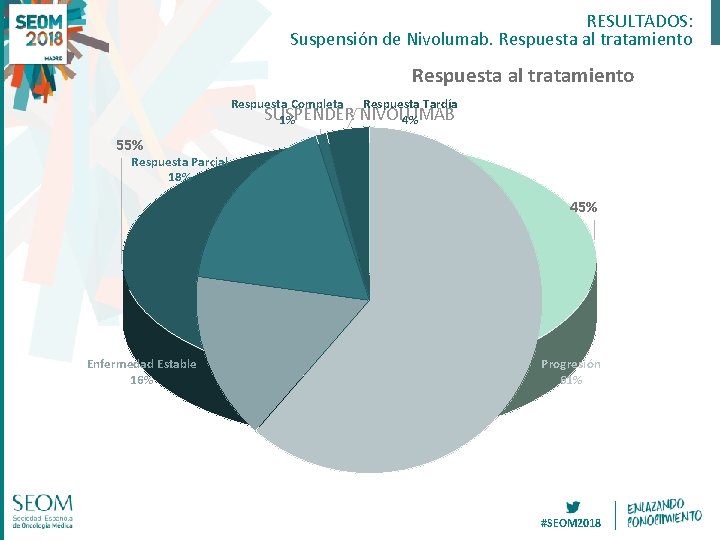
RESULTADOS: Suspensión de Nivolumab. Respuesta al tratamiento Respuesta Completa Respuesta Tardía SUSPENDER NIVOLUMAB 1% 4% 55% Respuesta Parcial 18% 45% Enfermedad Estable 16% Progresión 61% SÍ NO #SEOM 2018
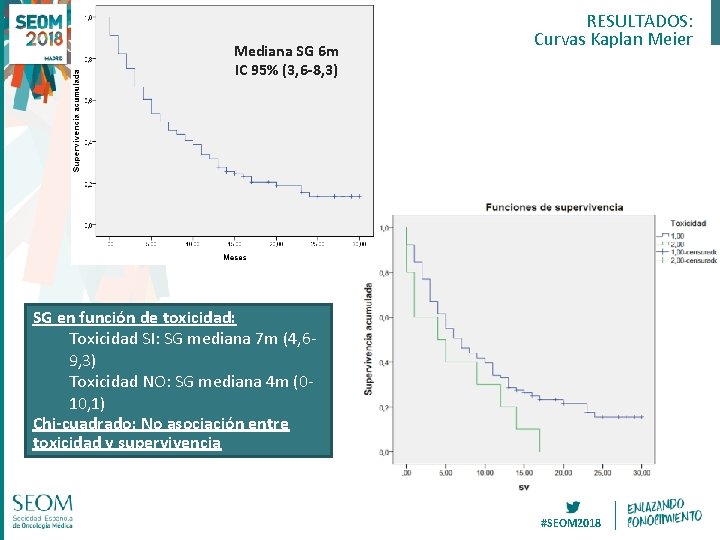
Mediana SG 6 m IC 95% (3, 6 -8, 3) RESULTADOS: Curvas Kaplan Meier SG en función de toxicidad: Toxicidad SI: SG mediana 7 m (4, 69, 3) Toxicidad NO: SG mediana 4 m (010, 1) Chi-cuadrado: No asociación entre toxicidad y supervivencia #SEOM 2018
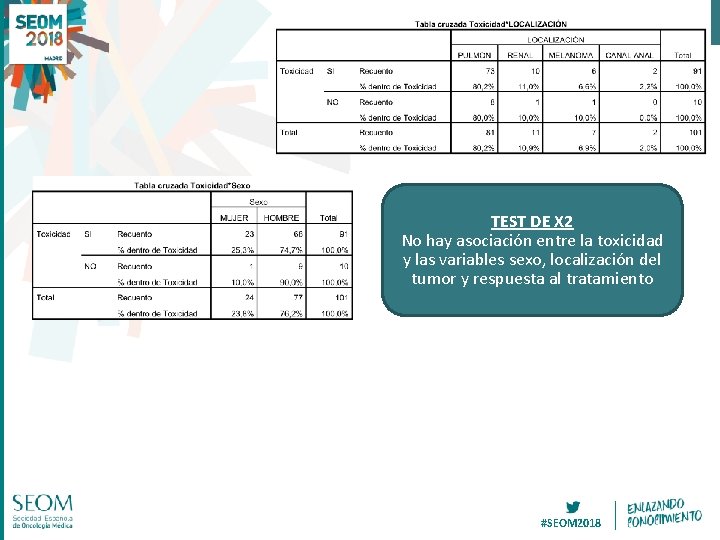
TEST DE X 2 No hay asociación entre la toxicidad y las variables sexo, localización del tumor y respuesta al tratamiento #SEOM 2018

CONCLUSIONES q. Nivolumab: toxicidad relacionada con la actividad del sistema inmune. q. Reversible. q. Corticoides. q. No se ha visto toxicidad diferente a la ya publicada. q. Primeros pacientes tratados con nivolumab. q. Datos no concluyentes por ser la muestra pequeña, mezclar diferentes tumores primarios… q. Realizar más estudios y generar más hipótesis. #SEOM 2018

MUCHAS GRACIAS #SEOM 2018
- Slides: 10