TOXICIDAD CEREBRAL EXPOSICIN ACCIDENTAL E INTENCIONAL REVISIN A

TOXICIDAD CEREBRAL: EXPOSICIÓN ACCIDENTAL E INTENCIONAL. REVISIÓN. A. Domingo, A. Camins, A. Ramos, E. Salvadó, J. P. Vives, A. Saurí. Hospital Universitari Joan XXIII Institut de Diagnòstic per la Imatge Tarragona

INTRODUCCIÓN Debido tanto a exposición intencional como accidental, algunos tóxicos (alcohol), drogas de ocio (heroína, cocaína, anfetaminas) y otros tipos de tóxicos cerebrales, tales como productos químicos (metanol), fármacos terapéuticos (quimioterapia, insulina, agentes inmunosupresivos) o tóxicos medioambientales (organofosfatos, monóxido de carbono. . . ), pueden causar daño cerebral agudo o permanente. OBJETIVOS: Revisar algunos de los tipos más comunes de tóxicos cerebrales incluyendo alcohol (efectos agudo y crónico), metanol, fármacos terapéuticos, drogas de ocio y tóxicos medioambientales. Describir algunos hallazgos radiológicos característicos que pueden ayudar a identificar la etiología subyacente.
ENCEFALOPATÍA ALCOHÓLICA Normalmente dosis-relacionada. Alcohol cruza BHE. NEUROTOXICIDAD DIRECTA EFECTOS CRÓNICOS : atrofia cerebral (degeneración cortical y cerebelar) y enfermedad de Marchiafava-Bignami EFECTOS CRÓNICOS : normalmente relacionados con transtornos metabólicos: encefalopatía de Wernicke (WE), mielinolisis, encefalopatía hepática. EFECTOS INDIRECTOS/ SECUNDARIOS EFECTOS AGUDOS : normalmente debidos a trauma craneal (hemorragia subaracnoidea, hemorragia intracerebral, fractura de calota).
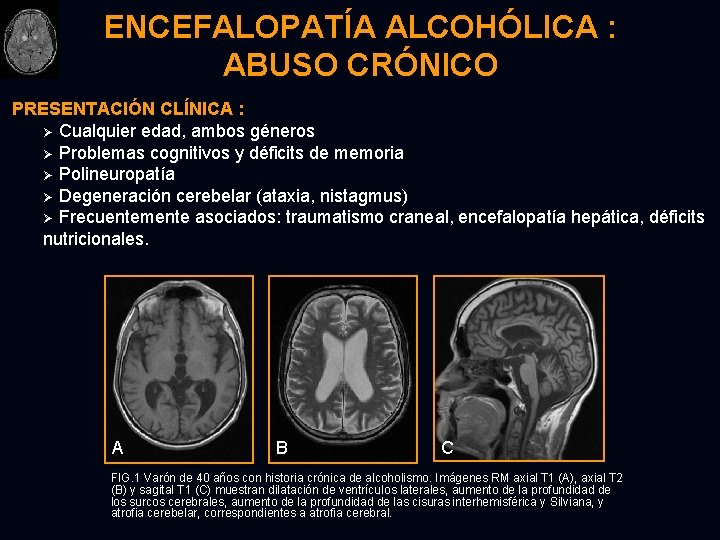
ENCEFALOPATÍA ALCOHÓLICA : ABUSO CRÓNICO PRESENTACIÓN CLÍNICA : Ø Cualquier edad, ambos géneros Ø Problemas cognitivos y déficits de memoria Ø Polineuropatía Ø Degeneración cerebelar (ataxia, nistagmus) Ø Frecuentemente asociados: traumatismo craneal, encefalopatía hepática, déficits nutricionales. A B C FIG. 1 Varón de 40 años con historia crónica de alcoholismo. Imágenes RM axial T 1 (A), axial T 2 (B) y sagital T 1 (C) muestran dilatación de ventrículos laterales, aumento de la profundidad de los surcos cerebrales, aumento de la profundidad de las cisuras interhemisférica y Silviana, y atrofia cerebelar, correspondientes a atrofia cerebral.
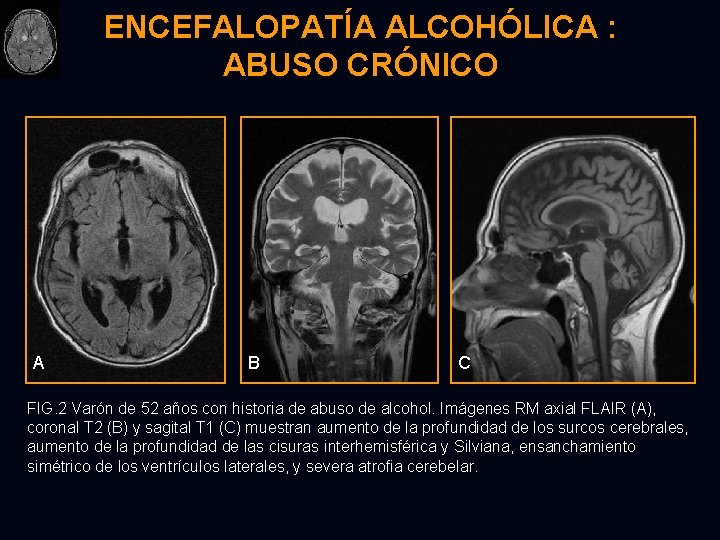
ENCEFALOPATÍA ALCOHÓLICA : ABUSO CRÓNICO A B C FIG. 2 Varón de 52 años con historia de abuso de alcohol. Imágenes RM axial FLAIR (A), coronal T 2 (B) y sagital T 1 (C) muestran aumento de la profundidad de los surcos cerebrales, aumento de la profundidad de las cisuras interhemisférica y Silviana, ensanchamiento simétrico de los ventrículos laterales, y severa atrofia cerebelar.

ENCEFALOPATÍA ALCOHÓLICA : ENFERMEDAD MARCHIAFAVA-BIGNAMI Ø Ø Complicación rara del abuso crónico. Resulta de una desmielinización y progresiva necrosis (cavidades quísticas) del cuerpo calloso (rodilla → cuerpo → esplenio). Fase tardía: atrofia CC (pérdida axonal). Ocasionalmente afecta otros tractos de sustancia blanca, pedúnculos cerebelares, fibras U y sustancia gris cortical. Debut clínico: pérdida de conocimiento, desconexión interhemisférica. Forma crónica: demencia progresiva.

ENCEFALOPATÍA ALCOHÓLICA : ENFERMEDAD MARCHIAFAVA-BIGNAMI RM: afectación del cuerpo calloso Aguda: T 2: hiperintensidad del CC (puede permanecer o recuperar la normal intensidad con total remielinización). T 1: hipointensidad. DW: hiperintensidad con disminución del ADC (edema citotóxico). Subaguda: hiperintensidad con aumento del ADC (desmielinización o necrosis). Crónica: atrofia residual CC.
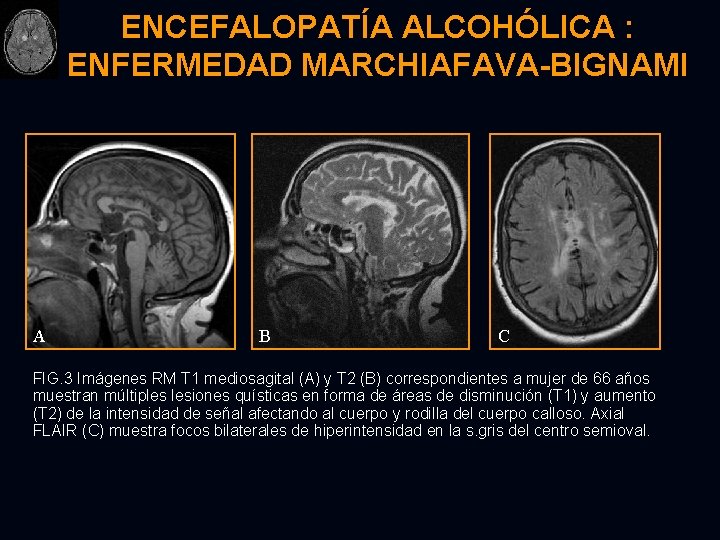
ENCEFALOPATÍA ALCOHÓLICA : ENFERMEDAD MARCHIAFAVA-BIGNAMI A B C FIG. 3 Imágenes RM T 1 mediosagital (A) y T 2 (B) correspondientes a mujer de 66 años muestran múltiples lesiones quísticas en forma de áreas de disminución (T 1) y aumento (T 2) de la intensidad de señal afectando al cuerpo y rodilla del cuerpo calloso. Axial FLAIR (C) muestra focos bilaterales de hiperintensidad en la s. gris del centro semioval.

ENCEFALOPATÍA ALCOHÓLICA : ENFERMEDAD MARCHIAFAVA-BIGNAMI A B FIG. 4 Imágenes RM T 1 mediosagital (A) y T 2 (B) correspondientes a varón de 61 años. Imágenes RM muestran múltiples lesiones quísticas como áreas de disminución (T 1) y aumento (T 2) de la intensidad de señal afectando al cuerpo calloso, que presenta una intensidad de señal anormal de forma difusa (aumentada en T 2) y moderada atrofia. DIAGNÓSTICO DIFERENCIAL (CLÍNICO): Fase aguda: Fase crónica : Encefalopatía de Wernicke Alzheimer Mielinolisis aguda Demencia multi-infarto Enfermedad de Pick Demencia de Korsakoff

ENCEFALOPATÍA ALCOHÓLICA : ENCEFALOPATÍA DE WERNICKE Ø Ø Complicación rara tratable causada por déficit de tiamina (vit B 12), habitualmente asociada a pobre ingesta oral en alcohólicos crónicos (no exclusivamente: hiperalimentación prolongada, cáncer en estadio terminal, rechazo alimentario, vómitos recurrentes). Localización habitual : cuerpos mamilares, tálamo medial, hipotálamo, s. gris periacueductal, paredes del 3 r y suelo del 4 o ventrículos, vermis superior. Debut agudo → TRÍADA CLÁSICA : ataxia, oftalmoplejía y confusión. Responde a tiamina intravenosa.

ENCEFALOPATÍA ALCOHÓLICA : ENCEFALOPATÍA DE WERNICKE RM: T 2 y FLAIR: hiperintensidad simétrica en localizaciones afectas. T 1 contraste: realce de los cuerpos mamilares, periacueducto y 3 r ventrículo. DW: lesiones hiperintensas con disminución (edema citotóxico) / aumento (edema vasogénico) del ADC. Las lesiones pueden desaparecer con tratamiento (tiamina). ANATOMOPATOLOGÍA: FASE AGUDA : necrosis, proliferación vascular, proliferación astroglial y microglial, hemorragias petequiales. FASE CRÓNICA : cuerpos mamilares, atrofia y dilatación del 3 r ventrículo.
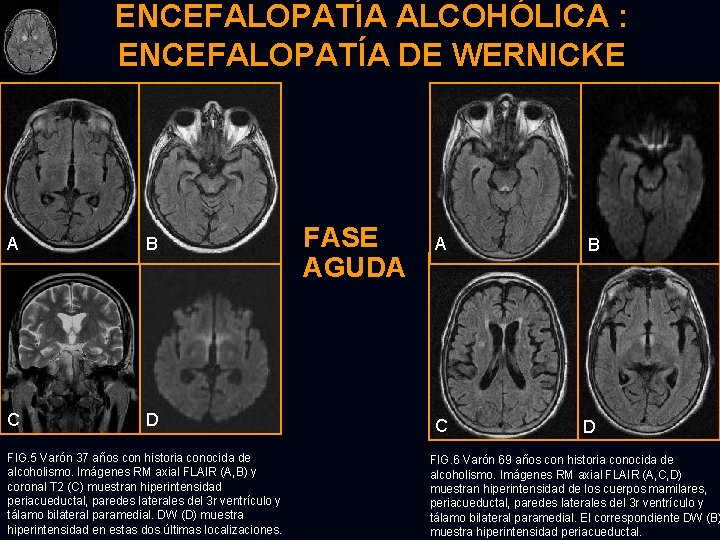
ENCEFALOPATÍA ALCOHÓLICA : ENCEFALOPATÍA DE WERNICKE A B C D FIG. 5 Varón 37 años con historia conocida de alcoholismo. Imágenes RM axial FLAIR (A, B) y coronal T 2 (C) muestran hiperintensidad periacueductal, paredes laterales del 3 r ventrículo y tálamo bilateral paramedial DW (D) muestra hiperintensidad en estas dos últimas localizaciones. FASE AGUDA A B C D FIG. 6 Varón 69 años con historia conocida de alcoholismo. Imágenes RM axial FLAIR (A, C, D) muestran hiperintensidad de los cuerpos mamilares, periacueductal, paredes laterales del 3 r ventrículo y tálamo bilateral paramedial. El correspondiente DW (B) muestra hiperintensidad periacueductal.

ENCEFALOPATÍA ALCOHÓLICA : ENCEFALOPATÍA DE WERNICKE A B C FASE CRÓNICA A B C FIG. 7 y FIG. 8. Varón 56 años y mujer 50 años. Imágenes RM mediosagital T 1 (7 A, 8 A) y axial FLAIR (7 B, 7 C, 8 B, 8 C) muestran atrofia de los cuerpos mamilares, atrofia cerebelar, dilatación ventricular, surcos profundos y pequeños focos hiperintensos en la s. blanca periventricular.

MIELINOLISIS Ø Ø Ø Destrucción de la vaina de mielina con preservación neuronal y axonal en sitios característicos del cerebro y cerebelo. Pontina central (CPM: porción central de la base de la protuberancia) o extrapontina (EPM: ganglios basales, caudado, tálamos, cuerpos geniculares, cápsulas interna y externa y unión sustancia gris-blanca). EPM aislada es rara. 75% asociada a alcoholismo crónico o hiponatremia rápidamente corregida. Otros: malnutrición, pacientes crónicamente debilitados y receptores de transplantes.

MIELINOLISIS CURSO CLINICO : bifásico Ø Hiponatremia → encefalopatía generalizada Ø 2 -3 días → corrección de hiponatremia → mielinolisis → cuadriparesia espástica. PATOGÉNESIS: desconocida. Hipótesis: Ø Daño osmótico endotelial Ø Excesiva deshidratación cerebral Ø Compromiso metabólico DIAGNÓSTICO DIFERENCIAL : Ø Infarto (CPM: preservación de neuronas y axones) Ø Metástasis Ø Glioma Ø Esclerosis múltiple (CPM: no reacción inflamatoria) Ø Encefalitis Ø Radiación y quimioterapia
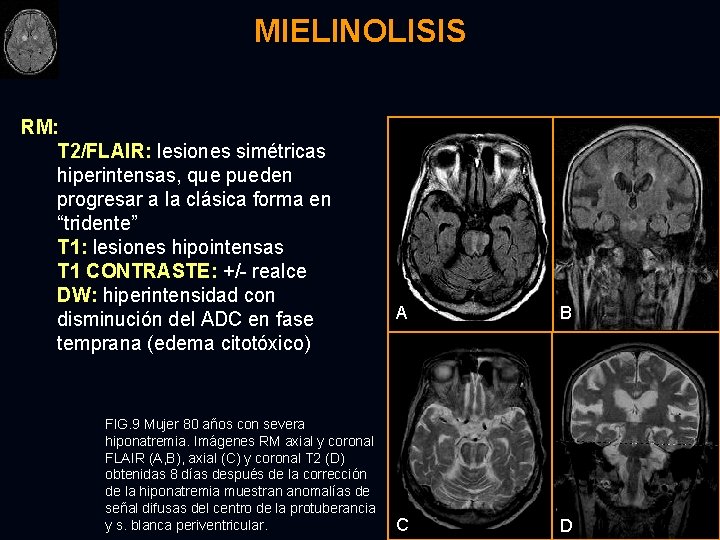
MIELINOLISIS RM: T 2/FLAIR: lesiones simétricas hiperintensas, que pueden progresar a la clásica forma en “tridente” T 1: lesiones hipointensas T 1 CONTRASTE: +/- realce DW: hiperintensidad con disminución del ADC en fase temprana (edema citotóxico) FIG. 9 Mujer 80 años con severa hiponatremia. Imágenes RM axial y coronal FLAIR (A, B), axial (C) y coronal T 2 (D) obtenidas 8 días después de la corrección de la hiponatremia muestran anomalías de señal difusas del centro de la protuberancia y s. blanca periventricular. A B C D

DEGENERACIÓN HEPATOCEREBRAL Adquirida (no wilsoniana). Síndrome potencialmente reversible en enfermedad hepática crónica asociada a múltiples insultos metabólicos. La encefalopatía hepática es la más común → raramente progresa a AHD → síndrome extrapiramidal: movimientos anormales, disartria, rigidez, temblor intencional, ataxia, disminución de las funciones intelectuales. PATOLOGÍA: Proliferación difusa de células Alzheimer tipo-II. Ø Cambios espongiformes en s. gris. Ø Otros: gliosis cortical, necrosis laminar neuronal, atrofia de núcleos lenticulares, polimicrocavitación de la unión corticomedular, estriado y s. blanca cerebelar. Ø DIAGNÓSTICO DIFERENCIAL : Sobrecarga hepática de cobre: enfermedad de Wilson, enfermedades colestáticas Ø Hiperalimentación Ø Microangiopatía e infartos en SIDA Ø Encefalopatía hipóxico-isquémica Ø Neurofibromatosis tipo I Ø Trastornos endocrinos que conllevan a calcificaciones de los ganglios basales (hiper/hipo paratiroidismo, hipotiroidismo) Ø Toxicidad por manganeso (asociación con hiperintensidad de la Ø
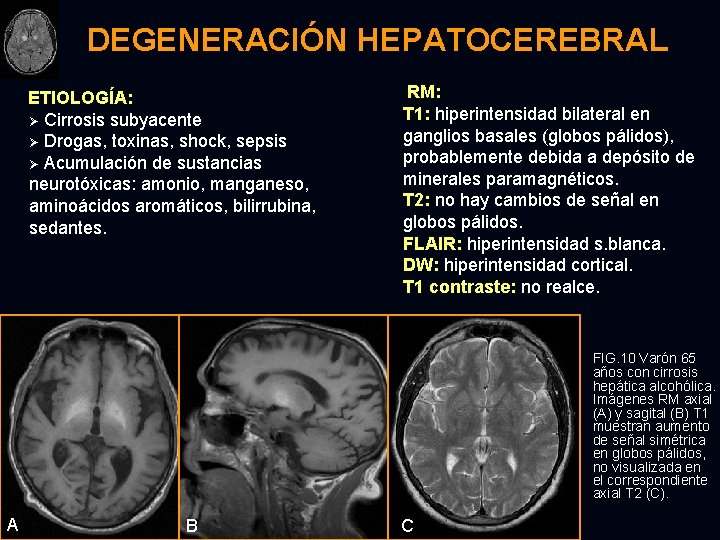
DEGENERACIÓN HEPATOCEREBRAL ETIOLOGÍA: Ø Cirrosis subyacente Ø Drogas, toxinas, shock, sepsis Ø Acumulación de sustancias neurotóxicas: amonio, manganeso, aminoácidos aromáticos, bilirrubina, sedantes. RM: T 1: hiperintensidad bilateral en ganglios basales (globos pálidos), probablemente debida a depósito de minerales paramagnéticos. T 2: no hay cambios de señal en globos pálidos. FLAIR: hiperintensidad s. blanca. DW: hiperintensidad cortical. T 1 contraste: no realce. FIG. 10 Varón 65 años con cirrosis hepática alcohólica. Imágenes RM axial (A) y sagital (B) T 1 muestran aumento de señal simétrica en globos pálidos, no visualizada en el correspondiente axial T 2 (C). A B C

COCAÍNA Adolescentes y adultos de mediana edad : causa común de infarto clínico aparente en adultos jóvenes (incluso sin factores de riesgo conocidos). Infarto hemorrágico asociado a anomalía vascular subyacente (50% de los casos). Muy adictiva: cada vez más disponible (aumento en la pureza y disminución en precio). Prevalencia en aumento: efectos crónicos retrasados aún por descubrir. Serias complicaciones: infarto/isquemia cerebral, hemorragia intraparenquimatosa, hemorragia subaracnoidea, convulsiones, vasculitis cerebral, espasmo arterial cerebral, y muerte. Uso: intranasal, intravenoso, intramuscular, fumada. Embarazo: hipoxia fetal, hemorragia intracerebral, malformaciones congénitas. Debut clínico: convulsiones, infarto, cefalea. Complicaciones sistémicas: insomnio, pérdida de apetito, disminución de la libido.

COCAÍNA DIAGNÓSTICO DIFERENCIAL : Ø Ø Hemorragia hipertensiva Malformaciones vasculares Hemorragia intratumoral Trombosis seno dural con infarto hemorrágico RM: T 2: ACM (50 -80%) → oclusión transitoria en territorio ACM → infarto incompleto → hiperintensidades T 2. Ligado a la edad y sin relación a los años de abuso. DW: puede mostrar restricción a la difusión. T 1 contraste: realce de infartos subagudos. Cocainómanos sin aparentes síntomas cerebrovasculares → ↑riesgo de daño s. blanca (cerebral subcortical e insular).
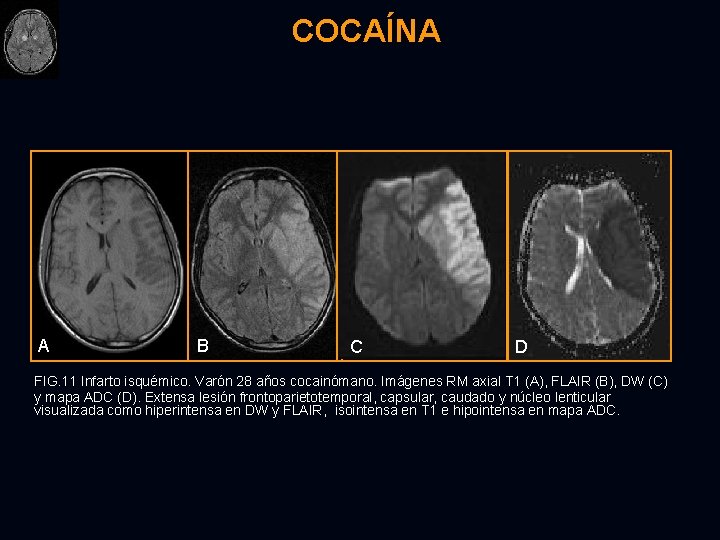
COCAÍNA A B C D FIG. 11 Infarto isquémico. Varón 28 años cocainómano. Imágenes RM axial T 1 (A), FLAIR (B), DW (C) y mapa ADC (D). Extensa lesión frontoparietotemporal, capsular, caudado y núcleo lenticular visualizada como hiperintensa en DW y FLAIR, isointensa en T 1 e hipointensa en mapa ADC.

ANFETAMINA Mismo tipo de infartos que cocaína: hemorragias y episodios TIA -like. Infarto (metanfetamina cristal = forma fumada ). Uso: oral, intranasal, parenteral. Debut clínico: cefalea severa, déficit focal y pérdida de conciencia en las primeras horas de ingesta en un adicto crónico. Patología: Ø Ø Vasoespasmo +/- trombosis superimpuesta. Uso crónico e intravenoso → vasculitis (similar a PAN)→ curso subagudo progresivo (cefalea, encefalopatía, isquemia bilateral o hemorragia). Angiografía: estrechamiento focal.
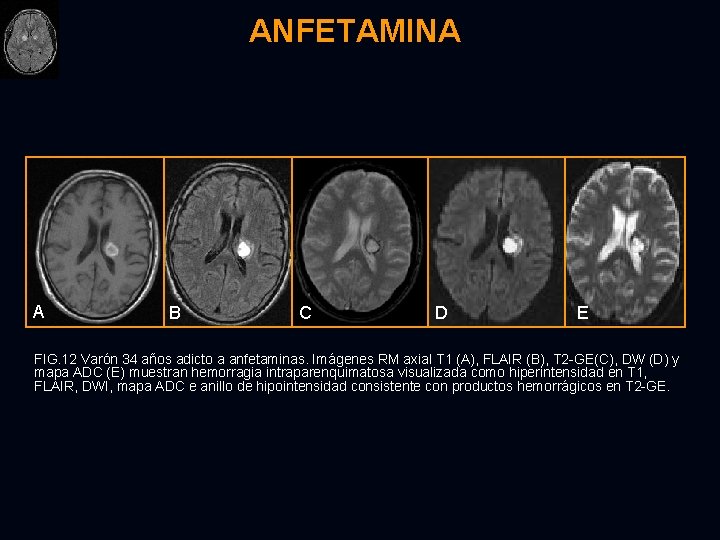
ANFETAMINA A B C D E FIG. 12 Varón 34 años adicto a anfetaminas. Imágenes RM axial T 1 (A), FLAIR (B), T 2 - GE(C), DW (D) y mapa ADC (E) muestran hemorragia intraparenquimatosa visualizada como hiperintensidad en T 1, FLAIR, DWI, mapa ADC e anillo de hipointensidad consistente con productos hemorrágicos en T 2 -GE.
HEROÍNA Intravenosa, inhalada (“chasing the dragon”) o inyección subcutánea (“skin-popping”). Euforia Inicial, aumento de la alerta y ansiedad Náuseas y vómitos EFECTOS: Efectos autonómicos : pupilas pequeñas, flushing, sequedad de boca Tos y supresión de la respiración Leucoencefalopatía tóxica : cerebelar, signos piramidales y bulbares, espasmo, muerte Paro cardiorespiratorio (vómito y aspiración) → Encefalopatía post-anóxica retardada: coma prolongado y compresión nerviosa (poplitea y cubital)

HEROÍNA Complicaciones infecciosas debidas a inyección Endocarditis infecciosa Infartos embólicos Otros: absceso cerebral, meningitis, arteritis séptica y aneurisma micótico (hemorragia intracerebral). Leucoencefalopatía tóxica: degeneración espongiforme s. blanca (edema intramielínico). Afectación cerebelar: característica de “chasing toxicity” T 2: hiperintensidad en s. blanca cerebral y cerebelar, pedúnculos cerebrales, tractos corticospinales, lemnisco medial y tracto solitario. DW: hiperintensidad con disminución del ADC (reversible)
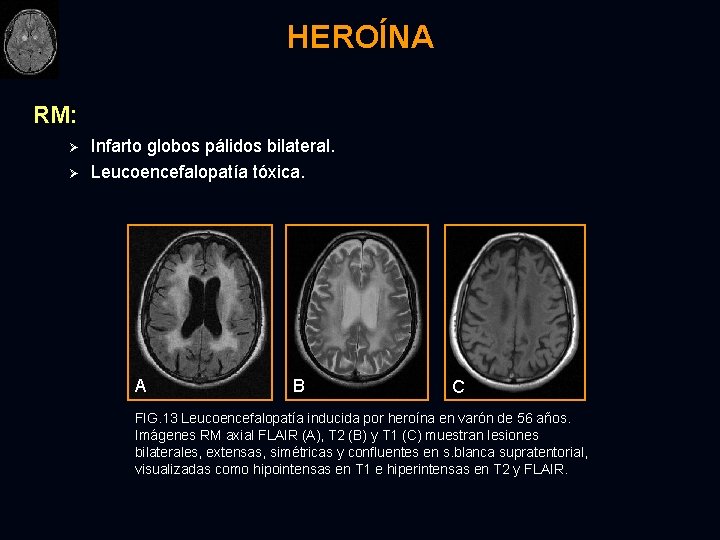
HEROÍNA RM: Ø Ø Infarto globos pálidos bilateral. Leucoencefalopatía tóxica. A B C FIG. 13 Leucoencefalopatía inducida por heroína en varón de 56 años. Imágenes RM axial FLAIR (A), T 2 (B) y T 1 (C) muestran lesiones bilaterales, extensas, simétricas y confluentes en s. blanca supratentorial, visualizadas como hipointensas en T 1 e hiperintensas en T 2 y FLAIR.

METANOL Líquido altamente tóxico, claro e incoloro, con sabor y gusto similar al etanol. Ingesta accidental/intencional: disolventes industriales, anticongelantes y líquidos de limpieza, alteración fraudulenta de bebidas alcohólicas. Ingesta: acidosis metabólica, ceguera, disfunción neurológica permanente, muerte. PRESENTACIÓN CLÍNICA: ØSusceptibilidad individual. Ø Habitualmente periodo de latencia de 12 -24 horas después de la ingesta (metil alcohol se metaboliza en formaldehído y ácido fórmico, más tóxico que metanol). Ø Síntomas iniciales: molestias visuales (necrosis nervio óptico o desmielinización). Ø Síntomas SNC : cefalea, mareo, convulsiones, estupor, coma. Otros: síntomas gastrointestinales.
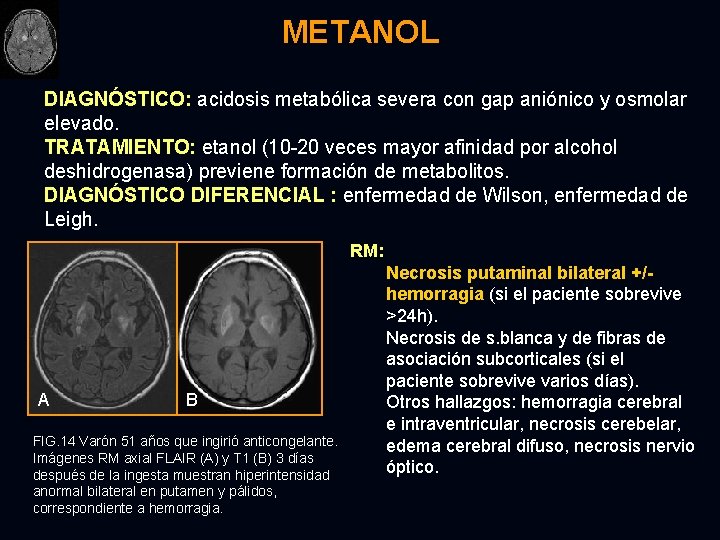
METANOL DIAGNÓSTICO: acidosis metabólica severa con gap aniónico y osmolar elevado. TRATAMIENTO: etanol (10 -20 veces mayor afinidad por alcohol deshidrogenasa) previene formación de metabolitos. DIAGNÓSTICO DIFERENCIAL : enfermedad de Wilson, enfermedad de Leigh. RM: A B FIG. 14 Varón 51 años que ingirió anticongelante. Imágenes RM axial FLAIR (A) y T 1 (B) 3 días después de la ingesta muestran hiperintensidad anormal bilateral en putamen y pálidos, correspondiente a hemorragia. Necrosis putaminal bilateral +/hemorragia (si el paciente sobrevive >24 h). Necrosis de s. blanca y de fibras de asociación subcorticales (si el paciente sobrevive varios días). Otros hallazgos: hemorragia cerebral e intraventricular, necrosis cerebelar, edema cerebral difuso, necrosis nervio óptico.

TOXICIDAD CO : Ø Ø Ø Inhalación accidental/intencional CO → carboxihemoglobina en sangre → encefalopatía anóxico-isquémica → lesiones bilaterales. Globos pálidos, s. blanca cerebral, ganglios basales, sustancia negra, tálamos, cuerpo calloso, corteza cerebral, hipocampo. Estadio agudo (período asintomático 2 -3 semanas) → encefalopatía retardada PRESENTACIÓN AGUDA : inespecífica (cefalea, náuseas, vómitos, pérdida de conciencia, coma, muerte). ENCEFALOPATÍA RETARDADA : deterioración mental, incontinencia urinaria, alteraciones intestinales, manifestaciones neuropsiquiátricas.
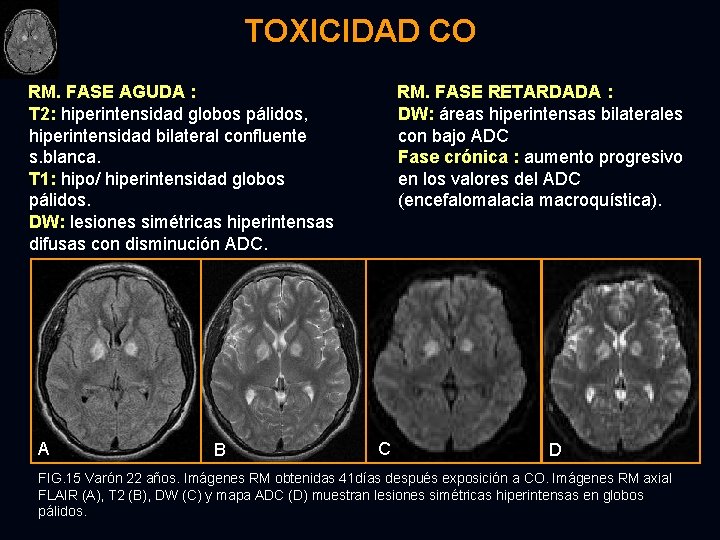
TOXICIDAD CO RM. FASE AGUDA : T 2: hiperintensidad globos pálidos, hiperintensidad bilateral confluente s. blanca. T 1: hipo/ hiperintensidad globos pálidos. DW: lesiones simétricas hiperintensas difusas con disminución ADC. A B RM. FASE RETARDADA : DW: áreas hiperintensas bilaterales con bajo ADC Fase crónica : aumento progresivo en los valores del ADC (encefalomalacia macroquística). C D FIG. 15 Varón 22 años. Imágenes RM obtenidas 41 días después exposición a CO. Imágenes RM axial FLAIR (A), T 2 (B), DW (C) y mapa ADC (D) muestran lesiones simétricas hiperintensas en globos pálidos.

QUIMIOTERAPIA AGENTES QUIMIOTERÁPICOS : Ø Ø Ø Ø Metotrexate (intratecal/intravenoso) Ciclofosfamida Cisplatino 5 -fluorouracil Carmustina (BCNU) Carmofur L-asparaginasa Vincristina EFECTOS COLATERALES : Ø Ø Ø Leucoencefalopatía (lesiones s. blanca difusas y simétricas) Microangiopatía mineralizante (niños, calcificación perivascular, metotrexate intratecal combinado con radioterapia) Posterior reversible encephalopathy syndrome (PRES: alteración de la autorregulación cerebrovascular, que causa hipertensión aguda. En pacientes pediátricos la presión sanguínea puede elevarse mínimamente) Hemorragia (algunos fármacos agravan trombocitopenia subyacente en pacientes con enfermedades hematológicas malignas) Trombosis Dural Venosa (no hay señal de flujo en senos durales afectos)
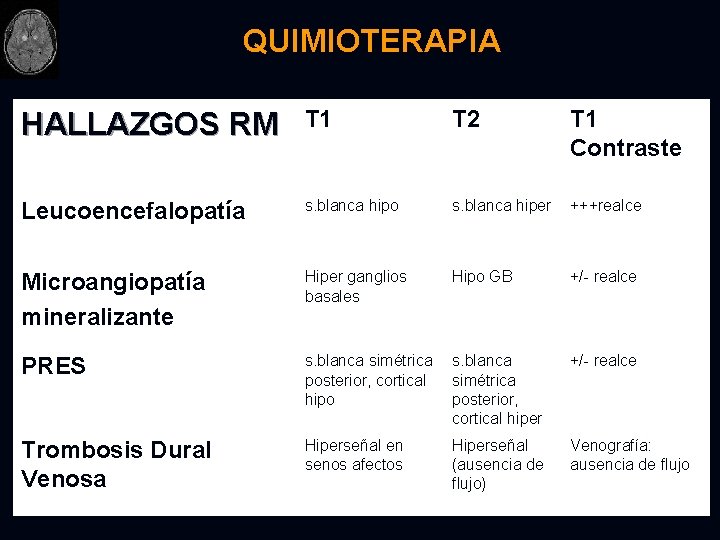
QUIMIOTERAPIA HALLAZGOS RM T 1 T 2 T 1 Contraste Leucoencefalopatía s. blanca hipo s. blanca hiper +++realce Microangiopatía mineralizante Hiper ganglios basales Hipo GB +/- realce PRES s. blanca simétrica posterior, cortical hipo s. blanca simétrica posterior, cortical hiper +/- realce Trombosis Dural Venosa Hiperseñal en senos afectos Hiperseñal (ausencia de flujo) Venografía: ausencia de flujo
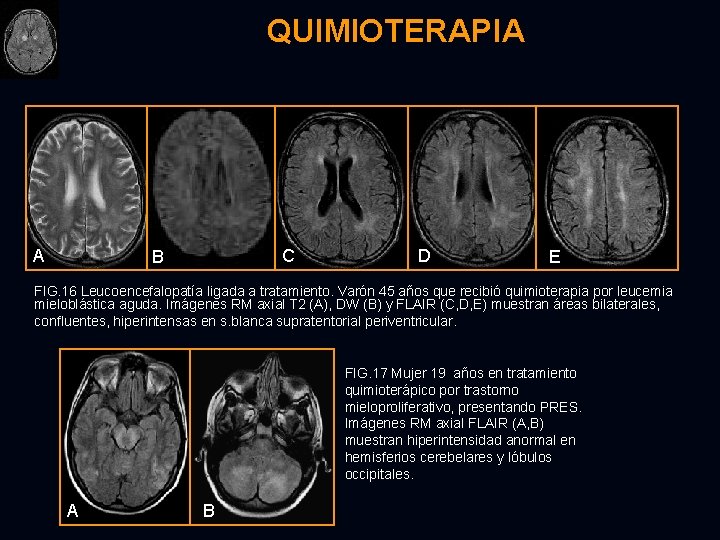
QUIMIOTERAPIA A C B D E FIG. 16 Leucoencefalopatía ligada a tratamiento. Varón 45 años que recibió quimioterapia por leucemia mieloblástica aguda. Imágenes RM axial T 2 (A), DW (B) y FLAIR (C, D, E) muestran áreas bilaterales, confluentes, hiperintensas en s. blanca supratentorial periventricular. FIG. 17 Mujer 19 años en tratamiento quimioterápico por trastorno mieloproliferativo, presentando PRES. Imágenes RM axial FLAIR (A, B) muestran hiperintensidad anormal en hemisferios cerebelares y lóbulos occipitales. A B
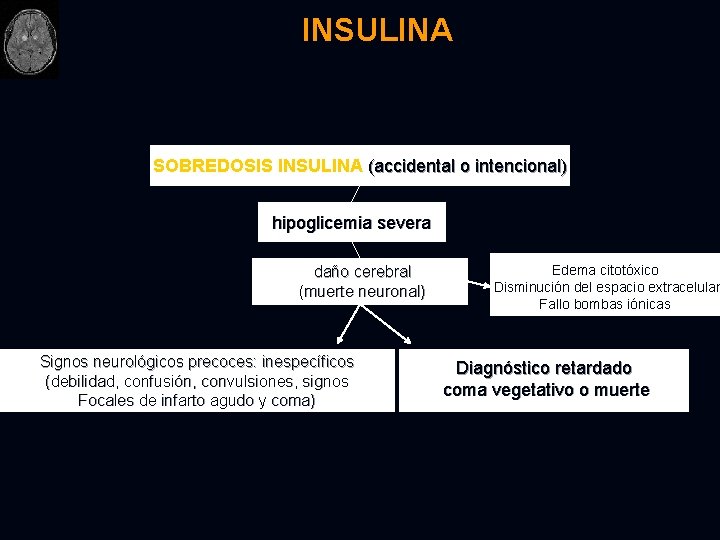
INSULINA SOBREDOSIS INSULINA (accidental o intencional) hipoglicemia severa daño cerebral (muerte neuronal) Signos neurológicos precoces: inespecíficos (debilidad, confusión, convulsiones, signos Focales de infarto agudo y coma) Edema citotóxico Disminución del espacio extracelular Fallo bombas iónicas Diagnóstico retardado coma vegetativo o muerte

INSULINA DIAGNÓSTICO DIFERENCIAL : lesiones hiperintensas en DW (signos tempranos de cambios isquémicos en el infarto) → posible trampa en pacientes diabéticos (riesgo aumentado para ambos, hipoglicemia e infarto). RM: S. Gris: ganglios basales bilaterales (caudados y núcleos lenticulares), corteza cerebral, sustancia negra e hipocampo. T 2/FLAIR: hiperintensidad T 1: hipointensidad DWI: hiperintensidad ADC: disminución A B C D E FIG. 18 Varón 43 años presenta coma hipoglicémico accidental debido a sobredosis de insulina. Imágenes RM axial FLAIR (A), T 2 (B) y DW (C) muestran hiperintensidad bilateral de caudados y núcleos lenticulares. Imágenes RM axial FLAIR (D) y DW (E) muestran aumento de señal de la corteza supratentorial.

ORGANOFOSFATOS OP: grupo diverso de compuesto químicos usados en el ámbito doméstico e industrial: insecticidas, gases nerviosos, agentes oftálmicos y antihelmínticos. Absorción: cutánea, ingerida, inhalada o inyectada. El debut y severidad de los síntomas depende del componente específico, cantidad, vía de exposición, y tasa de degradación metabólica. EXPOSICIÓN Efectos colaterales agudos muscarínicos y nicotínicos Accidental/ocupacional y suicida: Anticolinesterasas: 3 síndromes neurológicos agudos: Ø Ø Ø Crisis aguda colinérgica (potencialmente letal) Paresia de nervios craneales + debilidad muscular proximal Polineuropatía retardada Dosis baja crónica: Cambios en el neurocomportamiento (OP induce trastornos neuropsiquiátricos) Dosis masiva crónica: Síndrome extrapiramidal (EPS): temblor, rigidez e hipocinesias con pobre respuesta a levodopa. RM: Focos difusos de hiperseñal en tractos de s. blanca subcortical y periventricular, compatibles con desmielinización (recuerda a la desmielinización de la esclerosis múltiple – siendo la lesión primaria una degeneración axonal seguida de desmielinización).
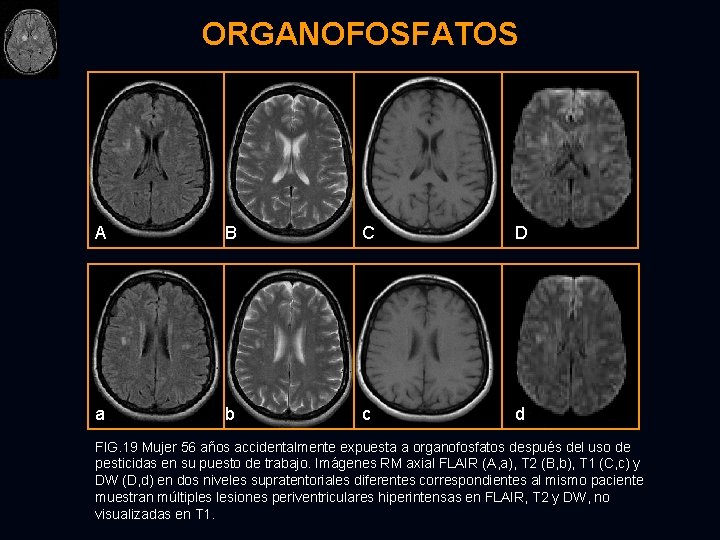
ORGANOFOSFATOS A B C D a b c d FIG. 19 Mujer 56 años accidentalmente expuesta a organofosfatos después del uso de pesticidas en su puesto de trabajo. Imágenes RM axial FLAIR (A, a), T 2 (B, b), T 1 (C, c) y DW (D, d) en dos niveles supratentoriales diferentes correspondientes al mismo paciente muestran múltiples lesiones periventriculares hiperintensas en FLAIR, T 2 y DW, no visualizadas en T 1.
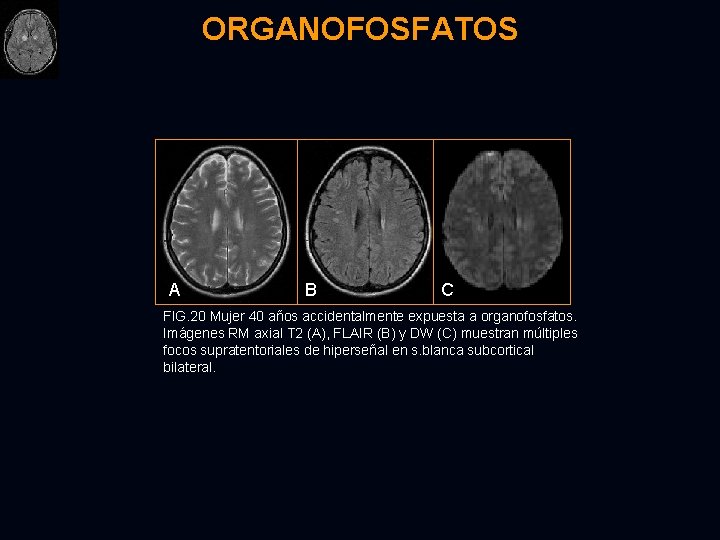
ORGANOFOSFATOS A B C FIG. 20 Mujer 40 años accidentalmente expuesta a organofosfatos. Imágenes RM axial T 2 (A), FLAIR (B) y DW (C) muestran múltiples focos supratentoriales de hiperseñal en s. blanca subcortical bilateral.

CONCLUSIONES C Habitualmente difícil atribuir un síndrome clínico específico a un tóxico cerebral en particular. C Agente causal frecuentemente desconocido al debut clínico. C Abuso de polidrogas común → hace el dx más difícil. C La Neuroimagen puede proporcionar información para el diagnóstico. C Frecuente afectación de la s. blanca (difusa y simétricamente), también ganglios basales. C TC generalmente inespecífico → disminución de la atenuación de la s. blanca. C RM puede proporcionar información útil, aunque a veces también inespecífica. El uso de DW y perfusión puede añadir información de utilidad. C Aunque existe frecuente solapamiento radiológico entre diferentes entidades clínicas, la distribución de las lesiones puede añadir información para identificar el agente causal.

BIBLIOGRAFÍA Ø Ø Ø Ø Ø Ø Ø Ø Ø Rabin BM, Meyer JR, Berlin JW, Marymount MH, Palka PS, Russell EJ. Radiation-induced changes in the central nervous system and head and neck. Radiographics. 1996 Sep; 16(5): 1055 -72. Lee J, Lacomis D, Comu S, Jacobsohn J, Kanal E. Acquired hepatocerebral degeneration: MR and pathologic findings. AJNR Am J Neuroradiol. 1998 Mar; 19(3): 485 -7. Matsusue E, Kinoshita T, Ohama E, Ogawa T. Cerebral cortical and white matter lesions in chronic hepatic encephalopathy: MR-pathologic correlations. AJNR Am J Neuroradiol. 2005 Feb; 26(2): 347 -51. Kinoshita T, Sugihara S, Matsusue E, Fujii S, Ametani M, Ogawa T. Pallidoreticular damage in acute carbon monoxide poisoning: diffusion-weighted MR imaging findings. AJNR Am. J Neuroradiol. 2005 Aug; 26(7): 1845 -8. Ruzek KA, Campeau NG, Miller GM. Early diagnosis of central pontine myelinolysis with diffusion-weighted imaging. AJNR Am J Neuroradiol. 2004 Feb; 25(2): 210 -3. Yuh WT, Simonson TM, D'Alessandro MP, Smith KS, Hunsicker LG. Temporal changes of MR findings in central pontine myelinolysis. AJNR Am J Neuroradiol. 1995 Apr; 16(4 Suppl): 975 -7. Bartlett E, Mikulis DJ. Chasing "chasing the dragon" with MRI: leukoencephalopathy in drug abuse. Br J Radiol. 2005 Nov; 78(935): 997 -1004. Keogh CF, Andrews GT, Spacey SD, Forkheim KE, Graeb DA. Neuroimaging features of heroin inhalation toxicity: "chasing the dragon“. AJR Am J Roentgenol. 2003 Mar; 180(3): 847 -50. Hill MD, Cooper PW, Perry JR. Chasing the dragon--neurological toxicity associated with inhalation of heroin vapour: case report. CMAJ. 2000 Jan 25; 162(2): 236 -8. Brown E, Prager J, Lee HY, Ramsey RG. CNS complications of cocaine abuse: prevalence, pathophysiology, and neuroradiology. AJR Am J Roentgenol. 1992 Jul; 159(1): 137 -47. Bartzokis G, Goldstein IB, Hance DB, Beckson M, Shapiro D, Lu PH, Edwards N, Mintz J, Bridge P. The incidence of T 2 -weighted MR imaging signal abnormalities in the brain of cocaine-dependent patients is age-related and region-specific. AJNR Am J Neuroradiol. 1999 Oct; 20(9): 1628 -35. Goel D, Singhal A, Srivastav RK, Verma A, Lamba A. Magnetic resonance imaging changes in a case of extra-pyramidal syndrome after acute organophosphate poisoning. Neurol India. 2006 Jun; 54(2): 207 -9. Kamel F, Hoppin JA. Association of pesticide exposure with neurologic dysfunction and disease. Environ Health Perspect. 2004 Jun; 112(9): 950 -8. Sener RN. Acute carbon monoxide poisoning: diffusion MR imaging findings. AJNR Am J Neuroradiol. 2003 Aug; 24(7): 1475 -7. Kim JH, Chang KH, Song IC, Kim KH, Kwon BJ, Kim HC, Kim JH, Han MH. Delayed encephalopathy of acute carbon monoxide intoxication: diffusivity of cerebral white matter lesions. AJNR Am J Neuroradiol. 2003 Sep; 24(8): 1592 -7. Rubinstein D, Escott E, Kelly JP. Methanol intoxication with putaminal and white matter necrosis: MR and CT findings. AJNR Am J Neuroradiol. 1995 Aug; 16(7): 1492 -4. Moritani T. , Ekholm S. , Westesson, P. L. Diffusion-weighted MR imaging of the Brain. Publisher: Springer-Verlag 2005. Blanco M, Casado R, Vazquez F, Pumar JM. CT and MR imaging findings in methanol intoxication. AJNR Am J Neuroradiol. 2006 Feb; 27(2): 452 -4. Gaul HP, Wallace CJ, Auer RN, Fong TC. MR findings in methanol intoxication. AJNR Am J Neuroradiol. 1995 Oct; 16(9): 1783 -6. Diagnostic Imaging: Brain. Anne G. Osborn, Karen L. Salzman, Susan I. Blaser. Pub. Date: June 2004. ISBN: 0721629059. Publisher: Elsevier Health Sciences. Edition Number: 1 Diamond I, Messing RO. Neurologic effects of alcoholism. West J Med. 1994 Sep; 161(3): 279 -87. Zhong C, Jin L, Fei G. MR Imaging of nonalcoholic Wernicke encephalopathy: a follow-up study. AJNR Am J Neuroradiol. 2005 Oct; 26(9): 2301 -5. Bae SJ, Lee HK, Lee JH, Choi CG, Suh DC. Wernicke's encephalopathy: atypical manifestation at MR imaging. AJNR Am J Neuroradiol. 2001 Sep; 22(8): 1480 -2. Gambini A, Falini A, Moiola L, Comi G, Scotti G. Marchiafava-Bignami disease: longitudinal MR imaging and MR spectroscopy study. AJNR Am J Neuroradiol. 2003 Feb; 24(2): 249 -53. Teke E, Sungurtekin H, Sahiner T, Atalay H, Gur S. Organophosphate poisoning case with atypical clinical survey and magnetic resonance imaging findings. J Neurol Neurosurg Psychiatry. 2004 Jun; 75(6): 936 -7. Vazquez E, Lucaya J, Castellote A, Piqueras J, Sainz P, Olive T, Sanchez-Toledo J, Ortega JJ. Neuroimaging in pediatric leukemia and lymphoma: differential diagnosis. Radiographics. 2002 Nov-Dec; 22(6): 1411 -28. Arbelaez A, Pajon A, Castillo M. Acute Marchiafava-Bignami disease: MR findings in two patients. AJNR Am J Neuroradiol. 2003 Nov-Dec; 24(10): 1955 -7. Lai PH, Chen C, Liang HL, Pan HB. Hyperintense basal ganglia on T 1 -weighted MR imaging. AJR Am J Roentgenol. 1999 Apr; 172(4): 1109 -15. Sener RN. Diffusion MR imaging changes associated with Wilson disease. AJNR Am J Neuroradiol. 2003 May; 24(5): 965 -7. Moritani T, Smoker WR, Sato Y, Numaguchi Y, Westesson PL. Diffusion-weighted imaging of acute excitotoxic brain injury. AJNR Am J Neuroradiol. 2005 Feb; 26(2): 21628. Vargas MI, Lenz V, Bin JF, Bogorin A, Abu Eid M, Jacques C, Marin H, Kindo S, Zollner G, Dietemann JL. Brain MR imaging of chronic alcoholism. J Radiol. 2003 Apr; 84(4 Pt 1): 369 -79. Imbesi SG. Diffuse cerebral vasculitis with normal results on brain MR imaging. AJR Am J Roentgenol. 1999 Dec; 173(6): 1494 -6. Provenzale JM, Barboriak DP. Brain infarction in young adults: etiology and imaging findings. AJR Am J Roentgenol. 1997 Oct; 169(4): 1161 -8.
- Slides: 40