Tour d Innovation Info Ziel Vorgehen Musteraufgabe 2

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Tour d´ Innovation Abschlusspräsentation B. Hanssmann A. Hall

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Kunde: Hr. Rinnus Chemielehrer Thema: Lernprogramm Elektrochemie

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Ziele: • Bedienerfreundlich • Erklärung Begriffe • verständlich
Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b
Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b
Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3
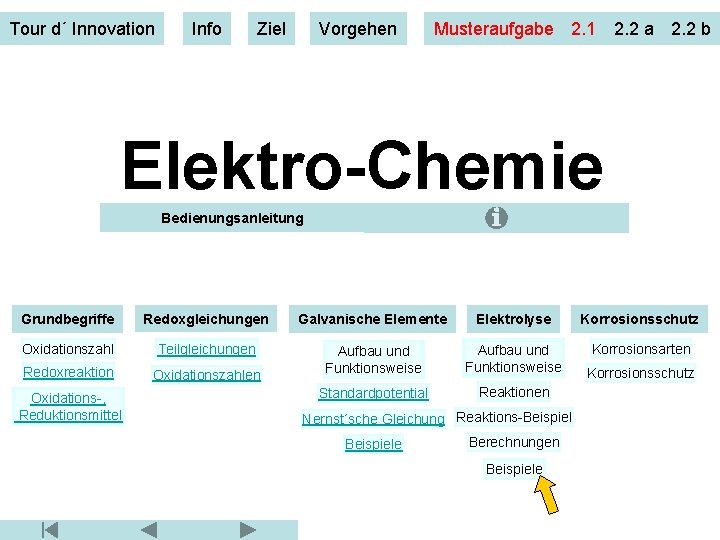
Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Elektro-Chemie Bedienungsanleitung Grundbegriffe Redoxgleichungen Galvanische Elemente Elektrolyse Korrosionsschutz Oxidationszahl Teilgleichungen Oxidationszahlen Aufbau und Funktionsweise Korrosionsarten Redoxreaktion Aufbau und Funktionsweise Standardpotential Reaktionen Oxidations-, Reduktionsmittel Nernst´sche Gleichung Reaktions-Beispiele Berechnungen Beispiele Korrosionsschutz

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Bedienungsanleitung Grundbegriffe Redoxgleichungen Galvanische Elemente Elektrolyse Aufbau und Funktionsweise Reaktionen Reaktions-Beispiel Berechnungen Beispiele 4) Schmelzflusselektrolyse Herstellung unedler Metalle, z. B. Aluminium, Natrium. Reaktionen (vereinfacht) bei Aluminiumherstellung Anode aus Graphitblöcken: C + 2 O 2 CO 2 + 4 e- x 3 x 4 Kathode aus Graphit (Wanne): Al 3+ + 3 e. Al Gesamtreaktion: 3 C + 6 O 2 - + 4 Al 3+ 3 CO 2 + 4 Al Elektrolyt: geschmolzenes Kryolith (Na 3 Al. F 6) mit Aluminiumoxid (Al 2 O 3) Beachte: Kryolith (80%) dient zur Erhöhung der Leitfähigkeit und zur Senkung der Schmelztemperatur (Arbeitstemperatur : 960°C) Die Anode (Graphit) wird verbraucht und muss nachgeführt werden. Korrosionsschutz Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss.

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3
Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Elektro-Chemie Bedienungsanleitung Grundbegriffe Redoxgleichungen Galvanische Elemente Elektrolyse Korrosionsschutz Oxidationszahl Teilgleichungen Oxidationszahlen Aufbau und Funktionsweise Korrosionsarten Redoxreaktion Aufbau und Funktionsweise Standardpotential Reaktionen Oxidations-, Reduktionsmittel Nernst´sche Gleichung Reaktions-Beispiele Berechnungen Beispiele Korrosionsschutz
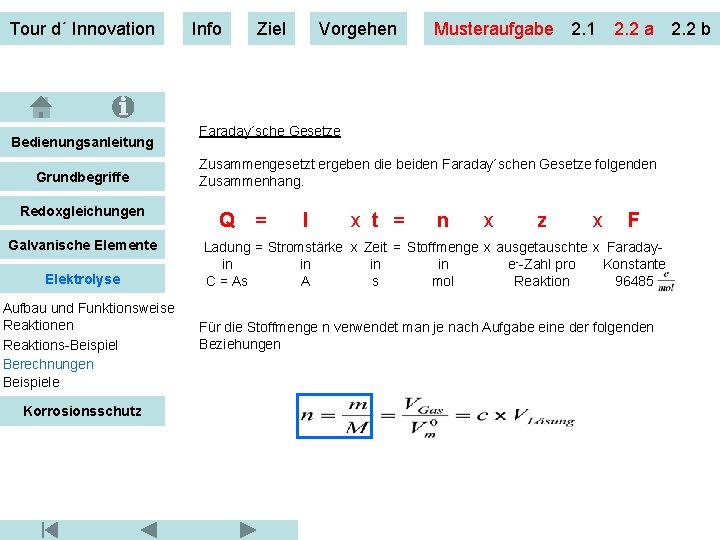
Tour d´ Innovation Bedienungsanleitung Grundbegriffe Redoxgleichungen Galvanische Elemente Elektrolyse Aufbau und Funktionsweise Reaktionen Reaktions-Beispiel Berechnungen Beispiele Korrosionsschutz Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Faraday´sche Gesetze Zusammengesetzt ergeben die beiden Faraday´schen Gesetze folgenden Zusammenhang. Q = I x t = n x z x F Ladung = Stromstärke x Zeit = Stoffmenge x ausgetauschte x Faradayin in e--Zahl pro Konstante C = As A s mol Reaktion 96485 Für die Stoffmenge n verwendet man je nach Aufgabe eine der folgenden Beziehungen
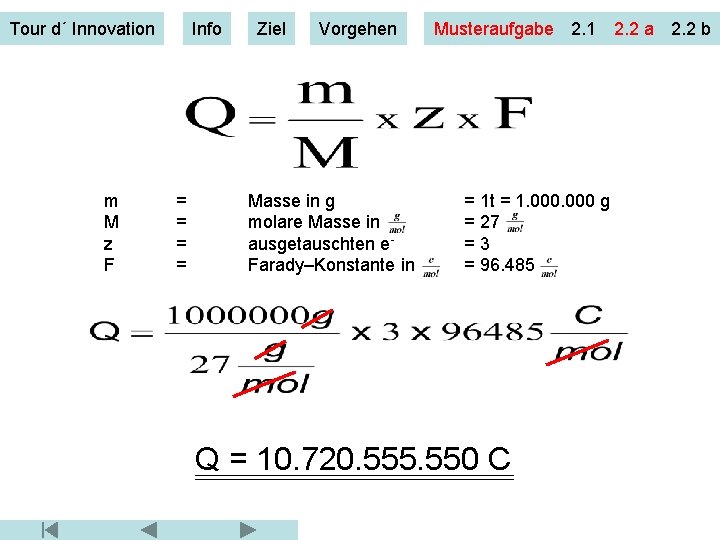
Tour d´ Innovation m M z F Info = = Ziel Vorgehen Masse in g molare Masse in ausgetauschten e. Farady–Konstante in Musteraufgabe 2. 1 2. 2 a 2. 2 b = 1 t = 1. 000 g = 27 =3 = 96. 485 Q = 10. 720. 555. 550 C

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3
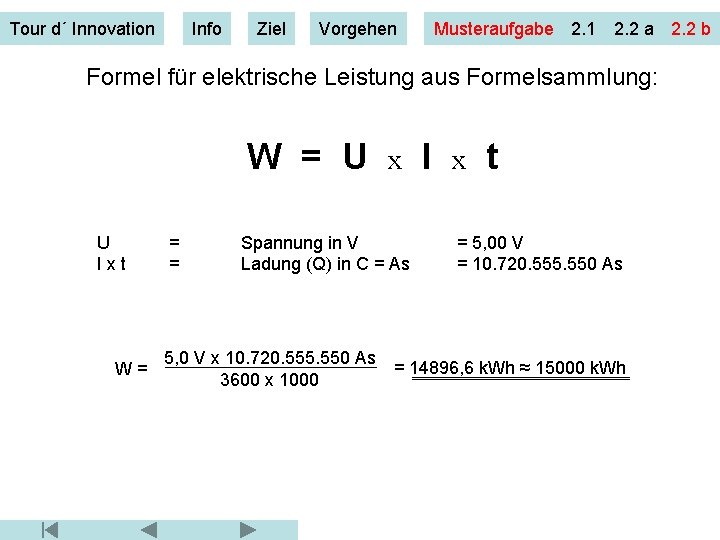
Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Formel für elektrische Leistung aus Formelsammlung: W = U U Ixt W= = = x Spannung in V Ladung (Q) in C = As I x t = 5, 00 V = 10. 720. 555. 550 As 5, 0 V x 10. 720. 555. 550 As = 14896, 6 k. Wh ≈ 15000 k. Wh 3600 x 1000

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Auszug aus einer Abituraufgabe zum Thema Elektrochemie Punkte: 1 Gewinnung und Verwendung von Aluminium Mitte des 19. Jahrhunderts wurde Aluminium durch Reaktion von Aluminiumchlorid mit Natrium hergestellt. Formulieren Sie die Reaktionsgleichung und begründen Sie, weshalb Natrium als Reaktionspartner geeignet ist. 2 2 Heute wird Aluminium aus Aluminiumoxid durch Schmelzelektrolyse an Graphitelektroden hergestellt. 2. 1 Formulieren Sie die an den Elektroden ablaufenden Reaktionen und begründen Sie, welche Elektrode in bestimmten Zeitabständen ersetzt werden muss. 3 2. 2 Bei einer Spannung von U = 5 V und einer Stromstärke von I = 100 000 A soll m = 1 t Aluminium hergestellt werden. Berechnen Sie: a) die hierfür notwendige Ladung Q, b) sowie die elektrische Arbeit W. 3

Tour d´ Innovation Info Ziel Vorgehen Musteraufgabe 2. 1 2. 2 a 2. 2 b Ende
- Slides: 23