Tots elements que es troben als ssers vius
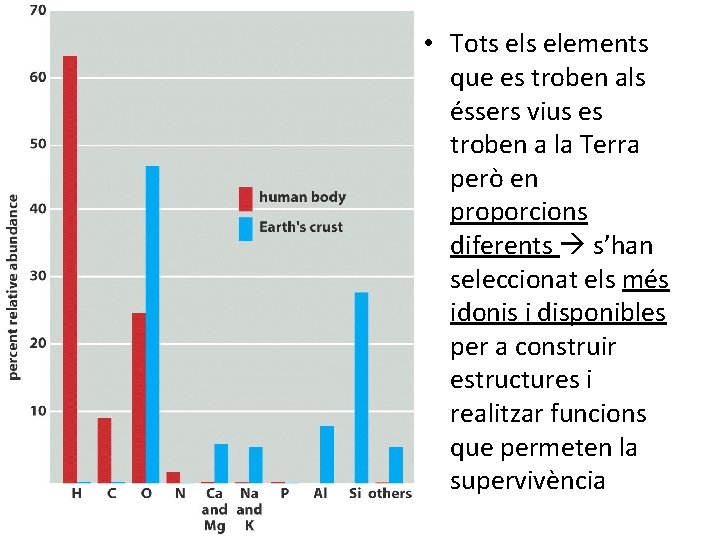
• Tots elements que es troben als éssers vius es troben a la Terra però en proporcions diferents s’han seleccionat els més idonis i disponibles per a construir estructures i realitzar funcions que permeten la supervivència
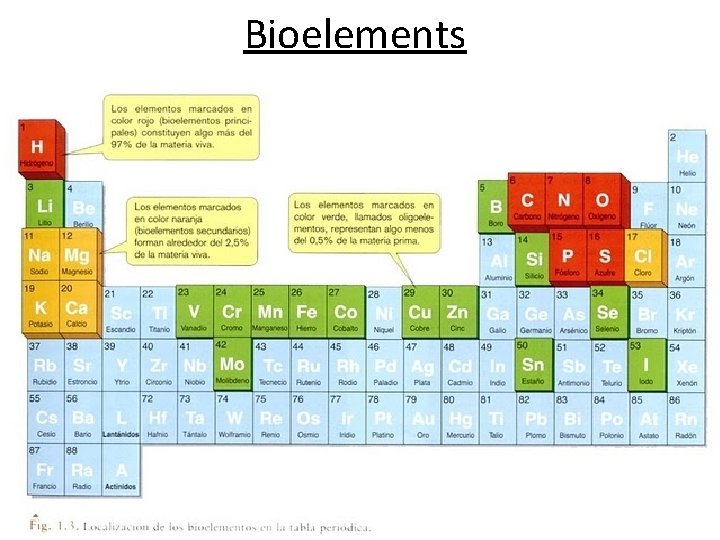
Bioelements

Bioelements primaris: C, H, O, N, S i P a totes les biomolècules org 95% 97% fonamental a proteïnes i ac. nuclèics, molts glúcids i lípids en 2 aa (Cys, Met) i algunes prot (vit, Co. A) en ac. nuclèics, Coenzims (NADP+, NAD+. . . ) i fosfolípids
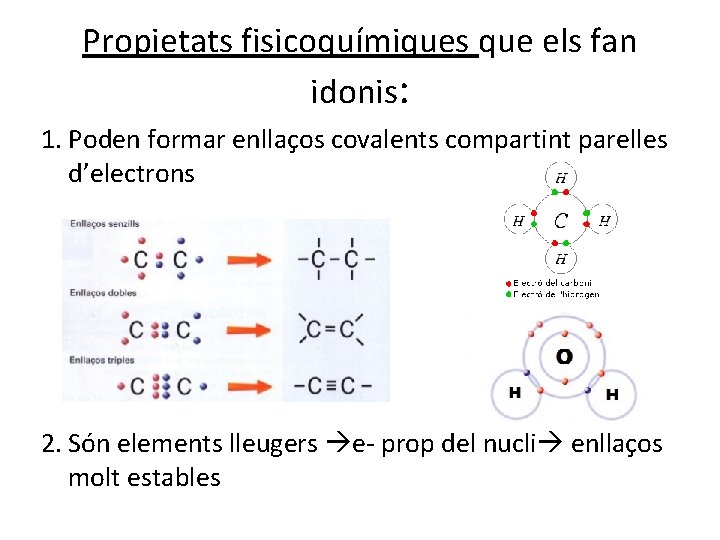
Propietats fisicoquímiques que els fan idonis: 1. Poden formar enllaços covalents compartint parelles d’electrons 2. Són elements lleugers e- prop del nucli enllaços molt estables
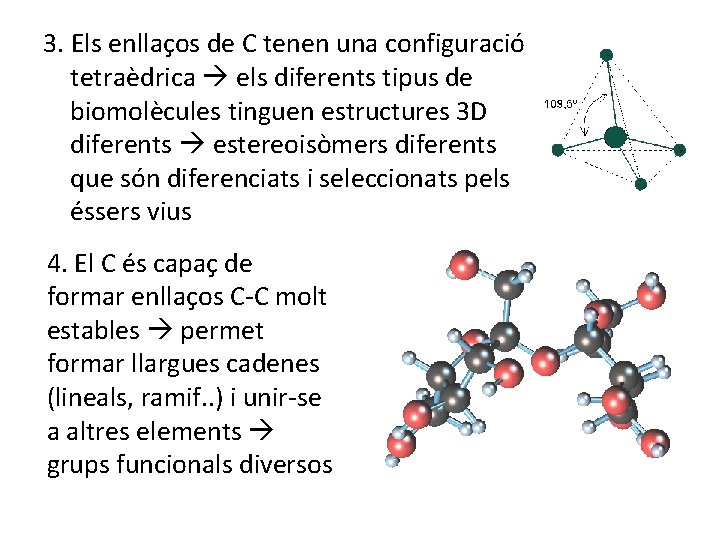
3. Els enllaços de C tenen una configuració tetraèdrica els diferents tipus de biomolècules tinguen estructures 3 D diferents estereoisòmers diferents que són diferenciats i seleccionats pels éssers vius 4. El C és capaç de formar enllaços C-C molt estables permet formar llargues cadenes (lineals, ramif. . ) i unir-se a altres elements grups funcionals diversos

5. Els compostos formats per C, H, O, N es troben en estat reduït als éssers vius l’Oxigen els pot oxidar formant compostos de baixa energia l’energia que es desprèn es aprofitada per a funcions vitals

Bioelements secundaris: a tots els éssers vius (2. 5% del pes total) • Ca (2% del total) Ca. CO 3 als ossos, impuls nerviós, coagulació sang, contracció muscular • Mg forma part de la clorofil·la, catalitzador, estabilitza ribosomes membrana, ac nuclèics • Na, K i Cl ions dissolts, impuls nerviós, estomes. . .

Oligoelements (0. 5% del total)

Biomolècules inorgàniques es troben a la matèria viva i inert Aigua Sals minerals Gassos
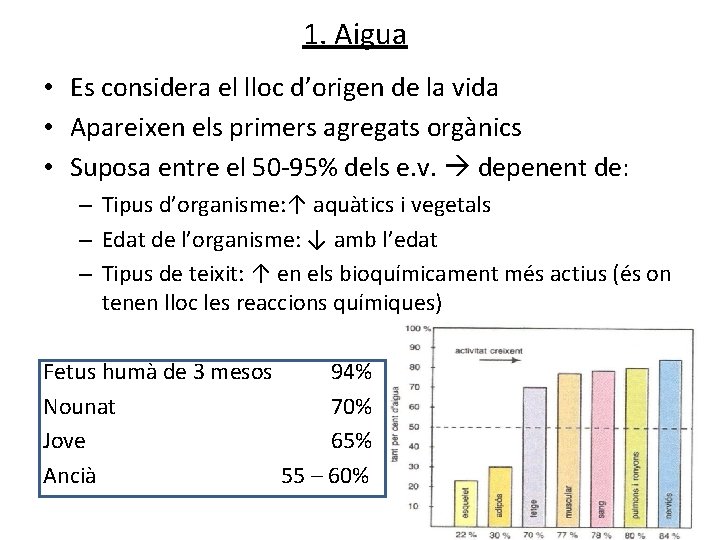
1. Aigua • Es considera el lloc d’origen de la vida • Apareixen els primers agregats orgànics • Suposa entre el 50 -95% dels e. v. depenent de: – Tipus d’organisme: ↑ aquàtics i vegetals – Edat de l’organisme: ↓ amb l’edat – Tipus de teixit: ↑ en els bioquímicament més actius (és on tenen lloc les reaccions químiques) Fetus humà de 3 mesos 94% Nounat 70% Jove 65% Ancià 55 – 60%
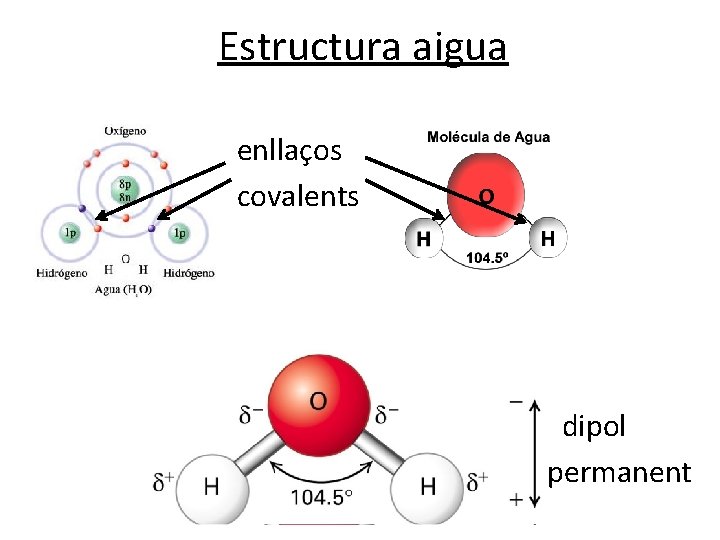
Estructura aigua • • enllaços covalents dipol permanent
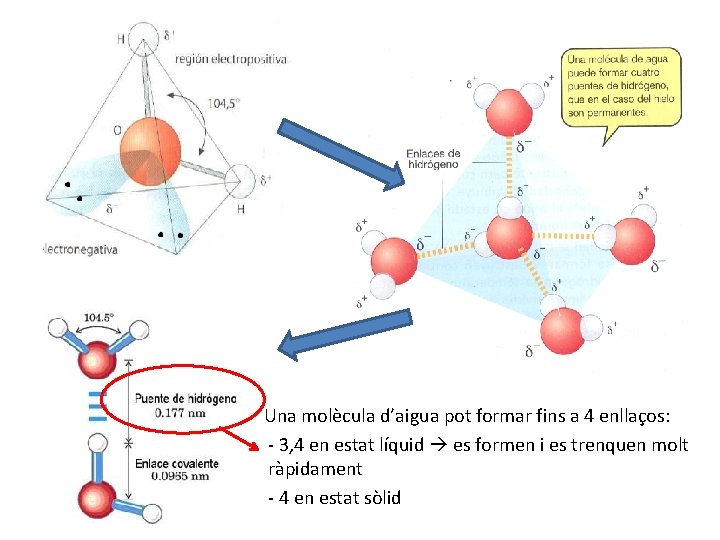
» » » Una molècula d’aigua pot formar fins a 4 enllaços: - 3, 4 en estat líquid es formen i es trenquen molt ràpidament - 4 en estat sòlid
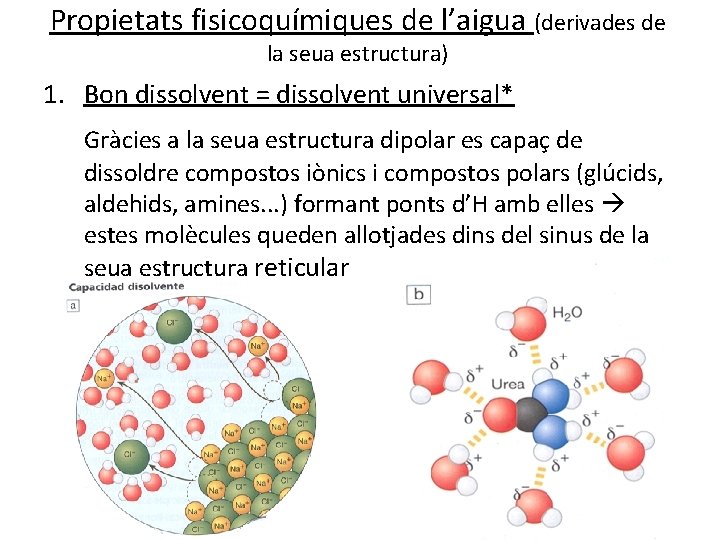
Propietats fisicoquímiques de l’aigua (derivades de la seua estructura) 1. Bon dissolvent = dissolvent universal* Gràcies a la seua estructura dipolar es capaç de dissoldre compostos iònics i compostos polars (glúcids, aldehids, amines. . . ) formant ponts d’H amb elles estes molècules queden allotjades dins del sinus de la seua estructura reticular

• Segons si es poden dissoldre en aigua o no: • Hidrofíliques (polars) • Hidrofòbiques (apolars) • Amfipàtiques: tenen regions polars i apolars (ac grassos) • Permet (importància biològica): – És el medi on transcorren la majoria de reaccions del metabolisme – Absorció d’elements del sòl (dissolts a l’aigua) a través de l’arrel de la planta – Circulació de substàncies dissoltes per tot l’organisme – Expulsar substàncies tòxiques dissoltes a l’orina – Dissol també gasos com l’O 2 (per a la respiració aquàtica) i CO 2 (per a la fotosíntesi dins l’aigua)

2. Dilatació anòmala de l’aigua A diferència d’altres substàncies l’aigua sòlida és menys densa que l’aigua líquida (i per això el gel sura damunt de l’aigua)
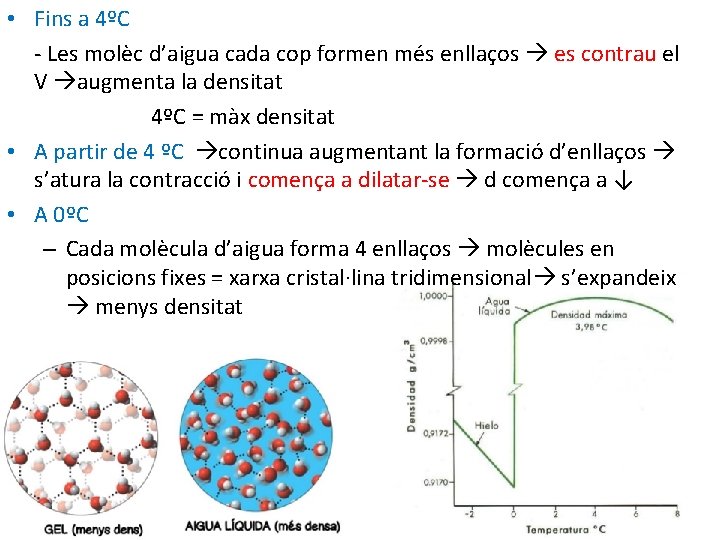
• Fins a 4ºC - Les molèc d’aigua cada cop formen més enllaços es contrau el V augmenta la densitat 4ºC = màx densitat • A partir de 4 ºC continua augmentant la formació d’enllaços s’atura la contracció i comença a dilatar-se d comença a ↓ • A 0ºC – Cada molècula d’aigua forma 4 enllaços molècules en posicions fixes = xarxa cristal·lina tridimensional s’expandeix menys densitat
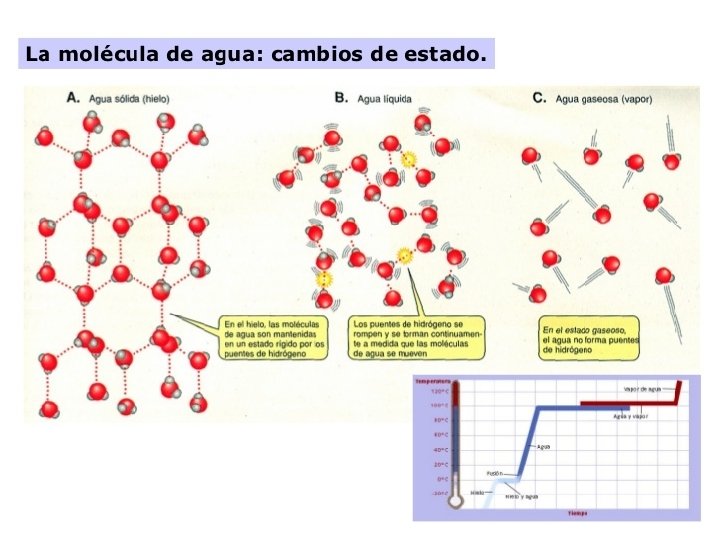


• Permet que la vida continue per baix d’un llac gelat xq no s’enfonsa i xq a més fa d'aïllant tèrmic

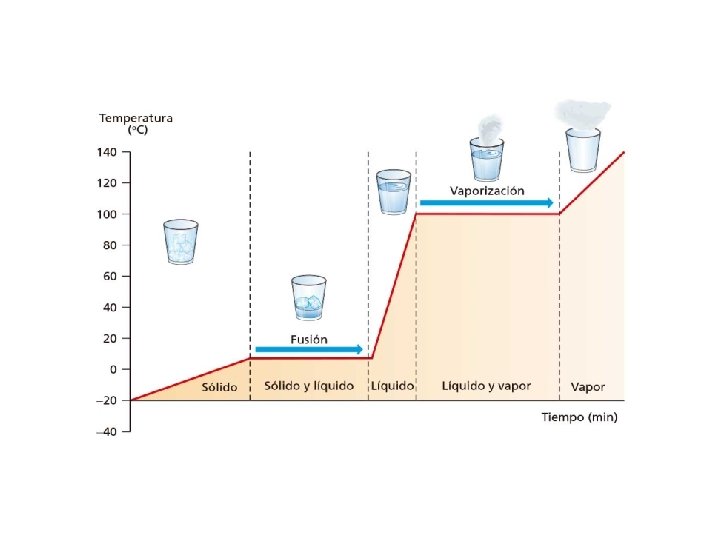
3. Calor específica elevada És la quantitat de calor que hi ha que a portar a 1 g d’aigua per a pujar la Tª 1ºC L’aigua té una calor específica de 1 cal/g ºC Es capaç d'absorbir (o perdre) molta calor sense augmentar (o disminuir) la Tª xq la que emprarà per a trencar els enllaços intermolec (ponts d’H) abans que per a pujar la temperatura grans canvis de calor quasi sense canvi de temperatura Bon amortidor tèrmic = evita canvis bruscos de temperatura Ex: citoplasma
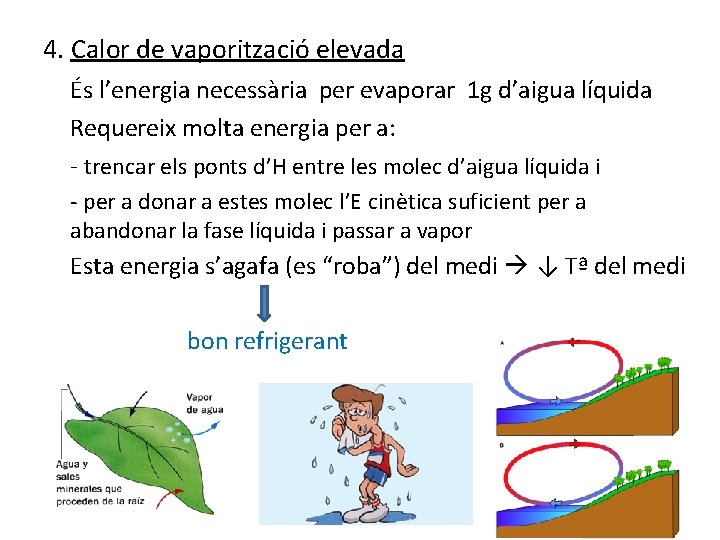
4. Calor de vaporització elevada És l’energia necessària per evaporar 1 g d’aigua líquida Requereix molta energia per a: - trencar els ponts d’H entre les molec d’aigua líquida i - per a donar a estes molec l’E cinètica suficient per a abandonar la fase líquida i passar a vapor Esta energia s’agafa (es “roba”) del medi ↓ Tª del medi bon refrigerant
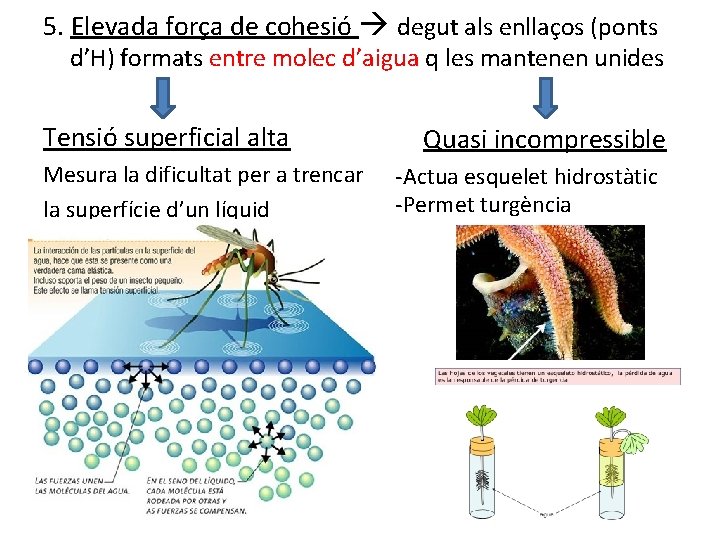
5. Elevada força de cohesió degut als enllaços (ponts d’H) formats entre molec d’aigua q les mantenen unides Tensió superficial alta Mesura la dificultat per a trencar la superfície d’un líquid Quasi incompressible -Actua esquelet hidrostàtic -Permet turgència

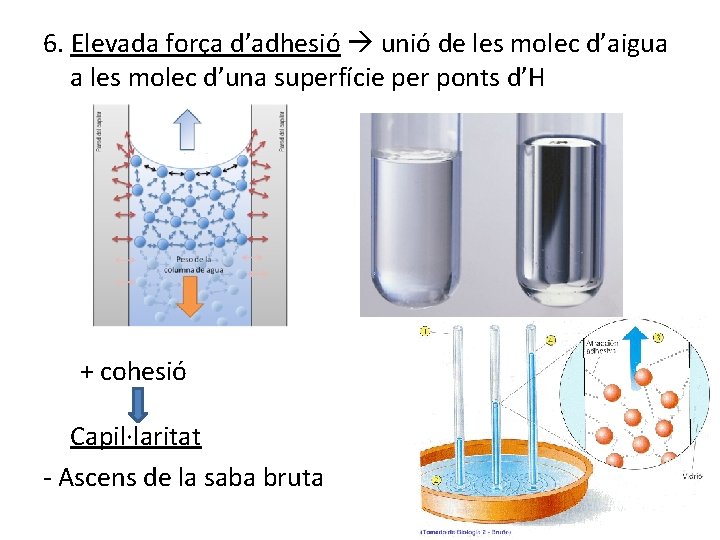
6. Elevada força d’adhesió unió de les molec d’aigua a les molec d’una superfície per ponts d’H + cohesió Capil·laritat - Ascens de la saba bruta

7. Dissociació de l’aigua - L’aigua és capaç de dissociar-se en ions (ionitzar-se) degut a les forces dels ponts d’H entre elles: Per açò, químicament NO és una substància pura - Ara bé la capacitat de ionització de l’aigua és molt baixa: de cada 107 molec, sols 1 es troba ionitzada Producte iònic (KW) a 25ºC: - Si varia qualsevol dels dos ions (afegint un àcid H+ o una base OH-) suposaria una variació de l’altre per a que el producte continue constant
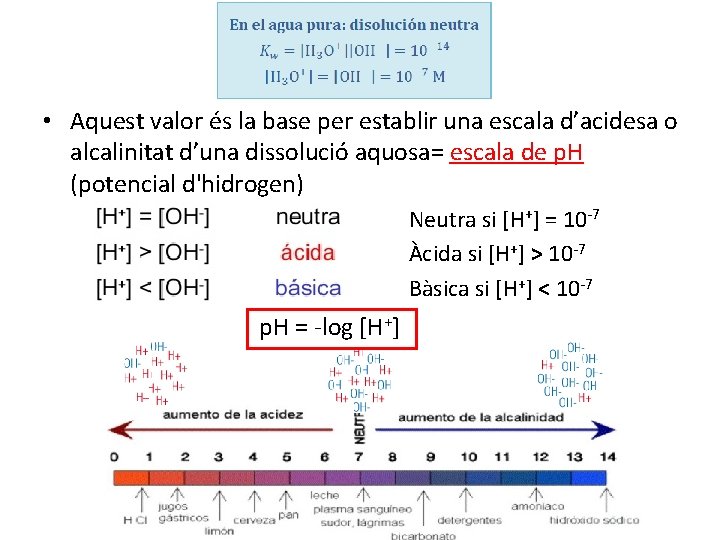
• Aquest valor és la base per establir una escala d’acidesa o alcalinitat d’una dissolució aquosa= escala de p. H (potencial d'hidrogen) Neutra si [H+] = 10 -7 Àcida si [H+] > 10 -7 Bàsica si [H+] < 10 -7 p. H = -log [H+]

2. Sals minerals 2. 1 Sòlides o precipitades (insolubles en aigua) – Carbonat càlcic FUNCIÓ: forma estructures dures: • Closques de gasteròpodes i bivalves, coralls, crustacis, diatomees, ossos. . . – Fosfat càlcic FUNCIÓ: esquelètica=forma els ossos 2. 2 Dissoltes (solubles en aigua) es troben dissociades en els seus ions corresponents (electròlits): – Anions (-): Cl-, HCO 3 -… – Cations (+): K+, Na+, Mg 2+ , Ca 2+

• FUNCIONS de les sals dissoltes: 1. Funció tamponadora = Regulació del p. H Mantenen el p. H cte (dins i fora de la cèl·lula) sistemes tampó o buffer: ü Mantenen els valor de p. H cte (amortigüen els canvis de p. H) ü Formats per una dissolució d’àcid dèbil – base conjugada que actuen com a dador de H+ (l’àcid) i acceptor de H+ (base) ü Les proteïnes també són capaces de tamponar ü Els més comuns als éssers vius són: § tampó bicarbonat § tampó fosfat
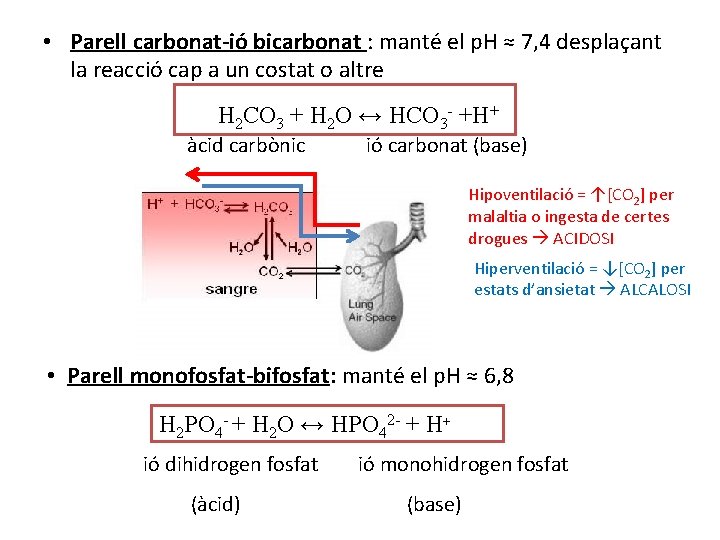
• Parell carbonat-ió bicarbonat : manté el p. H ≈ 7, 4 desplaçant la reacció cap a un costat o altre H 2 CO 3 + H 2 O ↔ HCO 3 - +H+ àcid carbònic ió carbonat (base) Hipoventilació = ↑[CO 2] per malaltia o ingesta de certes drogues ACIDOSI Hiperventilació = ↓[CO 2] per estats d’ansietat ALCALOSI • Parell monofosfat-bifosfat: manté el p. H ≈ 6, 8 H 2 PO 4 - + H 2 O ↔ HPO 42 - + H+ ió dihidrogen fosfat (àcid) ió monohidrogen fosfat (base)

• 2. Funcions catalítiques: – – Com cofactors enzimàtics Cu, Mn, Mg, Zn Formen part de proteïnes Fe (Hb i Mb) Mg (clorofil·la) Contracció muscular i coagulació de la sang Mg Impuls nerviós (Ca) • 3. Funcions nutrients – Els organismes autòtrofs utilitzen algunes als com NO 3 -, SO 4 -2, PO 4 -3 per a sintetitzar compostos orgànics • 4. Funcions osmòtiques – Processos relacionats en la distribució de l’aigua dins i fora de les cèl·lules Na+, K+, Cl- i Ca+2
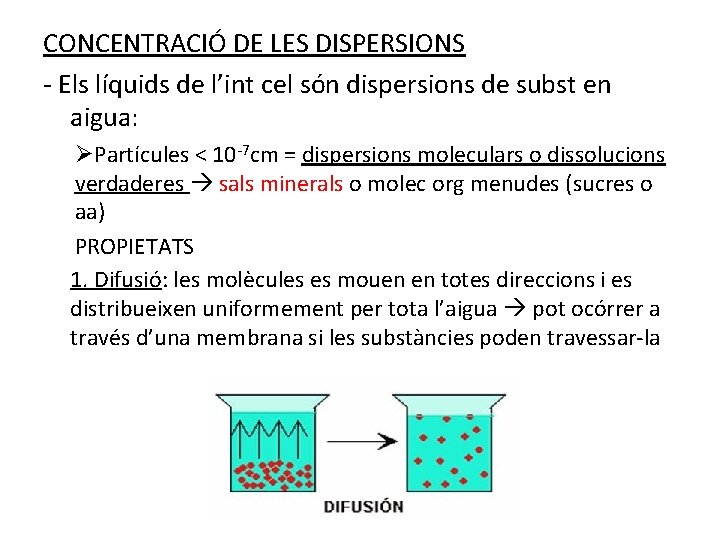
CONCENTRACIÓ DE LES DISPERSIONS - Els líquids de l’int cel són dispersions de subst en aigua: ØPartícules < 10 -7 cm = dispersions moleculars o dissolucions verdaderes sals minerals o molec org menudes (sucres o aa) PROPIETATS 1. Difusió: les molècules es mouen en totes direccions i es distribueixen uniformement per tota l’aigua pot ocórrer a través d’una membrana si les substàncies poden travessar-la
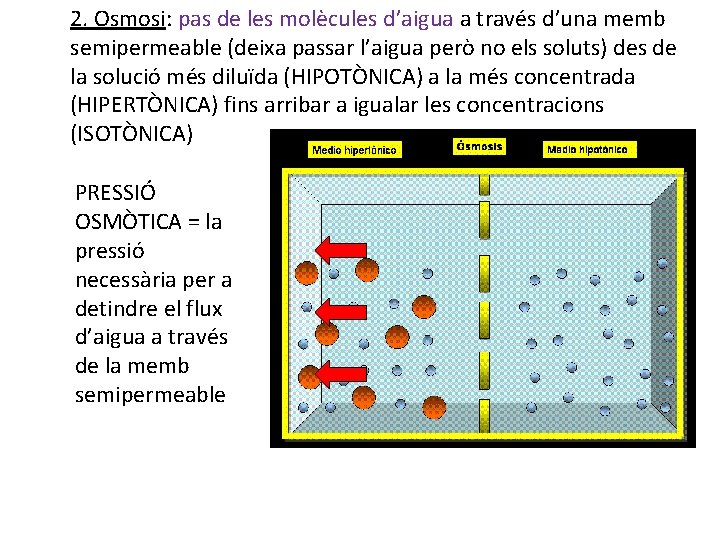
2. Osmosi: pas de les molècules d’aigua a través d’una memb semipermeable (deixa passar l’aigua però no els soluts) des de la solució més diluïda (HIPOTÒNICA) a la més concentrada (HIPERTÒNICA) fins arribar a igualar les concentracions (ISOTÒNICA) PRESSIÓ OSMÒTICA = la pressió necessària per a detindre el flux d’aigua a través de la memb semipermeable

La mb plasmàtica és semipermeable → hi ha que mantindre una concentració de sals dins de la cèl·lula igual a la del medi extern per a que no hi haja guany ni pèrdua d’aigua. Si introduïm la cèl·lula en: MEDI HIPOTÒNIC CÈL·LULA ANIMAL • Entra aigua a la cèl·lula → s’infla MEDI HIPERTÒNIC CÈL·LULA ANIMAL • → ↓ el seu VOLUM= PLASMÒLISI fins a rebentar → LISI CÈL·LULA VEGETAL • • Ix aigua de la cèl·lula → s'encongeix • La cèl·lula es DESHIDRATA i perd les seus funcions fisiològiques Entra aigua a la cèl·lula → s’infla però NO SE LISA → la rígida paret CÈL·LULA VEGETAL cel·lular ho impedeix. • Ix aigua de la cèl·lula → s’encongeix, La pressió de la cèl·lula espentant allunyant-se de la paret cel·lular, el contra la paret s’anomena pressió resultat és la PLASMÒLISI de TURGÈNCIA. • La cèl·lula queda deshidratada i perd les seus funcions fisiològiques.
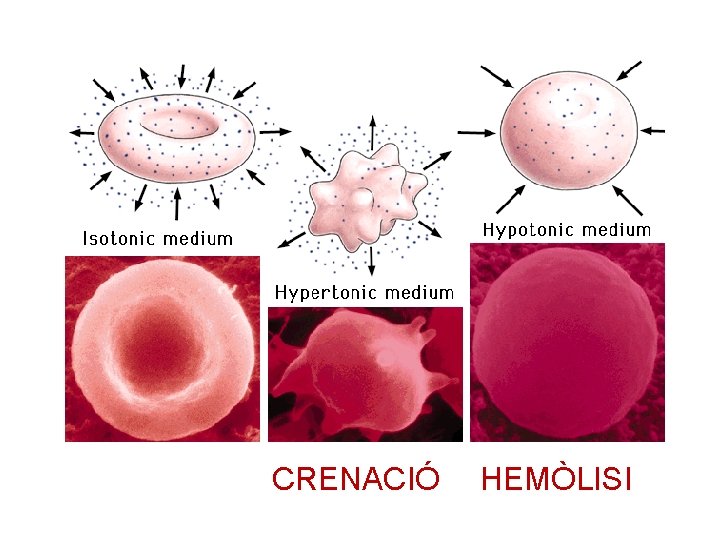
CRENACIÓ HEMÒLISI

ØPartícules entre 10 -5 i 10 -7 cm = dispersions col·loïdals molèc org grans (polisacàrids, prot, ac nuclèics) PROPIETATS: 1. Podem trobar-les en 2 estats: ü Sol = aspecte líquid perifèria del citoplasma = ectoplasma ü Gel = aspecte sòlid centre del citoplasma=endoplasma Es pot passar d’un estat a altre creació de pseudòpodes 2. Elevada viscositat 3. Elevat poder adsorbent atracció que exerceix un sòlid sobre les molèc d’un líquid o gas: Ag-Ac, EZ-substrat 4. Efecte Tyndall: si les dispersions s'il·luminen lateralment sobre fons fosc s’observa opalescència per la reflexió dels raigs de llum (els col·loides dispersen la llum)
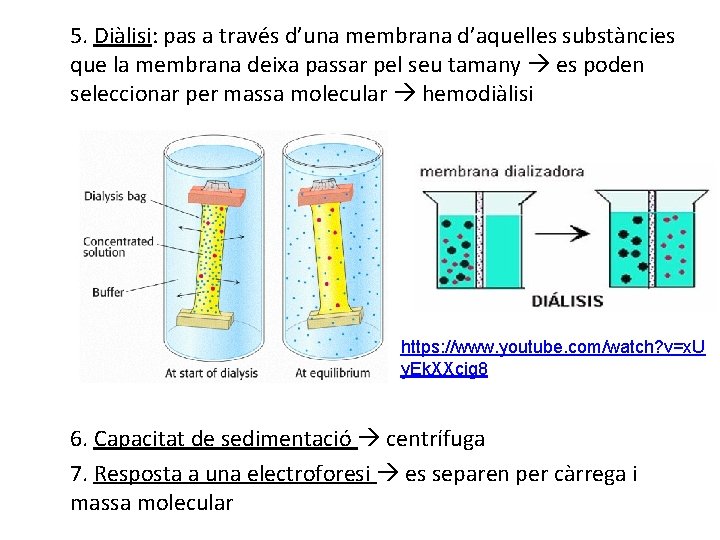
5. Diàlisi: pas a través d’una membrana d’aquelles substàncies que la membrana deixa passar pel seu tamany es poden seleccionar per massa molecular hemodiàlisi https: //www. youtube. com/watch? v=x. U y. Ek. XXcig 8 6. Capacitat de sedimentació centrífuga 7. Resposta a una electroforesi es separen per càrrega i massa molecular
- Slides: 37