tomo e Modelos Atmicos Professora Vernica Prodssimo Cabral

Átomo e Modelos Atómicos Professora: Verônica Prodóssimo Cabral
Demócrito (Sec. V a. c. ) defendeu a ideia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 – 370 A. C. ) Modelo baseado apenas na intuição e na lógica.
Modelo proposto por Demócrito: Toda a matéria é constituída por átomos e vazio; O átomo é uma partícula pequeníssima, invisível, e que não pode ser dividida; Os átomos encontram-se em constante movimento; Universo constituído por um número infinito de átomos, indivisíveis e eternos;

Modelo proposto por Dalton: A matéria é composta por pequenos corpúsculos, que não se subdividem – os Átomos; Os átomos do mesmo elemento são iguais entre si – têm a mesma massa; A matéria é formada pela união de diferentes átomos em proporções definidas. Átomo

Thomson(1904) Descobriu o elétron Thomson realizou uma série de experiências utilizando um tubo de raios catódicos (tubo semelhante aos tubos existentes no interior dos televisores). Neste tubo, eram efectuadas descargas eléctricas através de um gás rarefeito. J. J. Thomson (1856 - 1940) Tubo de raios catódicos

Os raios catódicos movimentam um molinete ou catavento de mica, permitindo concluir que são dotados de massa.
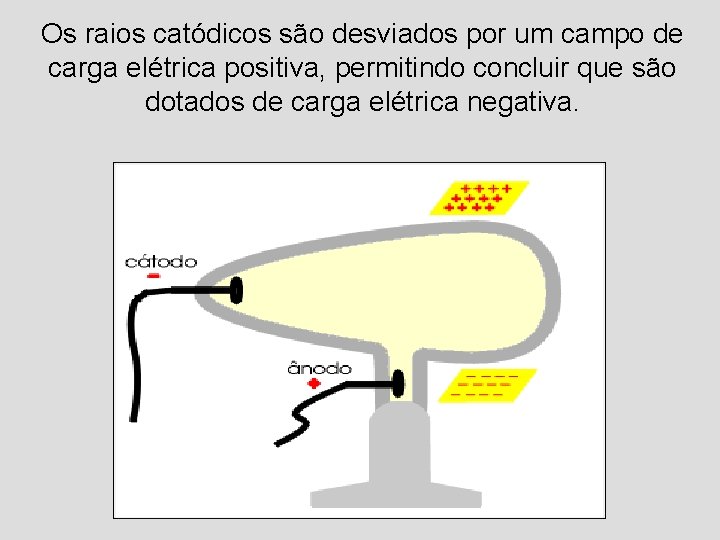
Os raios catódicos são desviados por um campo de carga elétrica positiva, permitindo concluir que são dotados de carga elétrica negativa.
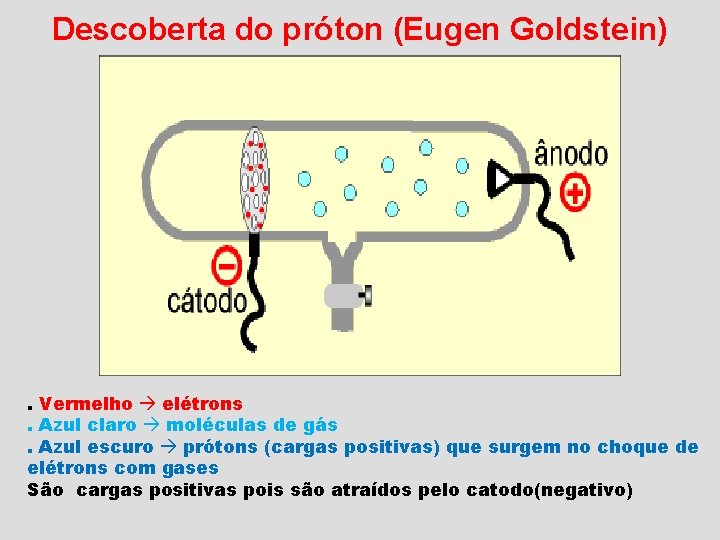
Descoberta do próton (Eugen Goldstein) . Vermelho elétrons. Azul claro moléculas de gás. Azul escuro prótons (cargas positivas) que surgem no choque de elétrons com gases São cargas positivas pois são atraídos pelo catodo(negativo)
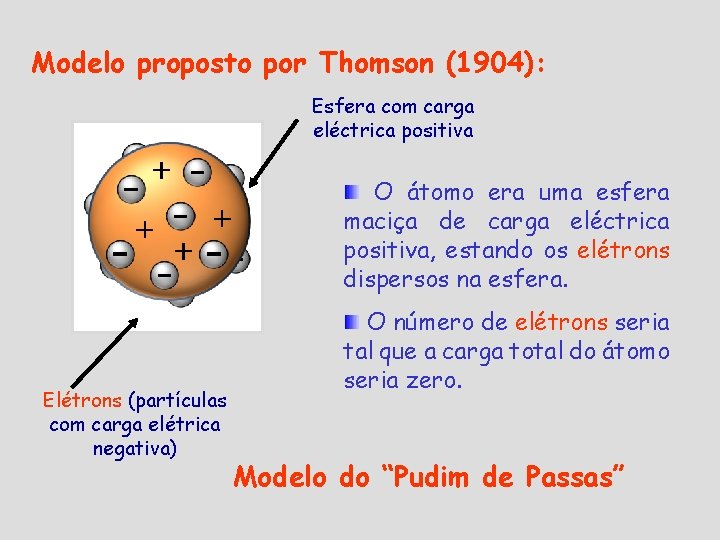
Modelo proposto por Thomson (1904): Esfera com carga eléctrica positiva O átomo era uma esfera maciça de carga eléctrica positiva, estando os elétrons dispersos na esfera. Elétrons (partículas com carga elétrica negativa) O número de elétrons seria tal que a carga total do átomo seria zero. Modelo do “Pudim de Passas”

Rutherford (1911) Cientista neozelandês, estudou com J. J. Thomson. Ernest Rutherford (1871 - 1937) Em 1908 realizou uma experiência que lhe permitiu propor um novo modelo atómico.
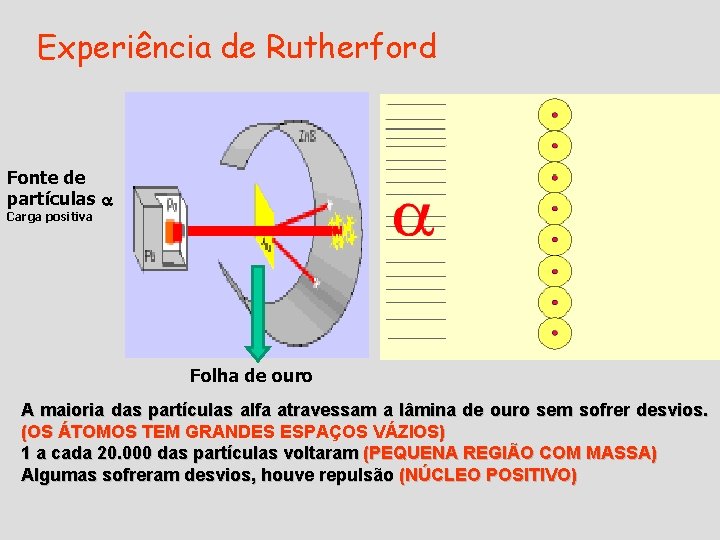
Experiência de Rutherford Fonte de partículas Carga positiva Folha de ouro A maioria das partículas alfa atravessam a lâmina de ouro sem sofrer desvios. (OS ÁTOMOS TEM GRANDES ESPAÇOS VÁZIOS) 1 a cada 20. 000 das partículas voltaram (PEQUENA REGIÃO COM MASSA) Algumas sofreram desvios, houve repulsão (NÚCLEO POSITIVO)

Descoberta do nêutron (Chadwick) O choque de dois núcleos liberaram partículas que não foram atraídas nem pelo polo (-) e nem pelo (+), então esta partícula não tem carga (NEUTRON)
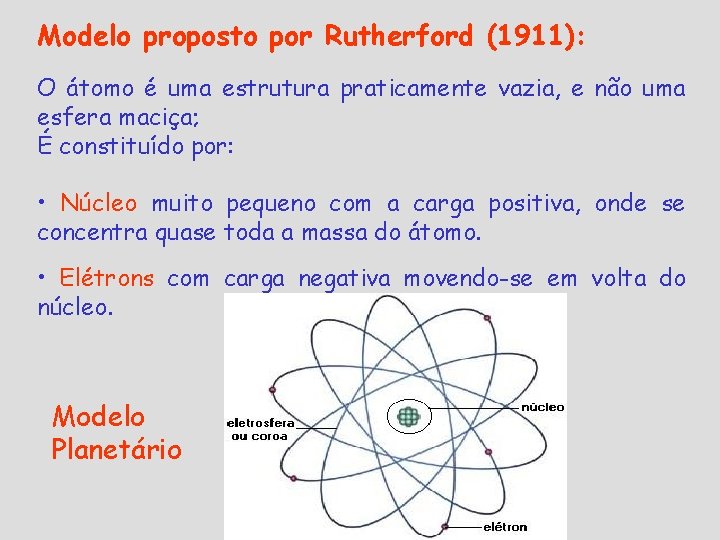
Modelo proposto por Rutherford (1911): O átomo é uma estrutura praticamente vazia, e não uma esfera maciça; É constituído por: • Núcleo muito pequeno com a carga positiva, onde se concentra quase toda a massa do átomo. • Elétrons com carga negativa movendo-se em volta do núcleo. Modelo Planetário

Bohr (1913) 1º postulado: Os elétrons descrevem órbitas circulares estacionárias ao redor do núcleo, sem emitirem nem absorverem energia. Niels Bohr (1885 - 1962)

Bohr (1913) Niels Bohr (1885 - 1962) 2º postulado: Fornecendo energia a um átomo, um ou mais elétrons a absorvem e saltam para níveis mais afastados do núcleo. Ao voltarem as suas órbitas originais, devolvem a energia recebida em forma de luz


Evolução do Modelo atómico… Modelo de Dalton BOLA DE BILHAR Modelo de Thomson PUDIM DE PASSAS Modelo de Rutherford Modelo de Bohr PLANETÁRIO NÍVEIS DE ENERGIA
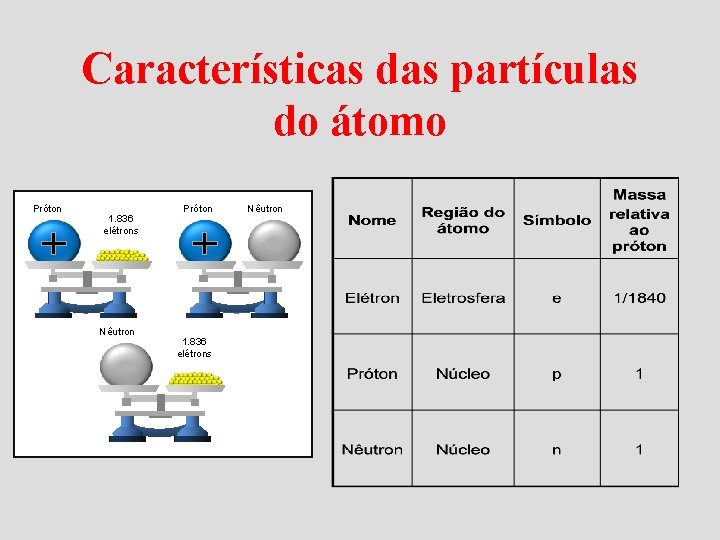
Características das partículas do átomo Próton 1. 836 elétrons Nêutron

“Fotografar” os átomos. . . Hoje em dia dispomos de potentes microscópios que nos permitem obter imagens dos átomos: são os microscópios electrónicos.

Dimensão dos átomos Um ponto final pode conter mais de 3 milhões de átomos.
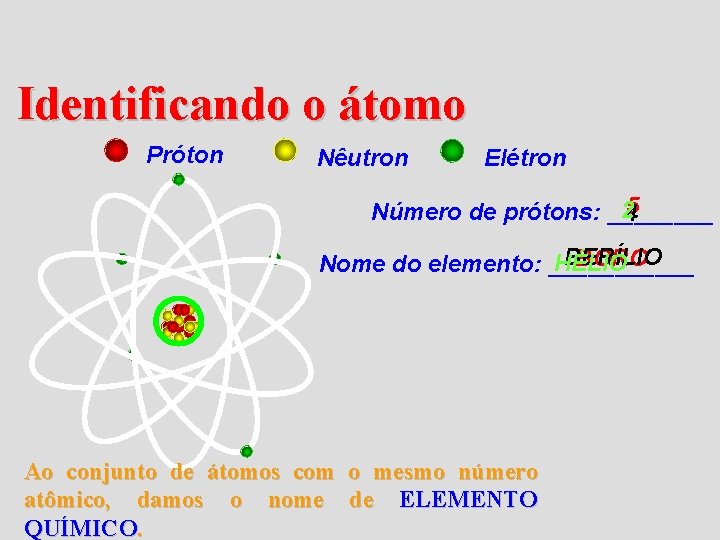
Identificando o átomo Próton Nêutron Elétron 5 24 Número de prótons: ____ BERÍLIO BORO HÉLIO Nome do elemento: ______ Ao conjunto de átomos com o mesmo número atômico, damos o nome de ELEMENTO QUÍMICO.
- Slides: 21