TOMA DE MUESTRAS EN MICROBIOLOGIA IMPORTANCIA EN EL

TOMA DE MUESTRAS EN MICROBIOLOGIA: IMPORTANCIA EN EL DIAGNÓSTICO DE LAS INFECCIONES Dra. Montserrat Ruiz García S. Microbiología Hospital General Universitario de Elche Seminario 17 de marzo de 2014

Manual de toma de muestras: Autores • Sociedad valenciana Clínica (SVAMC) – – – – – de Ana Lloret Caballería (Coordinadora) Manuel Canós Cabedo Concepción Gimeno Cardona Damiana González Granda Pilar López García Jose Miguel Nogueira Coito Victoria Ortiz de la Tabla Ducasse Gloria Royo García Alberto Yagüe Muñoz • Consellería de Sanitat – Francisca Almenar Roig – Gregorio Gómez Soriano Microbiología
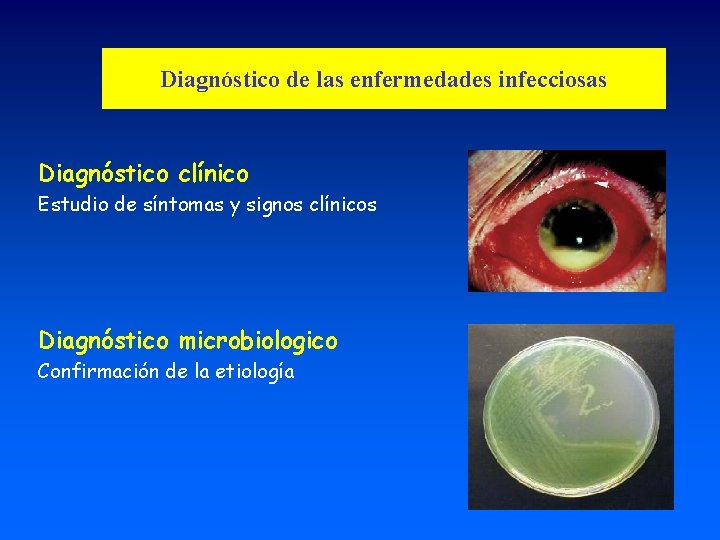
Diagnóstico de las enfermedades infecciosas Diagnóstico clínico Estudio de síntomas y signos clínicos Diagnóstico microbiologico Confirmación de la etiología

Diagnóstico microbiológico de las enfermedades infecciosas • Demostración de la presencia del microorganismo • De sus productos • De la respuesta inmune

Toma de muestras “Toda al información diagnóstica que el laboratorio de Microbiología puede proporcionar, DEPENDE DE LA CALIDAD DE LA MUESTRA RECIBIDA”

Toma de muestras en Microbiología El término calidad incluye – Muestra apropiada – Bien recogida – Transporte adecuado

Toma de muestras en Microbiología Indicadores de nivel de calidad (FASE PREANALÍTICA) – Número de muestras rechazadas – Muestras contaminadas – Adecuación de las peticiones a las muestras

“Es IMPRESCINDIBLE la comunicación entre el personal sanitario y Microbiología para optimizar la toma de muestras y aumentar la calidad en la fase preanalítica”

VOLANTE DE PETICIÓN DATOS DEL PACIENTE Filiación y datos administrativos Para evitar errores, es importante utilizar etiquetas con CÓDIGO DE BARRAS y comprobar que la etiqueta del volante coincide con la de la muestra



Manual de toma de muestras: objetivo • El objetivo de este Manual es hacer recomendaciones sobre: – – Muestras más adecuadas Forma de recogida Transporte Conservación • Señalando: – – – El material necesario La técnica de obtención El volumen Número de muestras Modo de transporte según características de las muestras o microorganismos a investigar

CRITERIOS DE RECHAZO DE MUESTRAS OBJETIVOS • Evitar el informe de resultados con escaso o nulo valor, o que provoquen confusión acerca del diagnóstico y tratamiento del paciente • Prevenir los problemas de seguridad biológica que se puedan producir en el personal del laboratorio

CRITERIOS DE RECHAZO • Muestra no etiquetada de forma que pueda llevar a la confusión • Transporte/almacenamiento inadecuado • Tiempo excesivo desde la toma de la muestra • Contenedor inadecuado, roto o no estéril

CRITERIOS DE RECHAZO • Muestras contaminación exterior evidente • Muestras no adecuadas a la petición solicitada • Cantidad insuficiente • Muestra previamente manipulada • Suero en tubo no primario

VOLANTE DE PETICIÓN DATOS DE LA MUESTRA • Fecha de obtención • Naturaleza del producto • Localización exacta de la toma • Procedimiento de extracción • Indicar si se ha aplicado alguna técnica especial: punción vesical, etc.

VOLANTE DE PETICIÓN DATOS CLÍNICO-EPIDEMIOLÓGICOS • Fecha de comienzo de la enfermedad • Sospecha diagnóstica • Estado inmunitario • Tto. antibiótico, aunque lo ideal es recoger la muestra antes de iniciarlo

VOLANTE DE PETICIÓN ÁREA PARA LA SOLICITUD • Determinaciones – CULTIVO: Bacterias Hongos Mycobacterias Anaerobios Mycoplasmas – VIRUS – SEROLOGÍA • Indicar la sospecha de microorganismos poco habituales o exigentes – – – Nocardia Vibrio cholerae Actinomyces Brucella Legionella



CARACTERISTICAS ESPECIALES DE LA TOMA DE MUESTRAS EN MICROBIOLOGIA

OBTENCIÓN DE LA MUESTRA GENERALIDADES • Sitio exacto de la lesión • Aplicar precauciones universales • Máximas condiciones contaminaciones de asepsia para • No poner en contacto con desinfectantes evitar

OBTENCIÓN DE LA MUESTRA GENERALIDADES • Tomar lo antes posible • Antes del tratamiento antibiótico • Recoger preferentemente por aspiración en lugar de hisopos o torundas • Cantidad adecuada • Identificación correcta

UROCULTIVOS • La muestra adecuada es la primera orina de la mañana recogida en un contenedor estéril • Procedimiento: – Lavado de genitales – DESECHAR LA PRIMERA PARTE DE LA MICCIÓN (FLORA URETRAL) – RECOGER LA SEGUNDA PARTE DE LA MICCIÓN • La orina de los niños que no controlan los esfínteres debe recogerse en una bolsa colectora

UROCULTIVOS • El volumen mínimo debe estar entre 1 y 10 ml – Hongos o micobacterias (20 ml) – Parásitos (> 50 ml) • Si no se procesa en una hora, mantener en nevera • En catéteres permanentes no recoger del reservorio, hay que pinchar con una aguja estéril en el catéter

COPROCULTIVOS • Recoger la parte con moco, pus o sangre • Cantidad necesaria: 1 -2 gramos o 5 -10 ml • Si no se procesa en una hora, mantener en nevera; salvo que se sospeche Shigella (en este caso, mantener a temperatura ambiente)

COPROCULTIVOS • Si es necesario recoger hisopos (neonatos o adultos debilitados), utilizar medio de transporte • Solicitar los estudios especiales indicando datos clínicos y/o epidemiológicos: – Clostridium difficile, Vibrio spp, Escherichia coli O 157: H 7

PARÁSITOS EN HECES • Tres muestras de tres días alternos • Volumen: 2 -4 gramos • Si la muestra es líquida, hay que procesarla de inmediato y si es sólida, puede mantenerse a 4ºC • Indicar datos epidemiológicos (viajes, residencia en el extranjero, etc) • OXIUROS: Técnica de Graham (colocación de un celofán transparente en los bordes del ano y después adherir en un porta de cristal).
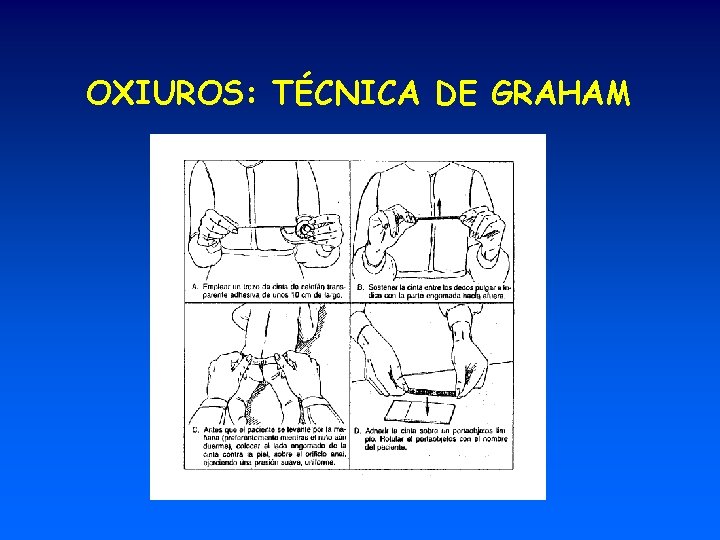
OXIUROS: TÉCNICA DE GRAHAM

EXTRACCIÓN DE HEMOCULTIVOS

HEMOCULTIVOS 1. - Rotular los frascos con las etiquetas del paciente, indicando si es la 1ª o la 2ª extracción 2. - Desinfección de los tapones de los frascos con un antiséptico 3. - Seleccionar la vena y desinfectar la zona de venipunción en círculos excéntricos, primero con etanol 70º(30 segundos), luego con povidona iodada (1 minuto). Dejar secar un minuto

HEMOCULTIVOS 4. - Utilizar guantes estériles para la extracción de sangre 5. - Inocular en cada frasco: aerobio (color azul) y anaerobio (color dorado) el volumen adecuado de sangre (8 ml) comenzando por el frasco anaerobio 6. - Agitar suavemente el frasco y enviarlo inmediatamente al servicio de Microbiología. En el laboratorio de Microbiología se deben introducir en la estufa de 37ºC.

FRASCOS DE HEMOCULTIVOS
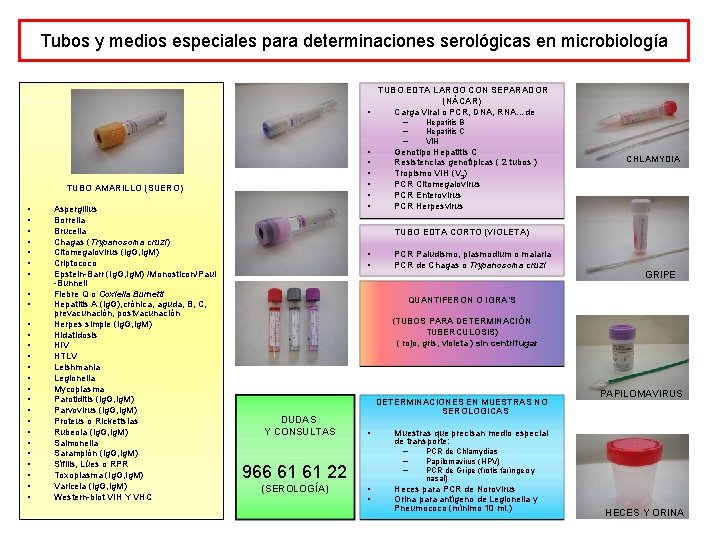
Tubos y medios especiales para determinaciones serológicas en microbiología TUBO EDTA LARGO CON SEPARADOR (NÁCAR) • Carga Viral o PCR, DNA, RNA…de – – – • • • TUBO AMARILLO (SUERO) • • • • • • • Aspergillus Borrelia Brucella Chagas (Trypanosoma cruzi) Citomegalovirus (Ig. G, Ig. M) Criptococo Epstein-Barr (Ig. G, Ig. M) /Monosticon/Paul -Bunnell Fiebre Q o Coxiella Burnetti Hepatitis A (Ig. G), crónica, aguda, B, C, prevacunación, postvacunación Herpes simple (Ig. G, Ig. M) Hidatidosis HIV HTLV Leishmania Legionella Mycoplasma Parotiditis (Ig. G, Ig. M) Parvovirus (Ig. G, Ig. M) Proteus o Rickettsias Rubeola (Ig. G, Ig. M) Salmonella Sarampión (Ig. G, Ig. M) Sífilis, Lúes o RPR Toxoplasma (Ig. G, Ig. M) Varicela (Ig. G, Ig. M) Western-blot VIH Y VHC Hepatitis B Hepatitis C VIH Genotipo Hepatitis C Resistencias genotípicas ( 2 tubos ) Tropismo VIH (V 3) PCR Citomegalovirus PCR Enterovirus PCR Herpesvirus CHLAMYDIA TUBO EDTA CORTO (VIOLETA) • • PCR Paludismo, plasmodium o malaria PCR de Chagas o Trypanosoma cruzi GRIPE QUANTIFERON O IGRA’S (TUBOS PARA DETERMINACIÓN TUBERCULOSIS) ( rojo, gris, violeta ) sin centrifugar DUDAS Y CONSULTAS DETERMINACIONES EN MUESTRAS NO SEROLOGICAS • (SEROLOGÍA) Muestras que precisan medio especial de transporte: – – – 966 61 61 22 • • PAPILOMAVIRUS PCR de Chlamydias Papilomavirus (HPV) PCR de Gripe (frotis faríngeo y nasal) Heces para PCR de Norovirus Orina para antígeno de Legionella y Pneumococo (mínimo 10 ml. ) HECES Y ORINA

TRACTO RESPIRATORIO • Superior: Exudado faringo-amigdalino – Utilizar medio de transporte – Amígdalas y faringe posterior – No tocar boca, lengua o úvula • Inferior: Esputo – Primera hora de la mañana en envase estéril – Enjuagar la boca con agua – Expectoración profunda, no saliva – Si el procesamiento se retrasa más de una hora: nevera – No almacenar más de un día

TRACTO GENITAL • Exudado vaginal – Utilizar torundas con medio de transporte – No refrigerar. Almacenar a temperatura ambiente o en estufa a 37ºC – Si hay sospecha de gonococo, Chlamydias o Mycoplasmas, obtener un exudado endocervical • Exudado uretral: – Utilizar torundas con medio de transporte – No refrigerar. Almacenar a temperatura ambiente o en estufa a 37ºC – Tomar antes de la primera micción de la mañana o después de una hora de la última micción


PIEL Y TEJIDOS BLANDOS • Ulceras y heridas – Lavar previamente con suero fisiológico – Recoger la muestra con jeringa y aguja. Si no hay suficiente cantidad, se instila suero fisiológico y se aspira – Si esto no es posible, recoger en torunda • Exantemas: Igual que las úlceras y heridas • Abscesos – Punción aspiración con jeringa y aguja. Inoculación en medio para anaerobios

Laboratorio de Microbiología • • Jefe de Sección: Dra. Gloria Royo García Facultativos: – Pilar López García – Victoria Sánchez Hellín – Montserrat Ruiz García • Supervisora: Minerva Conca • Teléfonos: 966 61 61 21 (bacteriología) 966 61 61 22 (serología) 966 61 64 94 (supervisora) • E-mail: micro_elx@gva. es
- Slides: 42