TITULAES CIDOBASE Titulaes cidobase 1 O que 1

TITULAÇÕES ÁCIDO-BASE

Titulações ácido-base 1 O que é? 1 Como se faz? 1 Ponto de equivalência 1 Curvas de titulação 1 Indicadores ácido-base 1 Cálculo da concentração

O que é uma titulação? A titulação é uma operação analítica utilizada em análise volumétrica com o objectivo de determinar a concentração de soluções.

Numa titulação ácido-base. . . ocorre uma reacção completa entre um ácido e uma base (neutralização): ácido + base sal + água por exemplo: HCl(aq) + Na. OH(aq) Na. Cl(aq) + H 2 O(l)

Como se executa uma titulação? Titulação consiste na adição de uma solução de concentração rigorosamente conhecida titulante - a outra solução de concentração desconhecida titulado - até que se atinja o ponto de equivalência.

Titulado é. . . uma solução de concentração desconhecida mas de volume rigorosamente medido que se coloca dentro de um Erlenmeyer (ou goblé).

Titulante é. . . ------- . . . uma solução de concentração conhecida rigorosamente que dentro da bureta. se coloca

Ponto de equivalência é. . . a altura da titulação em que a relação entre o número de moles do titulante adicionadas e o número de moles do titulado é a prevista pela estequiometria da reacção: nácido = nbase

Como se detecta o ponto de equivalência? Existem dois métodos: Potenciométrico Colorimétrico

Método Potenciométrico Durante a titulação introduz-se um eléctrodo de p. H no titulado, o que permite medir o p. H ao longo da titulação e traçar a curva de titulação.
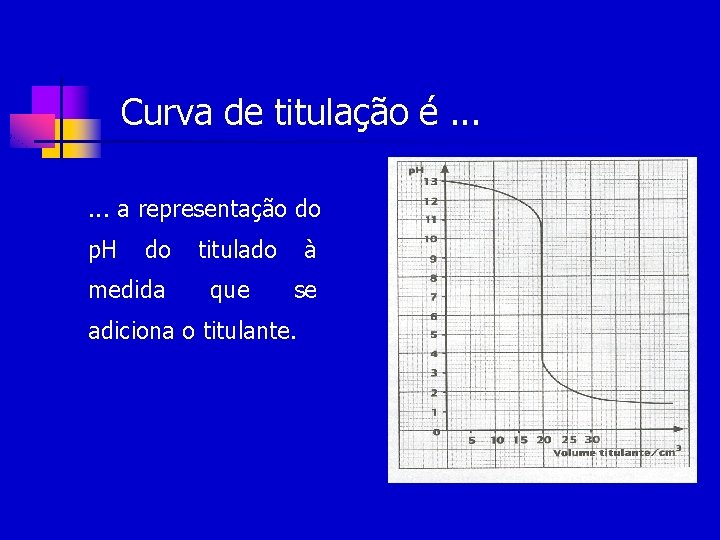
Curva de titulação é. . . a representação do p. H do medida titulado que à se adiciona o titulante.
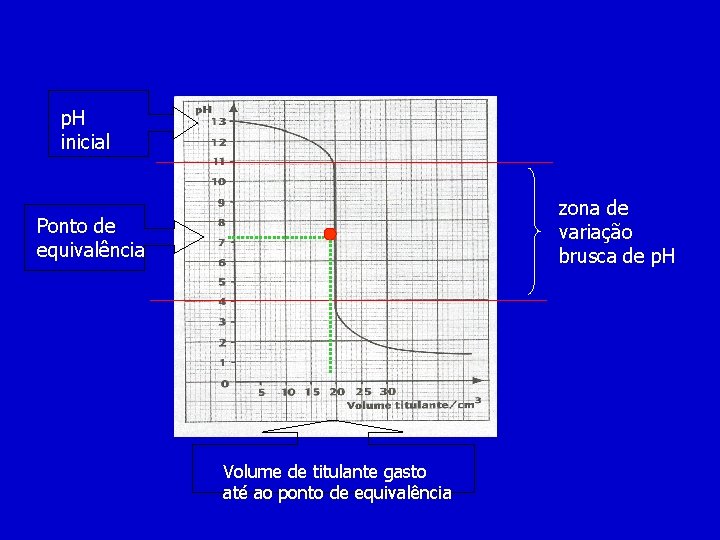
p. H inicial zona de variação brusca de p. H Ponto de equivalência Volume de titulante gasto até ao ponto de equivalência

A curva de titulação permite: ( identificar a titulação ( identificar titulante/titulado ( ler o volume de titulante gasto até ao ponto de equivalência

Identificação da titulação As titulações ácido base podem ser de três tipos: ( Ácido forte-base forte ( Ácido fraco-base forte ( Ácido forte-base fraca e distinguem -se pelo p. H no ponto de equivalência.
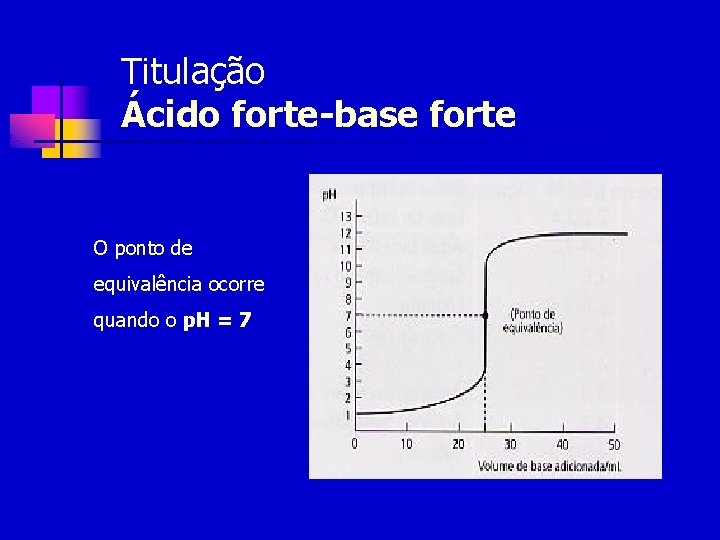
Titulação Ácido forte-base forte O ponto de equivalência ocorre quando o p. H = 7
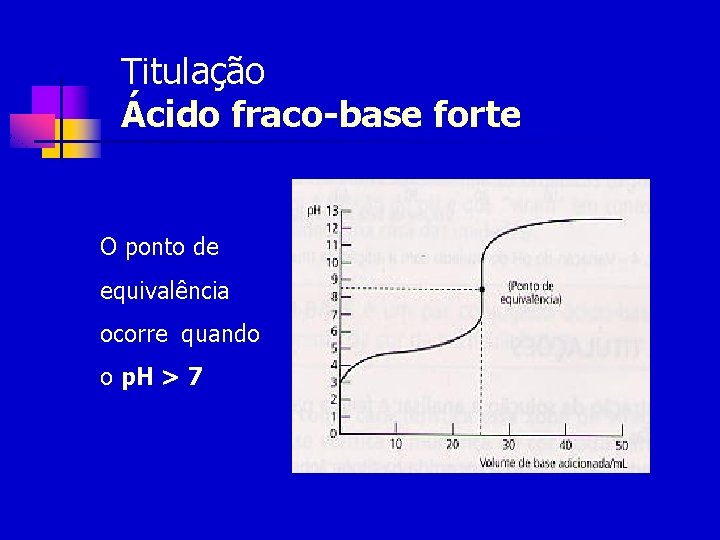
Titulação Ácido fraco-base forte O ponto de equivalência ocorre quando o p. H > 7
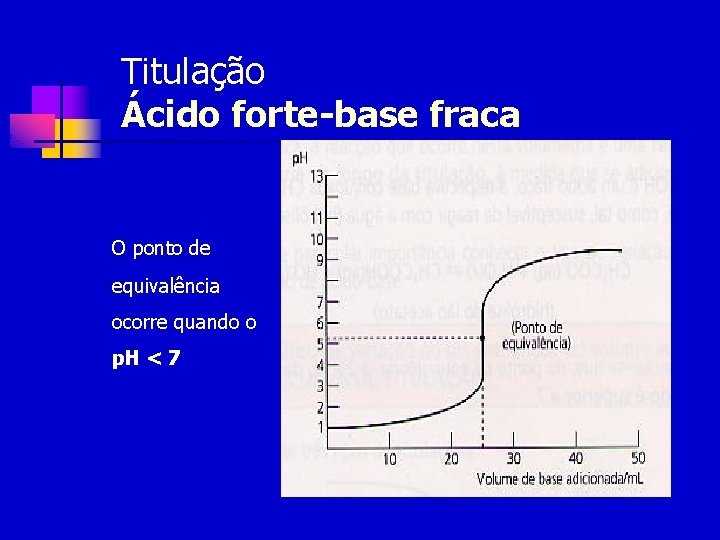
Titulação Ácido forte-base fraca O ponto de equivalência ocorre quando o p. H < 7
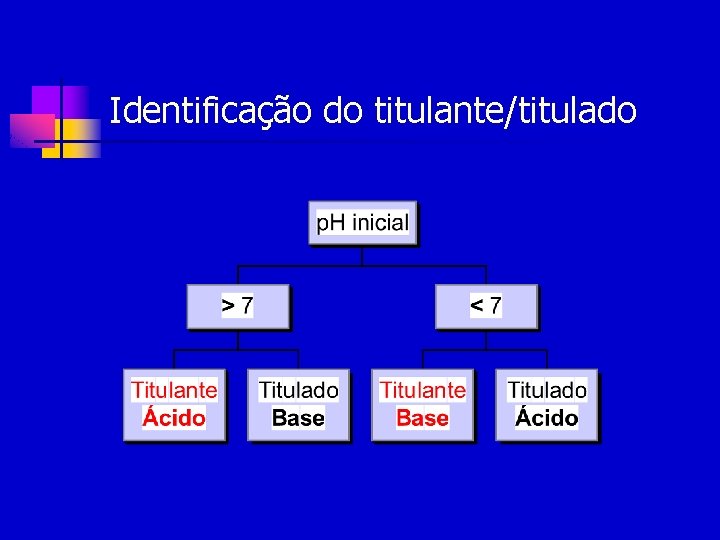
Identificação do titulante/titulado

Método Colorimétrico Adiciona-se ao titulado um indicador ácido-base que muda de cor quando se atinge o ponto de equivalência.

Um indicador ácido-base é. . . uma substância (ácido ou base fraco) que têm a particularidade de apresentar cores diferentes na forma ácida e na forma básica: Hind Ind - + H+

Num meio ácido. . . o equilíbrio desloca-se para a esquerda e a solução apresenta a cor 1 (da espécie Hind). Hind Ind- + H+ Cor 1 Cor 2

Num meio alcalino. . . o equilíbrio desloca-se para a direita e a solução apresenta a cor 2. Hind Ind- + H+ Cor 1 Cor 2

Existe uma gama de valores de p. H nos quais nenhuma das formas do indicador predomina e a cor não é bem definida Zona de viragem de cor do indicador
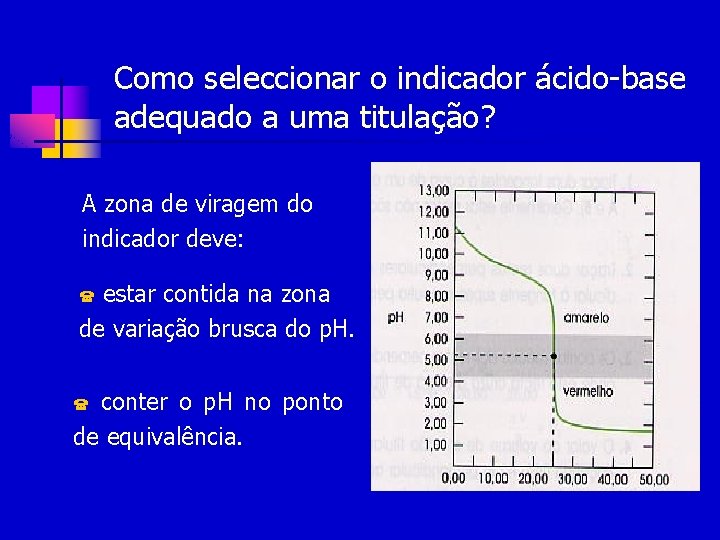
Como seleccionar o indicador ácido-base adequado a uma titulação? A zona de viragem do indicador deve: estar contida na zona de variação brusca do p. H. ( conter o p. H no ponto de equivalência. (

Cálculo da concentração - 1 No início da titulação: Concentração: conhecida, CA Titulante(A) Volume: desconhecido Concentração: desconhecida Titulado(B) Volume: conhecido, VB

Cálculo da concentração - 2 No fim da titulação: Concentração: conhecida, CA Titulante(A) Volume: conhecido, VA Concentração: desconhecida Titulado(B) Volume: conhecido, VB

Cálculo da concentração - 3 Como: C= n/V n=Cx. V Temos no fim da titulação (ponto de equivalência): n. A = n B ou C A x V A= CB x V B
- Slides: 27