Titrasi Asam Basa Dalam titrasi asam basa sejumlah


Titrasi Asam Basa Dalam titrasi asam basa, sejumlah volume tertentu suatu asam atau basa yang telah diketahui konsentrasinya secara pasti direaksikan dengan sejumlah volume tertentu suatu basa atau asam yang konsentrasinya belum diketahui.
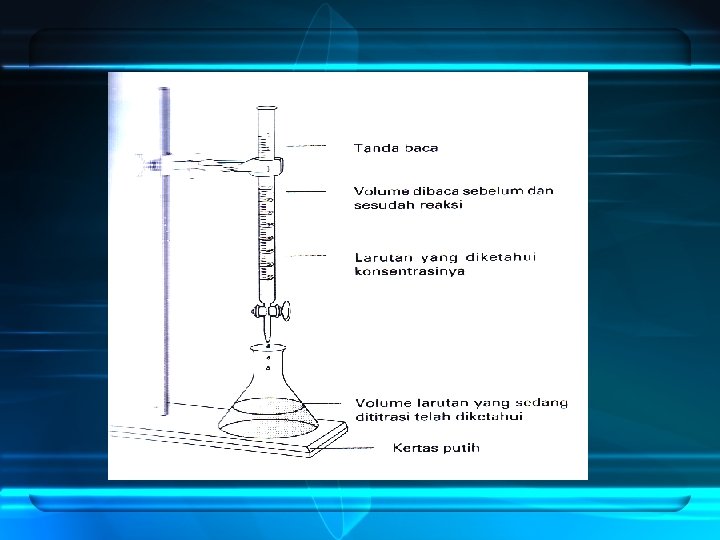

Tipe Titrasi Asam-Basa 1. Titrasi Asam Kuat-Basa Kuat 2. Titrasi Asam Kuat-Basa Lemah 3. Titrasi Asam Lemah-Basa Kuat 4. Titrasi Asam Lemah-Basa Lemah

1. Titrasi Asam Kuat-Basa Kuat Reaksi antara asam kuat dan basa kuat merupakan reaksi netralisasi antara ion H+ dan ion OH─ membentuk molekul air (H 2 O) sehingga pada saat titik ekuivalen dicapai p. H = 7.

Contoh: 1. Untuk menitrasi 45 ml larutan H 2 SO 4 x. M dibutuhkan larutan Na. OH 0, 6 M sebanyak 25 ml. Tentukan konsentrasi H 2 SO 4!

Jawab: Reaksi yang terjadi: 2 Na. OH(aq)+ H 2 SO 4(aq →Na 2 SO 4(aq)+H 2 O(aq) mol asam 2 × Ma. Va 2 ×Ma. 45 ml Ma = mol basa = Mb. Vb = 0, 6 M × 25 ml 2 × 45 ml = 0, 167 M Maka [ H 2 SO 4 ] = 0, 167 M

2. Titrasi Asam Kuat-Basa Lemah Titrasi asam kuat dan basa lemah akan menghasilkan garam yang bersifat asam sehingga pada saat titik ekuivalen dicapai p. H larutan < 7.
Contoh: 1. Untuk menitrasi 25 ml larutan HCl x. M dibutuhkan larutan NH 3 0, 1 M sebanyak 50 ml. Tentukan konsentrasi HCl!

Jawab: Reaksi yang terjadi: HCl(aq)+ NH 3(aq) →NH 4 Cl (aq) mol asam Ma. Va Ma. 25 ml Ma = mol basa = Mb. Vb = 0, 1 M × 50 ml 25 ml = 0, 2 M Maka [ HCl ] = 0, 2 M

3. Titrasi Asam Lemah-Basa Kuat Titrasi asam lemah dan basa kuat akan menghasilkan garam yang bersifat basa sehingga pada saat titik ekuivalen dicapai p. H larutan > 7.

Contoh: 1. Untuk menitrasi 20 ml larutan CH 3 COOH x. M dibutuhkan larutan KOH 0, 1 M sebanyak 10 ml. Tentukan konsentrasi CH 3 COOH!

Jawab: Reaksi yang terjadi: CH 3 COOH(aq)+ KOH(aq →CH 3 COOK(aq)+H 2 O(aq) mol asam Ma. Va Ma. 20 ml Ma = = mol basa Mb. Vb 0, 1 M × 10 ml 20 ml = 0, 05 M Maka [ CH 3 COOH ] = 0, 05 M

4. Titrasi Asam Lemah-Basa Lemah Reaksi antara asam lemah dan basa lemah merupakan reaksi netralisasi antara ion H+ dan ion OH─ membentuk molekul air (H 2 O) sehingga pada saat titik ekuivalen dicapai p. H = 7.

Contoh: 1. Untuk menitrasi 25 ml larutan NH 3 x. M dibutuhkan larutan CH 3 COOH 0, 1 M sebanyak 50 ml. Tentukan konsentrasi NH 3!

Jawab: Reaksi yang terjadi: CH 3 COOH(aq)+ NH 3(aq →CH 3 COONH 4(aq) mol asam = mol basa Ma. Va = Mb. Vb 0, 1 x 50 ml = Mb × 25 ml Mb = 0, 1 M × 50 ml 25 ml = 0, 2 M Maka [ NH 3 ] = 0, 2 M

Indikator Yang Sesuai Tipe Titrasi Asam-Basa 1. 2. 3. 4. Titrasi Asam Kuat-Basa Kuat Titrasi Asam Kuat-Basa Lemah Titrasi Asam Lemah-Basa Kuat Titrasi Asam Lemah-Basa Lemah

1. Titrasi Asam Kuat-Basa Kuat Karena titik ekuivalen dicapai pada p. H larutan = 7, maka indikator yang sesuai adalah indikator bromtimol blue dengan trayek p. H = 6, 0 – 7, 6 (kuning – biru)

2. Titrasi Asam Kuat. Basa Lemah Karena titik ekuivalen dicapai pada p. H larutan < 7, maka indikator yang sesuai adalah indikator metil merah dengan trayek p. H = 4, 8 – 6, 0 (merah – kuning) atau bromkresol ungu dengan trayek p. H = 5, 2 – 6, 8 (kuning – ungu)

3. Titrasi Asam Lemah. Basa Kuat Karena titik ekuivalen dicapai pada p. H larutan > 7, maka indikator yang sesuai adalah indikator phenolftalein dengan trayek p. H = 8, 3 – 10, 1 (tidak berwarna – merah) atau timol blue dengan trayek p. H = 8, 0 – 9, 6 (kuning – biru)

4. Titrasi Asam Lemah. Basa Lemah Karena titik ekuivalen dicapai pada p. H larutan = 7, maka indikator yang sesuai adalah indikator bromtimol blue dengan trayek p. H = 6, 0 – 7, 6 (kuning – biru)
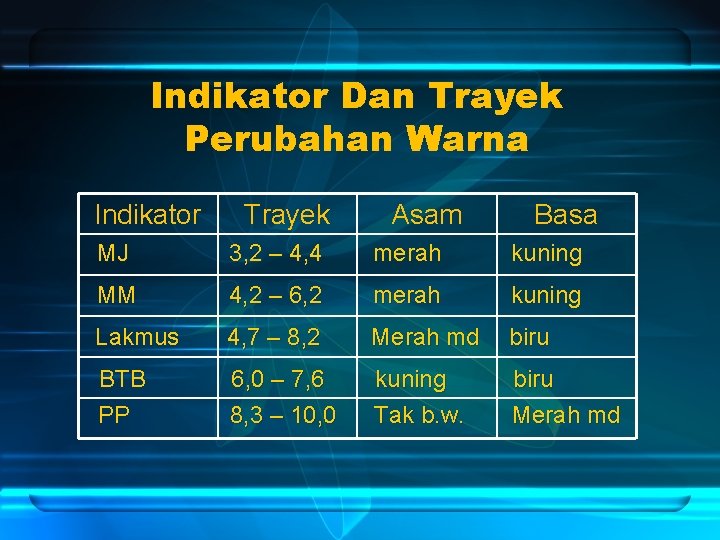
Indikator Dan Trayek Perubahan Warna Indikator Trayek Asam Basa MJ 3, 2 – 4, 4 merah kuning MM 4, 2 – 6, 2 merah kuning Lakmus 4, 7 – 8, 2 Merah md biru BTB PP 6, 0 – 7, 6 8, 3 – 10, 0 kuning Tak b. w. biru Merah md

Contoh: 1. Dari hasil pengujian air limbah diperoleh p. H = 8, maka warna sampel pengujian indikator metil merah, bromtimol biru, dan phenol ptalein berturut-turut adalah. . . Metil merah = kuning Bromtimol biru = biru Phenolptalein = tak berwarna

Contoh: 2. Larutan A diuji dengan indikator metil merah = kuning metil jingga = kuning brom timol biru = biru phenolptalein = tak berwarna Jawab: p. H larutan A berkisar ( 7, 6 - 8, 3 )
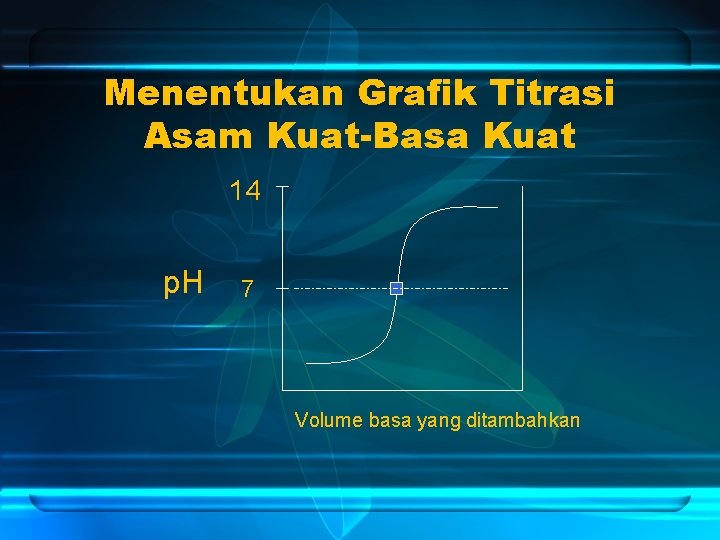
Menentukan Grafik Titrasi Asam Kuat-Basa Kuat 14 p. H 7 Volume basa yang ditambahkan

Menentukan Grafik Titrasi Asam Kuat-Basa Lemah 14 p. H 7 Volume basa yang ditambahkan

Menentukan Grafik Titrasi Asam Lemah-Basa Kuat 14 p. H 7 Volume basa yang ditambahkan

Menentukan Grafik Titrasi Asam Lemah-Basa Lemah 14 p. H 7 Volume basa yang ditambahkan


- Slides: 30