TITOLAZIONI ACIDOBASE Prof Salvatore Andini Acidi e basi

TITOLAZIONI ACIDO-BASE Prof. Salvatore Andini

Acidi e basi 1 - Autoprotolisi dell’acqua 2 H 2 O H 3 O+ + OHEquilibrio tutto spostato verso i reagenti Acqua pura a 25 °C ci sono solo 1. 00 10 -7 moli delle 55. 5 presenti sono dissociate (2 molecole ogni miliardo)
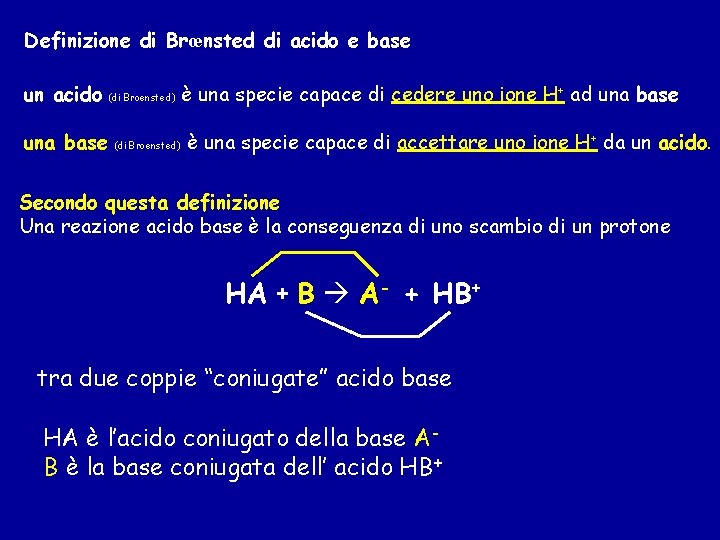
Definizione di Brœnsted di acido e base un acido una base (di Broensted) è una specie capace di cedere uno ione H+ ad una base è una specie capace di accettare uno ione H+ da un acido. Secondo questa definizione Una reazione acido base è la conseguenza di uno scambio di un protone HA + B A- + HB+ tra due coppie “coniugate” acido base HA è l’acido coniugato della base AB è la base coniugata dell’ acido HB+
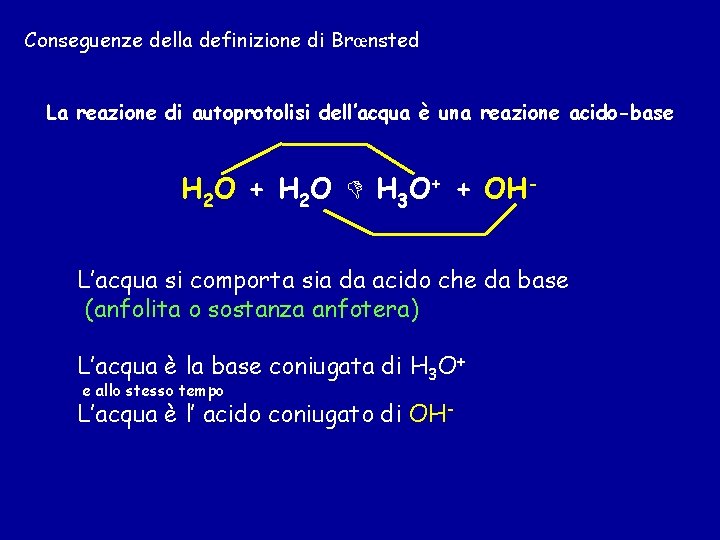
Conseguenze della definizione di Brœnsted La reazione di autoprotolisi dell’acqua è una reazione acido-base H 2 O + H 2 O H 3 O+ + OHL’acqua si comporta sia da acido che da base (anfolita o sostanza anfotera) L’acqua è la base coniugata di H 3 O+ e allo stesso tempo L’acqua è l’ acido coniugato di OH-
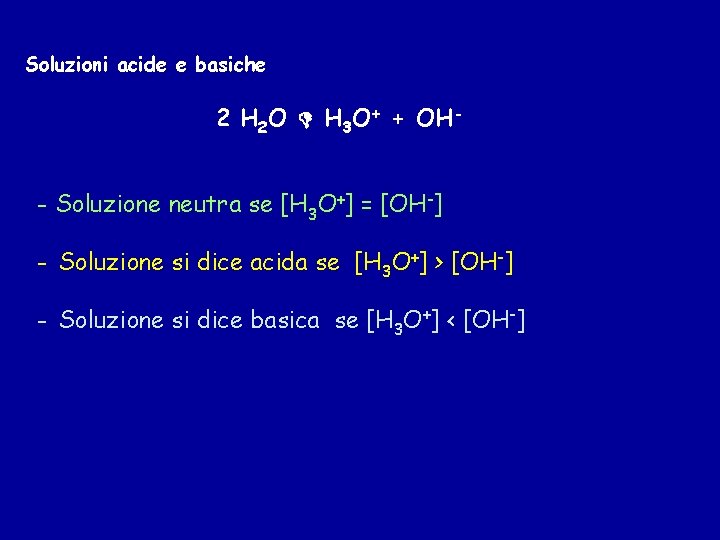
Soluzioni acide e basiche 2 H 2 O H 3 O+ + OH- - Soluzione neutra se [H 3 O+] = [OH-] - Soluzione si dice acida se [H 3 O+] > [OH-] - Soluzione si dice basica se [H 3 O+] < [OH-]

Conseguenze della definizione di Brœnsted La reazione di dissociazione di un acido è una reazione acidobase: HA + H 2 O H 3 O+ + AIn cui l’acqua si comporta da base La reazione di dissociazione di una base è una reazione acido-base: B + H 2 O BH+ + OHIn cui l’acqua si comporta da acido

Forza degli acidi e delle basi - Acidi e basi forti Un acido o una base si dice forte se si “dissocia” completamente per ogni concentrazione iniziale HCl + H 2 O H 3 O+ + Cl. Na. OH Na+ + OH- acido cloridrico è una acido forte sodio idrossido è una base forte H 3 O + è l’acido più forte che esiste in acqua indissociato OH- è la base più forte che esiste in acqua indissociata

Forza degli acidi e delle basi - Acidi e basi a forza nulla (debolissimi) Un acido o una base si dicono debolissimi o a forza nulla se la loro dissociazione non comporta variazioni significative nella concentrazione degli ioni idronio (H 3 O+) e idrossido (OH-) in soluzione. Lo ione cloruro (la base coniugata di HCl) è una base a forza nulla: HCl + H 2 O H 3 O+ + Cl- la reazione non avviene Lo ione sodio (l’acido coniugato di Na. OH) è un acido a forza nulla: Na. OH OH- + Na+ la reazione non avviene
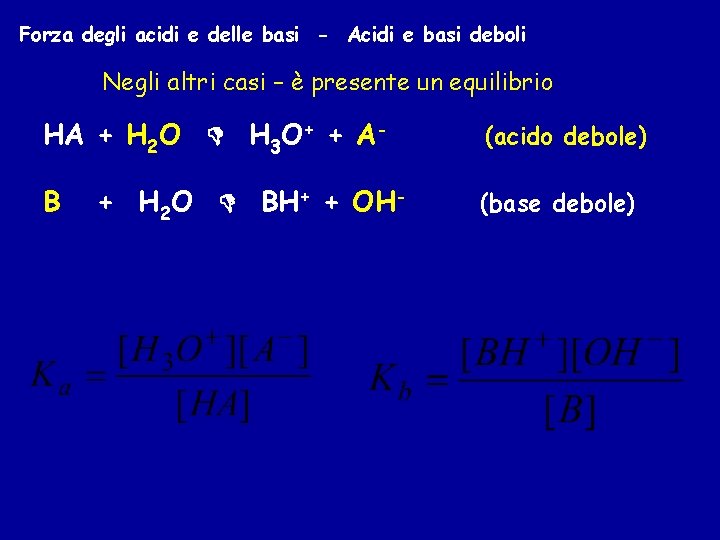
Forza degli acidi e delle basi - Acidi e basi deboli Negli altri casi – è presente un equilibrio HA + H 2 O H 3 O+ + A- (acido debole) B (base debole) + H 2 O BH+ + OH-
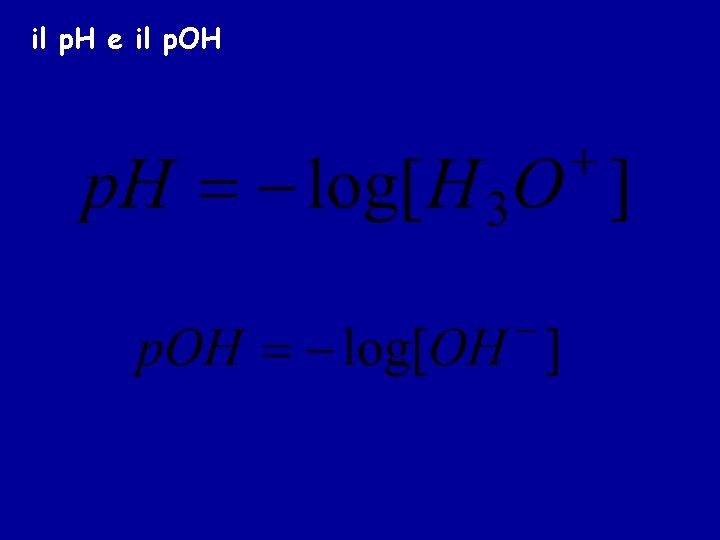
il p. H e il p. OH

Relazione tra p. H e il p. OH 2 H 2 O H 3 O+ + OH- Kw Kw= [H 3 O+][OH-] = 1. 0 x 10 -14 -log Kw = p. Kw= -log[H 3 O+] – log[OH-] = p. H + p. OH = 14. 0
![Il p. H e la sua scala p. H = -log [H 3 O+] Il p. H e la sua scala p. H = -log [H 3 O+]](http://slidetodoc.com/presentation_image_h2/dab6bb6ba37d0c472523e2e774bbef50/image-12.jpg)
Il p. H e la sua scala p. H = -log [H 3 O+] p. OH = -log [OH-] p. H + p. OH = p. Kw = 14 Soluzioni basiche p. H 0 1 2 3 basicità crescente 4 5 6 7 8 9 10 11 12 13 14 14 13 12 11 10 9 8 7 6 5 4 acidità crescente Soluzioni acide 3 2 1 0 p. OH

Relazione tra p. H e il p. OH la soluzione è neutra se il p. H=7; quando il p. H < 7 la soluzione è acida; quando il p. H > 7 la soluzione è basica.

Relazione tra Ka e Kb di una coppia acido-base. Una conseguenza della presenza dell’ autoprotolisi dell’acqua è che le forze di un acido e di una base coniugati non sono indipendenti HA + H 2 O H 3 O+ + A- Ka A- + H 2 O HA Kb + OH-

Relazione tra Ka e Kb di una coppia acido-base p. Kw = p. Ka + p. Kb a 25 °C p. Ka + p. Kb= 14. 0
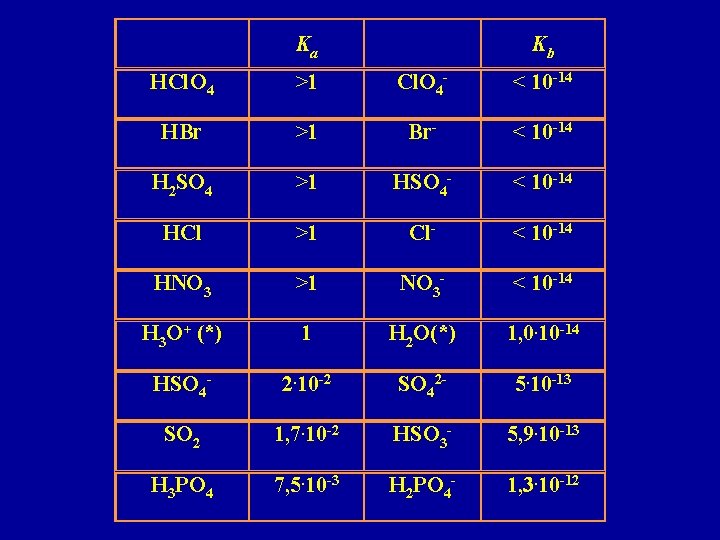
Ka Kb HCl. O 4 >1 Cl. O 4 - < 10 -14 HBr >1 Br- < 10 -14 H 2 SO 4 >1 HSO 4 - < 10 -14 HCl >1 Cl- < 10 -14 HNO 3 >1 NO 3 - < 10 -14 H 3 O+ (*) 1 H 2 O(*) 1, 0. 10 -14 HSO 4 - 2. 10 -2 SO 42 - 5. 10 -13 SO 2 1, 7. 10 -2 HSO 3 - 5, 9. 10 -13 H 3 PO 4 7, 5. 10 -3 H 2 PO 4 - 1, 3. 10 -12
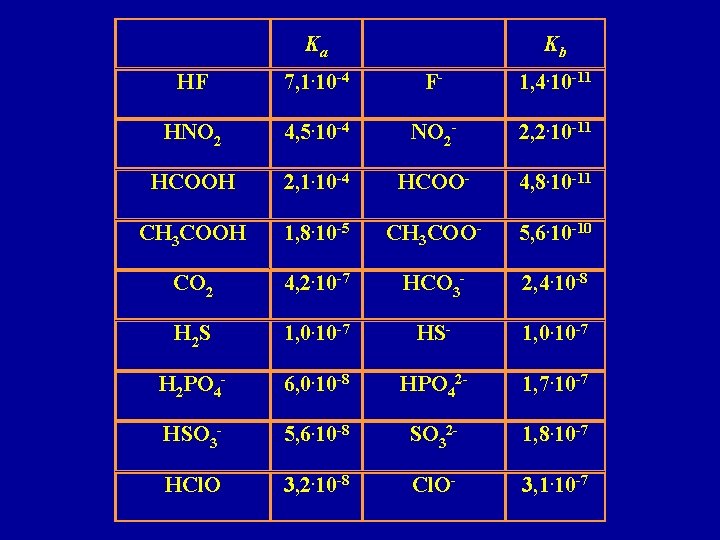
Ka Kb HF 7, 1. 10 -4 F- 1, 4. 10 -11 HNO 2 4, 5. 10 -4 NO 2 - 2, 2. 10 -11 HCOOH 2, 1. 10 -4 HCOO- 4, 8. 10 -11 CH 3 COOH 1, 8. 10 -5 CH 3 COO- 5, 6. 10 -10 CO 2 4, 2. 10 -7 HCO 3 - 2, 4. 10 -8 H 2 S 1, 0. 10 -7 HS- 1, 0. 10 -7 H 2 PO 4 - 6, 0. 10 -8 HPO 42 - 1, 7. 10 -7 HSO 3 - 5, 6. 10 -8 SO 32 - 1, 8. 10 -7 HCl. O 3, 2. 10 -8 Cl. O- 3, 1. 10 -7
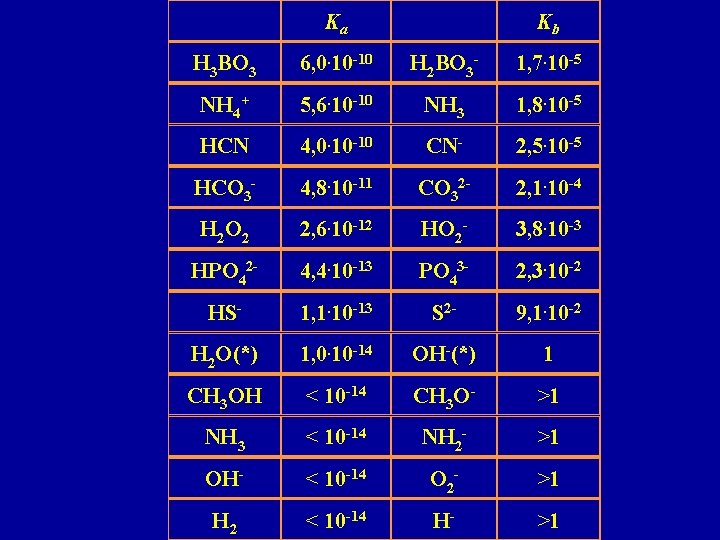
Ka Kb H 3 BO 3 6, 0. 10 -10 H 2 BO 3 - 1, 7. 10 -5 NH 4+ 5, 6. 10 -10 NH 3 1, 8. 10 -5 HCN 4, 0. 10 -10 CN- 2, 5. 10 -5 HCO 3 - 4, 8. 10 -11 CO 32 - 2, 1. 10 -4 H 2 O 2 2, 6. 10 -12 HO 2 - 3, 8. 10 -3 HPO 42 - 4, 4. 10 -13 PO 43 - 2, 3. 10 -2 HS- 1, 1. 10 -13 S 2 - 9, 1. 10 -2 H 2 O(*) 1, 0. 10 -14 OH-(*) 1 CH 3 OH < 10 -14 CH 3 O- >1 NH 3 < 10 -14 NH 2 - >1 OH- < 10 -14 O 2 - >1 H 2 < 10 -14 H- >1

Titolazioni acido-base Titolazione = è una operazione il cui scopo è la determinazione del titolo di una soluzione. Consiste nell’aggiungere volumi noti di una soluzione a concentrazione nota di un titolante ad un volume noto di una soluzione a concentrazione ignota. Il titolante deve reagire in modo rapido, completo e con stechiometria ben definita con la sostanza da titolare. Nel caso delle titolazioni acido-base, il titolante è costituito quindi da acidi e basi forti. La sostanza da titolare può essere una base o un acido qualsiasi.
Acido Base sale C? Punto equivalente • Una titolazione termina quando le moli di titolante uguagliano quelle della sostanza da titolare: C MA V A = M B V B Come si riconesce il Punto equivalente?

Gli indicatori Indicatore = sostanza che cambia colore tra la sua forma acida e quella basica (VIRARE) HIn + H 2 O In- + H 3 O+ Indicatori universali Cartina tornasole

Cambio di colore nella fenolftaleina Incolore soluzioni p. H < 8. 2 Viola soluzioni p. H > 8. 2 Il colore viola dell'indicatore deprotonato (p. H > 8) è dovuto alla estesa delocalizzazione degli elettroni nel sistema pi greco coniugato.
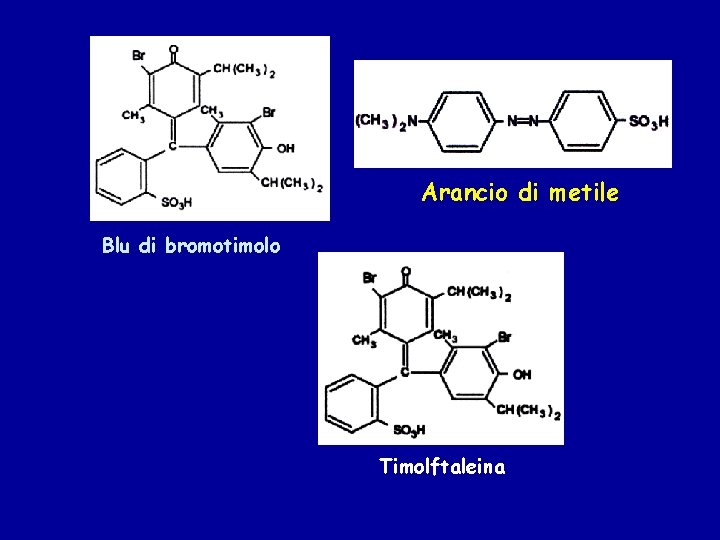
Arancio di metile Blu di bromotimolo Timolftaleina

Arancio di metile
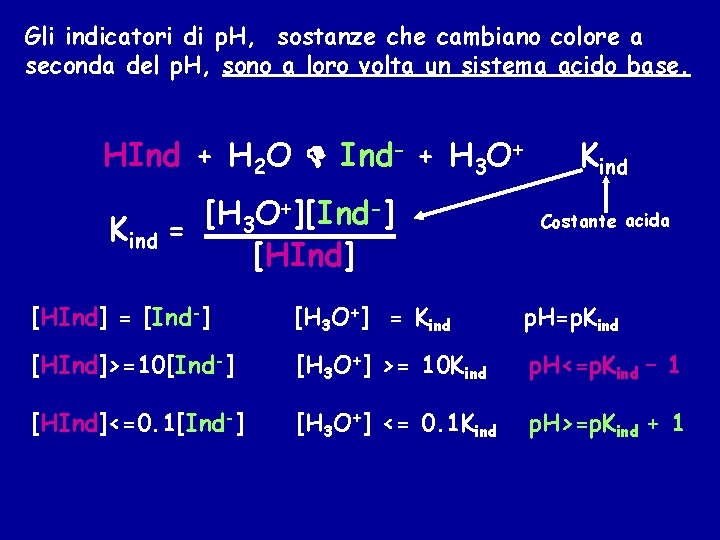
Gli indicatori di p. H, sostanze che cambiano colore a seconda del p. H, sono a loro volta un sistema acido base. HInd + H 2 O Ind- + H 3 O+ +][Ind-] [H O 3 Kind = [HInd] Kind Costante acida [HInd] = [Ind-] [H 3 O+] = Kind p. H=p. Kind [HInd]>=10[Ind-] [H 3 O+] >= 10 Kind p. H<=p. Kind – 1 [HInd]<=0. 1[Ind-] [H 3 O+] <= 0. 1 Kind p. H>=p. Kind + 1
![[HInd] = [Ind-] [H 3 O+] = Kind p. H=p. Kind [HInd]>=10[Ind-] [H 3 [HInd] = [Ind-] [H 3 O+] = Kind p. H=p. Kind [HInd]>=10[Ind-] [H 3](http://slidetodoc.com/presentation_image_h2/dab6bb6ba37d0c472523e2e774bbef50/image-26.jpg)
[HInd] = [Ind-] [H 3 O+] = Kind p. H=p. Kind [HInd]>=10[Ind-] [H 3 O+] >= 10 Kind p. H<=p. Kind – 1 [HInd]<=0. 1[Ind-] [H 3 O+] <= 0. 1 Kind p. H<=p. Kind + 1 Colore della forma acida Colore della forma basica p. Kind-1 p. Kind+1 p. H Intervallo di viraggio L'indicatore essendo una specie acido-base reagisce e può spostare il punto equivalente. Deve essere molto colorato ed usato in piccola quantità.
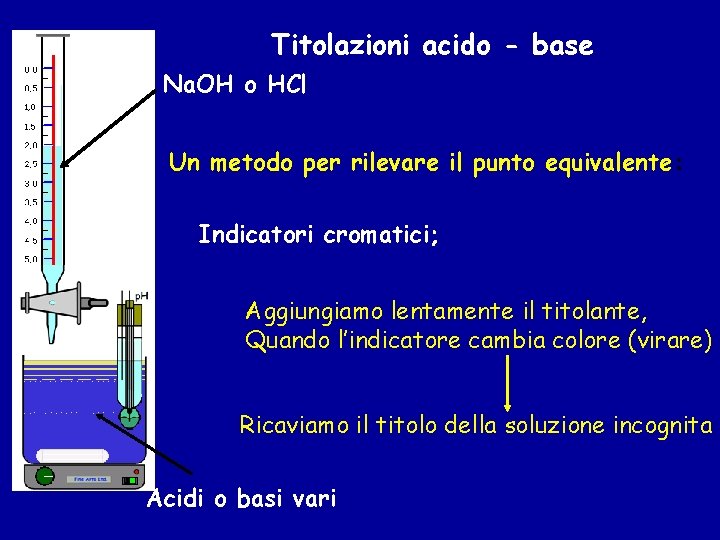
Titolazioni acido - base Na. OH o HCl Un metodo per rilevare il punto equivalente: Indicatori cromatici; Aggiungiamo lentamente il titolante, Quando l’indicatore cambia colore (virare) Ricaviamo il titolo della soluzione incognita Acidi o basi vari
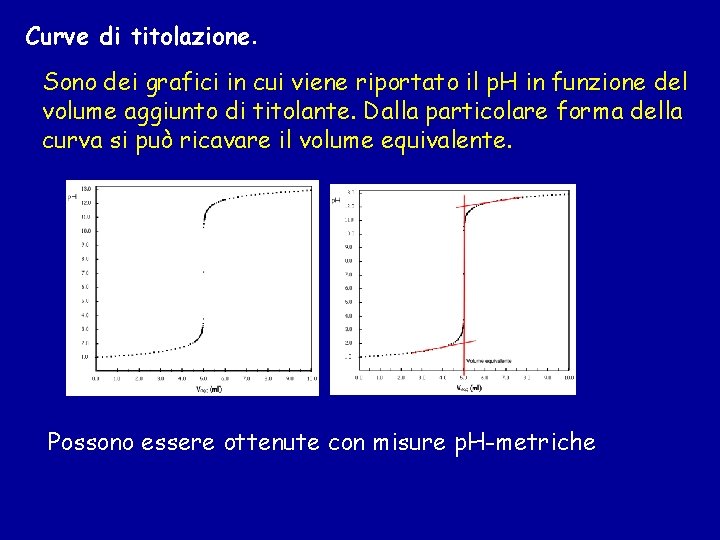
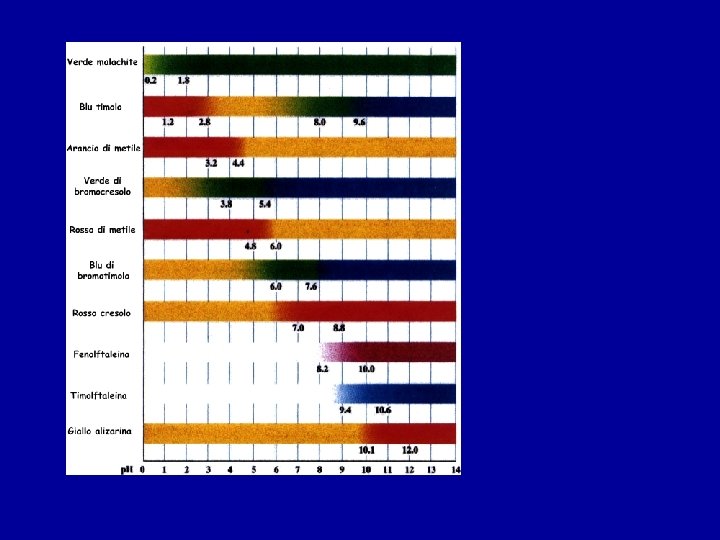
Curve di titolazione. Sono dei grafici in cui viene riportato il p. H in funzione del volume aggiunto di titolante. Dalla particolare forma della curva si può ricavare il volume equivalente. Possono essere ottenute con misure p. H-metriche
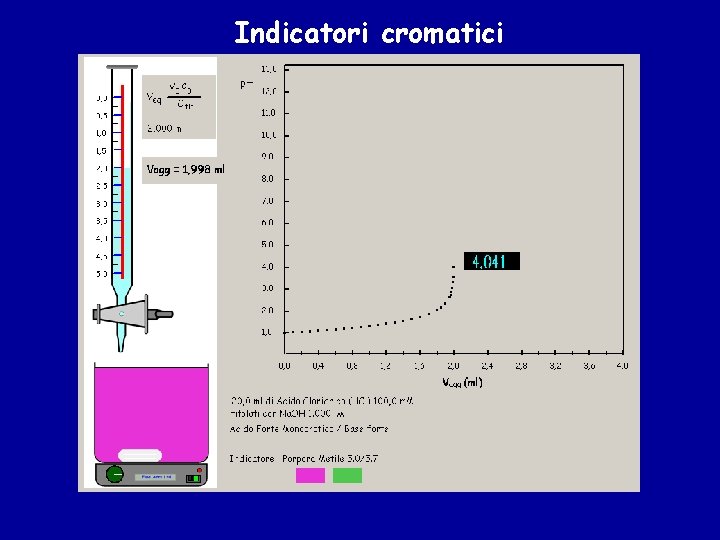
Indicatori cromatici
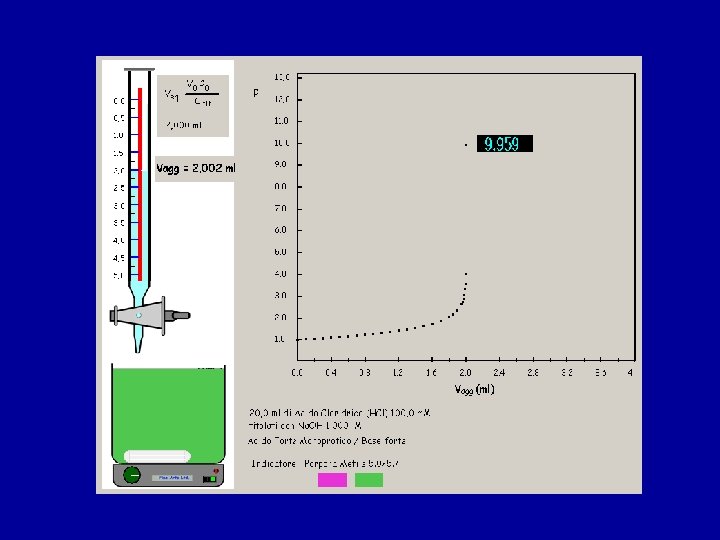
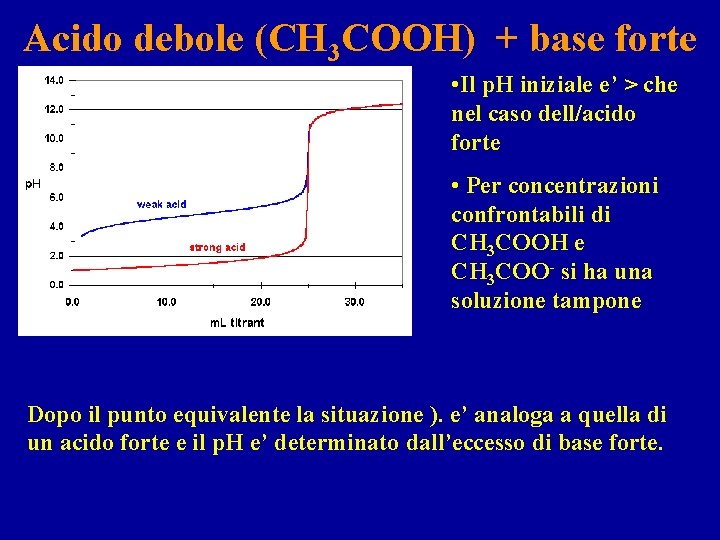
Acido debole (CH 3 COOH) + base forte • Il p. H iniziale e’ > che nel caso dell/acido forte • Per concentrazioni confrontabili di CH 3 COOH e CH 3 COO- si ha una soluzione tampone Dopo il punto equivalente la situazione ). e’ analoga a quella di un acido forte e il p. H e’ determinato dall’eccesso di base forte.
- Slides: 32