TITOLAZIONI ACIDO BASE La reazione tra una sostanza

TITOLAZIONI ACIDO BASE La reazione tra una sostanza basica ed un acido forte e tra una sostanza acida ed una base forte hanno tutti i requisiti per essere impiegate nei metodi di analisi. CH 3 COOH + Na+ + OH CH 3 COO + H 2 O + Na+ HCO 3 + H+ + Cl H 2 CO 3 + Cl La reazione tra protoliti deboli, in generale, non sono utilizzabili per determinazioni analitiche: NH 3 + CH 3 COOH = NH 4+ + CH 3 COO K = KA(NH 3)/KA(CH 3 COOH) =10 9. 24/10 4. 76 =10 4. 48

TITOLAZIONI ACIDO BASE Q TITOLAZIONE VOLUMETRICA: misura del volume di titolante Q TITOLAZIONE PER PESATA: misura della massa di titolante O o PUNTO EQUIVALENTE (p. e. ) della titolazione: punto teorico di arresto della titolazione in cui il numero di equivalenti del titolando e del titolante sono uguali PUNTO FINALE (p. f. ) della titolazione: punto di arresto della aggiunta di titolante a seguito di una variazione di proprietà chimico fisiche della soluzione (variazione di colore, variazione di potenziale, ecc. ) che indica il termine della reazione ERRORE DI TITOLAZIONE: deriva dalla non coincidenza tra il punto equivalente ed il punto finale. Definisce le condizioni sperimentali per eseguire una titolazione (metodo migliore per individuare il punto finale, ecc. ) CURVA DI TITOLAZIONE: andamento della concentrazione della specie da titolare (p. H, p. Cl (= log[Cl ]), ecc. ) o di una grandezza dipendente da tale concentrazione (forza elettromotrice, ecc. ) in funzione del volume di titolante aggiunto I metodi di analisi che utilizzano reazioni acido base si suddividono in: Titolazioni di basi con acidi forti (acidimetria) Titolazioni di acidi con basi forti (alcalimetria)

TITOLAZIONI ACIDO BASE La titolazione è una procedura di laboratorio per determinare l’ammontare o la concentrazione (o titolo) di una sostanza (titolando). Consiste nella misura della quantità di reattivo, detto titolante (aggiunto come soluzione a concentrazione nota) necessaria per raggiungere l’equivalenza (uguaglianza degli equivalenti di titolando con gli equivalenti di titolante), secondo una reazione specifica. Se C è la concentrazione (espressa in Normalità, cioè in equivalenti/dm 3) del titolando e CT indica quella del titolante ( in Normalità), si ha: CT = C Se invece si usano le concentrazioni molari, nel caso della titolazione di H 2 SO 4 con Na. OH: CT = 2 C Utilizzando le concentrazioni in equivalenti/dm 3, è valida sempre l’equazione: CT = C
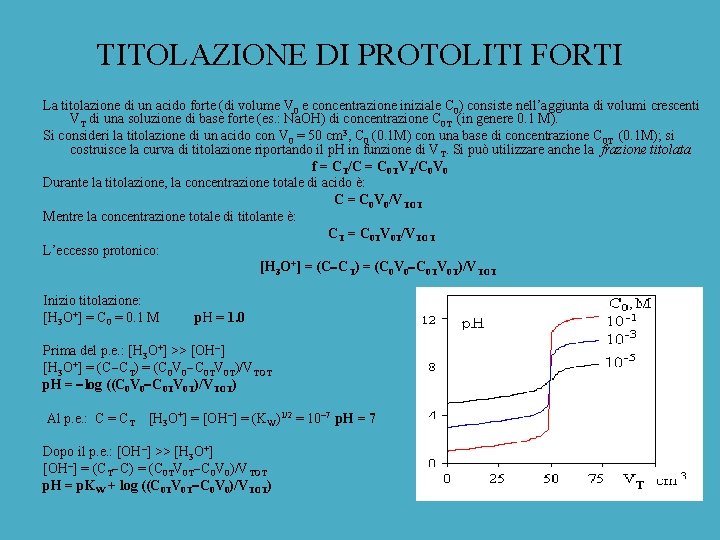
TITOLAZIONE DI PROTOLITI FORTI La titolazione di un acido forte (di volume V 0 e concentrazione iniziale C 0) consiste nell’aggiunta di volumi crescenti VT di una soluzione di base forte (es. : Na. OH) di concentrazione C 0 T (in genere 0. 1 M). Si consideri la titolazione di un acido con V 0 = 50 cm 3, C 0 (0. 1 M) con una base di concentrazione C 0 T (0. 1 M); si costruisce la curva di titolazione riportando il p. H in funzione di VT. Si può utilizzare anche la frazione titolata f = CT/C = C 0 TVT/C 0 V 0 Durante la titolazione, la concentrazione totale di acido è: C = C 0 V 0/VTOT Mentre la concentrazione totale di titolante è: CT = C 0 TV 0 T/VTOT L’eccesso protonico: [H 3 O+] = (C CT) = (C 0 V 0 C 0 TV 0 T)/VTOT Inizio titolazione: [H 3 O+] = C 0 = 0. 1 M p. H = 1. 0 Prima del p. e. : [H 3 O+] >> [OH ] [H 3 O+] = (C CT) = (C 0 V 0 C 0 TV 0 T)/VTOT p. H = log ((C 0 V 0 C 0 TV 0 T)/VTOT) Al p. e. : C = CT [H 3 O+] = [OH ] = (KW)1/2 = 10 7 p. H = 7 Dopo il p. e. : [OH ] >> [H 3 O+] [OH ] = (CT C) = (C 0 TV 0 T C 0 V 0)/VTOT p. H = p. KW + log ((C 0 TV 0 T C 0 V 0)/VTOT)
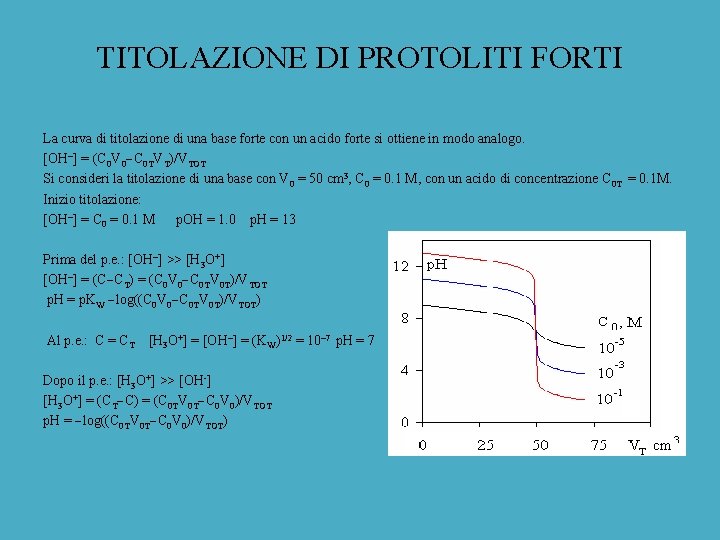
TITOLAZIONE DI PROTOLITI FORTI La curva di titolazione di una base forte con un acido forte si ottiene in modo analogo. [OH ] = (C 0 V 0 C 0 TVT)/VTOT Si consideri la titolazione di una base con V 0 = 50 cm 3, C 0 = 0. 1 M, con un acido di concentrazione C 0 T = 0. 1 M. Inizio titolazione: [OH ] = C 0 = 0. 1 M p. OH = 1. 0 p. H = 13 Prima del p. e. : [OH ] >> [H 3 O+] [OH ] = (C CT) = (C 0 V 0 C 0 TV 0 T)/VTOT p. H = p. KW log((C 0 V 0 C 0 TV 0 T)/VTOT) Al p. e. : C = CT [H 3 O+] = [OH ] = (KW)1/2 = 10 7 p. H = 7 Dopo il p. e. : [H 3 O+] >> [OH-] [H 3 O+] = (CT C) = (C 0 TV 0 T C 0 V 0)/VTOT p. H = log((C 0 TV 0 T C 0 V 0)/VTOT)

INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI ACIDO BASE INDICATORI ACIDO BASE Coppia acido base dove l’acido e la base coniugata hanno colori differenti (indicatori bicolori) o almeno una delle due forme è colorata (indicatori monocolori). Intervallo di viraggio: intervallo di p. H in cui si manifesta il cambiamento di colore. Gli indicatori sono acidi o basi organiche deboli, utilizzate in concentrazioni minime, per non alterare la concentrazione idrogenionica della soluzione. HIn + H 2 O = In + H 3 O+ colore acida colore basico KI = [In ][H 3 O+]/[HIn] p. H = p. KI + log [In ]/[HIn] p. H > p. KI : colore basico p. H < p. KI : colore acido p. H = p. KI : colore intermedio Il colore di una forma si distingue dall’altro se: [In ]/[HIn] = 10 (colore forma basica) [In ]/[HIn] = 0. 1 (colore forma acida) Intervallo di viraggio: p. KI – 1 p. H p. KI +1 In pratica l’intervallo di viraggio può essere maggiore o minore di p. KI – 1 p. KI +1 in dipendenza del tono ed intensità dei colori dell’indicatore.

INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI ACIDO BASE Esempio rosso metile (p. KI = 5. 0): intervallo 4. 2 6. 2 fenolftaleina (p. KI = 9. 6): intervallo 8. 0 9. 8 verde bromocresolo (p. KI = 4. 7): intervallo 3. 8 5. 4 Quindi per utilizzare l’indicatore come sistema per individuare il punto finale, occorre una variazione nella titolazione di almeno 3 unità di p. H. Con l’impiego degli indicatori acido base, il punto equivalente è apprezzato con una incertezza di 0. 4 unità p. H. Ciò si realizza durante la titolazione confrontando il colore della soluzione incognita con il colore assunto dall’indicatore in soluzioni avente lo stesso p. H del punto equivalente. Risultati migliori si ottengono utilizzando metodi strumentali, come la potenziometria. Infatti, in tal caso l’errore diminuisce a 0. 05 unità p. H.
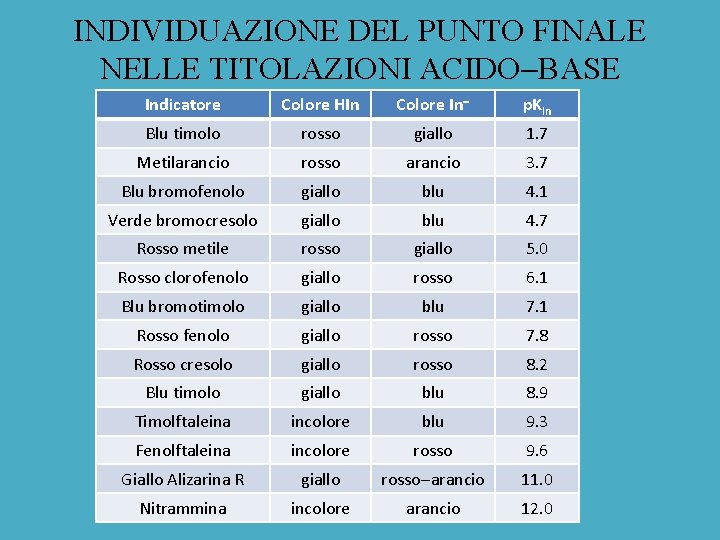
INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI ACIDO BASE Indicatore Colore HIn Colore In p. KIn Blu timolo rosso giallo 1. 7 Metilarancio rosso arancio 3. 7 Blu bromofenolo giallo blu 4. 1 Verde bromocresolo giallo blu 4. 7 Rosso metile rosso giallo 5. 0 Rosso clorofenolo giallo rosso 6. 1 Blu bromotimolo giallo blu 7. 1 Rosso fenolo giallo rosso 7. 8 Rosso cresolo giallo rosso 8. 2 Blu timolo giallo blu 8. 9 Timolftaleina incolore blu 9. 3 Fenolftaleina incolore rosso 9. 6 Giallo Alizarina R giallo rosso arancio 11. 0 Nitrammina incolore arancio 12. 0

ERRORE DI TITOLAZIONE DI PROTOLITI FORTI L’errore di titolazione rappresenta l’errore derivante dall’incertezza nell’individuazione del punto equivalente (valore del p. H al punto equivalente) Si commette un errore di titolazione quando il p. H al punto finale (p. f. ) non coincide con il punto equivalente (p. e. ). Nelle titolazioni acido base, al punto equivalente (p. e. ), indicando con C la concentrazione totale di titolando e con CT la concentrazione totale di titolante, si ha: CT = C Si definisce “errore di titolazione”: L’errore di titolazione relativo è: Errore percentuale: = CT – C R = (CT – C)/C R 100 Si osserva che: • R aumenta con la diluizione (volume ottimale di titolante 20 cm 3, con un volume totale di circa 150 200 cm 3); • non utilizzare reattivi concentrazioni superiori a 0. 2 M altrimenti si possono avere effetti della forza ionica sulle costanti di equilibrio e quindi sul p. H del punto equivalente.

ERRORE DI TITOLAZIONE DI PROTOLITI FORTI Esempio Una soluzione del volume di 25 cm 3 di HCl 0. 010 M è titolata con 24. 8 cm 3 di Na. OH 0. 010 M. Calcolare l’errore di titolazione. C = 0. 00502 M CT = 0. 00498 M R = (0. 00498 0. 00502) M/0. 00502 M = 0. 008 = 0. 8% Esempio Una soluzione del volume di 20 cm 3 di HNO 3 0. 0755 M è titolata con 22. 7 cm 3 di Na. OH 0. 0696 M. Calcolare l’errore di titolazione. C = 0. 0354 M CT = 0. 0370 M R = (0. 0370 0. 0354) M/0. 0354 M = 0. 045 = 4. 5% Una titolazione è applicabile come metodo analitico accurato se R 0. 001 = 0. 1%

ERRORE DI TITOLAZIONE DI PROTOLITI FORTI Titolazione di acidi forti Esempio Una soluzione di HCl 0. 02 M è titolata con Na. OH 0. 02 M utilizzando come indicatore visuale il rosso fenolo. Calcolare l’errore di titolazione. In una titolazione tra protoliti forti, al punto equivalente si ha: [H 3 O+] = [OH ] =10 7 M, p. H = 7. 0 La concentrazione al punto finale del titolando è: C = 0. 01 M (abbiamo aggiunto un uguale volume di Na. OH, quindi il volume finale è il doppio di quello iniziale). Utilizzando come indicatore il rosso fenolo, il p. H al punto finale sarà: p. HP. F = (p. KI + 1) = 7. 8 + 1 = 8. 8 Poiché si è superato il punto equivalente, l’errore è proporzionale alla quantità di base aggiunta in eccesso quindi si ha: R = [OH ]/C [OH ] = KW/[H 3 O+] = 10 5. 2 M R = 10 5. 2 M/0. 01 M = 6× 10 4 = 0. 06% La titolazione può essere condotta con l’utilizzo del rosso fenolo come indicatore

ERRORE DI TITOLAZIONE DI PROTOLITI FORTI Titolazione di basi forti Esempio Una soluzione di KOH 0. 02 M è titolata con HCl 0. 02 M utilizzando come indicatore visuale il metilarancio. Calcolare l’errore di titolazione. In una titolazione tra protoliti forti, al punto equivalente si ha: [H 3 O+] = [OH ] = 10 7 M, p. H = 7. 0 La concentrazione al punto finale del titolando è: C = 0. 01 M Utilizzando come indicatore il metilarancio, il p. H al punto finale sarà: p. HP. F = (p. KI 1) = 3. 7 1 = 2. 7 Poiché si è superato il punto equivalente, l’errore è proporzionale alla quantità di acido aggiunta in eccesso quindi si ha: R = [H 3 O+]/C R = 10 2. 7 M/0. 01 M = 2× 10 3 = 20% La titolazione non può essere condotta con l’utilizzo del metilarancio come indicatore

CURVA DI TITOLAZIONE DI PROTOLITI DEBOLI MONOPROTICI TITOLAZIONE DI UN ACIDO DEBOLE Si consideri la titolazione di una soluzione C 0 = 0. 1 M HNO 2 (p. KA = 3. 35) e di volume iniziale V 0 = 50 cm 3 con Na. OH, di concentrazione C 0 T, aggiungendo volumi crescenti VT. Durante la titolazione: C = C 0 V 0/VTOT CT = C 0 TV 0 T/VTOT Inizio titolazione: H 3 O+ = NO 2 = (KAC 0)½ p. H = ½(3. 35 + 1) = 2. 17 Prima del p. e. : Aggiungendo un volume VT di base Na. OH si ha: NO 2 = C 0 TVT/VTOT = CT [HNO 2 = C NO 2 = (C 0 V 0 C 0 TVT)/VTOT = (C CT) [NO 2 [H 3 O+] CT [H 3 O+] KA = [HNO 2 (C CT) CT p. H = p. KA + log ——— C CT
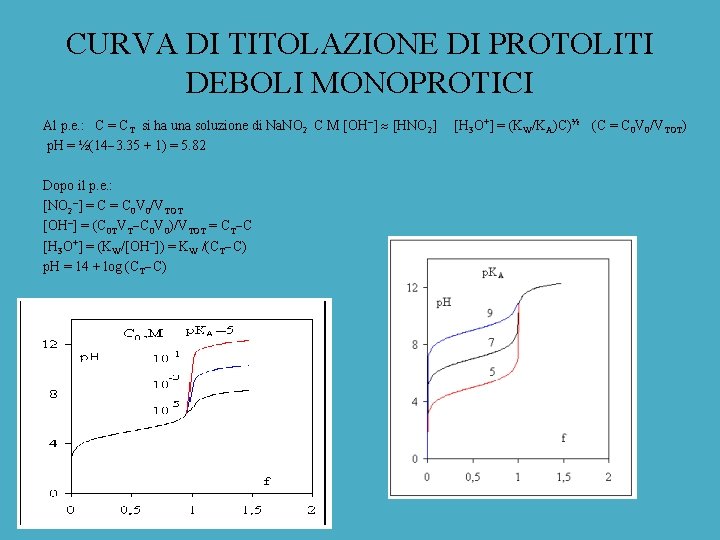
CURVA DI TITOLAZIONE DI PROTOLITI DEBOLI MONOPROTICI Al p. e. : C = C si ha una soluzione di Na. NO C M OH HNO H O = (K /K )C) (C = C V /V T p. H = ½(14 3. 35 + 1) = 5. 82 Dopo il p. e. : NO 2 = C 0 V 0/VTOT [OH ] = (C 0 TVT C 0 V 0)/VTOT = CT C H 3 O+ = (KW/[OH ]) = KW /(CT C) p. H = 14 + log (CT C) 2 2 3 + W A ½ 0 0 TOT)
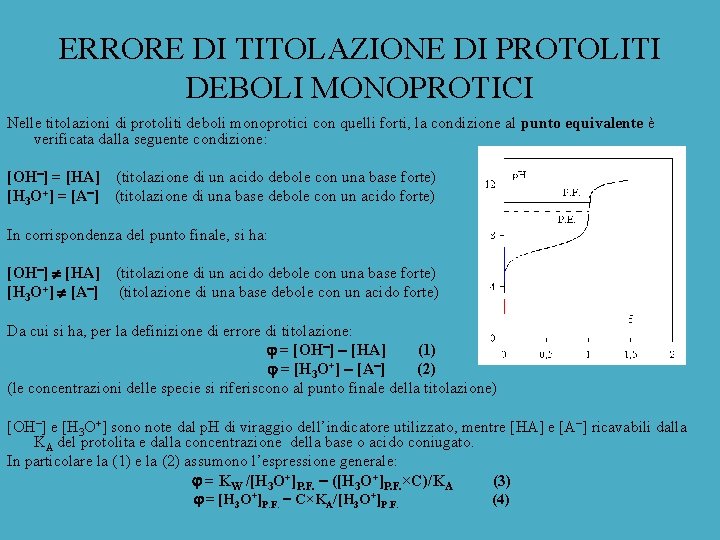
ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI MONOPROTICI Nelle titolazioni di protoliti deboli monoprotici con quelli forti, la condizione al punto equivalente è verificata dalla seguente condizione: [OH ] = [HA] (titolazione di un acido debole con una base forte) [H 3 O+] = [A ] (titolazione di una base debole con un acido forte) In corrispondenza del punto finale, si ha: [OH ] [HA] (titolazione di un acido debole con una base forte) [H 3 O+] [A ] (titolazione di una base debole con un acido forte) Da cui si ha, per la definizione di errore di titolazione: = [OH ] [HA] (1) = [H 3 O+] [A ] (2) (le concentrazioni delle specie si riferiscono al punto finale della titolazione) [OH ] e [H 3 O+] sono note dal p. H di viraggio dell’indicatore utilizzato, mentre [HA] e [A ] ricavabili dalla KA del protolita e dalla concentrazione della base o acido coniugato. In particolare la (1) e la (2) assumono l’espressione generale: = KW /[H 3 O+]P. F. ([H 3 O+]P. F. ×C)/KA (3) = [H 3 O+]P. F. C×KA/[H 3 O+]P. F. (4)

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI MONOPROTICI Esempio Calcolare l’errore di titolazione per HNO 2 C 0 = 0. 1 M (p. KA = 3. 35) con Na. OH C 0 T = 0. 1 M. Al p. e. abbiamo una soluzione di Na. NO 2 0. 05 M. Il p. H al punto equivalente è: p. H = ½(p. KW + log C + p. KA) = ½(14 1. 30 + 3. 35) = 8. 02 L’indicatore consigliato è il rosso fenolo che ha un p. H di viraggio, p. HP. F. , di 8. 8. In accordo all’equazione (3) si ha: = KW /[H 3 O+]P. F. ([H 3 O+]P. F. ×C)/KA = 10 14 M 2/10 8. 8 M (10 8. 8 M× 0. 05 M)/10 3. 35 M = 0. 012% L’errore di titolazione è positivo in quanto ci siamo fermati dopo il punto equivalente. Esempio Calcolare l’errore di titolazione per CH 3 COOH C 0 = 0. 01 M (p. KA = 4. 76) con Na. OH C 0 T = 0. 01 M. Al p. e. abbiamo una soluzione di CH 3 COONa 0. 005 M. Il p. H al punto equivalente è: p. H = ½(p. KW + log C + p. KA) = ½(14 2. 30+4. 76) = 8. 23 L’indicatore consigliato è il rosso fenolo che ha un p. H di viraggio, p. HP. F. , di 8. 8. In accordo all’equazione (3) si ha: = KW /[H 3 O+]P. F. ([H 3 O+]P. F. ×C)/KA = 10 14 M 2/10 8. 8 M (10 8. 8 M× 0. 005 M)/10 4. 76 M = 0. 12% L’errore di titolazione è positivo in quanto ci siamo fermati dopo il punto equivalente.

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI MONOPROTICI Esempio Calcolare l’errore di titolazione per NH 4 Cl C 0 = 0. 1 M (p. KA = 9. 24) con Na. OH C 0 T = 0. 1 M. Al p. e. abbiamo una soluzione di NH 3 0. 05 M. Il p. H al punto equivalente è: p. H = ½(p. KW + log C + p. KA) = ½(14 1. 30 + 9. 24) = 11. 0 L’indicatore consigliato è la fenolftaleina che ha un p. H di viraggio, p. HP. F. , di 10. 6. In accordo all’equazione (3) si ha: = KW /[H 3 O+]P. F. ([H 3 O+]P. F. ×C)/KA = 10 14 M 2/10 10. 6 M (10 10. 6 M× 0. 05 M)/10 9. 24 M = 3. 57% L’errore di titolazione è negativo in quanto ci siamo fermati prima del punto equivalente. Esempio Calcolare l’errore di titolazione per Na. NO 2 C 0 = 0. 01 M (p. KA = 3. 35) con HCl C 0 T = 0. 01 M. Al p. e. abbiamo una soluzione di HNO 2 0. 005 M. Il p. H al punto equivalente è: p. H = ½(p. KA log C) = ½(3. 35 + 2. 30) = 2. 82 L’indicatore consigliato è il metilarancio che ha un p. H di viraggio, p. HP. F. , di 2. 7. In accordo all’equazione (4) si ha: = [H 3 O+]P. F. C×KA/[H 3 O+]P. F = 10 2. 7 M (0. 005 M× 10 3. 35 M/10 2. 7 M) = 17. 5% L’errore di titolazione è positivo in quanto ci siamo fermati dopo il punto equivalente.

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI MONOPROTICI Esempio Calcolare l’errore di titolazione per CH 3 COONa C 0 = 0. 1 M (p. KA = 4. 76) con HCl C 0 T = 0. 1 M. Al p. e. abbiamo una soluzione di CH 3 COOH 0. 05 M. Il p. H al punto equivalente è: p. H = ½(p. KA log C) = ½(4. 76 + 1. 30) = 3. 03 L’indicatore che si potrebbe utilizzare è il blu di bromofenolo che ha un p. H di viraggio, p. H P. F. , di 3. 1. In accordo all’equazione (4) si ha: = [H 3 O+]P. F. C×KA/[H 3 O+]P. F = 10 3. 1 M (0. 05 M× 10 4. 76 M/10 3. 1 M) = 0. 6% L’errore di titolazione è negativo in quanto ci siamo fermati prima del punto equivalente. Esempio Calcolare l’errore di titolazione per NH 3 C 0 = 0. 01 M (p. KA = 9. 24) con HCl C 0 T = 0. 01 M. Al p. e. abbiamo una soluzione di NH 4 Cl 0. 005 M. Il p. H al punto equivalente è: p. H = ½(p. KA log C) = ½(9. 24 + 2. 30) = 5. 77 L’indicatore che si potrebbe utilizzare è il blu di bromotimolo che ha un p. H di viraggio, p. H P. F. , di 5. 1. In accordo all’equazione (4) si ha: = [H 3 O+]P. F. C×KA/[H 3 O+]P. F = 10 5. 1 M (0. 005 M× 10 9. 24 M/10 5. 1 M) = 0. 15% L’errore di titolazione è positivo in quanto ci siamo fermati dopo il punto equivalente.

CURVA DI TITOLAZIONE DI PROTOLITI DEBOLI POLIVALENTI ACIDO DIPROTICO Si consideri la titolazione di un acido diprotico, H 2 CO 3 (p. KA 1 = 6. 35, p. KA 2 = 10. 33), indicato con H 2 A, di concentrazione C 0 = 0. 1 M e volume iniziale V 0 = 100 cm 3. Le reazioni che avvengono durante la titolazione con una base forte, come Na. OH, a concentrazione C 0 T, per aggiunta di volumi VT, sono: H 2 CO 3 + OH HCO 3 + H 2 O KA 1/KW = 107. 65 HCO 3 + OH CO 32 + H 2 O KA 2/KW = 103. 67 Bilancio di massa dell’acido C = C 0 V 0/VTOT Bilancio di massa del titolante CT = C 0 TVT/VTOT Inizio titolazione: p. H = ½(p. KA 1 log. C 0) = 3. 67 Prima del I p. e. : [HA ] = CT = C 0 V 0/VTOT [H 2 A] = C–[HA ] = C CT CT×[H 3 O+] KA 1 = C CT Da cui p. H = p. KA 1 + log C CT

CURVA DI TITOLAZIONE DI PROTOLITI DEBOLI POLIVALENTI Al I p. e. : C = CT soluzione di Na. HA C M p. H = ½(p. KA 1 + p. KA 2) = 8. 34 Dopo il I p. e. : HA + OH A 2 + H 2 O [H 2 A] 0 [A 2 ] = CT C Dal bilancio di massa: [HA ] = C [A 2 ] = 2 C CT (CT C)×[H 3 O+] KA 2 = 2 C CT (CT C) Da cui p. H = p. KA 2 + log (2 C CT) Al II p. e. : 2 C = CT soluzione di Na 2 A C M p. H = ½(p. KA 2 + p. KW + log C ) = 11. 42 Dopo il II p. e. : [OH ] = (CT 2 C) p. H = p. KW log (CT 2 C)
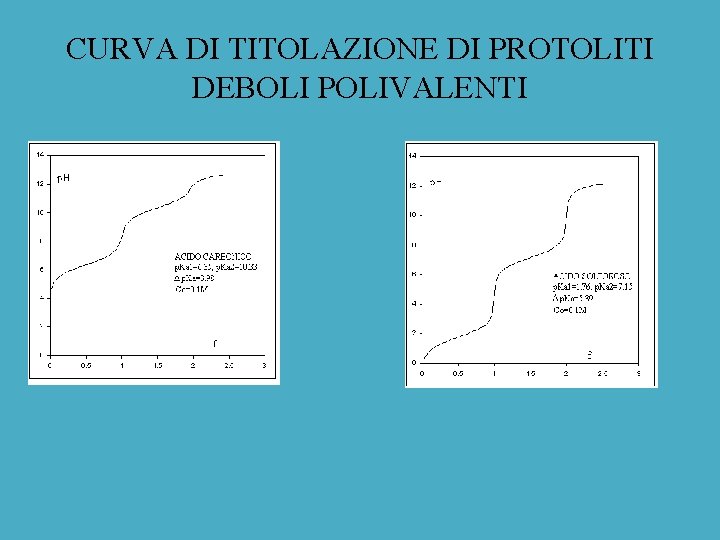
CURVA DI TITOLAZIONE DI PROTOLITI DEBOLI POLIVALENTI

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI POLIPROTICI Esempio Calcolare l’errore di titolazione per H 2 SO 3 C 0 = 0. 1 M (p. KA 1 = 1. 76; p. KA 2 = 7. 15) con Na. OH C 0 T = 0. 1 M arrestando l’aggiunta di titolante al I punto equivalente. Al I p. e. abbiamo una soluzione di Na. HSO 3 0. 05 M che è un anfolita quindi: [H 2 SO 3] = [SO 32 ] Il p. H al punto equivalente è: p. H = ½(p. KA 1 + p. KA 2) = ½(1. 76 + 7. 15) = 4. 45 L‘errore di titolazione è: = [H 2 SO 3] [SO 32 ] (le concentrazioni si riferiscono al punto finale) L’indicatore che si potrebbe utilizzare è il blu di bromofenolo che ha un p. H di viraggio, p. H P. F. , di 5. 1. Poiché ci arrestiamo dopo il p. e. [SO 32 ] [H 2 SO 3] e l’errore di titolazione è positivo. Le concentrazioni di SO 32 e H 2 SO 3 si ottengono dal p. H di arresto della titolazione e dalle costanti acide. In particolare si ha: [SO 32 ]P. F. = [HSO 3 ]×KA 2/[H 3 O+]P. F. = (0. 05 M× 10 7. 15 M)/10 5. 1 M = 4. 45× 10 4 M [H 2 SO 3]P. F. = [HSO 3 ]×[H 3 O+]P. F. /KA 1 = (0. 05 M× 10 5. 1 M)/10 1. 76 M = 2. 28× 10 5 M L’errore di titolazione è: = [SO 32 ]P. F. [H 2 SO 3]P. F. = 4. 45× 10 4 M 2. 28× 10 5 M = 0. 84%

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI POLIPROTICI Esempio Calcolare l’errore di titolazione per H 2 SO 3 C 0 = 0. 1 M (p. KA 1 = 1. 76; p. KA 2 = 7. 15) con Na. OH C 0 T = 0. 1 M arrestando l’aggiunta di titolante al II punto equivalente. Al II p. e. abbiamo una soluzione di Na 2 SO 3 0. 033 M Il p. H al punto equivalente è: p. H = ½(p. KW + p. KA 2 + log C) = ½(14 + 7. 15 1. 48) = 9. 84 L‘errore di titolazione è: = [OH ] 2[H 2 SO 3] L’indicatore che si potrebbe utilizzare è il blu timolo che ha un p. H di viraggio, p. H P. F. , di 9. 9. Poiché ci arrestiamo dopo il p. e. l’errore di titolazione è positivo. In particolare si ha: = KW /[H 3 O+]P. F. 2([H 3 O+]2 P. F. ×C)/KA 1 KA 2 = 10 14 M 2/10 9. 9 M 2(10 19. 8 M 2× 0. 033 M)/10 1. 76 M× 10 7. 15 M = 0. 24%

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI POLIPROTICI Esempio Un campione di Na 2 CO 3 C 0 = 0. 1 M (p. KA 1 = 6. 36; p. KA 2 = 10. 33) è titolato con HCl C 0 T = 0. 1 M arrestando l’aggiunta di titolante al I punto equivalente, calcolare l’errore di titolazione. Al I p. e. abbiamo una soluzione di Na. HCO 3 0. 05 M che è un anfolita e si ha: [H 2 CO 3] = [CO 32 ] Il p. H al punto equivalente è: p. H = ½(p. KA 1 + p. KA 2) = ½(6. 36 + 10. 33) = 8. 34 L‘errore di titolazione è: = [H 2 CO 3] [CO 32 ] (le concentrazioni si riferiscono al punto finale) L’indicatore che si potrebbe utilizzare è la fenolftaleina che ha un p. H di viraggio, p. H P. F. , di 8. 6. Poiché ci arrestiamo prima del p. e. [CO 32 ] [H 2 CO 3] l’errore di titolazione è negativo. Le concentrazioni di CO 32 e H 2 CO 3 si ottengono dal p. H di arresto della titolazione e dalle costanti acide. In particolare si ha: [CO 32 ]P. F. = [HCO 3 ]×KA 2/[H 3 O+]P. F. = (0. 05 M× 10 10. 33 M)/10 8. 6 M = 9. 31× 10 4 M [H 2 CO 3]P. F. = [HCO 3 ]×[H 3 O+]P. F. /KA 1 = (0. 05 M× 10 9. 6 M)/10 6. 36 M = 2. 88× 10 5 M L’errore di titolazione è, quindi: = [H 2 CO 3]P. F. [CO 32 ]P. F. = 2. 88× 10 5 M 9. 31× 10 4 M = 1. 8%

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI POLIPROTICI Esempio Un campione di Na 2 CO 3 C 0 = 0. 1 M (p. KA 1 = 6. 36; p. KA 2 = 10. 33) è titolato con HCl C 0 T = 0. 1 M arrestando l’aggiunta di titolante al II punto equivalente, calcolare l’errore di titolazione. Al II p. e. abbiamo una soluzione di H 2 CO 3 0. 033 M Il p. H al punto equivalente è: p. H = ½(p. KA 1 log C) = ½(6. 36 + 1. 48) = 3. 92 L‘errore di titolazione è: = [H 3 O+] 2[CO 32 ] L’indicatore che si potrebbe utilizzare è il rosso metile che ha un p. H di viraggio, p. H P. F. , di 4. 0. Poiché ci arrestiamo prima del p. e. l’errore di titolazione è negativo. In particolare si ha: = 2(C×KA 1×KA 2/[H 3 O+]2 P. F. ) [H 3 O+]P. F. = 2(0. 033 M× 10 6. 36 M× 10 10. 33 M/10 8. 0 M 2) 10 4. 0 M = 0. 2%

ERRORE DI TITOLAZIONE DI PROTOLITI DEBOLI POLIPROTICI Esempio Si consideri una soluzione di acido tartarico, H 2 T (p. KA 1 = 3. 02, p. KA 2 = 4. 53) che rappresenta l’acido in maggiore quantità nel vino, C 0 = 0. 1 M titolata con una soluzione di Na. OH C 0 T = 0. 1 M. Calcolare l’errore di titolazione arrestando l’aggiunta di titolante al II punto equivalente. Al II p. e. abbiamo una soluzione di Na 2 T 0. 033 M Il p. H al II punto equivalente è: p. H = ½(p. KW + p. KA 2 + log C) = ½(14 + 4. 53 1. 48) = 8. 52 L‘errore di titolazione in questo caso è: = [OH ] 2[H 2 T] L’indicatore che si potrebbe utilizzare è il rosso fenolo che ha un p. H di viraggio, p. HP. F. , di 8. 8. Poiché ci arrestiamo dopo il p. e. l’errore di titolazione è positivo. In particolare si ha: = KW/[H 3 O+]P. F. 2(C×[H 3 O+]2 P. F. /KA 1×KA 2) = 10 14 M 2/10 8. 8 M 2(0. 033 M× 10 17. 6 M 2/10 7. 57 M 2) = 0. 013%

TITOLAZIONI DI COMPLESSAZIONE Le reazioni di formazione di complessi stabili possono essere utilizzate per la determinazione di cationi in miscele incognite. Le titolazioni di complessazione consistono nella determinazione di un metallo, aggiungendo volumi crescenti di una soluzione di legante di concentrazione nota. I leganti utilizzati possono essere: o monodentati: Cl , Br , CN , ecc. o polidentati: trietilammina, acido etilendiamminotetracetico (EDTA), ecc. TITOLAZIONI CON EDTA (CHELOMETRIA) Le costanti di formazione dei chelati sono maggiori di quelle dei complessi analoghi con leganti monodentati. Il legante più utilizzato è l’EDTA, un acido esaprotico (nella forma completamente protonata carica, H 6 Y 2+). p. KA = 1. 5 HOOC CH 2 COOH p. KA = 0 p. KA = 6. 16 +HN CH 2 NH+ p. KA = 10. 3 p. KA = 2. 7 HOOC CH 2 COOH p. KA = 2. 01
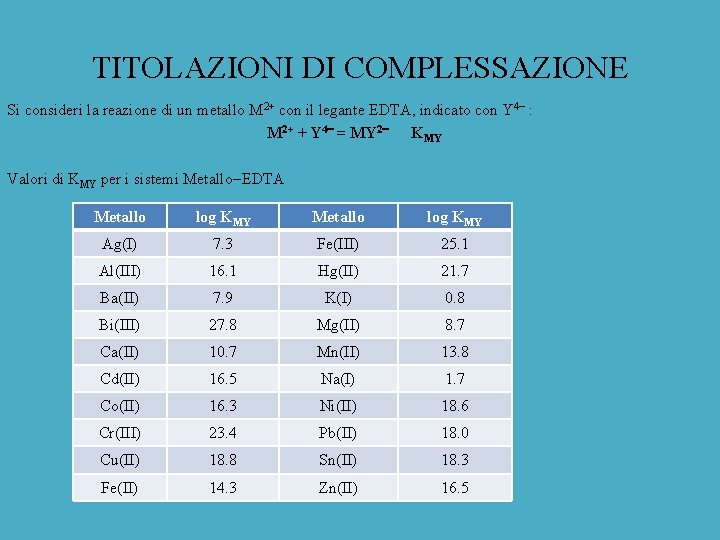
TITOLAZIONI DI COMPLESSAZIONE Si consideri la reazione di un metallo M 2+ con il legante EDTA, indicato con Y 4 : M 2+ + Y 4 = MY 2 KMY Valori di KMY per i sistemi Metallo EDTA Metallo log KMY Ag(I) 7. 3 Fe(III) 25. 1 Al(III) 16. 1 Hg(II) 21. 7 Ba(II) 7. 9 K(I) 0. 8 Bi(III) 27. 8 Mg(II) 8. 7 Ca(II) 10. 7 Mn(II) 13. 8 Cd(II) 16. 5 Na(I) 1. 7 Co(II) 16. 3 Ni(II) 18. 6 Cr(III) 23. 4 Pb(II) 18. 0 Cu(II) 18. 8 Sn(II) 18. 3 Fe(II) 14. 3 Zn(II) 16. 5
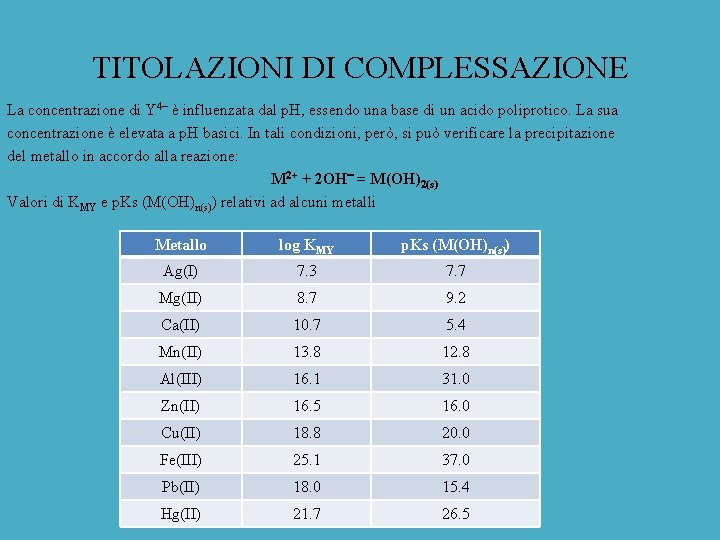
TITOLAZIONI DI COMPLESSAZIONE La concentrazione di Y 4 è influenzata dal p. H, essendo una base di un acido poliprotico. La sua concentrazione è elevata a p. H basici. In tali condizioni, però, si può verificare la precipitazione del metallo in accordo alla reazione: M 2+ + 2 OH = M(OH)2(s) Valori di KMY e p. Ks (M(OH)n(s)) relativi ad alcuni metalli Metallo log KMY p. Ks (M(OH)n(s)) Ag(I) 7. 3 7. 7 Mg(II) 8. 7 9. 2 Ca(II) 10. 7 5. 4 Mn(II) 13. 8 12. 8 Al(III) 16. 1 31. 0 Zn(II) 16. 5 16. 0 Cu(II) 18. 8 20. 0 Fe(III) 25. 1 37. 0 Pb(II) 18. 0 15. 4 Hg(II) 21. 7 26. 5

TITOLAZIONI DI COMPLESSAZIONE Influenza del p. H sugli equilibri di complessazione Nella zona di p. H basico, l’equilibrio acido base, per la specie H 4 Y, che predomina è: HY 3 + H 2 O = Y 4 + H 3 O+ Quindi la concentrazione totale di EDTA è: CT ≈ [HY 3 ] + [Y 4 -] (le specie H 4 Y, H 3 Y e H 2 Y 2 sono trascurabili) La frazione di EDTA presente come Y 4 è: [Y 4 ] 4 = [Y 4 ] = 4×CT Poiché [HY 3 ] = [Y 4 ]×[H 3 O+]/KA 4 si ha: [Y 4 ] 4 = = CT [HY 3 ] + [Y 4 ] Semplificando si ha: 1 4 = 1 + H 3 O+ /KA 4

TITOLAZIONI DI COMPLESSAZIONE COSTANTE CONDIZIONALE La costante termodinamica di stabilità del complesso MY 2 è data: MY 2 KMY = da cui si ha: KMY 4 = [M 2+] [Y 4 ] ([M 2+] ( 4 CT) [M 2+] CT MY 2 Si definisce costante condizionale la grandezza: K’MY = KMY 4 = [M 2+] CT Si chiama costante “condizionale” perché è costante quando il p. H è costante riarrangiando si ha: KMY K’MY = con KA 4 = 10 -10. 3 1 + H 3 O+ /KA 4 Dall’equazione si osserva che all’aumentare del p. H la costante condizionale aumenta e si ha: K’MY KMY

TITOLAZIONI DI COMPLESSAZIONE SCELTA DELLE CONDIZIONI DI TITOLAZIONE SCELTA DEL p. H DI TITOLAZIONE Dalla definizione di costante condizionale K’MY: KMY K’MY = 1 + H 3 O+ /KA 4 Per avere valori elevati di K’MY (reazione di complessazione spostata a destra) conviene eseguire la titolazione ad un p. H elevato, in modo tale che K’MY KMY Occorre però valutare la possibile precipitazione del catione come idrossido, che sottrae metallo al legante. Limite massimo di p. H per eseguire la titolazione

CURVA DI TITOLAZIONE COMPLESSOMETRICA La titolazione permette la determinazione di un metallo (es. M 2+ ) contenuto in una soluzione di volume V 0 e concentrazione iniziale (incognita) C 0, aggiungendo volumi crescenti VT di una soluzione di legante Y 4 (EDTA) di concentrazione C 0 T (in genere 0. 02 0. 05 M). Per un generico punto della titolazione: M 2+ + Y 4 = MY 2 K’MY = MY 2 ×( M 2+ × Y 4 ) 1 CM = C 0 V 0/VTOT = M 2+ + MY 2 CT = C 0 TVT/VTOT = Y 4 + MY 2 dove VTOT = V 0+VT In analogia alle titolazioni acido base, si sceglie come variabile dipendente la grandezza p. M = log [M 2+] Si consideri la titolazione di un metallo con p. K’MY = 20, ad un p. H fissato (p. K’MY = log K’MY). Ponendo V 0 = 50 cm 3, C 0 = 0. 01 M e C 0 T = 0. 01 M , si costruisce la curva di titolazione riportando il p. M in funzione della frazione titolata f = CT/CM = C 0 TVT/C 0 V 0
![CURVA DI TITOLAZIONE COMPLESSOMETRICA Inizio titolazione: [M 2+] = C 0 = 0. 01 CURVA DI TITOLAZIONE COMPLESSOMETRICA Inizio titolazione: [M 2+] = C 0 = 0. 01](http://slidetodoc.com/presentation_image/26be13d6799f5580dc4058a5758cf6cd/image-34.jpg)
CURVA DI TITOLAZIONE COMPLESSOMETRICA Inizio titolazione: [M 2+] = C 0 = 0. 01 M p. M = 2 Prima del p. e. : [M 2+] >> [Y 4 ] [M] = CM CT p. M = log (CM CT) Al p. e. : CM = CT [M 2+] = [Y 4 ] = (CM /K’MY)1/2 [M 2+] = [Y 4 ] = 10 8. 85 M p. M = 8. 85 Dopo il p. e. : [Y 4 ] >> [M 2+] [Y 4 ] = CT–CM [M 2+] = CM/( K’MY×[Y 4 ]) p. M = p. K’MY + log ((CT CM)/CM)

INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI COMPLESSOMETRICHE Gli indicatori per la determinazione dei cationi si chiamano indicatori metallocromici. Sono acidi organici (H 3 I) che assumono una colorazione quando sono complessati ai cationi metallici differente dal colore della forma libera. Anche per il complesso Metallo Indicatore (I) occorre considerare la costante condizionale: M 2+ + Y 4 = MY 2 K’MY M 2+ + I 3 = MI K’MI Caratteristiche dell’indicatore: o K’MI elevata; o K’MI < K’MY (al p. e. Y deve spostare I dal metallo); o Velocità di dissociazione di MI elevata. Intervallo di viraggio M 2+ + I 3 = MI p. M = log M 2+ = log K’MI log ( MI / I 3 ) Come per gli indicatori acido base, il colore di una forma prevale sull’altra quando la sua concentrazione è 10 volte maggiore. In analogia agli indicatori acido base si ottiene l’intervallo di viraggio: p. M = log. K’MI 1

INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI COMPLESSOMETRICHE Il valore del p. H della titolazione influisce anche il punto di viraggio (in quanto varia la costante condizionale dell’indicatore). La scelta dell’indicatore si effettua valutando [M]p. e. e scegliendo un indicatore per cui: p. Mp. e. = log K’MI 1 ALCUNI INDICATORI METALLOCROMICI Nero Eriocromo T (NET) E’ un acido triprotico (H 3 I): p. KA 1 = 3. 9; p. KA 2 = 6. 3; p. KA 3 = 11. 6 p. KA 2 = 6. 3 p. KA 3 = 11. 6 H 2 I HI 2 I 3 rosso blu arancione I complessi Metallo–NET sono rossi. p. H di impiego: 7 11 Variazione di colore: rosso (M NET) – blu (HI 2 ) a p. H = 9 10 Impieghi: titolazione del Mg(II)
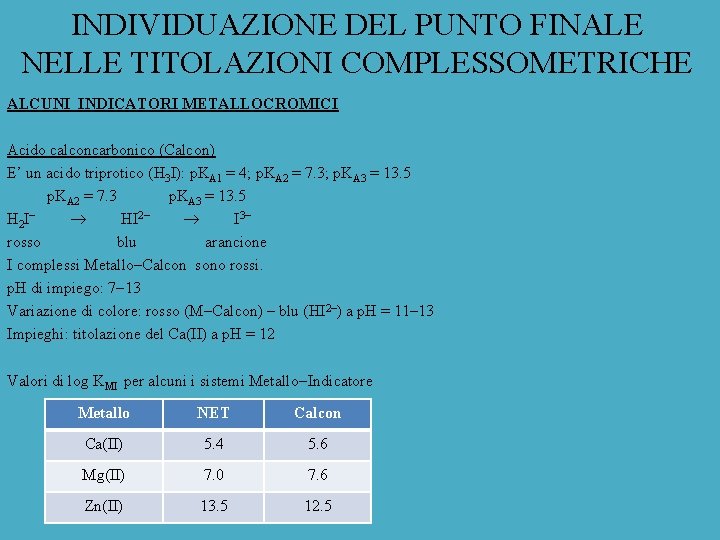
INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI COMPLESSOMETRICHE ALCUNI INDICATORI METALLOCROMICI Acido calconcarbonico (Calcon) E’ un acido triprotico (H 3 I): p. KA 1 = 4; p. KA 2 = 7. 3; p. KA 3 = 13. 5 p. KA 2 = 7. 3 p. KA 3 = 13. 5 H 2 I HI 2 I 3 rosso blu arancione I complessi Metallo–Calcon sono rossi. p. H di impiego: 7 13 Variazione di colore: rosso (M Calcon) – blu (HI 2 ) a p. H = 11 13 Impieghi: titolazione del Ca(II) a p. H = 12 Valori di log KMI per alcuni i sistemi Metallo Indicatore Metallo NET Calcon Ca(II) 5. 4 5. 6 Mg(II) 7. 0 7. 6 Zn(II) 13. 5 12. 5

ERRORE NELLE TITOLAZIONI COMPLESSOMETRICHE Al punto equivalente CT = CM Dai bilanci di massa si ottiene: Y 4 = M 2+ (al p. e. ) Dalla definizione di errore assoluto si ha: = CT CM L’errore relativo è: R = / CM = ( Y 4 M 2+ ) / CM Y 4 e M 2+ si riferiscono al punto finale della titolazione. o [M 2+] si ottiene in dipendenza del tipo di indicatore utilizzato in particolare deve essere verificato: p. MP. F. = log K’MI che corrisponde alla massima variazione di colore dell’indicatore. Tale uguaglianza si può raggiungere variando opportunamente il p. H, così da indurre una variazione della costante condizionale dell’indicatore tale da soddisfare la precedente equazione. o [Y 4 ] è ottenuta nota [M 2+] al punto finale e nota la costante condizionale del complesso MY 2 In accordo all’equazione K’MY = KMY 4 a p. H alcalini 4 1 e K’MY tende al suo massimo valore: KMY Occorre, tuttavia, valutare la possibile precipitazione di fasi solide, che sottraggono metallo al legante.

ERRORE NELLE TITOLAZIONI COMPLESSOMETRICHE Esempio Stabilire le condizioni di titolazione se una soluzione di Mg(II) CM = 0. 01 M (al punto finale) è titolata con EDTA (log KMY = 8. 7). Stabilire inoltre l’indicatore metallocromico più adatto nonché calcolare l’errore di titolazione. Per valutare le condizioni di titolazione, calcoliamo, anzitutto, il p. H di precipitazione di Mg(OH) 2(s) [OH ] = (Ks/[Mg 2+])1/2 = (10 9. 2 M 3/0. 01 M)1/2 = 10 3. 6 M da cui p. H = 10. 4 Il p. H minimo di titolabilità è 10 quindi è conveniente l’impiego del NET (p. H = 7 11) come indicatore A p. H = 10 si ha: 4 = (1 + (10 10 M/10 10. 26 M)) 1 = 0. 355 e K’MY = 108. 7 M 1 0. 355 = 108. 25 M 1 p. MP. E. = 1/2(log K’MY log CM) = 1/2(8. 25 + 2) = 5. 13 Deve verificarsi al punto equivalente: p. M = log K’MIn Per il NET si ha: log KMIn = 7. 0 (e KA 3 = 10 11. 6 M) A p. H = 10 si ha: 3 = 1/(1 + (10 10 M/10 11. 6 M)) = 0. 0245 e K’MIn = KMIn 3 = 107 M 0. 0245 = 105. 4 M log K’MIn = 5. 4 anziché p. M = 5. 13 riferito al punto equivalente l’errore di titolazione è positivo in quanto ci arrestiamo dopo il punto equivalente. L’errore che si commette è: [Mg 2+] = 10 5. 4 M = 3. 98 10 6 M Y = CM/(K’MY× Mg 2+ ) = 0. 01 M/(108. 25 M 1 10 5. 4 M) = 1. 41 10 5 M R = ( Y M )/CM = (1. 41 10 5 3. 98 10 6) M/0. 01 M = 1. 012 10 3 = 0. 1%

ERRORE NELLE TITOLAZIONI COMPLESSOMETRICHE Esempio Stabilire le condizioni di titolazione se una soluzione di Ca(II) CM = 0. 01 M (al punto finale) è titolata con EDTA (log KMY = 10. 7). Stabilire inoltre l’indicatore metallocromico più adatto nonché calcolare l’errore di titolazione. Per valutare le condizioni di titolazione, calcoliamo, anzitutto, il p. H di precipitazione di Ca(OH) 2(s) [OH ] = (Ks/[Ca 2+])1/2 = (10 5. 4 M 3/0. 01 M)1/2 = 10 1. 7 M da cui p. H = 12. 3 Il p. H minimo di titolabilità è 12 quindi se volessimo impiegare il NET (p. H = 7 11) come indicatore è possibile fino ad un p. H massimo di 11. A p. H = 11 si ha: 4 = (1 + (10 11 M/10 10. 26 M)) 1 = 0. 846 e K’MY = 1010. 7 M 1 0. 846 = 1010. 63 M 1 p. MP. E. = 1/2(log K’MY log CM) = 1/2(10. 63 + 2) = 6. 32 Deve verificarsi al punto equivalente: p. M = log K’MIn Per il NET si ha: log KMIn = 5. 4 (e KA 3 = 10 11. 6 M) A p. H = 11 si ha: 3 = 1/(1 + (10 11 M/10 11. 6 M)) = 0. 2 e K’MIn = KMIn 3 = 105. 4 M 0. 2 = 104. 7 M log K’MIn = 4. 7 anziché p. M = 6. 32 riferito al punto equivalente l’errore di titolazione è negativo in quanto ci arrestiamo prima del punto equivalente. L’errore che si commette è: [Mg 2+] = 10 4. 7 M = 2. 00 10 5 M Y = CM/(K’MY× Mg 2+ ) = 0. 01 M/(1010. 63 M 1 10 4. 7 M) = 1. 17 10 8 M R = ( Y M )/CM = (1. 17 10 8 2. 00 10 5) M/0. 01 M = 2. 0 10 3 = 0. 2% La titolazione può essere condotta con l’utilizzo dell’acido calconcarbonico come indicatore

EQUILIBRI DI SOLUBILITA’ Un equilibrio si dice eterogeneo quando coinvolge specie che si trovano in fasi differenti. Un semplice equilibrio eterogeneo è quello in cui una sostanza è distribuita tra una fase solida ed una liquida. L’equilibrio di solubilità si stabilisce tra un solido e la fase acquosa in equilibrio. SOLUBILITA’ E PRODOTTO DI SOLUBILITA’ Se in soluzione un composto poco solubile è in equilibrio con la fase liquida, tale soluzione si dice satura. In condizioni di pressione e temperatura fissate, la concentrazione di equilibrio della sostanza si dice solubilità. Se la concentrazione è maggiore di quella di equilibrio, la soluzione si dice soprassatura. La solubilità di una sostanza dipende anche dalla grandezza delle particelle. Per particelle con diametro maggiore di 10 m, non si notano più variazioni di solubilità. Considerando un solido poco solubile, come Ba. SO 4 in acqua si ha: Ba. SO 4(S) = Ba. SO 4(aq) K = [Ba. SO 4(aq)] Ba. SO 4(aq) = Ba 2+ + SO 42 K = [Ba 2+]×[SO 42 ]/[Ba. SO 4(aq)] K×[Ba. SO 4(aq)] = [Ba 2+]×[SO 42 ] = K×K = KS La costante Ks si chiama prodotto di solubilità del sale. KS = [Ba 2+]×[SO 42 ]

EQUILIBRI DI SOLUBILITA’ Il prodotto di solubilità consente di stabilire il punto di inizio precipitazione. Esempio Sia data una soluzione di Ag. NO 3 4 m. M. Calcolare la concentrazione di Cl da raggiungere affinché inizi a precipitare Ag. Cl. [Cl ] = Ks/[Ag+] = 4. 4× 10 8 M Esempio Discutere sull’ordine di precipitazione degli ioni Cl , Br , I e Cr. O 42 , presenti in una soluzione in Concentrazione uguale a 0. 01 M, per aggiunta di Ag. NO 3 0. 1 M. [Ag+]×[Cl ] = 10 9. 75 [Ag+]×[Br ] = 10 12. 27 [Ag+]×[I ] = 10 16. 09 [Ag+]2×[Cr. O 42 ] = 10 11. 9 Per stabilire ciò, occorre valutare la solubilità dei vari precipitati: Ag. Cl: s = 1. 33× 10– 5 M Ag. Br: s = 1. 36× 10– 6 M Ag. I: s = 1. 11× 10– 8 M Ag 2 Cr. O 4: s = 1. 08× 10– 4 M

EQUILIBRI DI SOLUBILITA’ Fattori che influenzano la solubilità in un composto poco solubile: § Effetto dello ione a comune; § Presenza di altri equilibri (acido base; complessazione, redox) EFFETTO DELLO IONE A COMUNE La solubilità di un composto poco solubile diminuisce per effetto dello ione in comune. Esempio Calcolare la solubilità di Ba. SO 4(S) in una soluzione 0. 01 M di Ba. Cl 2. (KS = 1. 1× 10 10) Ba. SO 4(aq) = Ba 2+ + SO 42 s+0. 01 s KS = [Ba 2+]×[SO 42 ] = (s + 0. 01)×s s Ks/0. 01 M = 1. 1 10 8 M in assenza di Ba. Cl 2 s =1. 04× 10 5 M

EQUILIBRI DI SOLUBILITA’ PRESENZA DI ALTRI EQUILIBRI (acido base; complessazione, redox) La solubilità di un composto poco solubile aumenta se il catione e/o anione è coinvolto in altri equilibri. Esempio Scrivere l’espressione della solubilità in acqua di: a) Ag. CN(S) (p. KS = 15. 8) b) Ca. F 2(S) (p. KS = 10. 5) a) Ag. CN(S) CN + H 2 O = HCN + H 3 O+ s = [Ag+] = CCN = [CN ] + [HCN] b) Ca. F 2(S) F + H 2 O = HF + H 3 O+ s = [Ca 2+] = ½×CF = [F ] + [HF]

EQUILIBRI DI SOLUBILITA’ Esempio Calcolare la solubilità di Ca. CO 3 in HCl 1. 0× 10 4 M (p. KS = 8. 3; p. KA 1 = 6. 36; p. KA 2 10. 33) p. H = 4 KS = [Ca 2+]×[CO 32 ] = 10 8. 3 [H 3 O+] Cca = [Ca 2+] = CCO 3 = [CO 32 ] + [HCO 3 ] = [CO 32 ]×(1 + ) 10 10. 33 Da cui si ha: [Ca 2+] = (10 8. 3×(1 + [H 3 O+]/10 10. 33))1/2 = 2. 6× 10 3 M

EQUILIBRI DI SOLUBILITA’ SEPARAZIONE MEDIANTE PRECIPITAZIONE FRAZIONATA E’ un metodo di separazione. La presenza di fenomeni secondari (coprecipitazione per occlusione, adsorbimento, formazione di soluzioni solide) può condurre a precipitati non puri. Esempio E’ possibile separare Ba(II) da Sr(II) da una soluzione contenente Ba. Cl 2 0. 01 M e Sr(NO 3)2 0. 01 M, mediante precipitazione con una soluzione di Na 2 SO 4 1 M ? [Ba 2+]×[SO 42 ] = 1. 1× 10 10 [Sr 2+]×[SO 42 ] = 2. 8× 10 7 In accordo ai valori di p. KS precipita prima Ba. SO 4. [Ba 2+]/[Sr 2+] = rapporto ionico = 4. 0× 10 3 Il rapporto ionico definisce le condizioni di precipitazione del secondo composto dopo che è avvenuta la precipitazione del primo composto. In particolare si ha: [Ba 2+] = 4. 0× 10 3×[Sr 2+] = 0. 01 M× 4. 0× 10 3 = 4. 0× 10 5 M Quest’ultimo valore rappresenta la quantità di Ba 2+ che rimane in soluzione quando inizia a precipitare lo ione Sr 2+ che in percentuale di ione libero è: % [Ba 2+] = (4. 0× 10 5 M/0. 01 M)× 100 = 0. 4% In accordo al valore si può ritenere che la separazione è pressoché “quantitativa”.

EQUILIBRI DI SOLUBILITA’ Esempio Ad una soluzione contenente Tl+ 0. 01 M, Pb 2+ 0. 02 M e Ag+ 0. 03 M è aggiunto Na. Cl 0. 1 M. Quale cloruro precipita per primo? E’ possibile, inoltre, separare i tre ioni metallici mediante precipitazione frazionata? Ks = [Tl+] [Cl ] = 10 3. 46 M 2; Ks = [Pb 2+] [Cl ]2 = 10 4. 08 M 3; Ks = [Ag+] [Cl ] = 10 9. 75 M 2 In accordo alle concentrazioni dei tre ioni metallici, la concentrazione di cloruro sarà: [Cl ] = (Ks/[Tl+]) = (10 3. 46 M 2/0. 01 M) = 10 1. 46 M [Cl ] = (Ks/Pb 2+])1/2 = (10 4. 08 M 3/0. 02 M)1/2 = 10 1. 19 M [Cl ] = (Ks/[Ag+]) =(10 9. 75 M 2/0. 03 M) = 10 8. 23 M Precipiteranno, quindi, nell’ordine: Ag. Cl, Tl. Cl, Pb. Cl 2 In particolare quando inizia a precipitare Tl. Cl, risulta che: [Ag+] = 10 9. 75 M 2/10 1. 46 M = 10 8. 29 M La percentuale di Ag+ in soluzione è: %[Ag+]restante = (10 8. 29 M/0. 03 M) 100 = 2 10 5% Quando, invece, inizia a precipitare Pb. Cl 2, risulta che: [Tl+] = 10 3. 46 M 2/10 1. 19 M = 10 2. 27 M La percentuale di Tl+ in soluzione è: %[Tl+]restante = (10 2. 27 M/0. 01 M) 100 = 54% E’ possibile separare quantitativamente Ag. Cl da Tl. Cl ma non eseguire la separazione tra Tl. Cl e Pb. Cl 2.

TITOLAZIONI DI PRECIPITAZIONE Sono titolazioni in cui si frutta la formazione di un composto poco solubile. Il reagente più utilizzato è lo ione Ag+, sottoforma di Ag. NO 3, che forma solidi insolubili con numerosi anioni (Argentimetria). Ag+ + Cl = Ag. Cl(S) Ag+ + Br = Ag. Br(S) Ag+ + I = Ag. I(S) 2 Ag+ + S 2 = Ag 2 S(S) Ag+ + SCN = Ag. SCN(S) 2 Ag+ + Cr. O 42 = Ag 2 Cr. O 4(S) 3 Ag+ + As. O 43 = Ag 3 As. O 4(S) 3 Ag+ + PO 43 = Ag 3 PO 4(S) 2 Ag+ + C 2 O 42 = Ag 2 C 2 O 4(S) 2 Ag+ + Mo. O 42 = Ag 2 Mo. O 4(S) 3 Ag+ + VO 43 = Ag 3 VO 4(S) 2 Ag+ + Se. O 42 = Ag 2 Se. O 4(S) 4 Ag+ + Fe(CN)64 = Ag 4 Fe(CN)6(S) p. Ks = 9. 7 p. Ks = 12. 3 p. Ks = 16. 1 p. Ks = 49. 2 p. Ks = 12. 0 p. Ks = 11. 9 p. Ks = 22. 0 p. Ks = 15. 8 p. Ks = 11. 0 p. Ks = 11. 6 p. Ks = 24. 0 p. Ks = 8. 9 p. Ks = 27. 1

CURVA DI TITOLAZIONE DI PRECIPITAZIONE Si consideri la precipitazione con una soluzione di Ag. NO 3. Prelevando un volume V 0 contenente un generico alogenuro X (X = Cl, Br, I, SCN, ecc. . . ) con Concentrazione iniziale C 0, si effettua la titolazione aggiungendo volumi crescenti VT della soluzione di Ag+ di concentrazione C 0 T (in genere 0. 05). Per un generico punto della titolazione ha luogo la reazione: Ag+ + X = Ag. X(S) [X ] = (C 0 V 0 C 0 TVT) / VTOT Ponendo C 0 V 0 / VTOT = C e C 0 TVT / VTOT = CT si ha: [X ] = C CT Introducendo la frazione titolata f = CT/C = C 0 TVT/ C 0 V 0, si può utilizzare f al posto di VT. Si consideri la titolazione di Cl , con p. Ks = 9. 7 Si utilizza come variabile indipendente p. X = log [Cl ]. Ponendo V 0 = 100 cm 3, C 0 = 0. 1 M e C 0 T = 0. 1 M , si costruisce la curva di titolazione. Inizio titolazione: [Cl ] = C 0 = 0. 1 M, p. X = 1
![CURVA DI TITOLAZIONE DI PRECIPITAZIONE Prima del p. e. : [Cl ] >> [Ag+] CURVA DI TITOLAZIONE DI PRECIPITAZIONE Prima del p. e. : [Cl ] >> [Ag+]](http://slidetodoc.com/presentation_image/26be13d6799f5580dc4058a5758cf6cd/image-50.jpg)
CURVA DI TITOLAZIONE DI PRECIPITAZIONE Prima del p. e. : [Cl ] >> [Ag+] [Cl ] = C CT p. Cl = log [Cl ] = C CT Al p. e. : CT = C [Ag+] = [Cl ] = (Ks)1/2 = 10 4. 8 M p. Cl = 4. 8 Dopo il p. e. : [Ag+] >> [Cl ] [Ag+] = Ks/[Cl ] = CT C [Cl ] = Ks/(CT C) p. Cl = p. Ks + log (CT C) 16 p. X Ag. I 12 Ag. Br 8 Ag. Cl 4 f 0 0 0. 5 1 1. 5 2

ERRORE DI TITOLAZIONE IN ARGENTIMETRIA Errore assoluto: = CT–C (dove CT rappresenta la concentrazione totale del titolante mentre C Rappresenta quella totale del titolando). Errore relativo: R = (CT–C)/C Considerando un sale poco solubile di argento che con l’anione forma un composto a stechiometria 1: 1 si ha: Al punto equivalente: [Ag+] = [X ] Al punto finale: [Ag+] ≠ [X ] L’errore di titolazione sarà: = Ag+ P. F. X P. F. R = ( Ag+ P. F. X- P. F. )/C L’errore di titolazione dipende dal prodotto di solubilità KS del solido (Ag. X(S)), con X = Cl, Br, I, SCN, ecc. . . )

METODI DI ANALISI IN ARGENTIMETRIA METODO DI MOHR Si utilizza come titolante una soluzione di Ag. NO 3 (in genere 0. 01 M). Nel caso della determinazione dei cloruri: Ag+ + Cl = Ag. Cl(S) p. Ks = 9. 7 (bianco) Sistema di rivelazione del punto finale: Soluzione di K 2 Cr. O 4 5% (w/w). La solubilità di Ag. Cl(S) ha una solubilità s = (Ks)½ = 10 4. 8 M che è inferiore a quella di Ag 2 Cr. O 4(S) dove (s = (Ks/4)1/3 = 10 4. 2 M) quindi precipita prima Ag. Cl. Al punto finale, l’eccesso di Ag+ reagisce con il cromato, formando un precipitato rosso mattone che indica la fine della titolazione in accordo alla reazione: 2 Ag+ + Cr. O 42 = Ag 2 Cr. O 4(S) (rosso mattone) Condizioni sperimentali: La titolazione è condotta per valori di p. H nell’intervallo 6 -9. Per ottenere tale condizione, si aggiunge KHCO 3, oppure Na 2 B 4 O 7× 10 H 2 O alla soluzione. q p. H inferiori si può avere la formazione di HCr. O 4 (KA = 1. 5× 10 8) e di Cr 2 O 72 p. Ks (Ag 2 Cr 2 O 7) = 6. 7 2 Cr. O 42 + 2 H+ = Cr 2 O 72 + H 2 O K = 43 q p. H superiori si forma Ag. OH(S) (p. Ks = 7. 7)

ERRORE DI TITOLAZIONE NEL METODO DI MOHR Si può stabilire la concentrazione che deve avere l’indicatore per eseguire la titolazione. Al p. e. [Ag+] = [Cl ] = 10 4. 8 M Quindi la concentrazione di cromato deve essere: [Cr. O 42 ] = 10 11. 9/[Ag+]2 = 5. 0× 10 3 M Questo valore di concentrazione impartisce alla soluzione una colorazione gialla molto intensa, che Coprirebbe la colorazione del precipitato di Ag 2 Cr. O 4. La concentrazione impiegata nella pratica è compresa nell’intervallo: 2. 0× 10 3 M [Cr. O 42 ] 4. 0× 10 3 M In particolare per [Cr. O 42 ] = 4. 0× 10 3 M si ottiene al punto finale (p. f. ): [Ag+]P. F. = (10 11. 9/[Cr. O 42 ])½ = (10 11. 9/4. 0× 10 3)½ = 10 4. 7 M Da cui si ha: [Cl ]P. F. = (Ks/[Ag+]P. F. ) = (10 9. 7/10 4. 7) = 10 5 M Poiché l’errore di titolazione è dato come: = CT C = [Ag+]P. F. [Cl ]P. F = [Ag+]P. F (Ks/[Ag+]P. F. ) Come si osserva l’entità dell’errore di titolazione dipende sia dalla concentrazione dell’indicatore sia dalla Natura del sale insolubile che si forma (valore del Ks). Inoltre l’errore di titolazione è anche inversamente proporzionale alla concentrazione dell’alogenuro titolato.

ERRORE DI TITOLAZIONE NEL METODO DI MOHR Esempio Calcolare l’errore relativo nella titolazione di una soluzione di Br 0. 01 M, con il metodo di Mohr utilizzando una soluzione di Cr. O 42 2. 5 m. M. In accordo alla concentrazione dello ione cromato, la concentrazione di Ag+ affinché inizi la precipitazione di Ag 2 Cr. O 4 deve essere: [Ag+] = (Ks/[Cr. O 42 ])1/2 = (10 11. 9/2. 5× 10 3)1/2 = 2. 24× 10 5 M Al tempo stesso, la quantità di Br che è in equilibrio nella soluzione è: [Br ] = Ks/[Ag+] = 10 12. 27/2. 24× 10 5 = 2. 40× 10 8 M Da ciò l’errore di titolazione è: = [Ag+] [Br ] [Ag+] = (2. 24× 10 5 M/0. 01 M)× 100 = 0. 2% Se C = 0. 1 M si ottiene: R = 0. 02%

ERRORE DI TITOLAZIONE NEL METODO DI MOHR Esempio Calcolare l’errore relativo nella titolazione di una soluzione di IO 3 0. 1 M, con il metodo di Mohr utilizzando una soluzione di Cr. O 42 2. 5 m. M. In accordo alla concentrazione dello ione cromato, la concentrazione di Ag+ affinché inizi la precipitazione di Ag 2 Cr. O 4 deve essere: [Ag+] = (Ks/[Cr. O 42 ])1/2 = (10 11. 9/2. 5× 10 3)1/2 = 2. 24× 10 5 M Al tempo stesso, la quantità di IO 3 che è in equilibrio nella soluzione è: [IO 3 ] = Ks/[Ag+] = 10 7. 51/2. 24× 10 5 = 1. 38× 10 3 M Da ciò l’errore di titolazione è: = [Ag+] [IO 3 ] = (1. 38× 10 3 M/0. 1 M)× 100 = 1. 4%

METODI DI ANALISI IN ARGENTIMETRIA METODO DI VOLHARD Il metodo consente la determinazione di alogenuri in soluzioni acide (0. 2 1 M) e consiste nell’aggiunta di un eccesso di una soluzione a titolo noto di Ag. NO 3 così da precipitare tutto l’alogenuro. L’eccesso di Ag+ è determinato mediante una titolazione di ritorno con KSCN (0. 1 M). Nel caso della titolazione dei cloruri: Ag+ + Cl = Ag. Cl(S) + Ag+ (eccesso) + SCN = Ag. SCN(S) p. Ks = 12. 0 Sistema di rivelazione del punto finale. L’indicatore è Fe 3+ (allume ferrico Fe(NH 4)(SO 4)2× 12 H 2 O), in concentrazione tale che al punto finale CFe = [Fe 3+] = 0. 01 M Fe 3+ + SCN = Fe. SCN 2+ log 1 = 2. 2 rosso Il colore si evidenzia quando [Fe. SCN 2+] = 10 5 M
![ERRORE DI TITOLAZIONE NEL METODO DI VOLHARD Al p. e. : [Ag+] = [SCN ERRORE DI TITOLAZIONE NEL METODO DI VOLHARD Al p. e. : [Ag+] = [SCN](http://slidetodoc.com/presentation_image/26be13d6799f5580dc4058a5758cf6cd/image-57.jpg)
ERRORE DI TITOLAZIONE NEL METODO DI VOLHARD Al p. e. : [Ag+] = [SCN ] = (Ks(Ag. SCN))1/2 = 10 6 M Al punto finale si ha: [SCN ]P. F. = [Fe. SCN 2+]/( 1×[Fe 3+]) = 10 5/(102. 2× 0. 01) = 10 5. 2 M = ([SCN ] + [Fe. SCN 2+])–[Ag+] = ([SCN ] + [Fe. SCN 2+])–(Ks(Ag. SCN)/[SCN ]) = (10 5. 2 M + 10 5 M) (10 12 M 2/10 5. 2 M) = 10 4. 79 M R% = (10 4. 79 M/0. 1 M) 100 = 0. 016%

METODI DI ANALISI IN ARGENTIMETRIA METODO DI FAJANS Reattivo titolante: Ag. NO 3 (0. 05 M) Nel caso della determinazione dei cloruri: Ag+ + Cl = Ag. Cl(S) p. Ks = 9. 7 Sistema di rivelazione del punto finale: Impiego di indicatori di adsorbimento, composti organici (acidi deboli) che sono adsorbiti dal precipitato con variazione di colore. Requisiti dell’indicatore: 1) deve possedere carica opposta ad Ag+; 2) deve legarsi al precipitato per adsorbimento secondario; 3) la variazione di colore deve avvenire al punto equivalente. Composizione del precipitato (formato da Ag. NO 3 + Na. Cl): q prima del p. e. : (Ag. Cl(S))n Cl Na+ q dopo il p. e. : (Ag. Cl(S))n Ag+ NO 3 Aggiungendo l’indicatore di adsorbimento (In ), ad es. la fluoresceina (Ka 10 8): (Ag. Cl(S))n Ag+ + In = (Ag. Cl(S))n Ag. In giallo verde rosa Il viraggio è reversibile

ERRORE DI TITOLAZIONE NEL METODO DI FAJANS Nel caso della determinazione di Cl : Al p. e. : [Ag+] = [Cl ] = 10 4. 8 M Assumendo che: Ag. In(S) = Ag+ + In Ks(Ag. In) = 10 7 ed impiegando, inoltre, una concentrazione di indicatore pari a [In ] = 0. 001 M si ottiene: [Ag+] = Ks(Ag. In)/[In ] =10 4 M In particolare: = [Ag+] Ks(Ag. Cl)/[Ag+] = 10 4 M (10 9. 7 M 2/10 4 M) = 10 4 M R% = (10 4 M/0. 1 M) 100 = 0. 1%

EQUILIBRI DI OSSIDO RIDUZIONE PROCESSI REDOX Ossidazione: perdita di elettroni Zn(S) Zn 2+ + 2 e Riduzione: acquisto di elettroni Cl 2(g) + 2 e 2 Cl In generale un qualunque processo redox coinvolge due specie Ox e Red (coppia redox) Ox + ne = Red (semireazione) Affinché si abbia trasferimento di elettroni occorre che gli elettroni ceduti da una coppia redox devono essere acquistati da una seconda coppia redox Ox 1 + n 1 e = Red 1 semireazione catodica (riduzione) Red 2 = Ox 2 + n 2 e semireazione anodica (ossidazione) Il processo globale sarà la reazione redox n 2 Ox 1 + n 1 Red 2 = n 1 Ox 2 + n 2 Red 1
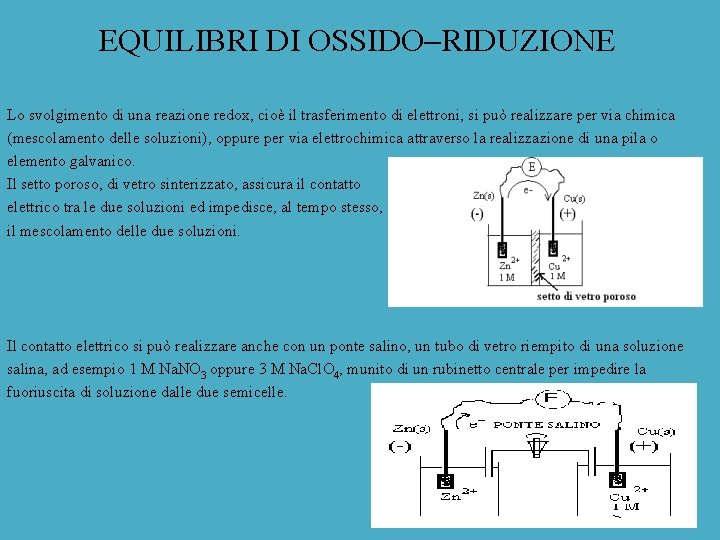
EQUILIBRI DI OSSIDO RIDUZIONE Lo svolgimento di una reazione redox, cioè il trasferimento di elettroni, si può realizzare per via chimica (mescolamento delle soluzioni), oppure per via elettrochimica attraverso la realizzazione di una pila o elemento galvanico. Il setto poroso, di vetro sinterizzato, assicura il contatto elettrico tra le due soluzioni ed impedisce, al tempo stesso, il mescolamento delle due soluzioni. Il contatto elettrico si può realizzare anche con un ponte salino, un tubo di vetro riempito di una soluzione salina, ad esempio 1 M Na. NO 3 oppure 3 M Na. Cl. O 4, munito di un rubinetto centrale per impedire la fuoriuscita di soluzione dalle due semicelle.

EQUILIBRI DI OSSIDO RIDUZIONE La relazione tra variazione di energia libera (ΔG) e la forza elettromotrice (E) di una pila è: ΔG = n. FE dove n rappresenta il numero di elettroni coinvolti nella reazione di ossidoriduzione mentre la grandezza F (96500 Coulomb/mol) è la costante di Faraday (carica elettrica trasportata da una mole di elettroni). La forza elettromotrice (f. e. m. ) o differenza di potenziale, di una pila, si indica con “E” mentre i potenziali dei singoli elettrodi si indicano con “e”. In particolare si ha: E = e(+) e( ) Quando tutte le specie coinvolte nelle semireazioni hanno concentrazioni pari a 1 M mentre le specie gassose si trovano alla pressione di 1 Atm, a 25 °C, si dice che le semicelle si trovano nelle rispettive condizioni standard. In tali condizioni la forza elettromotrice (f. e. m. o differenza di potenziale) si scrive come E°.

MISURA DELLA FORZA OSSIDANTE DI UNA SPECIE La misura della tendenza di una specie ad acquistare elettroni si misura dalla differenza di potenziale della costruita con la semireazione in esame, ad esempio Zn 2+ +2 e = Zn(S) e la semireazione di riferimento: 2 H++ 2 e = H 2(g) Si osserva, sperimentalmente, che l’elettrodo di Zn assume un potenziale negativo, in quanto la f. e. m. misurata è E = + 0. 763 V. Se tutte le concentrazioni delle specie sono pari a 1 M (per i gas si considera una pressione parziale di 1 Atm), i potenziali si chiamano “potenziali standard” e si indicano con l’apice ”°” E°=e°(+)-e°(-)= e°H – e°Zn Per la semireazione di riferimento: 2 H+ + 2 e = H 2(g) si pone per definizione e°H = 0 Allora si ha: E° = e°H – e°Zn = 0. 763 V da cui: e°Zn= 0. 763 V Nel caso del cadmio si ha: E° = + 0. 34 V, dove l’elettrodo di Cd è negativo ( ) E° = e°(+) e°( ) = e°H – e°Cd e°H = 0 e°Cd = E° = 0. 34 V

SCALA ELETTROCHIMICA DEGLI ELEMENTI Per convenzione, tutte le reazioni si scrivono come riduzione. In tal modo si costruisce la scala elettrochimica degli elementi. Nella tabella sono riportati alcuni potenziali di riduzione relativi ad alcuni elementi. Semireazione Au 3+ + 3 e = Au (S) Mn. O 4 + 8 H+ + 5 e = Mn 2+ + 4 H 2 O Ce 4+ + e = Ce 3+ Cr 2 O 72 + 14 H+ + 6 e = 2 Cr 3++7 H 2 O Ag+ + e = Ag(S) I 2 + 2 e = 2 I Cu 2+ + 2 e = Cu(S) Sn 4+ + 2 e = Sn 2+ H+ + e = ½H 2(g) Pb 2+ + 2 e = Pb(S) Sn 2+ + 2 e = Sn(S) Ni 2+ + 2 e = Ni(S) Cd 2+ + 2 e = Cd(S) Cr 3+ + 3 e = Cr(S) Zn 2+ + 2 e = Zn(S) Al 3+ + 3 e = Al(S) Ca 2+ + 2 e = Ca(S) e°, V +1. 50 +1. 49 +1. 43 +1. 33 +0. 80 +0. 54 +0. 34 +0. 15 0. 00 0. 13 0. 14 0. 25 0. 40 0. 74 0. 76 1. 50 2. 87 Il valore di e° misura la tendenza di una specie ad acquistare elettroni

REAZIONI SPONTANEE Una reazione è spontanea quando ΔG < 0 in termini di f. e. m si ha: E = e(+) e(-) > 0 Esempio Verificare se la reazione seguente è spontanea (in condizioni standard) Cu(S) + 2 Ag+ = Cu 2+ + 2 Ag(S) E° = e°(+) e°(-) = e°Ag–e°Cu = (0. 80 0. 34) V = 0. 46 V Assegnato il senso di percorrenza degli elettroni, la cella è rappresentata: ( ) Cu(s)/Cu 2+//Ag+/Ag(s) (+) con il polo (+) a destra

EQUAZIONE DI NERNST Il potenziale di un elettrodo dipende dalla natura della specie chimica e dalla concentrazione degli ioni in soluzione. RT [Ox] e = e° + log n F [Red] q Nel caso di semireazioni che contengono fasi solide il potenziale dipende solo dalla concentrazione degli ioni. Esempio Scrivere l’equazione di Nernst per la semicoppia Cu(II) Cu(s) Cu 2+ + 2 e = Cu(S) e° = + 0. 337 V e = e° + (0. 05916/2) log [Cu 2+] ([Cu(s)] = costante = 1) Esempio Scrivere l’equazione di Nernst per la semicoppia Fe(OH)3(s) Fe(OH)2(s) Fe(OH)3(S) + e = Fe(OH)2(S) + OH e° = 0. 56 V e = e° + 0. 05916 log (1/[OH ])

EQUAZIONE DI NERNST q Le sostanze gassose si esprimono in termini di pressione parziale Esempio Scrivere l’equazione di Nernst per la semicoppia Cl( I) Cl(0) Cl 2 + 2 e = 2 Cl e° = + 1. 36 V e = e° + (0. 05916/2) log p. Cl 2/[Cl ]2 q Nel caso di semireazioni che contengono ioni H+, o altre specie, il potenziale dipende dalle concentrazioni i tali ioni. Esempio Scrivere l’equazione di Nernst per il permanganato in ambiente acido Mn. O 4 + 8 H+ + 5 e = Mn 2+ + 4 H 2 O e° = + 1. 49 V e = e° + (0. 05916/5) log ([Mn. O 4 ][H+]8/[Mn 2+])

CALCOLO DELLA F. E. M. DI UNA PILA Una cella elettrochimica si schematizza scrivendo il polo negativo a sinistra. Le separazioni tra fasi sono indicate da una barra, mentre l’esistenza di un ponte salino si rappresenta con due barre. Così la pila Daniell si indica: ( ) Zn(s)/Zn 2+, 1 M // Cu 2+, 1 M /Cu(s) (+) Per valutare la f. e. m. di una pila (E) in condizioni diverse da quelle standard, occorre calcolare i potenziali dei singoli elettrodi con l’equazione di Nernst ed applicare l’equazione: E = e(+) e( ) Esempio Calcolare la f. e. m. della pila: ( ) Zn(s)/Zn 2+, 1 M // Cu 2+ , 1 M /Cu(s) (+) (e°Cu = + 0. 338 V, e°Zn = 0. 763 V) E = e(+) e( ) = e. Cu e. Zn E = e°Cu e°Zn = + 0. 338 V ( 0. 763 V) = + 1. 101 V Esempio Calcolare la f. e. m. della pila: ( ) Zn(s)/Zn 2+, 0. 05 M // Cu 2+ , 0. 01 M /Cu(s) (+) E = e(+) e( ) = e. Cu e. Zn e. Cu = e°Cu + (0. 05916/2) log [Cu 2+] = + 0. 338 V + (0. 05916/2) log (0. 01) = + 0. 279 V e. Zn= e°Zn + (0. 05916/2) log [Zn 2+] = 0. 763 V + (0. 05916/2) log (0. 05) = 0. 801 V E = + 1. 08 V

CALCOLO DELLA COSTANTE DI EQUILIBRIO DI UNA REAZIONE REDOX Per una generica reazione redox: n 2 Ox 1 + n 1 Red 2 = n 1 Ox 2 + n 2 Red 1 costituita dalle due semireazioni: Ox 1 + n 1 e = Red 1 e° 1 Red 2 = Ox 2 + n 2 e e° 2 si dimostra che la costante di equilibrio, a 25°C, è: n E° log K = 0. 05916 dove n = n 1 n 2 mentre E° = e° 1 e° 2 Dimostrazione Si consideri la reazione: 2 Ce 4+ + Sn 2+ = 2 Ce 3+ + Sn 4+ e (Ce 4+/Ce 3+) = + 1. 61 V; e (Sn 4+/Sn 2+) = + 0. 15 V All’equilibrio G = 0, n. FE = 0, quindi E = e. Ce e. Sn= 0 e. Ce = e. Sn e°Ce + (0. 05916/2) log [Ce 4+]2/[Ce 3+]2 = e°Sn + (0. 05916/2) log [Sn 4+]/[Sn 2+] e°Ce e°Sn= E = (0. 05916/2) log ([Ce 4+]2×[Sn 4+]/[Sn 2+]×[Ce 3+]2) = log K = 2×E /0. 05916 = 49. 4

TITOLAZIONI DI OSSIDO RIDUZIONE Alcune reazioni redox possono essere utilizzate per la determinazione di sostanze. In genere il titolante è rappresentato da un ossidante forte, in quanto l’impiego di riducenti porterebbe a degli inconvenienti per la presenza di O 2 (agente ossidante) nell’atmosfera. Si consideri come titolante Ox. T la cui semireazione é: Ox. T + n. Te = Red. T (e 0 T) ed il titolando Red la cui semireazione é: Ox + ne = Red (e 0) La reazione globale sarà: n. Ox. T + n. TRed = n. TOx + n. Red. T Le principali sostanze ossidanti utilizzate nelle titolazioni sono: (NH 4)2 Ce(SO 4)3 (solfato di cerio(IV) e ammonio) Ce 4+ + e = Ce 3+ e 0 T = + 1. 43 V KMn. O 4 (permanganato di potassio) Mn. O 4 + 5 Fe 2+ + 8 H+ = Mn 2+ + 5 Fe 3+ + 4 H 2 O e 0 T = + 1. 49 V K 2 Cr 2 O 7 (dicromato di potassio) Cr 2 O 72 + 6 e + 14 H+ = 2 Cr 3+ + 7 H 2 O e 0 T = + 1. 33 V I 2 (iodio) I 2(aq) + 2 e = 2 I e°T = + 0. 536 V

TITOLAZIONI DI OSSIDO RIDUZIONE POTENZIALE AL PUNTO EQUIVALENTE Il punto equivalente si raggiunge quando gli equivalenti di titolante sono uguali a quelli di titolando. In termini di Normalità, indicando con NT la normalità del titolante e con N quella del titolando, al punto equivalente si ha: NT = N La relazione tra Molarità e Normalità è: N = M n (dove n è il numero di elettroni scambiati) Indicando con CT la concentrazione molare del titolante Ox. T (Ox. T + n. Te = Red. T) e con C quella del titolando Red (Ox + ne = Red), al punto equivalente si ha: n. TCT = n. C (le concentrazioni si riferiscono al punto finale della titolazione) Per un processo generico: n. Ox. T + n. TRed = n. Red. T + n. TOx il potenziale al punto equivalente è: n. Te°T + ne° e. P. E. = n. T + n

TITOLAZIONI DI OSSIDO RIDUZIONE Dimostrazione Considerando la titolazione di Sn 2+ con Ce 4+, si ha: e°T = e°Ce = +1. 43 V e° = e°Sn = + 0. 15 V 2 Ce 4+ + Sn 2+ = 2 Ce 3+ + Sn 4+ Dai bilanci di massa: CSn = [Sn 2+] + [Sn 4+] CCe = [Ce 3+] + [Ce 4+] Al p. e. risulta: CCe = 2 CSn sostituendo si ha: [Ce 4+] = 2[Sn 2+] (valida solo al p. e. ) Scrivendo l’equazione di Nernst per il titolante ed il titolando si ha: [Ce 4+] 0. 05916 [Sn 4+] [Sn 4+] e = e°T + 0. 05916 log e = e° + log 2 e = 2 e° + 0. 05916 log [Ce 3+] 2 [Sn 2+] Sommando le due equazioni si ha: [Ce 4+]×[Sn 4+] e + 2 e = e°T + 2 e° + 0. 05916 log [Ce 3+]×[Sn 2+] Dalla stechiometria della reazione si ricava che [Ce 3+] = 2[Sn 4+] Sostituendo tale equazione nei bilanci di massa si ottiene: [Ce 4+] = 2[Sn 2+] (valido solo al p. e. ) Sostituendo nell’equazione si ha che l’argomento del logaritmo è 1. Al p. e. si ha che e = e. P. E. quindi: e°T + 2 e° 1. 43 + 2×(0. 15) e. P. E. = = + 0. 58 V 3 3

TITOLAZIONI DI OSSIDO RIDUZIONE L’equazione precedente non è di validità generale in quanto è valida solo per i sistemi le cui semireazioni non contengono specie polinucleari nonché H+ oppure OH. Esempio Scrivere l’espressione del potenziale al p. e. nella titolazione della specie Tl + con Mn. O 4 in ambiente acido (e°T = + 1. 49 V, e° = + 1. 25 V). La reazione tra il titolante (Mn. O 4 ) ed il titolando (Tl+) bilanciata è: 2 Mn. O 4 + 5 Tl+ +8 H+ = 2 Mn 2+ + 5 Tl 3+ + 4 H 2 O Al p. e. si ha per: n. TCT = n. C 5 CT = 2 C Con procedimento analogo a quello mostrato prima si ottiene: n. Te°T + ne° 0. 05916 e. P. E. = + log [H+]8 Se [H+] = 1 M si ha: n. T + n 7 5 e°T + 2 e° 0. 05916 e. P. E. = + log [H+]8 = + 1. 42 V 7

CURVA DI TITOLAZIONE DI OSSIDO RIDUZIONE Rappresenta la variazione del potenziale “e” della soluzione in funzione del volume di titolante aggiunto. Si consideri la titolazione di una soluzione di volume V 0 e di concentrazione iniziale C 0 di Fe 2+ a cui sono aggiunti volumi crescenti , VT, di una soluzione di Ce 4+ avente concentrazione iniziale C 0 T. Titolante: Ox. T + n. Te = Red. T Titolando: Red Ox + ne = Red Per questa titolazione si ha: Ox. T = Ce 4+ e Red = Fe 2+ Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ e°T = + 1. 43 V (semicoppia Ce) e° = + 0. 77 V (semicoppia Fe) Per un generico punto della titolazione: C = [Fe 2+] + [Fe 3+] = C 0 V 0/VTOT CT = [Ce 3+] + [Ce 4+] = C 0 TVT/VTOT dove VTOT = V 0 + VT Ponendo V 0 = 50 cm 3, C 0 = 0. 1 M e C 0 T = 0. 1 M, si costruisce la curva di titolazione riportando il potenziale “e” in funzione della frazione titolata f = CT/C = C 0 TVT/C 0 V 0 (in generale f = n. TCT/n. C = n. TC 0 TVT/(n. CTVT)
![CURVA DI TITOLAZIONE DI OSSIDO RIDUZIONE Prima del p. e. trascurando [Ce 4+] si CURVA DI TITOLAZIONE DI OSSIDO RIDUZIONE Prima del p. e. trascurando [Ce 4+] si](http://slidetodoc.com/presentation_image/26be13d6799f5580dc4058a5758cf6cd/image-75.jpg)
CURVA DI TITOLAZIONE DI OSSIDO RIDUZIONE Prima del p. e. trascurando [Ce 4+] si ha: [Ce 3+] = C 0 TVT/VTOT = CT [Fe 3+] = [Ce 3+] = CT (in accordo alla reazione tra titolante e tiolando) [Fe 2+] = (C 0 TV 0 C 0 TVT) /VTOT = C CT e = e° + 0. 05916 log ([Fe 3+]/[Fe 2+]) = e° + 0. 05916 log (CT/(C CT)) Al p. e. si ha: n. Te°T + ne° e. P. E. = + 1. 10 V n. T + n Dopo il p. e. si ha: [Fe 3+] >> [Fe 2+] [Ce 3+] = [Fe 3+] = C 0 TVT/VTOT = CT [Ce 4+] = (C 0 TVT C 0 V 0) /VTOT = CT C e = e°T + 0. 05916 log ([Ce 4+]/[Ce 3+]) = e°T + 0. 05916 log ((CT C)/C) In questa titolazione il punto di equivalenza coincide con il punto di massima pendenza della curva (punto di flesso).

CURVA DI TITOLAZIONE DI OSSIDO RIDUZIONE Esempio Costruire la curva di titolazione per la determinazione del Fe 2+ con una soluzione di KMn. O 4 in H 2 SO 4 0. 5 M (e°T = + 1. 49 V, e° = + 0. 77 V) Mn. O 4 + 5 Fe 2+ + 8 H+ = Mn 2+ + 5 Fe 3+ + 4 H 2 O CT = [Mn. O 4 ] + [Mn 2+] = C 0 TVT/VTOT C = [Fe 3+] + [Fe 2+] = C 0 V 0/VTOT Ponendo V 0 = 50 cm 3, C 0 = 0. 1 M e C 0 T = 0. 02 M, si costruisce la curva di titolazione riportando il Potenziale “e” in funzione di VT oppure della frazione titolata f : f = n. T CT /n. C = 5 C 0 TVT/C 0 V 0 Al p. e. si ha: e. P. E. = + 1. 37 V Come si può osservare dalla curva di titolazione, e come si può, inoltre, dimostrare matematicamente il punto di equivalenza, che corrisponde a [Fe 2+] = 5[Mn. O 4 ] non corrisponde al punto di flesso (massima pendenza), dove [Fe 2+] = [Mn. O 4 ], ma è spostato verso la semicoppia con e° maggiore.

INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE E’ un sistema redox costituito da una forma ossidata avente una colorazione differente da quella ridotta (Indicatori redox). Come per gli indicatori acido base, si definisce un intervallo di potenziale in cui avviene tale variazione di colore (intervallo di viraggio). IO + ne = IR e = e°In + (0. 05916/n) log ([IO ]/[IR]) il colore di In(Ox) predomina quando [IO ]/ [IR] > 10 il colore di In(Red) predomina quando [IO ]/ [IR] < 0. 1 L’intervallo di viraggio risulta: e = e°In 0. 05916/n Una volta calcolato il potenziale al punto equivalente (e. P. E. ), l’indicatore si sceglie in modo tale che: e. P. E. = e°In 0. 05916/n I più importanti indicatori redox sono la la ferroina e la difenilammina. La ferroina è un complesso tra Fe(II) e 3 molecole di 1, 10 fenantrolina (Phen). Il Fe(II) si ossida a Fe(III) in accordo alla reazione: Fe(Phen)3 3+ + e = Fe(Phen)3 2+ e°In = + 1. 06 V In base alla più intensa colorazione della forma Red, il viraggio è percettibile quando il potenziale è intorno a + 1. 12 V quindi non proprio uguale a e°In.
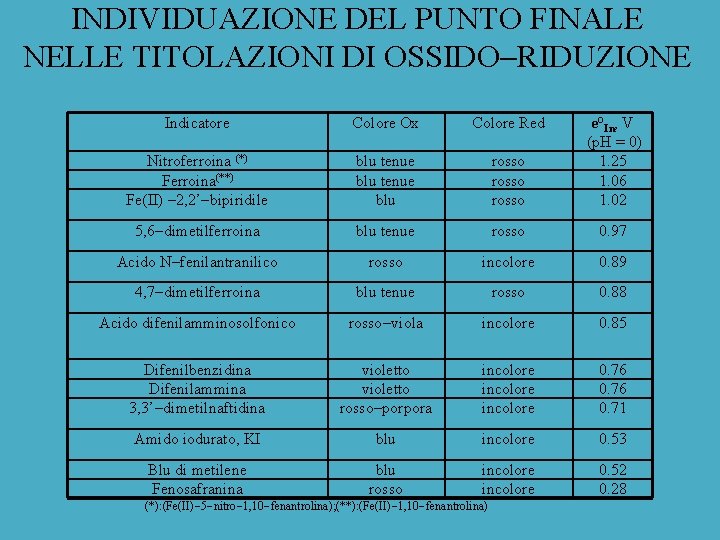
INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE Indicatore Colore Ox Colore Red Nitroferroina (*) Ferroina(**) Fe(II) – 2, 2’ bipiridile blu tenue blu rosso e°In, V (p. H = 0) 1. 25 1. 06 1. 02 5, 6 dimetilferroina blu tenue rosso 0. 97 Acido N fenilantranilico rosso incolore 0. 89 4, 7 dimetilferroina blu tenue rosso 0. 88 Acido difenilamminosolfonico rosso viola incolore 0. 85 Difenilbenzidina Difenilammina 3, 3’ dimetilnaftidina violetto rosso porpora incolore 0. 76 0. 71 Amido iodurato, KI blu incolore 0. 53 Blu di metilene Fenosafranina blu rosso incolore 0. 52 0. 28 (*): (Fe(II) 5 nitro 1, 10 fenantrolina); (**): (Fe(II) 1, 10 fenantrolina)

INDIVIDUAZIONE DEL PUNTO FINALE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE Reagenti che fungono da indicatori Alcuni reattivi sono intensamente colorati, per cui un loro eccesso o una loro scomparsa determina una variazione di colore. § KMn. O 4: la forma ossidata è intensamente colorata in viola (anche per concentrazioni 10 5 M). § I 2: lo iodio prodotto dalla reazione si estrae in CHCl 3 o con CCl 4, assumendo una colorazione viola). Tuttavia è più conveniente utilizzare la salda d’amido come indicatore per I 2. § Nelle titolazioni in cui partecipa Fe 2+ è possibile usare come indicatore anche lo ione SCN che forma con lo ione ferroso un complesso intensamente colorato in rosso.

ERRORE DI TITOLAZIONE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE Al punto equivalente di una titolazione redox, si verifica la condizione di equivalenza: n. TCT = n. C dove CT indica la concentrazione molare del titolante Ox. T (Ox. T + n. Te = Red. T) mentre C rappresenta quella del titolando Red (Ox + ne = Red). Le concentrazioni si riferiscono al punto finale della titolazione. Si definisce errore di titolazione assoluto l’espressione: = n. TCT n. C ed errore di titolazione relativo l’espressione: R = /n. C Se il potenziale del punto finale e. P. F. è maggiore del potenziale al punto equivalente e. P. E. , l’errore è stabilito dalle concentrazioni del titolante (che risulta in eccesso). Se e. P. F. > e. P. E. : [Ox. T] R = che si calcola dall’equazione di Nernst con e = e. P. F [Red. T] [Ox. T] log = (e. P. F. e°T)/0. 05916 [Red. T]
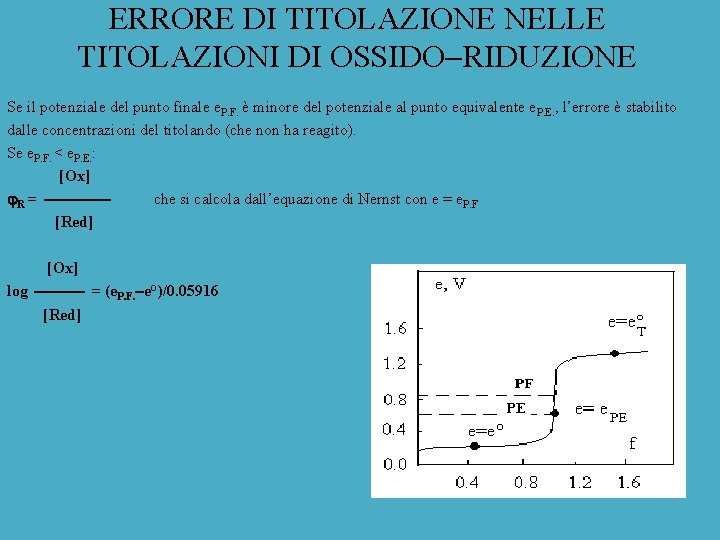
ERRORE DI TITOLAZIONE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE Se il potenziale del punto finale e. P. F. è minore del potenziale al punto equivalente e. P. E. , l’errore è stabilito dalle concentrazioni del titolando (che non ha reagito). Se e. P. F. < e. P. E. : [Ox] R = che si calcola dall’equazione di Nernst con e = e. P. F [Red] [Ox] log = (e. P. F. e°)/0. 05916 [Red]

ERRORE DI TITOLAZIONE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE Dimostrazione: Applicando l’equazione dell’errore alla titolazione con Ce 4+ si ha per la reazione: 2 Ce 4+ + Sn 2+ = 2 Ce 3+ + Sn 4+ Al p. e. : CT = 2 C Sostituendo i bilanci di massa e considerando che [Ce 3+] = 2[Sn 4+] si ha al p. e. : [Ce 4+] = 2[Sn 2+] Quindi: = [Ce 4+] 2[Sn 2+] R = ([Ce 4+] 2[Sn 2+])/2 C Superando il p. e. , l’errore dipende dalla [Ce 4+] in eccesso (al punto finale, [Sn 2+] è trascurabile) quindi [Ce 4+] R = = 2 C CT Poiché CT = [Ce 3+] + [Ce 4+] ≈ [Ce 3+] [Ce 4+] R = [Ce 3+]

ERRORE DI TITOLAZIONE NELLE TITOLAZIONI DI OSSIDO RIDUZIONE Nel caso della titolazione di Fe 2+: Ce 4+ + Fe 2+ = Ce 3+ + Fe 3+ Al l p. e. si può scrivere: CT = C Sostituendo i bilanci di massa e considerando che: [Ce 3+] = [Fe 3+] si ha al p. e. : [Ce 4+] = [Fe 2+] Quindi l’espressione dell’errore di titolazione è: = [Ce 4+] [Fe 2+] R = ([Ce 4+] [Fe 2+])/C Poiché la titolazione è stata fermata prima del p. e. , l’errore dipende dalla [Fe 2+] non titolata (al punto finale, [Ce 4+] è trascurabile). [Fe 2+] R = C Poichè C = [Fe 3+] + [Fe 2+] ≈ [Fe 3+] [Fe 2+] R = [Fe 3+]

METODI IN OSSIDIMETRIA Le sostanze più utilizzate sono: o (NH 4)2 Ce(SO 4)3 o KMn. O 4 o K 2 Cr 2 O 7 o Sistema I 2 / I (iodio/ioduro) Altre sostanze come HNO 3, Cl 2, H 2 O 2 non sono impiegate in quanto o non sono sufficientemente stabili oppure le relative reazioni possono non decorrere secondo un unico rapporto stechiometrico. IMPIEGO DI Ce(IV) (CERIMETRIA) Ce 4+ + e = Ce 3+ e° = + 1. 43 V (in H 2 SO 4 1 M) Il titolante si prepara da (NH 4)2 Ce(SO 4)3 o da (NH 4)Ce(NO 3)5(S), in soluzione H 2 SO 4 1 M, altrimenti precipita l’idrossido. A differenza del KMn. O 4, si possono condurre titolazioni in presenza di HCl (tranne per titolazioni che necessitano di far bollire la soluzione, dove il cerio ossida Cl 2). Non è una sostanza madre. Standard primari: As 2 O 3(S), Na 2 C 2 O 4(S), Fe(S)

METODI IN OSSIDIMETRIA ERRORE DI TITOLAZIONE IN CERIMETRIA Se e. P. F. > e. P. E. : [Ox. T] [Ce 4+] R = [Red. T] [Ce 3+] Si consideri la titolazione: 2 Ce 4+ + Sn 2+ = 2 Ce 3+ + Sn 4+ Se il punto finale è individuato con un indicatore redox che ha mostrato la variazione di colore ad un potenziale che si trova a + 0. 5 V oltre il valore di e. P. E. = + 0. 57 V si ha: e. P. F. = e. P. E. + 0. 6 V = 1. 07 V e. P. F. = e 0 T + 0. 05916 log ([Ce 4+]/[Ce 3+]) + 1. 07 V = 1. 43 V + 0. 05916 log ([Ce 4+]/[Ce 3+]) Da cui si ha: [Ce 4+]/[Ce 3+] = 10 6 = 10 4%

METODI IN OSSIDIMETRIA ERRORE DI TITOLAZIONE IN CERIMETRIA Nel caso della titolazione di Fe 2+: Ce 4+ + Fe 2+ = Ce 3+ + Fe 3+ Il potenziale al punto equivalente è: e. P. E. = (+ 1. 43 V + 0. 77 V)/2 = + 1. 10 V Se il potenziale del punto finale è di + 0. 5 V inferiore al p. e. si ha: e. P. F. = (+ 1. 10 V 0. 5 V) = + 0. 60 V Poiché la titolazione è stata fermata prima del p. e. si ha: [Fe 2+] R = [Fe 3+] e. P. F. = e 0 T + 0. 05916 log ([Fe 3+]/[Fe 2+]) + 0. 60 V = + 0. 77 V + 0. 05916 log ([Fe 3+]/[Fe 2+]) da cui si ha: [Fe 2+]/[Fe 3+] = 10+2. 87 = 10+4. 87%

METODI IN OSSIDIMETRIA IMPIEGO DI KMn. O 4 (PERMANGANOMETRIA) Si usa in ambiente acido (H 2 SO 4, HCl. O 4 , non HNO 3): Mn. O 4 + 5 e + 8 H+ = Mn 2+ + 4 H 2 O e 0 = + 1. 49 V (Peso Equivalente: P. E. = P. M. /5) Le reazioni sono differenti in condizioni diverse: Ambiente neutro o leggermente alcalino: Mn. O 4 + 3 e + 2 H 2 O = Mn. O 2(S) + 4 OH e° = + 1. 695 V (Peso Equivalente: P. E. = P. M. /3) Ambiente neutro: Mn. O 4 + e = Mn. O 42 e° = + 0. 564 V (Peso Equivalente: P. E. = P. M. ) KMn. O 4 è impiegato in soluzione acida per H 2 SO 4, in concentrazione 1 5 M; HCl può reagire, in presenza di alcune sostanze (come Fe 2+). La determinazione di As(III), Sb(III) e H 2 O 2 si può effettuare in presenza di HCl. Poiché lo ione Mn. O 4 , è colorato in violetto (Mn 2+ è incolore), il titolante ha anche la funzione di indicatore. Si conserva in bottiglie di vetro scure. Standard primari: Na 2 C 2 O 4, Fe metallico, H 2 C 2 O 4× 2 H 2 O, K 2 Cr 2 O 7, KIO 3, As 2 O 3.

METODI IN OSSIDIMETRIA ERRORE DI TITOLAZIONE IN PERMANGANOMETRIA Dopo il p. e. : (e. P. F. > e. P. E. ): [Ox. T] [Mn. O 4 ] R = = [Red. T] [Mn 2+] Nel punto finale si osserva la colorazione rosa della soluzione (goccia di KMn. O 4 in eccesso) quando [Mn. O 4 ] =10 5 M. Assumendo che [Mn 2+] ≈ CT , si calcola R. Se, ad esempio, risulta CT = 0. 01 M l’errore di titolazione sarà: 10 5 R = = 10 3 = + 0. 1% 10 2

METODI IN OSSIDIMETRIA IMPIEGO DI K 2 Cr. O 7 (BICROMATOMETRIA) Ambiente acido (HCl (< 2 M), H 2 SO 4, HCl. O 4) Cr 2 O 72 + 6 e + 14 H+ = 2 Cr 3+ + 7 H 2 O e 0 = + 1. 33 V (P. E. = P. M. /6) Il K 2 Cr 2 O 7 è una sostanza madre; questo è un vantaggio che si ha utilizzandolo come ossidante.

METODI IN OSSIDIMETRIA ERRORE DI TITOLAZIONE IN BICROMATOMETRIA Dopo il p. e. : (e. P. F. > e. P. E. ): [Ox. T] [Cr 2 O 72 ] R = = [Red. T] [Cr 3+]2 Si consideri la titolazione: Cr 2 O 72 + 6 Fe 2+ = 2 Cr 3+ + 6 Fe 3+ Se il punto finale è individuato con un indicatore redox come la ferroina che ha mostrato la variazione di colore ad un potenziale di + 1. 12 V, si ha: e. P. F. = e 0 T + (0. 05916/6) log ([Cr 2 O 72 ]/[Cr 3+]2) (ammettendo che la titolazione è condotta in 1 M H+) + 1. 12 V = 1. 33 V + (0. 05916/6) log ([Cr 2 O 72 ]/[Cr 3+]2) Da cui si ha: [Cr 2 O 72 ] /[Cr 3+]2 = 10 21 = 10 19%

ALTRI METODI IN OSSIDO RIDUZIONE IODIMETRIA E IODOMETRIA La semireazione che coinvolge lo iodio è: I 2(aq) + 2 e = 2 I e° = + 0. 536 V Il valore di e°, intermedio tra le sostanze ossidanti (alti e°) e riducenti (bassi e°) rende possibile l’uso della Semireazione in ossidazione ed in riduzione. Ø Impiego di soluzioni di I 2 come agente ossidante (Iodimetria metodo diretto): Determinazione dei solfiti: SO 32 + I 2 + H 2 O = SO 42 + 2 I + 2 H+ (oppure SO 32 + I 3 + H 2 O = SO 42 + 3 I + 2 H+ Ø Impiego di I come agente riducente (Iodometria metodo indiretto): I (aggiunto in eccesso) reagisce con un ossidante, trasformandosi in I 2 quest’ultimo è titolato con una soluzione a titolo noto di Na 2 S 2 O 3. Determinazione dell’ipoclorito: Cl. O + 2 I + 2 H+ = Cl + I 2 + H 2 O I 2 + 2 S 2 O 32 = 2 I + S 4 O 62 L’impiego di tale sistema è diffuso per la disponibilità di un indicatore visuale molto sensibile, l’amido, polisaccaride naturale di struttura elicoidale, che interagisce con I 2 impartendo una intensa colorazione azzurra. La reazione è reversibile. La soluzione acquosa di indicatore si chiama salda d’amido.

ALTRI METODI IN OSSIDO RIDUZIONE IODIMETRIA La soluzione titolante è costituita da una soluzione di iodio. I 2(s) è un solido poco solubile in acqua (1. 33× 10 3 M, a 25°C). In presenza di I la solubilità dello iodio aumenta per la formazione del complesso I 3 in accordo alla reazione: I 2(aq) + I = I 3 E’ possibile preparare una soluzione di concentrazione 0. 05 M di I 3 , sciogliendo 0. 12 moli di KI e 0. 05 moli di I 2(S) in 1 dm 3 di acqua. Poichè I 2(S) evapora facilmente occorre determinare il titolo della soluzione, impiegando uno standard Primario. Standard primari: As 2 O 3(S), Soluzione di Na 2 S 2 O 3 a titolo noto. E’ possibile, inoltre, preparare una soluzione a titolo noto di iodio, pesando una quantità nota di KIO 3 (sostanza madre) e KI in eccesso (es. 2 g). Con l’aggiunta di acido (es. HCl) si ha: IO 3 + 8 I + 6 H+ = 3 I 3 + 3 H 2 O

ALTRI METODI IN OSSIDO RIDUZIONE IODOMETRIA La sostanza riducente da determinare reagisce dapprima con un eccesso di I liberando I 2 che poi è titolato con una soluzione a titolo noto di Na 2 S 2 O 3. Nella determinazione dell’ipoclorito di sodio (principio attivo della candeggina), I (aggiunto in eccesso) reagisce con Cl. O , trasformandosi in I 2 in accordo alla reazione: Cl. O- + 2 I + 2 H+ = Cl + I 2 + H 2 O Lo iodio che si sviluppa è titolato con la soluzione di Na 2 S 2 O 3 in accordo alla reazione: I 2 + 2 S 2 O 32 = 2 I + S 4 O 62 Il tiosolfato di sodio non è uno standard primario. Si prepara dapprima una soluzione a titolo approssimato dal sale Na 2 S 2 O 3× 5 H 2 O e si standardizza con una sostanza madre. Standard primari: KIO 3, As 2 O 3, K 2 Cr 2 O 7
- Slides: 93