TiT 54 Cng thc phn t C 2











- Slides: 21

TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46

Néi dung bµi häc I - TÝnh chÊt vËt lÝ : II - CÊu t¹o ph©n tö : III - TÝnh chÊt ho¸ häc : IV - øng dông : V - §iÒu chÕ :

I. TÍNH CHẤT VẬT LÍ: TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: Rượu etylic (Etanol) là chất lỏng, không màu, mùi thơm, sôi ở 78, 30 C Nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiếu chất như: Iốt, benzen …. . Quan sát ống nghiệm đựng rượu Etylic, ? nhận xét về trạng thái, màu sắc, mùi vị? ? Rượu etylic (Etanol) là chất lỏng, không màu, mùi thơm, sôi ở 78, 30 C Quan sát thí nghiệm hòa tan rượu etylic trong nước, nhận xét khả năng tan của rượu trong nước ? Nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiếu chất như: Iốt, benzen …. .

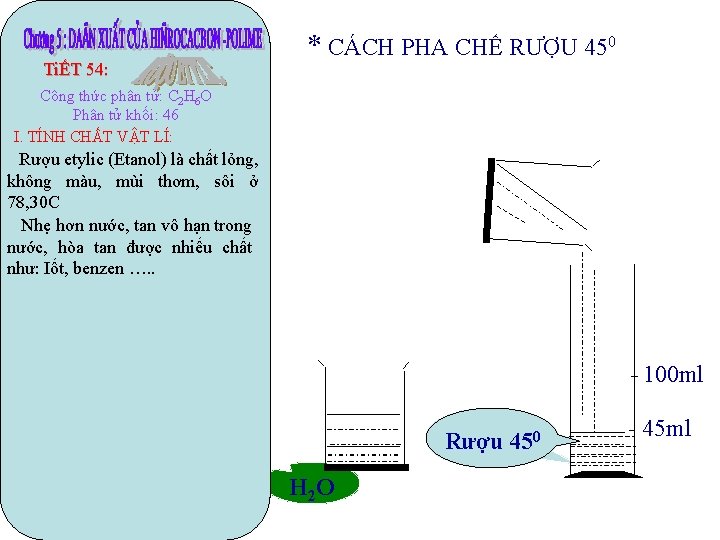
TiẾT 54: * CÁCH PHA CHẾ RƯỢU 450 Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: Rượu etylic (Etanol) là chất lỏng, không màu, mùi thơm, sôi ở 78, 30 C Nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiếu chất như: Iốt, benzen …. . 100 ml 450 Rượu C 2 H 5 OH H 2 O 45 ml

Định nghĩa: Độ rượu là số mol rượu etylic có trong 100 ml hỗn hợp rươu với nước TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: Rượu etylic (Etanol) là chất lỏng, không màu, mùi thơm, sôi ở 78, 30 C Nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiếu chất như: Iốt, benzen …. . Định nghĩa: Độ rượu là số mol rượu etylic có trong 100 ml hỗn hợp rươu. Với nước Công thức ? HaõCông y choïnthức ñaùp aùn ñuùng Soá ml röôïu Etylic nguyeân chaát coù trong 200 ml dung dòch röôïu Etylic 400 : A 100 ml B 120 ml C 40 ml D 80 ml

• Bạn trả lời sai rồi. Thử lại nhé!

Xin chúc mừng.

? Có thể pha chế được bao nhiêu lít rượu 250 từ 500 ml rượu 450 • * Bước 1: Tính toán • + Tìm thể tích rượu có trong 500 ml rượu 450 • + Tính thể tích dung dịch rượu 250 pha được • => Tính lượng nước cần thêm • * Bước 2: Pha chế

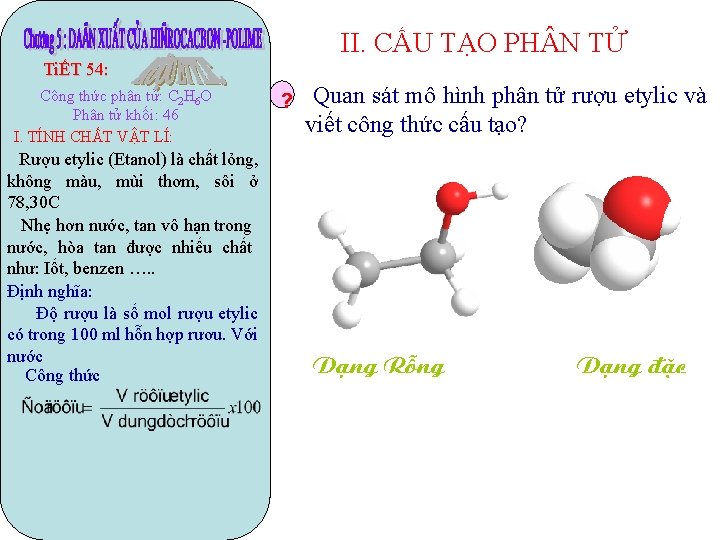
II. CẤU TẠO PH N TỬ TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: Rượu etylic (Etanol) là chất lỏng, không màu, mùi thơm, sôi ở 78, 30 C Nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiếu chất như: Iốt, benzen …. . Định nghĩa: Độ rượu là số mol rượu etylic có trong 100 ml hỗn hợp rươu. Với nước Công thức ? Quan sát mô hình phân tử rượu etylic và viết công thức cấu tạo? D¹ng Rçng D¹ng ®Æc

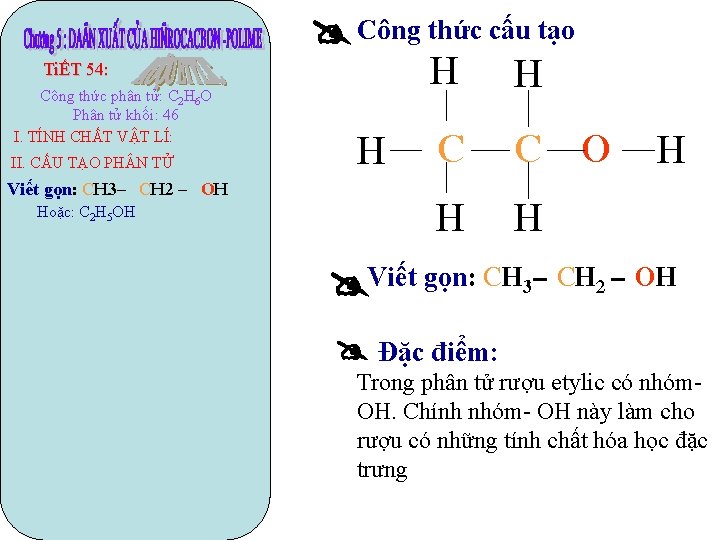
TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH Công thức cấu tạo H H H C C O H H H Viết gọn: CH 3– CH 2 – OH Đặc điểm: Trong phân tử rượu etylic có nhóm. OH. Chính nhóm- OH này làm cho rượu có những tính chất hóa học đặc trưng

TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Rượu etylic có cháy không? Quan sát t/n đốt cháy rượu etylic. Nhận xét hiện tượng xảy ra? ( Màu sắc, nhiệt độ). Rượu etylic cháy với ngọn lửa màu xanh, tỏa nhiều nhiệt. ?

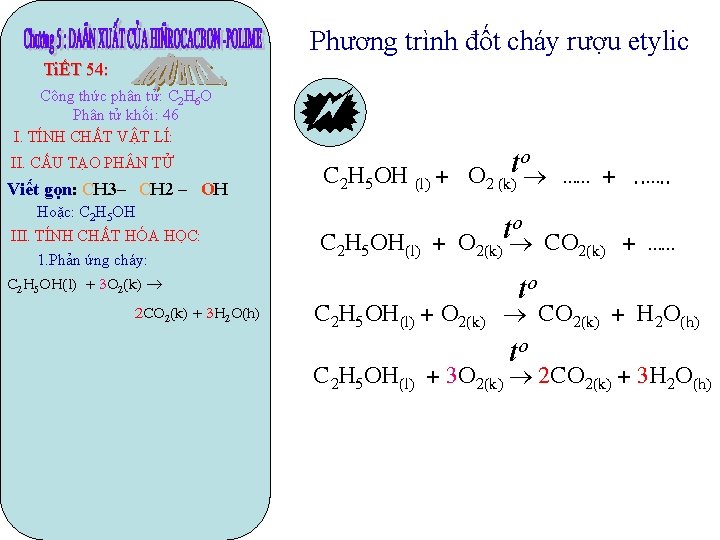
Phương trình đốt cháy rượu etylic TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) 57 56 55 54 53 52 51 50 49 48 47 46 45 44 43 42 41 40 39 38 37 36 35 34 33 32 31 30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 123456789 to C 2 H 5 OH (l) + O 2 (k) C 2 H 5 OH(l) + O 2(k) o t …… +. . …. . CO 2(k) + …… to C 2 H 5 OH(l) + O 2(k) CO 2(k) + H 2 O(h) to C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h)

2. Rượu etylic có phản ứng với natri không? TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) ? Quan sát t/n natri tác dụng với rượu etylic. Nhận xét hiện tượng xảy ra?

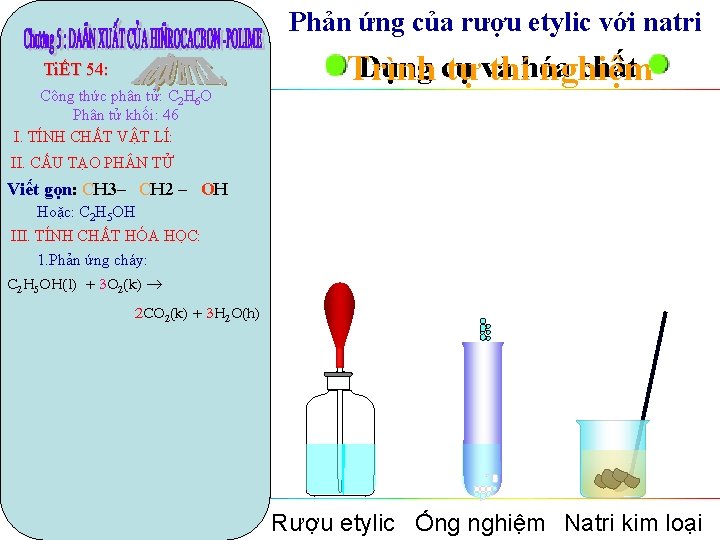
Phản ứng của rượu etylic với natri TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: Dụng cụ chất Trình tựvà thíhóa nghiệm II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) Rượu etylic Ống nghiệm Natri kim loại

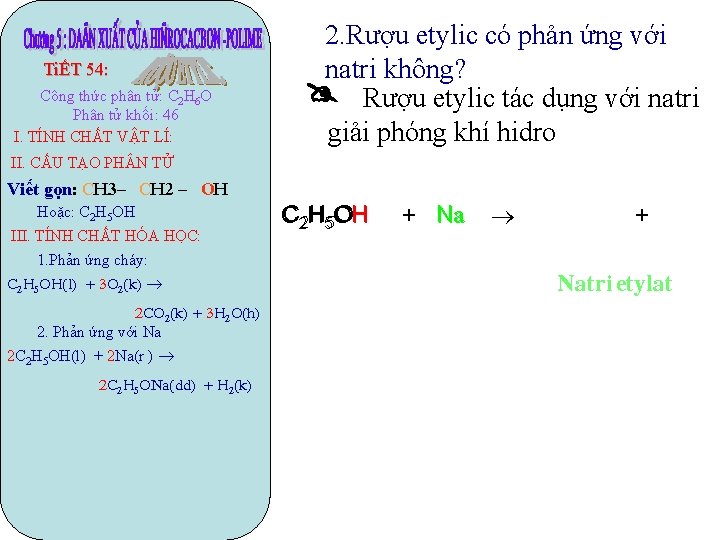
TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: 2. Rượu etylic có phản ứng với natri không? Rượu etylic tác dụng với natri giải phóng khí hidro II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) 2. Phản ứng với Na 2 C 2 H 5 OH(l) + 2 Na(r ) 2 C 2 H 5 ONa(dd) + H 2(k) OH C 2 H 5 OH + Natri etylat

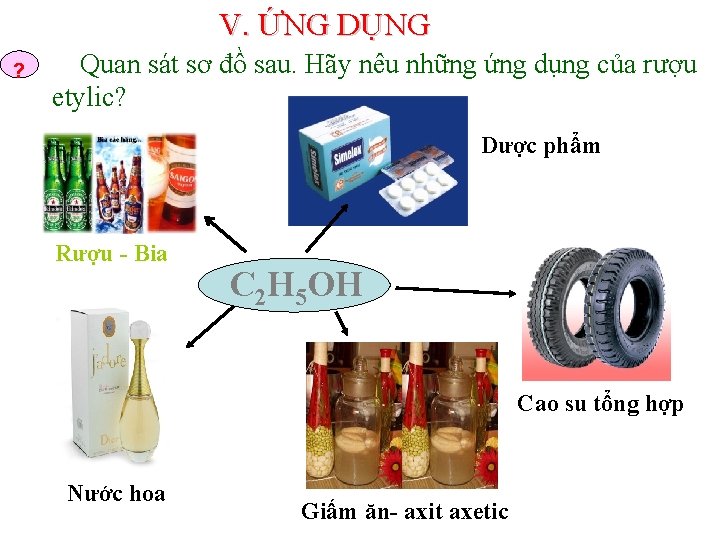
V. ỨNG DỤNG ? Quan sát sơ đồ sau. Hãy nêu những ứng dụng của rượu etylic? Dược phẩm Rượu - Bia C 2 H 5 OH Cao su tổng hợp Nước hoa Giấm ăn- axit axetic

Hãy chọn đáp án đúng? Những ứng dụng của rượu etylic ? TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) 2. Phản ứng với Na 2 C 2 H 5 OH(l) + 2 Na(r ) 2 C 2 H 5 ONa(dd) + H 2(k) IV. ỨNG DỤNG (SGK) 1. Sản xuất rượu bia để uống 2. Dùng làm chất diệt khuẩn 3. Dùng làm dung môi pha chế nước hoa 4. Là nguyên liệu sản xuất dấm ăn 5. Để tẩy trắng quần áo. 6. Sản xuất dược phẩm 7. Nguyên liệu sản xuất cao su tổng hợp 8. Làm nhiên liệu, chất đốt 9. Làm chất diệt côn trùng. Rượu etylic dùng làm nguyên liệu, nhiên liệu, dung môi ? Em hãy cho biết uống nhiều rượu có hại hay có lợi cho sức khỏe?

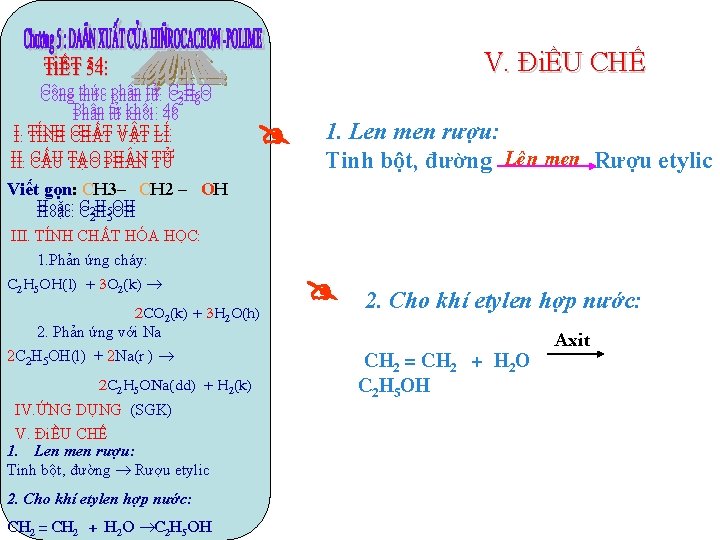
V. ĐiỀU CHẾ TiẾT 54: Công thức phân tử: C C 22 H H 66 O O Phân tử khối: 46 I. I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ TỬ 1. Len men rượu: Tinh bột, đường Leân men Rượu etylic Viết gọn: CH 3– CH 2 – OH Hoặc: C C 22 H H 55 OH OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) 2. Phản ứng với Na 2 C 2 H 5 OH(l) + 2 Na(r ) 2 C 2 H 5 ONa(dd) + H 2(k) IV. ỨNG DỤNG (SGK) V. ĐiỀU CHẾ 1. Len men rượu: Tinh bột, đường Rượu etylic 2. Cho khí etylen hợp nước: CH 2 = CH 2 + H 2 O C 2 H 5 OH Axit

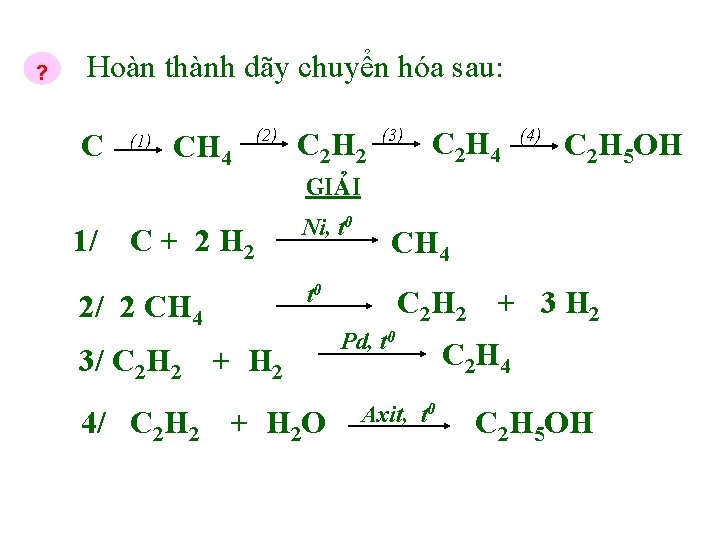
? Hoàn thành dãy chuyển hóa sau: C (1) CH 4 (2) C 2 H 2 (3) C 2 H 4 (4) C 2 H 5 OH GIAÛI 1/ C + 2 H 2 2/ 2 CH 4 Ni, t 0 CH 4 t 0 C 2 H 2 + 3 H 2 3/ C 2 H 2 + H 2 4/ C 2 H 2 + H 2 O Pd, t 0 Axit, t 0 C 2 H 4 C 2 H 5 OH

Đốt cháy hoàn toàn 9, 2 gam rượu etylic. Dẫn toàn bộ sản phẩm cháy đi qua nước vôi trong dư thu được kết tủa. Tính khối lượng kết tủa? GiẢI PT: C 2 H 5 OH PT: + 3 O 2 2 CO 2 0, 2 mol 0, 4 mol CO 2 + Ca(OH)2 Ca. CO 3 0, 4 mol + 3 H 2 O +Khối lượng kết tủa thu được là: m Ca. CO 3 = n MCa. CO 3. 3 = 0, 4. 100 = 40 (g)

TiẾT 54: Công thức phân tử: C 2 H 6 O Phân tử khối: 46 I. TÍNH CHẤT VẬT LÍ: II. CẤU TẠO PH N TỬ Viết gọn: CH 3– CH 2 – OH Hoặc: C 2 H 5 OH III. TÍNH CHẤT HÓA HỌC: 1. Phản ứng cháy: C 2 H 5 OH(l) + 3 O 2(k) 2 CO 2(k) + 3 H 2 O(h) 2. Phản ứng với Na 2 C 2 H 5 OH(l) + 2 Na(r ) 2 C 2 H 5 ONa(dd) + H 2(k) IV. ỨNG DỤNG (SGK) V. ĐiỀU CHẾ 1. Len men rượu: Tinh bột, đường Rượu etylic 2. Cho khí etylen hợp nước: CH 2 = CH 2 + H 2 O C 2 H 5 OH • Đọc phần “Em có biết” • Vì sao rượu etylic diệt được vi khuẩn? • Làm bài tập 2, 3, 4, 5 SGK trang 135 • Chuẩn bị bài 45: Axit axetic