TIPOS DE ORBTALES CAPACIDAD DE ENLACE DEL CARBONO


• TIPOS DE ORBÍTALES • CAPACIDAD DE ENLACE DEL CARBONO • HIBRIDACIÓN DE ORBÍTALES • TIPOS DE HIBRIDACIÓN

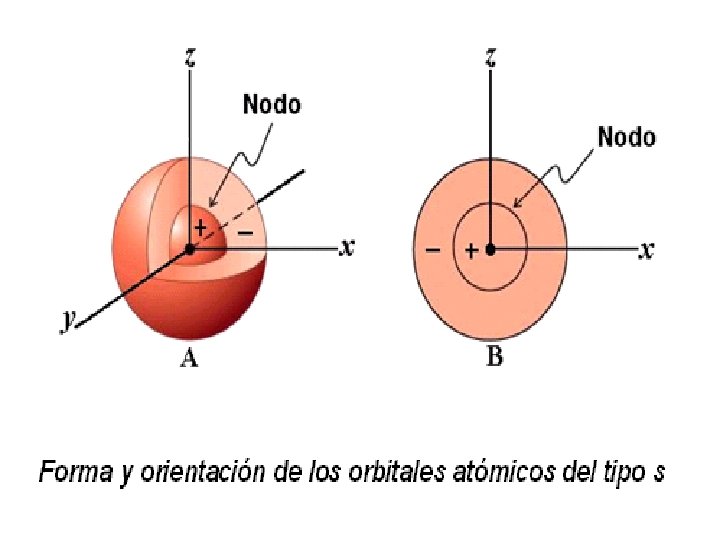
¿QUÉ ES UN ORBITAL? • REGIONES EN EL ESPACIO

¿QUÉ DETERMINA A ESE ORBITAL? • ESTOS ORBITALES SE DESCRIBEN POR MEDIO DE CUATRO PARÁMETROS, LLAMADOS NUMEROS CUÁNTICOS
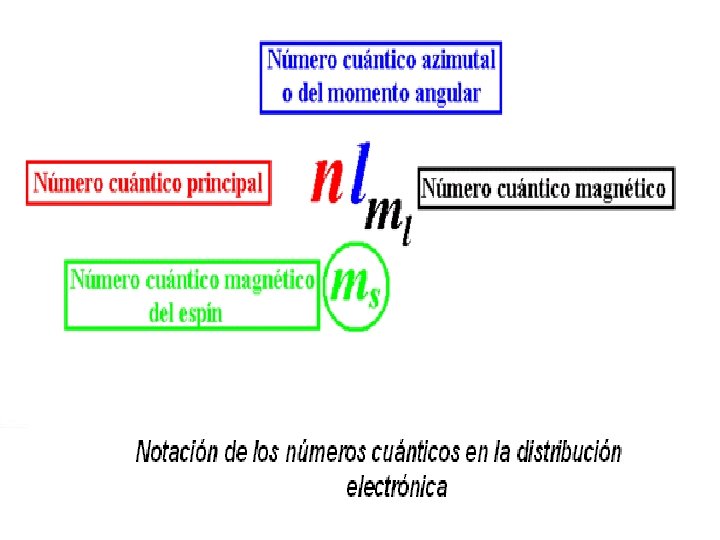


CAPACIDAD DE ENLACE DEL CARBONO • Tiene un número atómico igual a 6 y su configuración electrónica explica sus elevadas posibilidades de combinación consigo mismo y con otros elementos. ¿Cuál es la C. E. del carbono?

¿QUÉ SE PUEDE PREDECIR? • El carbono debe compartir los cuatro electrones externos, En enlaces covalentes. ¿Con quien los puede compartir? • Los cuatros enlaces resultantes deben ser diferentes.

PERO, ¿SON DIFERENTES? • Se sabe que son simétricos. ¿Cómo se explica esto? • Con la teoría de la hibridación

¿Qué es hibridación? • Linus pauling propuso una respuesta en 1931 al demostrar matemáticamente como se pueden combinar, o hibridar, un orbital s y tres orbítales p.
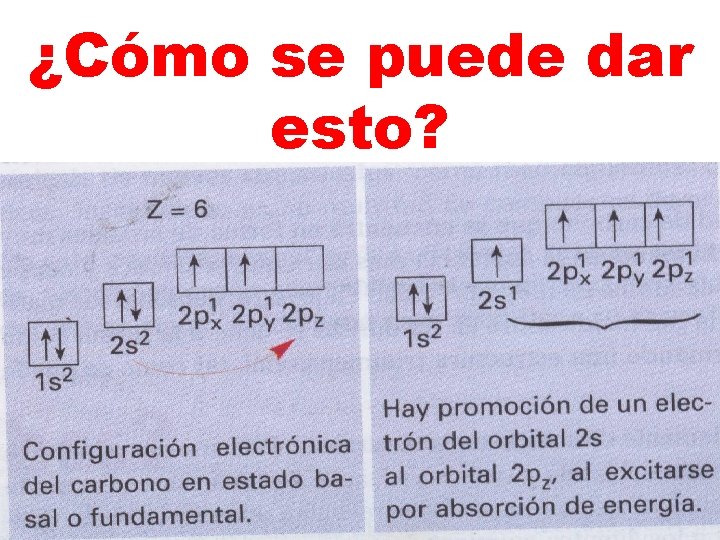
¿Cómo se puede dar esto?

¿Cómo y en que proporción se puede combinar el orbital s y los tres orbítales p? De tres maneras se puede mezclar o hibridar:

¿Cuáles son? 1. Hibridación 2. Hibridación 3. Hibridación sp 3 sp 2 sp

Hibridación sp 3 • Cuando se combinan el 2 s con los 2 p para formar cuatro orbítales híbridos sp 3, que se orientan en los vértices de un tetraedro
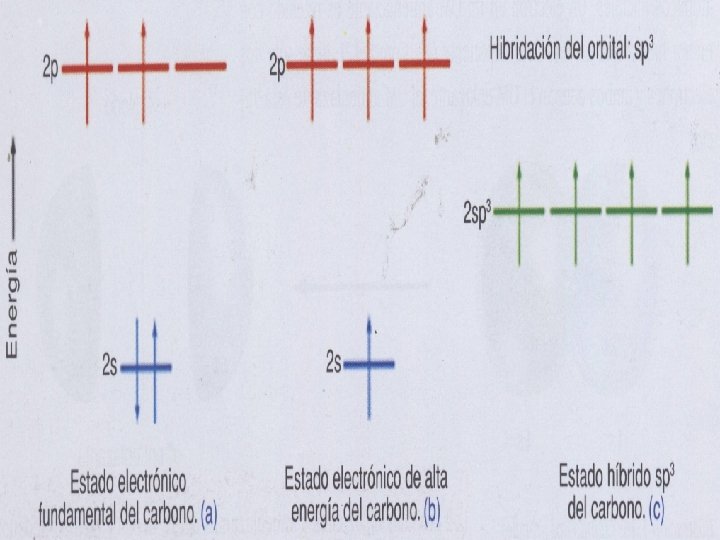
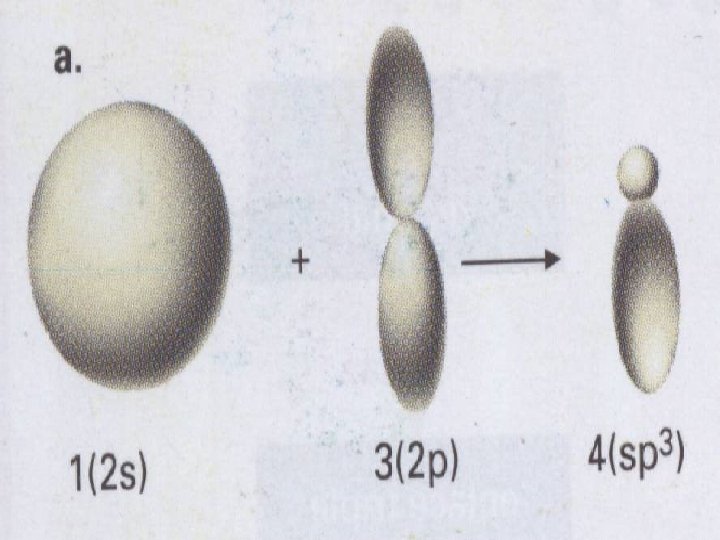
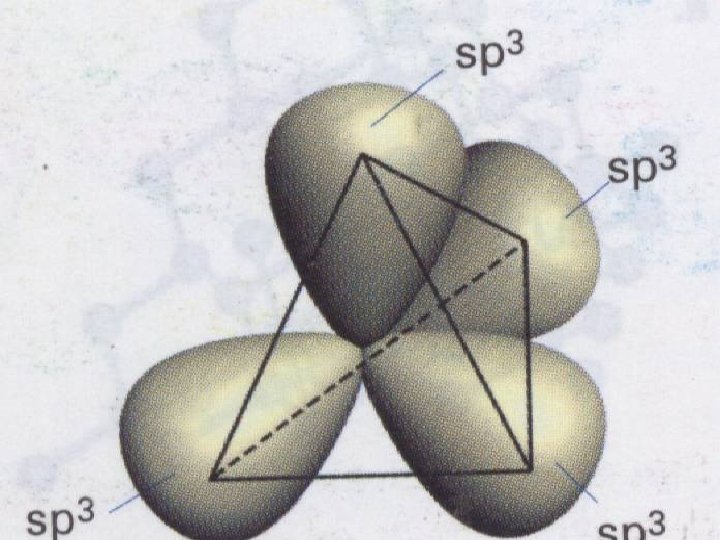
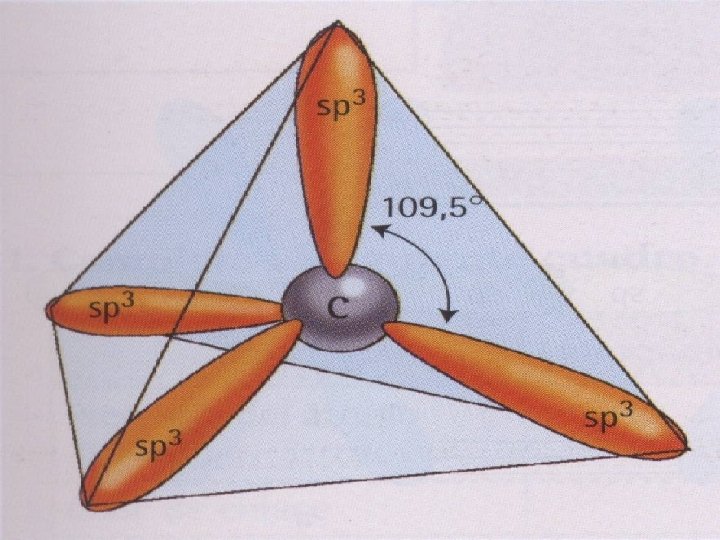
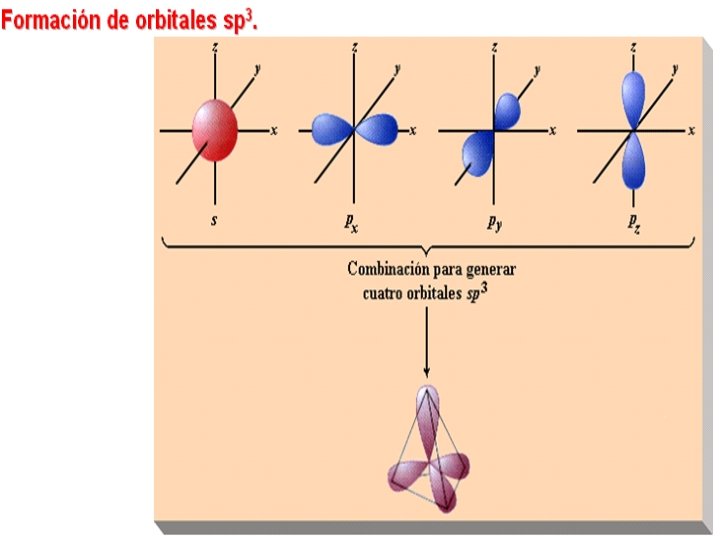
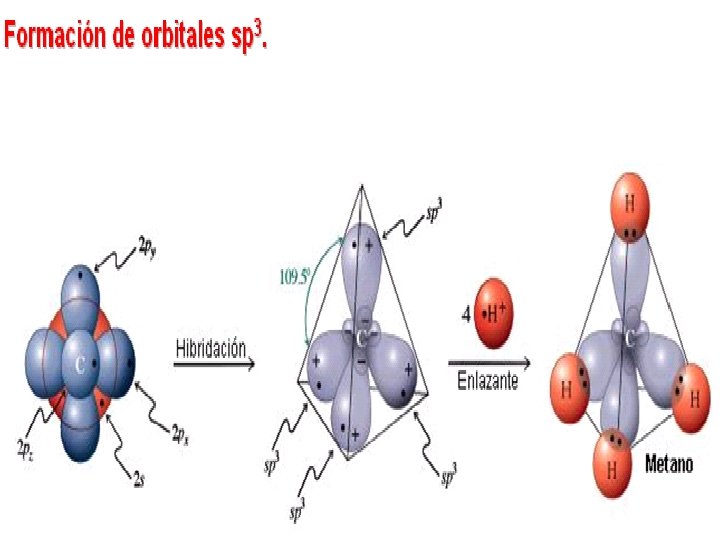
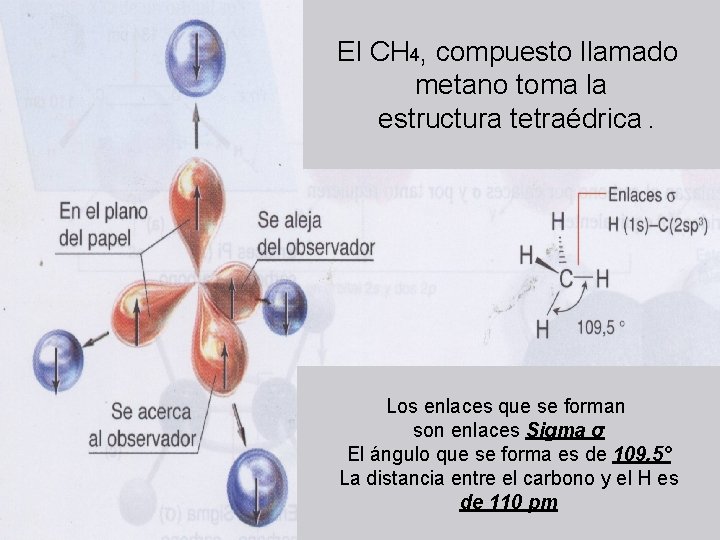
El CH 4, compuesto llamado metano toma la estructura tetraédrica. Los enlaces que se forman son enlaces Sigma σ El ángulo que se forma es de 109, 5° La distancia entre el carbono y el H es de 110 pm

Hibridación sp 2 • Cuando se combinan el 2 s con dos orbítales 2 p para formar tres orbítales híbridos sp 2, que se orientan en los vértices de un triangulo y el otro 2 p queda sin hibridar
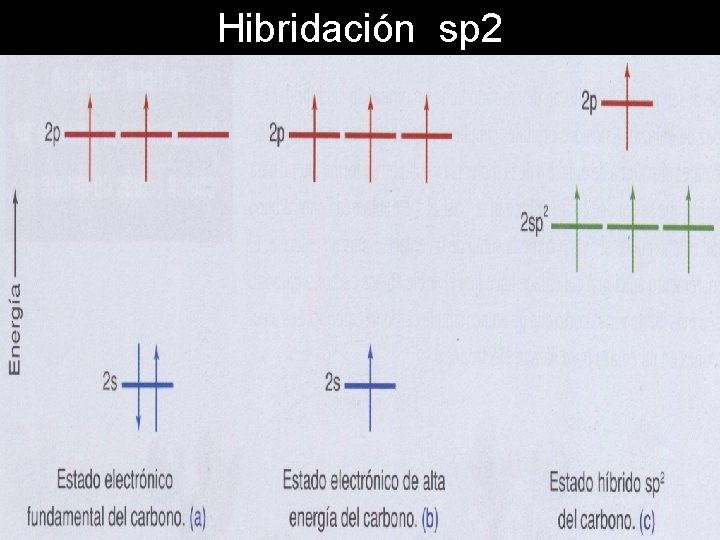
Hibridación sp 2
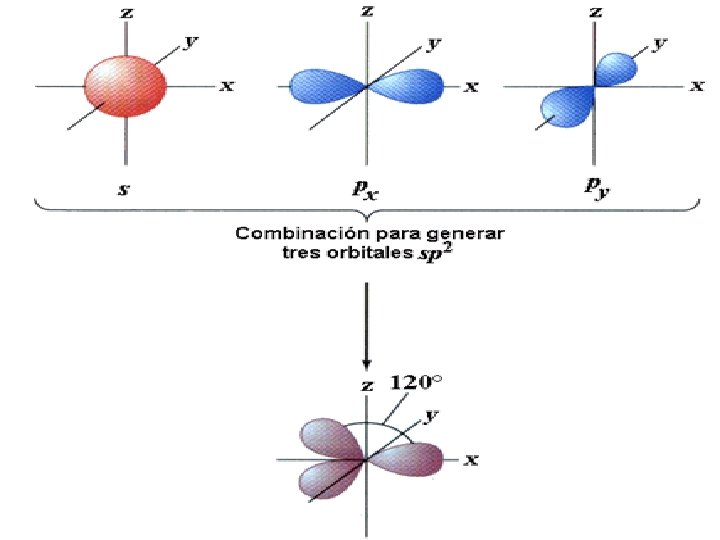
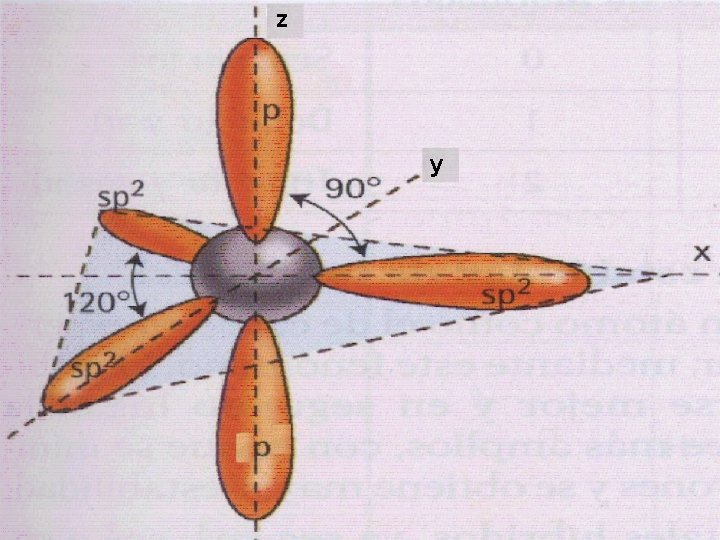
z y
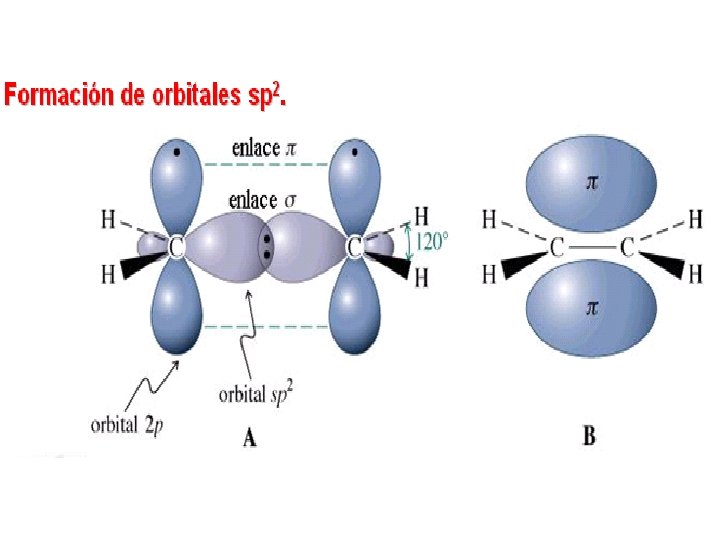

Hibridación sp • Cuando se combinan el 2 s con un orbítal 2 p para formar dos orbítales híbridos sp, que forman un ángulo de 180° y dos orbítales 2 p queda sin hibridar
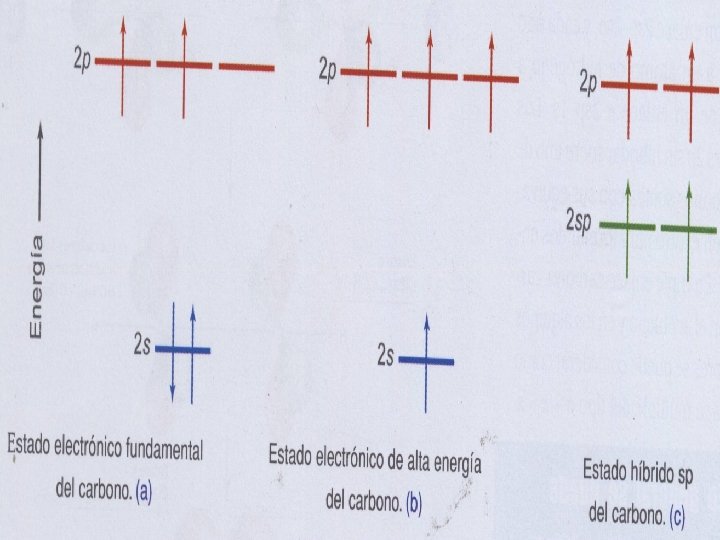
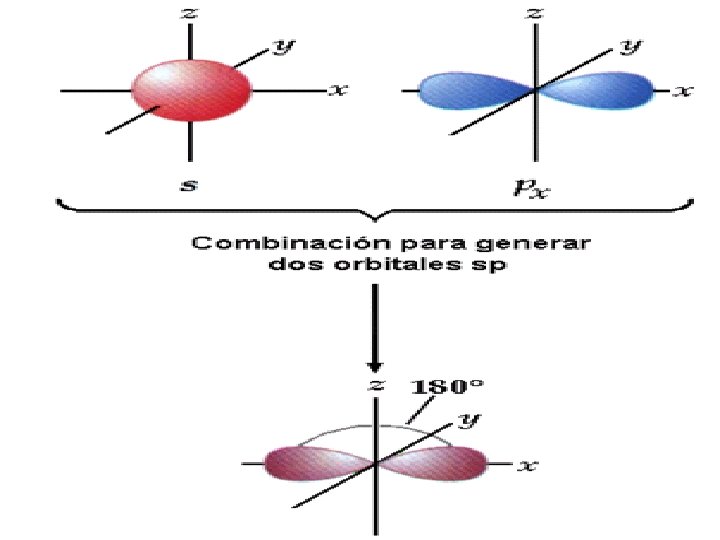
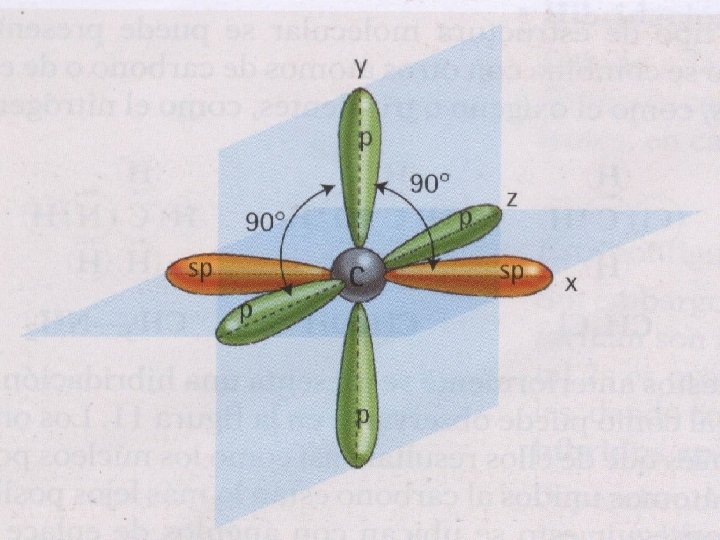
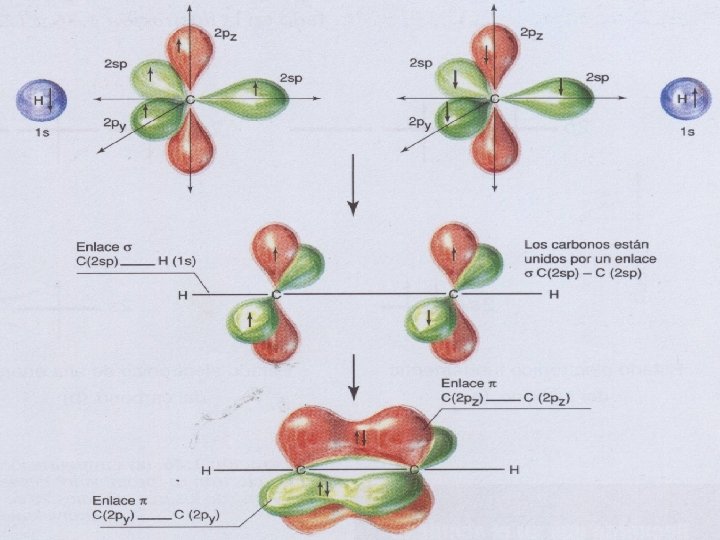
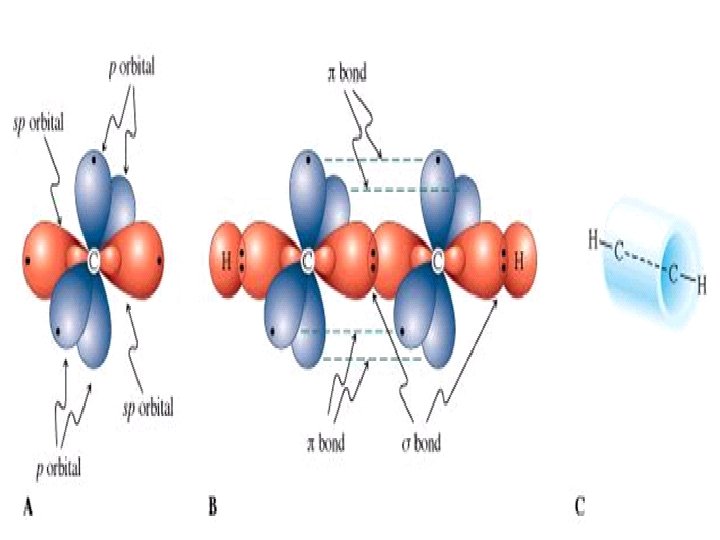
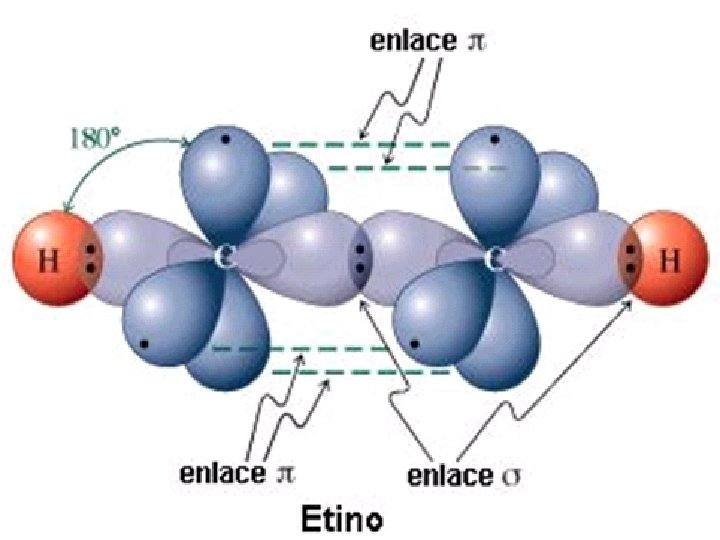
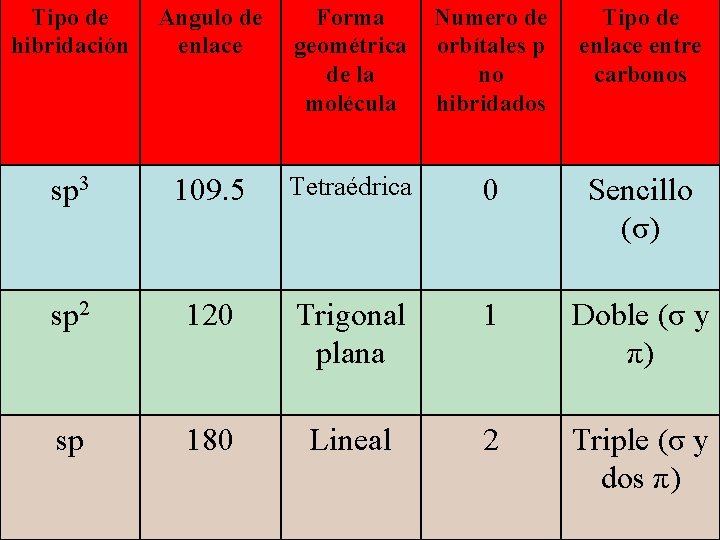
Tipo de hibridación Angulo de enlace Forma geométrica de la molécula Numero de orbítales p no hibridados Tipo de enlace entre carbonos sp 3 109. 5 Tetraédrica 0 Sencillo (σ) sp 2 120 Trigonal plana 1 Doble (σ y π) sp 180 Lineal 2 Triple (σ y dos π)

1. Seguir estudiando 2. Que diferencias hay entre un enlace σ y enlace de tipo π

3. Que diferencias hay entre un enlace σ de orbítales hibridados y un enlace de orbítales no hibridados (sean s -s, s-p, p-p). 4. Cual es la relación hibridación y la estabilidad de un enlace.

5. Resolver el taller de la pagina 17 del libro “química orgánica editorial santillana). 6. Consultar acerca de los compuestos orgánicos, clasificación y nomenclatura

- Slides: 39