Tik 2 vandenilio ir 1 deguonies atomu junginis



- Slides: 17


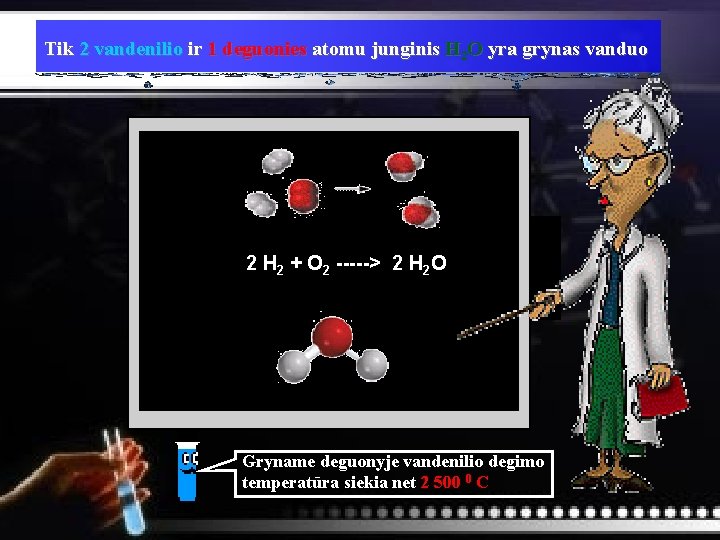
Tik 2 vandenilio ir 1 deguonies atomu junginis H 2 O yra grynas vanduo 2 H 2 + O 2 -----> 2 H 2 O Gryname deguonyje vandenilio degimo temperatūra siekia net 2 500 0 C

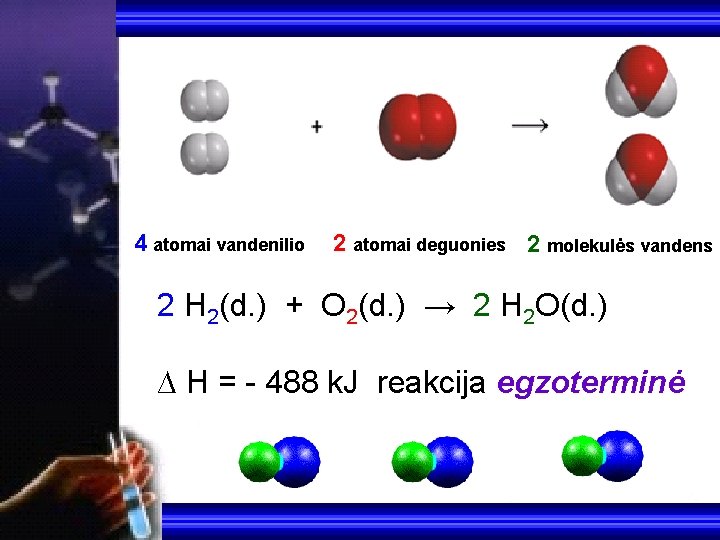
4 atomai vandenilio 2 atomai deguonies 2 molekulės vandens 2 H 2(d. ) + O 2(d. ) → 2 H 2 O(d. ) ∆ H = - 488 k. J reakcija egzoterminė

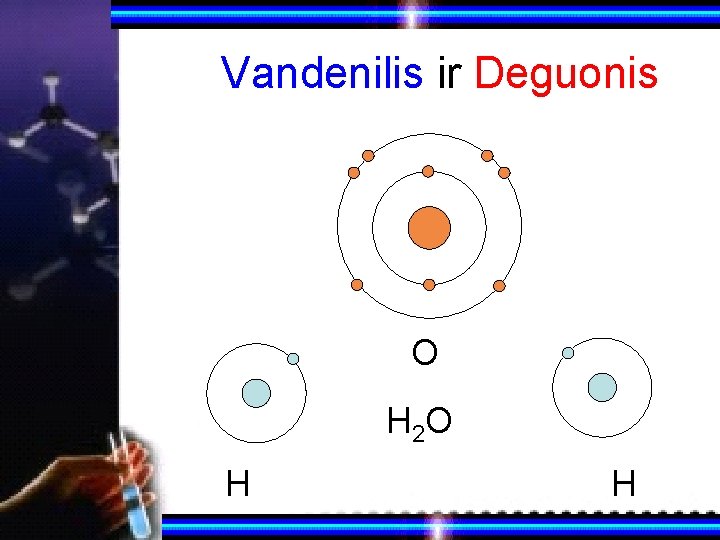
Vandenilis ir Deguonis O H 2 O H H

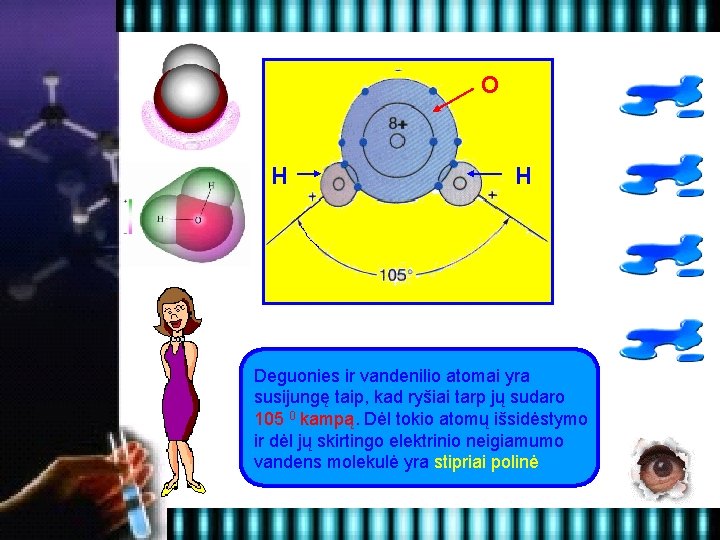
O H H Deguonies ir vandenilio atomai yra susijungę taip, kad ryšiai tarp jų sudaro 105 0 kampą. Dėl tokio atomų išsidėstymo ir dėl jų skirtingo elektrinio neigiamumo vandens molekulė yra stipriai polinė

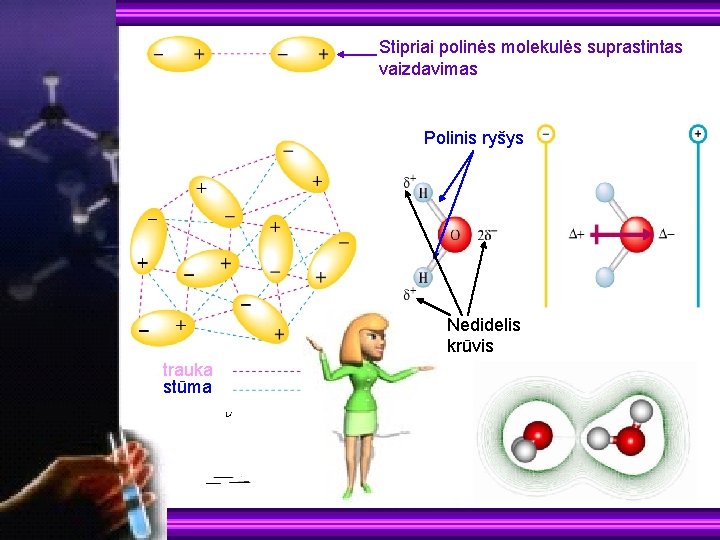
Stipriai polinės molekulės suprastintas vaizdavimas Polinis ryšys Nedidelis krūvis trauka stūma


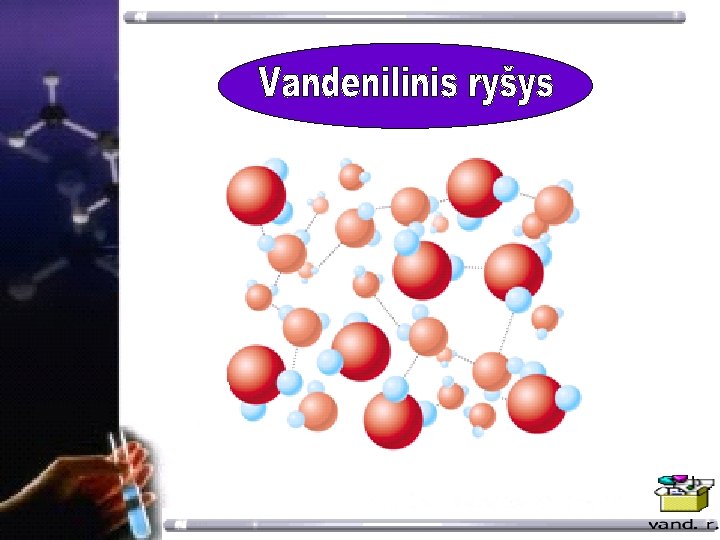
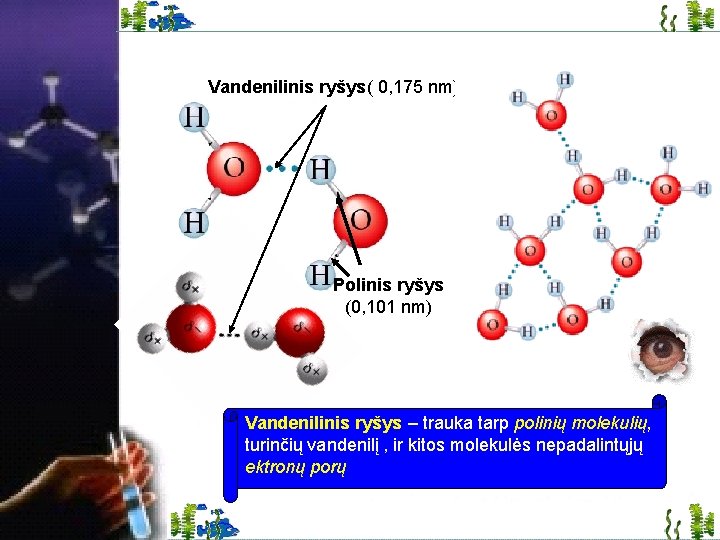
Vandenilinis ryšys( 0, 175 nm) Polinis ryšys (0, 101 nm) Vandenilinis ryšys – trauka tarp polinių molekulių, turinčių vandenilį , ir kitos molekulės nepadalintųjų ektronų porų

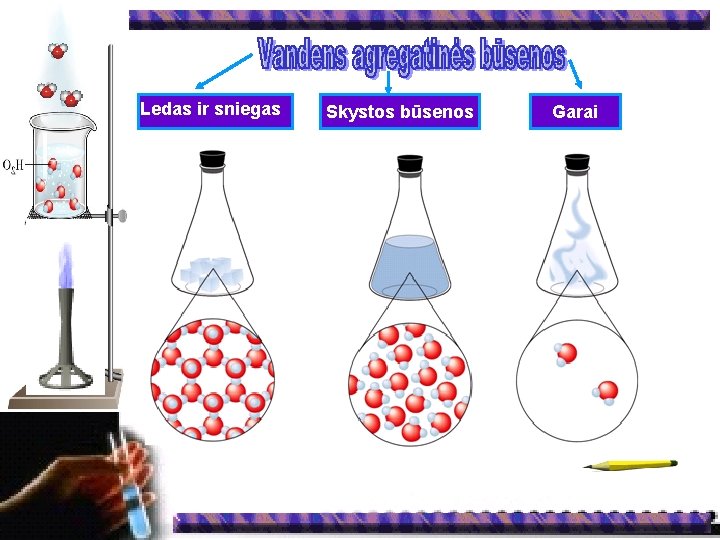
Ledas ir sniegas Skystos būsenos Garai

Vandens fizikinės savybės bespalvis, bekvapis skystis tankis 4 0 C temperatūroje 1, 0 g/cm 3 užšalimo temperatūra 0, 0 0 C virimo temperatūra 100, 0 0 C nelaidus elektrai 2 Vanduo, susidedantis tik iš deuterio (1 H) oksido D 2 O, vadinamas sunkiuoju vandeniu. Jis naudojamas branduoliniuose reak – toriuose greitiesiems neutronams lėtinti.

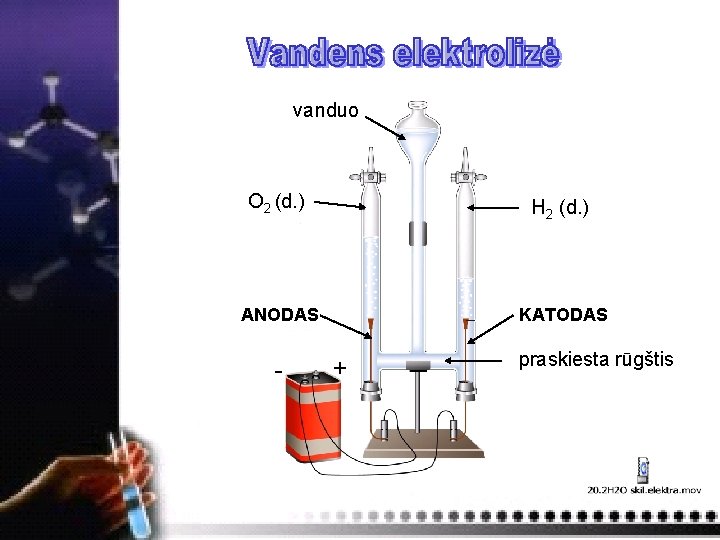
vanduo O 2 (d. ) H 2 (d. ) ANODAS KATODAS - + praskiesta rūgštis

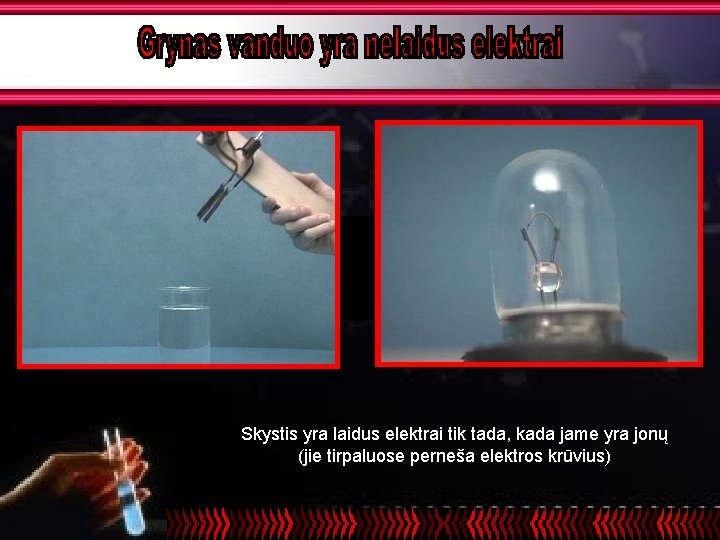
Skystis yra laidus elektrai tik tada, kada jame yra jonų (jie tirpaluose perneša elektros krūvius)

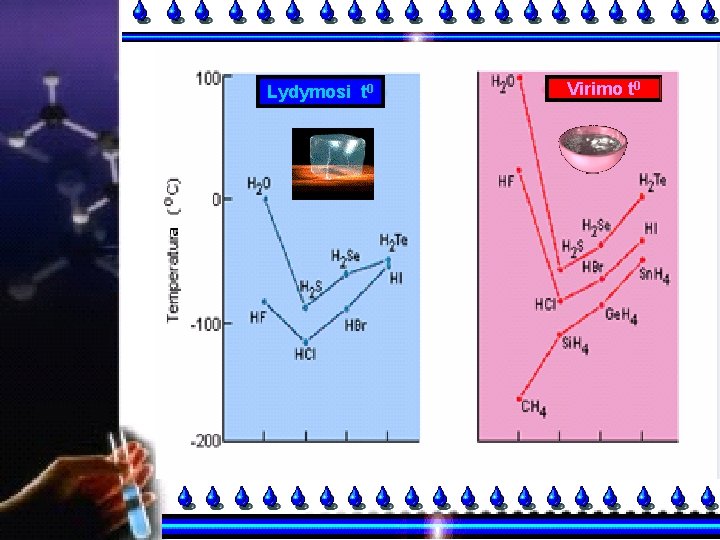
Lydymosi t 0 Virimo t 0

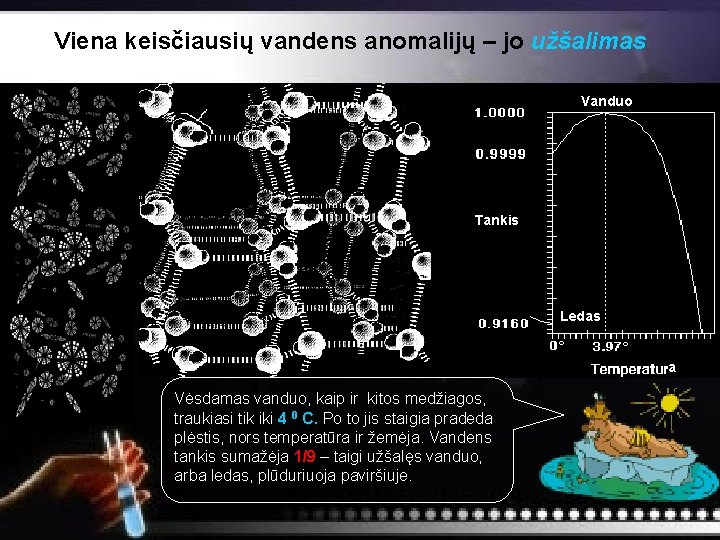
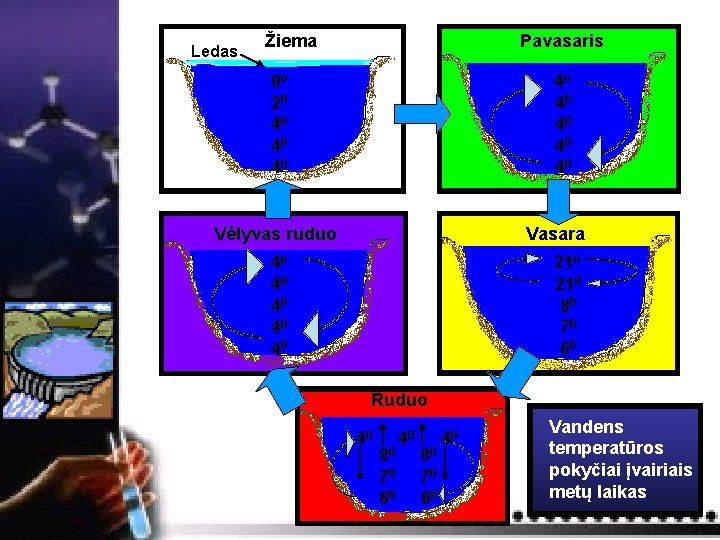
Viena keisčiausių vandens anomalijų – jo užšalimas Vanduo Tankis Ledas a Vėsdamas vanduo, kaip ir kitos medžiagos, traukiasi tik iki 4 0 C. Po to jis staigia pradeda plėstis, nors temperatūra ir žemėja. Vandens tankis sumažėja 1/9 – taigi užšalęs vanduo, arba ledas, plūduriuoja paviršiuje.

Ledas Žiema Pavasaris 0 o 20 40 4 o 40 40 Vėlyvas ruduo Vasara 4 o 40 40 21 o 210 80 70 60 Ruduo 40 80 70 60 40 Vandens temperatūros pokyčiai įvairiais metų laikas

Bandymai įrodantis kad šaltas vanduo yra sunkesnis nei karštas Bandymas 1 3 3 1 - Šaltas vanduo 2 - Karštas vanduo - Metaline sfera 3 11 2 a) Bandymas 2 1 2 b) 2 1

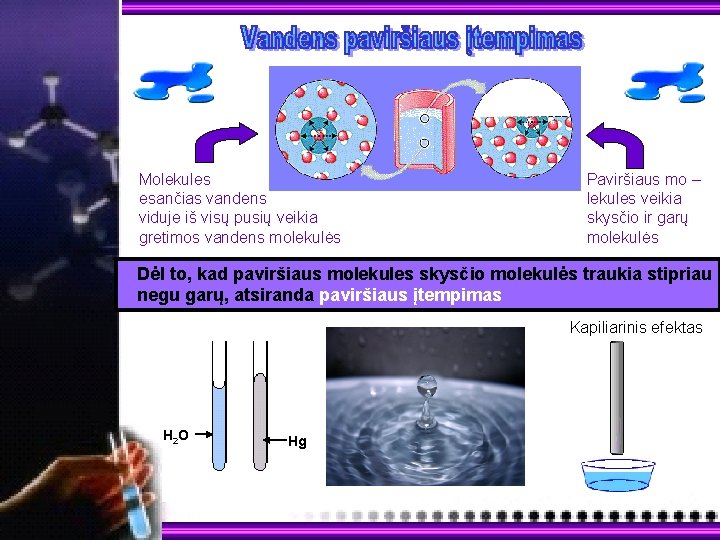
Molekules esančias vandens viduje iš visų pusių veikia gretimos vandens molekulės Paviršiaus mo – lekules veikia skysčio ir garų molekulės Dėl to, kad paviršiaus molekules skysčio molekulės traukia stipriau negu garų, atsiranda paviršiaus įtempimas Kapiliarinis efektas H 2 O Hg