THNG T 022018TTBYT Quy nh v Thc hnh

THÔNG TƯ 02/2018/TT-BYT Quy định về Thực hành tốt cơ sở bán lẻ thuốc Ngày ban hành: 22/01/2018 Ngày hiệu lực: 08/3/2018 Đối tượng áp dụng: Nhà thuốc, quầy thuốc, Tủ thuốc trạm y tế xã

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ THÀNH PHẦN HỒ SƠ THEO 46/2011/TT-BYT & 02/2018/TT-BYT TT 46/2011/TT-BYT n 1. Hồ sơ cấp mới: n + Đơn đăng ký kiểm tra n “Thực hành tốt nhà thuốc” (Mẫu số 1/GPP): -Bản chụp ĐKKD -Bản chính CCHND + Bản kê khai CSVC, TTB - TT 02/2018/TT-BYT 1. Hồ sơ cấp mới: Không có mẫu đơn (đi kèm với Đơn đề nghị cấp GCNĐĐKKDD) - Có Bản sao có chứng thực Danh mục TTB (gồm cả thông tin về hệ thống máy tính và phần mềm quản lý nối mạng)

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ THÀNH PHẦN HỒ SƠ THEO 46/2011/TT-BYT & 02/2018/TT-BYT (tt) Sơ đồ nhân sự, danh + Danh sách nhân sự; sách nhân sự, tên, chức danh, TĐCM + Bản tự kiểm tra GPP n Có (Bản tự kiểm tra Thực theo Danh mục kiểm tra hành tốt CSBLT theo (Checklist) tại Phụ lục II danh mục) Thông tư này. n Bản vẽ bố trí các khu vực của cơ sở bán lẻ n Danh mục các quy định, hồ sơ, tài liệu, quy trình n

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ THÀNH PHẦN HỒ SƠ THEO 46/2011/TT-BYT & 02/2018/TT-BYT (tt) 2. Hồ sơ tái đánh giá: 2. Hồ sơ Đề nghị đánh giá định kỳ việc duy trì đáp ứng GPP: nĐơn đăng ký tái kiểm tra nĐơn đề nghị đánh giá điều kiện bán lẻ thuốc định ký việc duy trì đáp ứng theo nguyên tắc, tiêu chuẩn “Thực hành tốt nhà GPP: thuốc” (Mẫu số 2/GPP) + Tài liệu cập nhật về CSVC, TTB, nhân sự + Báo cáo tóm tắt về hoạt động trong 3 năm

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ CÁC LOẠI HỒ SƠ THEO 46/2011/TT-BYT & 02/2018/TT-BYT (tt) 3. Cấp do thay đổi vị trí cơ sở bán lẻ thuốc tại cùng địa điểm kinh doanh 4. Văn bản thông báo về việc đồng ý với nội dung thay đổi, khi cơ sở: -Mở rộng cơ sở bán lẻ thuốc -Sửa chữa, thay đổi lớn về cấu trúc cơ sở bán lẻ thuốc

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ QUY TRÌNH ĐÁNH GIÁ THEO 46/2011/TT-BYT & 02/2018/TT-BYT * Khác về Danh mục kiểm tra: + Có thiết bị tự ghi nhiệt độ: điểm không chấp thuận + Có biển hiệu “sản phẩm này không phải là thuốc”…

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ XỬ LÝ KẾT QUẢ ĐÁNH GIÁ THEO 46/2011/TT-BYT & 02/2018/TT-BYT Cấp phép sau 05 ngày - Sau 10 hoặc 20 ngày kiểm tra Đạt - Nếu có BCKP: - Cấp phép sau 10 ngày + 05 ngày hoặc 15 ngày có nhận được Báo cáo văn bản yêu cầu KP kể từ khắc phục Đạt ngày đánh giá + Cấp phép sau 20 ngày nhận được BCKP đã đáp ứng yêu cầu + Văn bản trả lời chưa cấp nếu BCKP chưa đáp ứng yêu cầu -

MỘT SỐ ĐIỂM KHÁC BIỆT VỀ XỬ LÝ KẾT QUẢ ĐÁNH GIÁ THEO 46/2011/TT-BYT & 02/2018/TT-BYT (tt) Khắc phục trong 30 ngày + Cơ sở được bổ sung trong 06 tháng. Nếu không đạt, sau 12 tháng hồ sơ không còn giá trị - Cơ sở không đáp ứng: 05 - Cơ sở không đáp ứng ngày kể từ ngày đánh giá, (Có điểm không chấp SYT thông báo cho CSBLT thuận hoặc <80% tổng việc không đáp ứng GPP và điểm đạt): Nộp đơn kiểm chưa cấp GCN tra lại -Kết quả đạt sẽ thông báo trên trang thông tin điện tử

ĐÁNH GIÁ ĐỊNH KỲ VIỆC DUY TRÌ ĐÁP ỨNG THỰC HÀNH TỐT CƠ SỞ BÁN LẺ THUỐC n n n Thời gian định kỳ đánh giá: 03 năm Tháng 11 hàng năm, SYT công bố trên Trang Thông tin điện tử kế hoạch đánh giá định kỳ GPP của CSBLT trong năm kế tiếp Cơ sở nộp HS về SYT tối thiểu 30 ngày theo kế hoạch SYT được công bố Ví dụ: Thời gian dự kiến đánh giá: 18/8/2018 Nộp hồ sơ đề nghị đánh giá: trước 18/7/2018 Không nộp hồ sơ: sẽ có văn bản, trong 30 ngày kể từ khi có văn bản mà cơ sở không nộp: Thu hồi GCNĐĐKKDD + GPP

KIỂM SOÁT THAY ĐỔI VIỆC DUY TRÌ ĐÁP ỨNG THỰC HÀNH TỐT CƠ SỞ BÁN LẺ THUỐC (tt) Đề nghị cấp GCNĐĐKKDD hoặc B. cáo thay đổi: 1. Đã được cấp GCNĐĐKKDD nhưng thay đổi loại hình cơ sở kinh doanh dược hoặc thay đổi PVKD mà làm thay đổi điều kiện kinh doanh, thay đổi địa điểm KD (Có đánh giá thực tế) 2. Thay đổi vị trí cơ sở bán lẻ thuốc tại cùng địa điểm kinh doanh (Có đánh giá thực tế) 3. Mở rộng cơ sở bán lẻ thuốc (Không đánh giá thực tế) 4. Sửa chữa, thay đổi lớn về cấu trúc bán lẻ thuốc (Không đánh giá thực tế) n

ĐOÀN ĐÁNH GIÁ VIỆC ĐÁP ỨNG THỰC HÀNH TỐT CƠ SỞ BÁN LẺ THUỐC Quyền hạn: + Kiểm tra toàn bộ các khu vực liên quan đến hoạt động bán lẻ thuốc + Yêu cầu cung cấp hồ sơ, tài liệu + Thu thập tài liệu (chụp ảnh, quay video, sao chụp tài liệu) chứng minh tồn tại + Lấy mẫu thuốc gửi kiểm tra chất lượng + Lập biên bản yêu cầu tạm dừng hoạt động

ĐIỀU KHOẢN THI HÀNH THỰC HÀNH TỐT CƠ SỞ BÁN LẺ THUỐC Hiệu lực thi hành: 08/3/2018 n Với những hồ sơ nộp trước ngày 08/3/2018: Đánh giá theo Thông tư số 46/2011/TT-BYT n
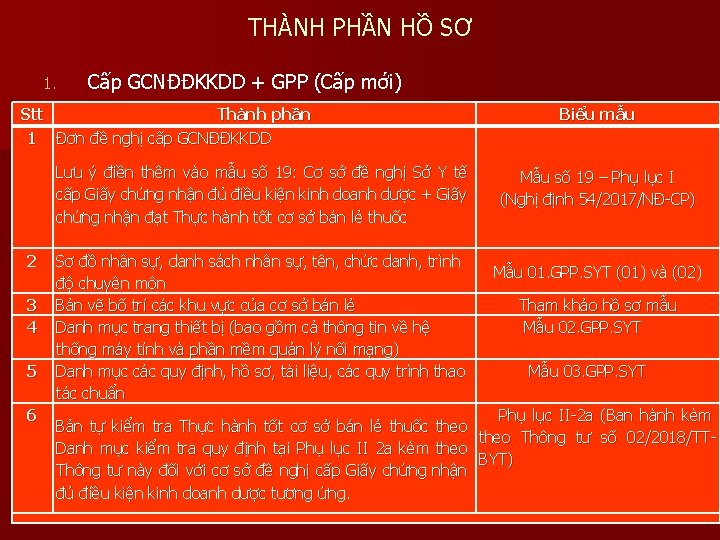
THÀNH PHẦN HỒ SƠ 1. Cấp GCNĐĐKKDD + GPP (Cấp mới) Stt Thành phần 1 Đơn đề nghị cấp GCNĐĐKKDD Lưu ý điền thêm vào mẫu số 19: Cơ sở đề nghị Sở Y tế cấp Giấy chứng nhận đủ điều kiện kinh doanh dược + Giấy chứng nhận đạt Thực hành tốt cơ sở bán lẻ thuốc 2 3 4 5 6 Biểu mẫu Mẫu số 19 – Phụ lục I (Nghị định 54/2017/NĐ-CP) Sơ đồ nhân sự, danh sách nhân sự, tên, chức danh, trình Mẫu 01. GPP. SYT (01) và (02) độ chuyên môn Tham khảo hồ sơ mẫu Bản vẽ bố trí các khu vực của cơ sở bán lẻ Danh mục trang thiết bị (bao gồm cả thông tin về hệ Mẫu 02. GPP. SYT thống máy tính và phần mềm quản lý nối mạng) Danh mục các quy định, hồ sơ, tài liệu, các quy trình thao Mẫu 03. GPP. SYT tác chuẩn Phụ lục II-2 a (Ban hành kèm Bản tự kiểm tra Thực hành tốt cơ sở bán lẻ thuốc theo Thông tư số 02/2018/TTDanh mục kiểm tra quy định tại Phụ lục II 2 a kèm theo BYT) Thông tư này đối với cơ sở đề nghị cấp Giấy chứng nhận đủ điều kiện kinh doanh dược tương ứng.
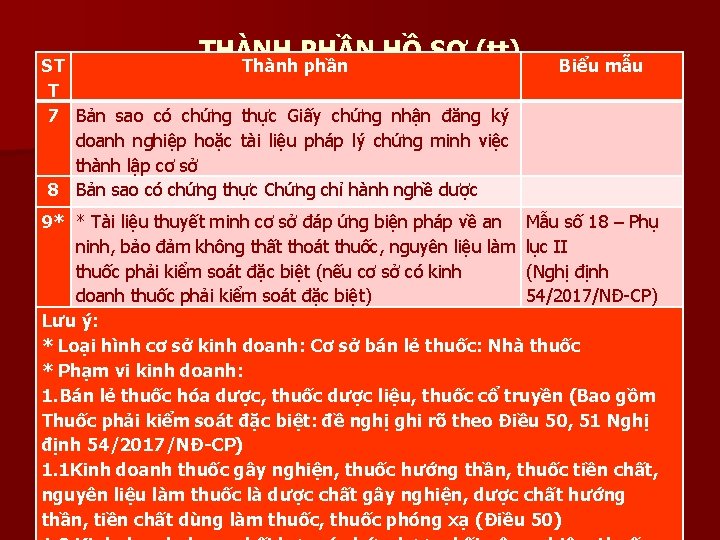
THÀNH PHẦN HỒ SƠ (tt) Thành phần ST T 7 Bản sao có chứng thực Giấy chứng nhận đăng ký doanh nghiệp hoặc tài liệu pháp lý chứng minh việc thành lập cơ sở 8 Bản sao có chứng thực Chứng chỉ hành nghề dược Biểu mẫu 9* * Tài liệu thuyết minh cơ sở đáp ứng biện pháp về an Mẫu số 18 – Phụ ninh, bảo đảm không thất thoát thuốc, nguyên liệu làm lục II thuốc phải kiểm soát đặc biệt (nếu cơ sở có kinh (Nghị định doanh thuốc phải kiểm soát đặc biệt) 54/2017/NĐ-CP) Lưu ý: * Loại hình cơ sở kinh doanh: Cơ sở bán lẻ thuốc: Nhà thuốc * Phạm vi kinh doanh: 1. Bán lẻ thuốc hóa dược, thuốc dược liệu, thuốc cổ truyền (Bao gồm Thuốc phải kiểm soát đặc biệt: đề nghị ghi rõ theo Điều 50, 51 Nghị định 54/2017/NĐ-CP) 1. 1 Kinh doanh thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc, thuốc phóng xạ (Điều 50)
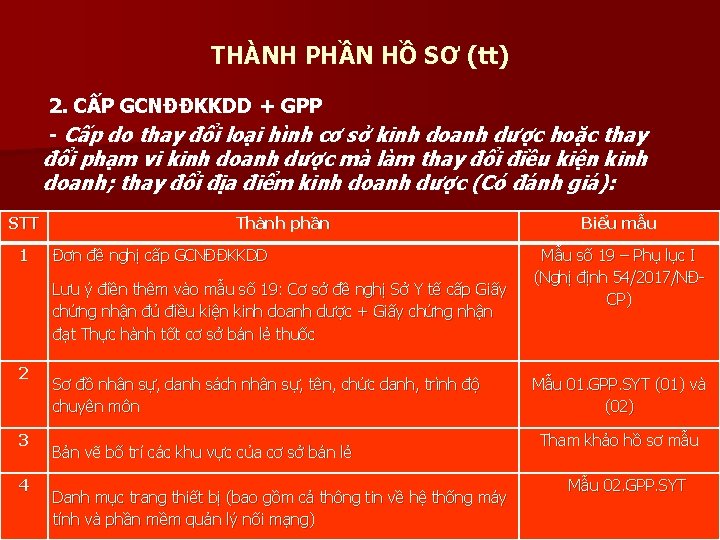
THÀNH PHẦN HỒ SƠ (tt) 2. CẤP GCNĐĐKKDD + GPP - Cấp do thay đổi loại hình cơ sở kinh doanh dược hoặc thay đổi phạm vi kinh doanh dược mà làm thay đổi điều kiện kinh doanh; thay đổi địa điểm kinh doanh dược (Có đánh giá): STT 1 Thành phần Đơn đề nghị cấp GCNĐĐKKDD Lưu ý điền thêm vào mẫu số 19: Cơ sở đề nghị Sở Y tế cấp Giấy chứng nhận đủ điều kiện kinh doanh dược + Giấy chứng nhận đạt Thực hành tốt cơ sở bán lẻ thuốc 2 3 4 Sơ đồ nhân sự, danh sách nhân sự, tên, chức danh, trình độ chuyên môn Bản vẽ bố trí các khu vực của cơ sở bán lẻ Danh mục trang thiết bị (bao gồm cả thông tin về hệ thống máy tính và phần mềm quản lý nối mạng) Biểu mẫu Mẫu số 19 – Phụ lục I (Nghị định 54/2017/NĐCP) Mẫu 01. GPP. SYT (01) và (02) Tham khảo hồ sơ mẫu Mẫu 02. GPP. SYT
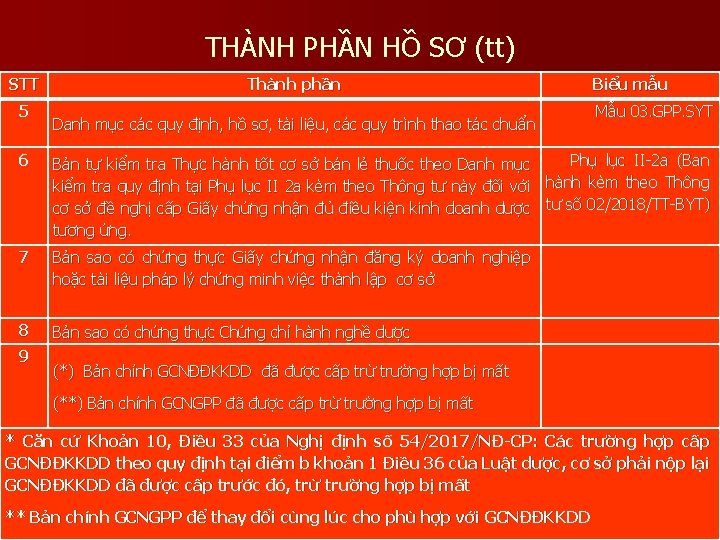
THÀNH PHẦN HỒ SƠ (tt) STT 5 Thành phần Danh mục các quy định, hồ sơ, tài liệu, các quy trình thao tác chuẩn Biểu mẫu Mẫu 03. GPP. SYT 6 Bản tự kiểm tra Thực hành tốt cơ sở bán lẻ thuốc theo Danh mục kiểm tra quy định tại Phụ lục II 2 a kèm theo Thông tư này đối với cơ sở đề nghị cấp Giấy chứng nhận đủ điều kiện kinh doanh dược tương ứng. 7 Bản sao có chứng thực Giấy chứng nhận đăng ký doanh nghiệp hoặc tài liệu pháp lý chứng minh việc thành lập cơ sở 8 Bản sao có chứng thực Chứng chỉ hành nghề dược 9 (*) Bản chính GCNĐĐKKDD đã được cấp trừ trường hợp bị mất Phụ lục II-2 a (Ban hành kèm theo Thông tư số 02/2018/TT-BYT) (**) Bản chính GCNGPP đã được cấp trừ trường hợp bị mất * Căn cứ Khoản 10, Điều 33 của Nghị định số 54/2017/NĐ-CP: Các trường hợp cấp GCNĐĐKKDD theo quy định tại điểm b khoản 1 Điều 36 của Luật dược, cơ sở phải nộp lại GCNĐĐKKDD đã được cấp trước đó, trừ trường hợp bị mất ** Bản chính GCNGPP để thay đổi cùng lúc cho phù hợp với GCNĐĐKKDD
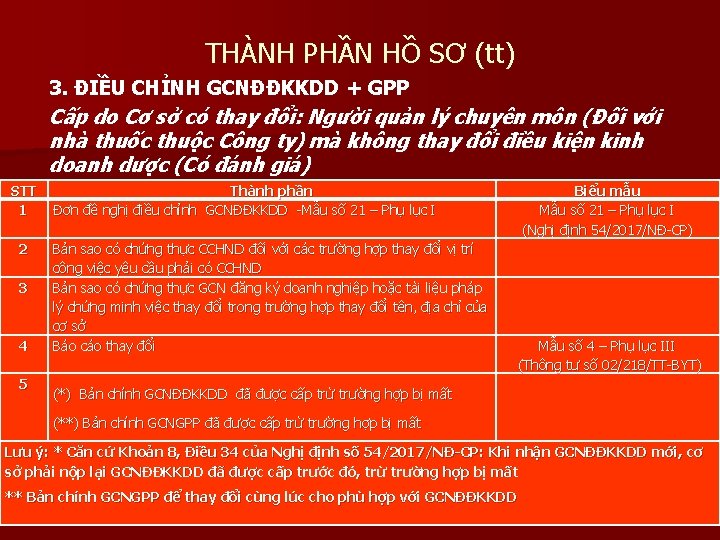
THÀNH PHẦN HỒ SƠ (tt) 3. ĐIỀU CHỈNH GCNĐĐKKDD + GPP Cấp do Cơ sở có thay đổi: Người quản lý chuyên môn (Đối với nhà thuốc thuộc Công ty) mà không thay đổi điều kiện kinh doanh dược (Có đánh giá) STT 1 2 3 4 5 Thành phần Đơn đề nghị điều chỉnh GCNĐĐKKDD -Mẫu số 21 – Phụ lục I Biểu mẫu Mẫu số 21 – Phụ lục I (Nghị định 54/2017/NĐ-CP) Bản sao có chứng thực CCHND đối với các trường hợp thay đổi vị trí công việc yêu cầu phải có CCHND Bản sao có chứng thực GCN đăng ký doanh nghiệp hoặc tài liệu pháp lý chứng minh việc thay đổi trong trường hợp thay đổi tên, địa chỉ của cơ sở Báo cáo thay đổi (*) Bản chính GCNĐĐKKDD đã được cấp trừ trường hợp bị mất Mẫu số 4 – Phụ lục III (Thông tư số 02/218/TT-BYT) (**) Bản chính GCNGPP đã được cấp trừ trường hợp bị mất Lưu ý: * Căn cứ Khoản 8, Điều 34 của Nghị định số 54/2017/NĐ-CP: Khi nhận GCNĐĐKKDD mới, cơ sở phải nộp lại GCNĐĐKKDD đã được cấp trước đó, trừ trường hợp bị mất ** Bản chính GCNGPP để thay đổi cùng lúc cho phù hợp với GCNĐĐKKDD
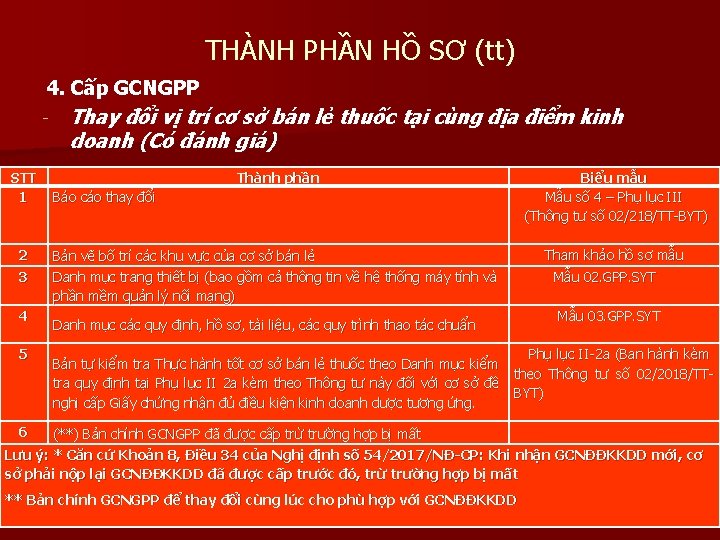
THÀNH PHẦN HỒ SƠ (tt) 4. Cấp GCNGPP STT 1 2 3 4 5 Thay đổi vị trí cơ sở bán lẻ thuốc tại cùng địa điểm kinh doanh (Có đánh giá) Thành phần Báo cáo thay đổi Biểu mẫu Mẫu số 4 – Phụ lục III (Thông tư số 02/218/TT-BYT) Tham khảo hồ sơ mẫu Bản vẽ bố trí các khu vực của cơ sở bán lẻ Danh mục trang thiết bị (bao gồm cả thông tin về hệ thống máy tính và Mẫu 02. GPP. SYT phần mềm quản lý nối mạng) Mẫu 03. GPP. SYT Danh mục các quy định, hồ sơ, tài liệu, các quy trình thao tác chuẩn Phụ lục II-2 a (Ban hành kèm Bản tự kiểm tra Thực hành tốt cơ sở bán lẻ thuốc theo Danh mục kiểm theo Thông tư số 02/2018/TTtra quy định tại Phụ lục II 2 a kèm theo Thông tư này đối với cơ sở đề BYT) nghị cấp Giấy chứng nhận đủ điều kiện kinh doanh dược tương ứng. 6 (**) Bản chính GCNGPP đã được cấp trừ trường hợp bị mất Lưu ý: * Căn cứ Khoản 8, Điều 34 của Nghị định số 54/2017/NĐ-CP: Khi nhận GCNĐĐKKDD mới, cơ sở phải nộp lại GCNĐĐKKDD đã được cấp trước đó, trừ trường hợp bị mất ** Bản chính GCNGPP để thay đổi cùng lúc cho phù hợp với GCNĐĐKKDD
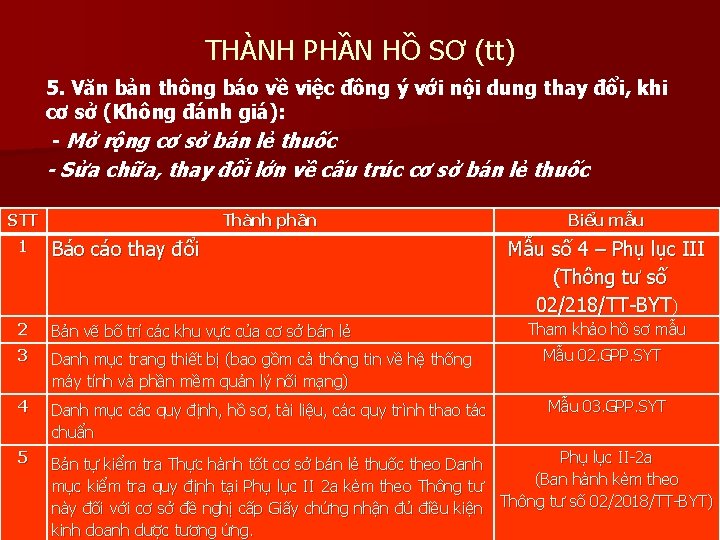
THÀNH PHẦN HỒ SƠ (tt) 5. Văn bản thông báo về việc đồng ý với nội dung thay đổi, khi cơ sở (Không đánh giá): - Mở rộng cơ sở bán lẻ thuốc - Sửa chữa, thay đổi lớn về cấu trúc cơ sở bán lẻ thuốc STT Thành phần Biểu mẫu 1 Báo cáo thay đổi 2 Bản vẽ bố trí các khu vực của cơ sở bán lẻ 3 Danh mục trang thiết bị (bao gồm cả thông tin về hệ thống máy tính và phần mềm quản lý nối mạng) 4 Danh mục các quy định, hồ sơ, tài liệu, các quy trình thao tác Mẫu 03. GPP. SYT chuẩn 5 Phụ lục II-2 a Bản tự kiểm tra Thực hành tốt cơ sở bán lẻ thuốc theo Danh (Ban hành kèm theo mục kiểm tra quy định tại Phụ lục II 2 a kèm theo Thông tư này đối với cơ sở đề nghị cấp Giấy chứng nhận đủ điều kiện Thông tư số 02/2018/TT-BYT) kinh doanh dược tương ứng. Mẫu số 4 – Phụ lục III (Thông tư số 02/218/TT-BYT) Tham khảo hồ sơ mẫu Mẫu 02. GPP. SYT
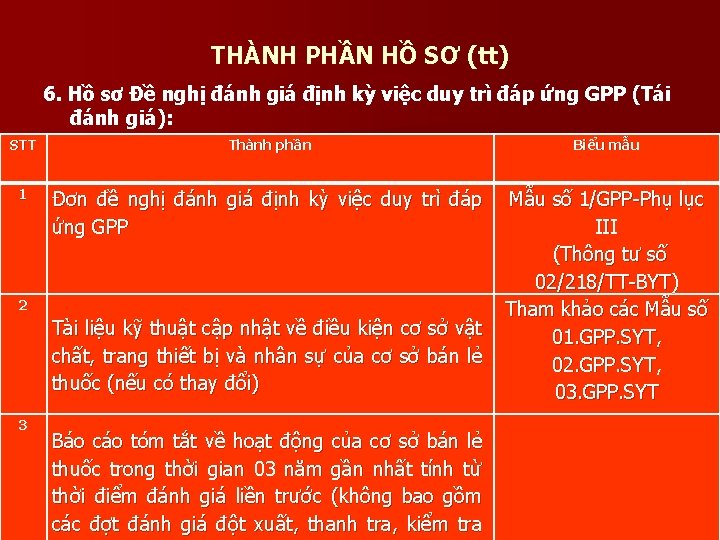
THÀNH PHẦN HỒ SƠ (tt) 6. Hồ sơ Đề nghị đánh giá định kỳ việc duy trì đáp ứng GPP (Tái đánh giá): STT Thành phần 1 Đơn đề nghị đánh giá định kỳ việc duy trì đáp ứng GPP 2 3 Biểu mẫu Mẫu số 1/GPP-Phụ lục III (Thông tư số 02/218/TT-BYT) Tham khảo các Mẫu số Tài liệu kỹ thuật cập nhật về điều kiện cơ sở vật 01. GPP. SYT, chất, trang thiết bị và nhân sự của cơ sở bán lẻ 02. GPP. SYT, thuốc (nếu có thay đổi) 03. GPP. SYT Báo cáo tóm tắt về hoạt động của cơ sở bán lẻ thuốc trong thời gian 03 năm gần nhất tính từ thời điểm đánh giá liền trước (không bao gồm các đợt đánh giá đột xuất, thanh tra, kiểm tra



HƯỚNG DẪN GHI CHÉP BIỂU MẪU (tt)

HƯỚNG DẪN GHI CHÉP BIỂU MẪU (tt)
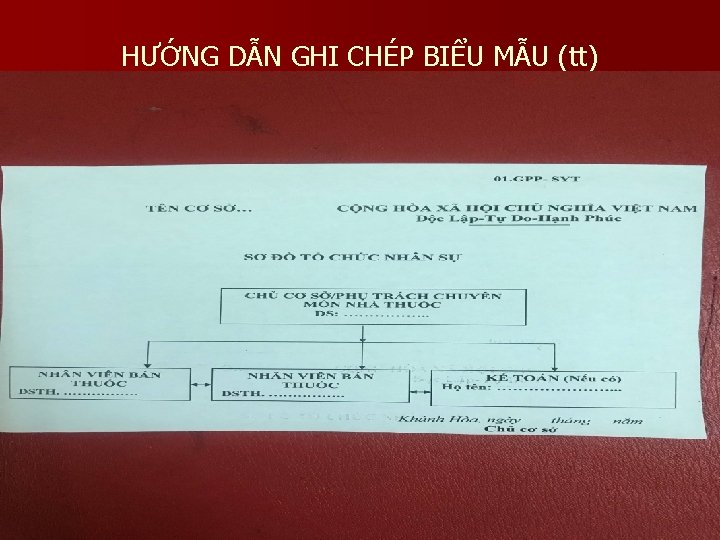
HƯỚNG DẪN GHI CHÉP BIỂU MẪU (tt)
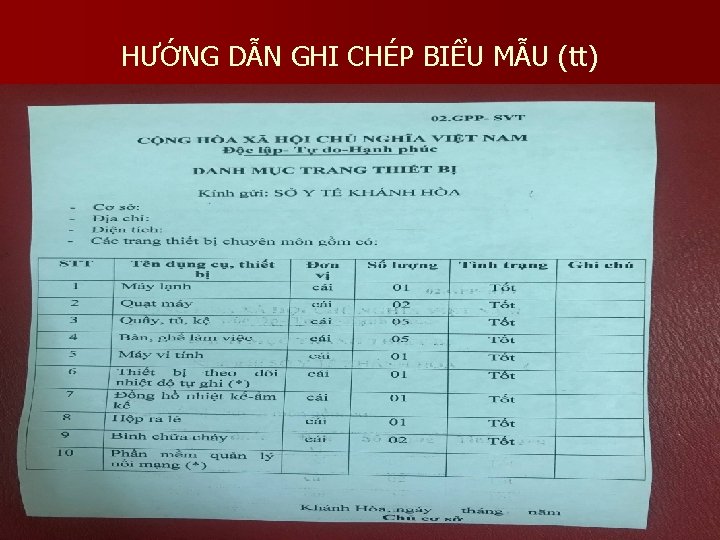
HƯỚNG DẪN GHI CHÉP BIỂU MẪU (tt)

HƯỚNG DẪN GHI CHÉP BIỂU MẪU (tt)

XIN TRỌNG CÁM ƠN!
- Slides: 28