Thng bng kim toan Mc tiu n Gii

Thăng bằng kiềm toan

Mục tiêu n Giới thiệu công cụ và các thông số thường dùng trong phân tích và đánh giá acid-based n Những rối loạn acid-base đơn giản n Tiếp cận một cách hệ thống rối loạn acid-base 2 2

Công cụ phân tích Acid – Base n Khí máu động mạch (p. H, CO 2 , HCO 3) n Điện giải đồ (Na, Cl) 3 3
![Khái niệm cơ bản n [H+] = 24 x (Pa. CO 2 / [HCO Khái niệm cơ bản n [H+] = 24 x (Pa. CO 2 / [HCO](http://slidetodoc.com/presentation_image_h/bbf7702d0c7e4f1d80e44d41afa54532/image-4.jpg)
Khái niệm cơ bản n [H+] = 24 x (Pa. CO 2 / [HCO 3 -]) n Diễn đạt bằng p. H, [H+] và p. H thay đổi nghịch chiều n RL toan kiềm nguyên phát Để giữ p. H không đổi cơ thể điều chỉnh sao cho Pa. CO 2/[HCO 3 -] không đổi (đáp ứng bù trừ) ¨ RL nguyên phát là CH (HCO 3 -) đáp ứng bù trừ sẽ là HH (Pa. CO 2) ¨ RL nguyên phát là HH (Pa. CO 2) đáp ứng bù trừ sẽ là CH (HCO 3 -) 4 4
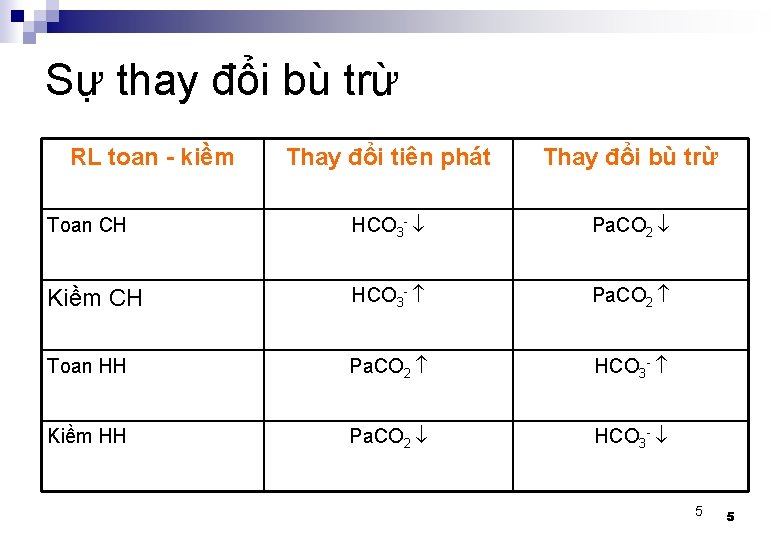
Sự thay đổi bù trừ RL toan - kiềm Thay đổi tiên phát Thay đổi bù trừ Toan CH HCO 3 - Pa. CO 2 Kiềm CH HCO 3 - Pa. CO 2 Toan HH Pa. CO 2 HCO 3 - Kiềm HH Pa. CO 2 HCO 3 - 5 5
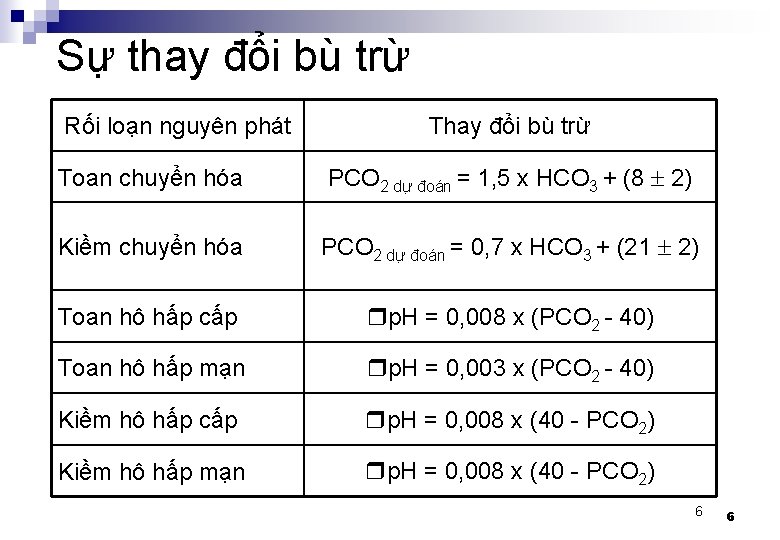
Sự thay đổi bù trừ Rối loạn nguyên phát Thay đổi bù trừ Toan chuyển hóa PCO 2 dự đoán = 1, 5 x HCO 3 + (8 2) Kiềm chuyển hóa PCO 2 dự đoán = 0, 7 x HCO 3 + (21 2) Toan hô hấp cấp p. H = 0, 008 x (PCO 2 - 40) Toan hô hấp mạn p. H = 0, 003 x (PCO 2 - 40) Kiềm hô hấp cấp p. H = 0, 008 x (40 - PCO 2) Kiềm hô hấp mạn p. H = 0, 008 x (40 - PCO 2) 6 6
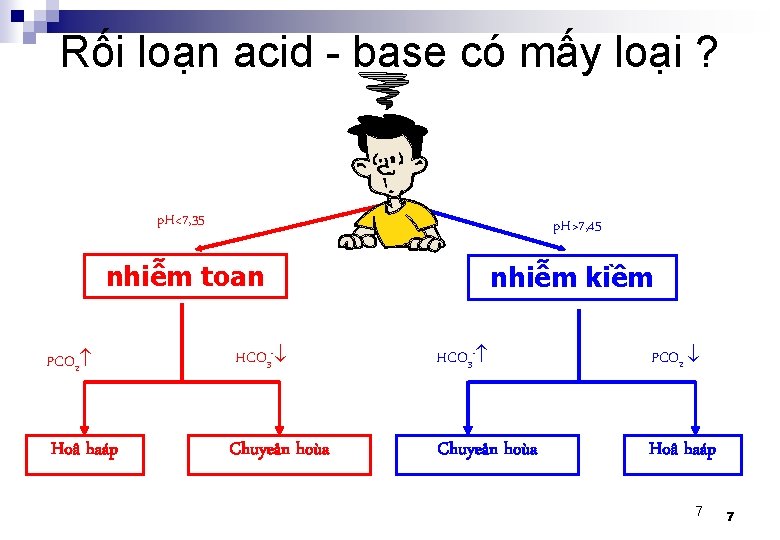
Rối loạn acid - base có mấy loại ? p. H<7, 35 p. H>7, 45 nhiễm toan nhiễm kiềm PCO 2 HCO 3 - PCO 2 Hoâ haáp Chuyeån hoùa Hoâ haáp 7 7

Rối loạn chuyển hoá tiên phát n Luật 1 ¨ RL toan - kiềm chuyển hóa nguyên phát nếu n p. H bất thường và p. H, PCO 2 thay đổi cùng chiều n Nhiễm toan chuyển hoá ¨ n p. H < 7, 36 và PCO 2 H+ + HCO 3 - H 2 CO 3 H 2 O + CO 2 Nhiễm kiềm chuyển hoá ¨ p. H > 7, 44 và PCO 2 H+ + HCO 3 - H 2 CO 3 H 2 O + CO 2 8 8

Rối loạn chuyển hoá tiên phát n Luật 2 ¨ RL Toan chuyển hóa PCO 2 dự đoán = 1, 5 x HCO 3 + (8 2) Kiềm chuyển hóa PCO 2 dự đoán = 0, 7 x HCO 3 + (21 2) toan kiềm hô hấp kèm theo nếu n Pa. CO 2 đo được > Pa. CO 2 dự đoán: toan hô hấp n Pa. CO 2 đo được < PCO 2 dự đoán: kiềm hô hấp 9 9

Rối loạn hô hấp tiên phát n Luật 3 ¨ RL toan-kiềm do hô hấp tiên phát khi: n Pa. CO 2 bất thường và Pa. CO 2 và p. H thay đổi ngược chiều nhau n Toan hô hấp n ¨ Pa. CO 2 > 44 mm. Hg ¨ p. H H+ + HCO 3 - H 2 CO 3 H 2 O + CO 2 Kiềm hô hấp ¨ Pa. CO 2 < 36 mm. Hg ¨ p. H H+ + HCO 3 - H 2 CO 3 H 2 O + CO 2 10 10
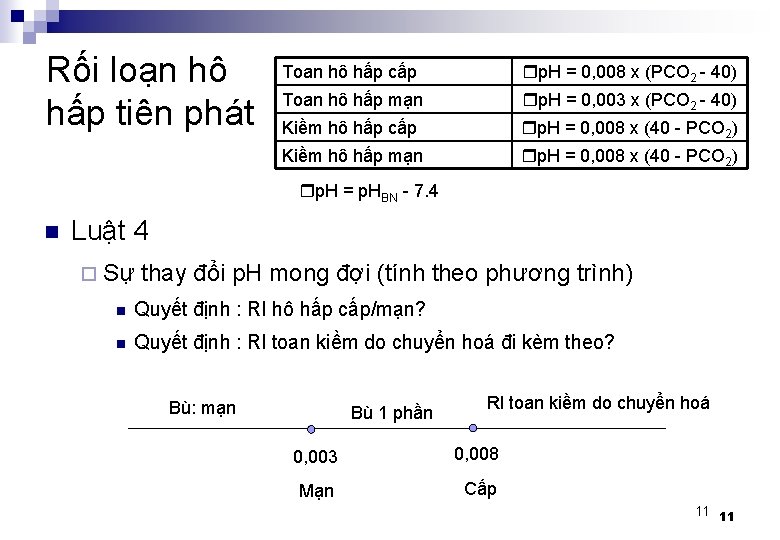
Rối loạn hô hấp tiên phát Toan hô hấp cấp p. H = 0, 008 x (PCO 2 - 40) Toan hô hấp mạn p. H = 0, 003 x (PCO 2 - 40) Kiềm hô hấp cấp p. H = 0, 008 x (40 - PCO 2) Kiềm hô hấp mạn p. H = 0, 008 x (40 - PCO 2) p. H = p. HBN - 7. 4 n Luật 4 ¨ Sự thay đổi p. H mong đợi (tính theo phương trình) n Quyết định : Rl hô hấp cấp/mạn? n Quyết định : Rl toan kiềm do chuyển hoá đi kèm theo? Bù: mạn Bù 1 phần Rl toan kiềm do chuyển hoá 0, 003 0, 008 Mạn Cấp 11 11

Rối loạn hỗn hợp n Luật 5 ¨ RL toan kiềm hỗn hợp n PCO 2 bất thường, p. H bình thường n p. H bất thường, PCO 2 bình thường 12 12

Áp dụng 5 qui luật đọc KMĐM 13 13

p. H thay đổi n p. H < 7. 36 nhiễm toan: ¨ Pa. CO 2 n giảm or BT toan CH nguyên phát (QL 1) Sự chênh lệch giữa Pa. CO 2 dự đoán và đo được sẽ cho biết toan kiềm HH kết hợp (QL 2) ¨ Pa. CO 2 tăng n toan HH nguyên phát Sự chênh lệch giữa p. H đo được và p. H chuẩn (7. 4) cho biết RL cấp or mãn và có RL toan kiềm CH kết hợp hay không (QL 4) 14 14

p. H thay đổi n p. H > 7. 44 nhiễm kiềm ¨ Pa. CO 2 n BT or cao kiềm CH nguyên phát So sánh chênh lệch về Pa. CO 2 cho biết RL toan kiềm HH kết hợp (QL 2) ¨ Pa. CO 2 thấp n kiềm HH là nguyên phát (QL 1) Sự chênh lệch giữa p. H đo được và p. H chuẩn (7. 4) cho biết RL cấp or mãn và có RL toan kiềm CH kết hợp hay không (QL 4) 15 15

p. H bình thường n Pa. CO 2 cao toan HH và kiềm CH hỗn hợp (QL 5) n Pa. CO 2 thấp kiềm HH và toan CH hỗn hợp n Pa. CO 2 BT và p. H BT có thể là toan CH đồng thời có kiềm CH 16 16

Anion Gap (khoảng trống anion) n AG = Na+ - (HCO 3 - + Cl-) = 12 ( 2) m. Eq/L n AG cho biết toan CH là do tích tụ acid hay do mất HCO 3¨ AG tăng tích tụ acid hữu cơ (lactic acid, ketoacids) hoặc suy thận không thải acid được ¨ AG BT toan CH mất HCO 317 17
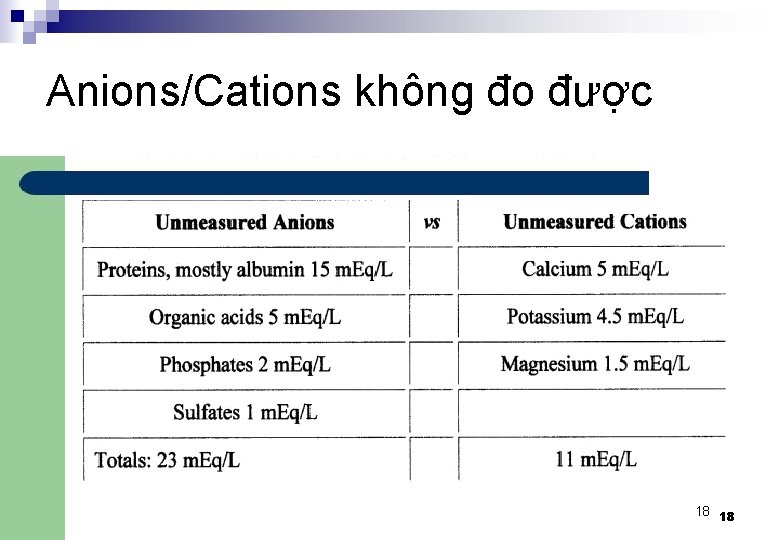
Anions/Cations không đo được 18 18

Qui tắc n Nếu AG 20 nhiễm toan CH nguyên phát dù p. H và bicarbonat như thế nào Chú ý: cơ thể không tạo ra một AG lớn nhằm bù trừ một rối loạn nguyên phát (AG phải là nguyên phát) 19 19

Tại sao? 1. AG > 20 là lớn hơn 4 lần độ lệch chuẩn và do vậy không thể là ngẫu nhiên. 2. Mặc dù AG có thể tăng vừa phải ở BN nhiễm kiềm chuyển hóa hay hô hấp (tăng anion proteins âm), thậm chí nhiễm kiềm nghiêm trọng cũng không bao giờ > 20 3. Nguyên nhân đặc hiệu của AG có thể được phát hiện trong ít nhất 30% cases nếu AG < 20 tới 77% nếu AG>20 và 100% nếu AG >* * Gabow et al. Diagnostic Importance of an increased serum anion gap. N Engl J med. 1980; 303: 854 -858 20 20

Vì thế, n Nếu có AG 20 có giá trị tiên đoán cao bị nhiễm toan chuyển hóa nguyên phát tiềm ẩn có thể phát hiện được 21 21

Excess AG n Tính toán excess AG (total anion gap – normal anion gap) và thêm vào nồng độ bicarbonate: ¨ Nếu: Excess AG + measured HCO 3 = > 30 kiềm chuyển hóa tiềm ẩn ¨ Nếu: Excess AG + measured HCO 3 < 23 toan chuyển hóa có AG tiềm ẩn 1. Excess AG = Total AG – Normal AG (12) 2. Excess AG + measured HCO 3 = > 30 or < 23? Chú ý: 1 mmol của acid không đo được sẽ chuẩn độ với 1 mmol bicarbonate ( anion gap = [ HCO 3]) 22 22

Cám ơn sự chú ý và lắng nghe! 23 23
- Slides: 23