TGAU Gwyddonaieth Ychwanegol Pennod 7 Bondio Adeiledd a

TGAU Gwyddonaieth Ychwanegol Pennod 7 Bondio, Adeiledd a Phriodweddau Cemegol CEMEG 2
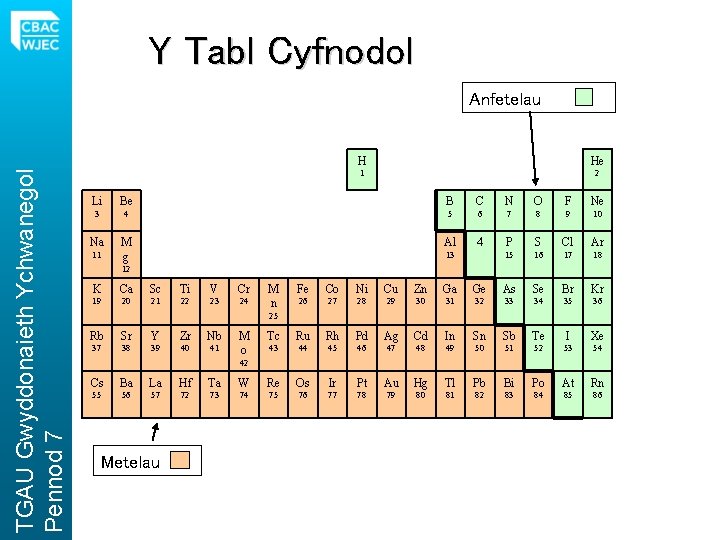
Y Tabl Cyfnodol TGAU Gwyddonaieth Ychwanegol Pennod 7 Anfetelau H He 1 2 Li Be B C N O F Ne 3 4 5 6 7 8 9 10 Na M g Al 4 11 13 P S Cl Ar 15 16 17 18 12 K Ca Sc Ti V Cr 19 20 21 22 23 24 M n Fe Co Ni Cu Zn Ga Ge As Se Br Kr 26 27 28 29 30 31 32 33 34 35 36 Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 43 44 45 46 47 48 49 50 51 52 53 54 25 Rb Sr Y Zr Nb 37 38 39 40 41 M o 42 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 55 56 57 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 Metelau
Cymharu Priodweddau Metelau ac Anfetelau TGAU Gwyddonaieth Ychwanegol Pennod 7 Metelau Anfetelau Dargludyddion da o drydan Dargludyddion gwael o drydan Dargludyddion da o wres Dargludyddion gwael o wres Hydrin (modd eu siapo) Heb fod yn hydrin (yn frau yn y ffurf solid) Hydwyth (gellir eu tynnu’n wifrau) Heb fod yn hydwyth Sgleiniog (pan wedi eu torri yn ffres) Ddim yn sgleiniog fel arfer Mae gan lawer ohonynt ymdoddbwynt uchel Ymdoddbwynt isel Mae gan lawer ohonynt ferwbwyntiau uchel Berwbwyntiau isel
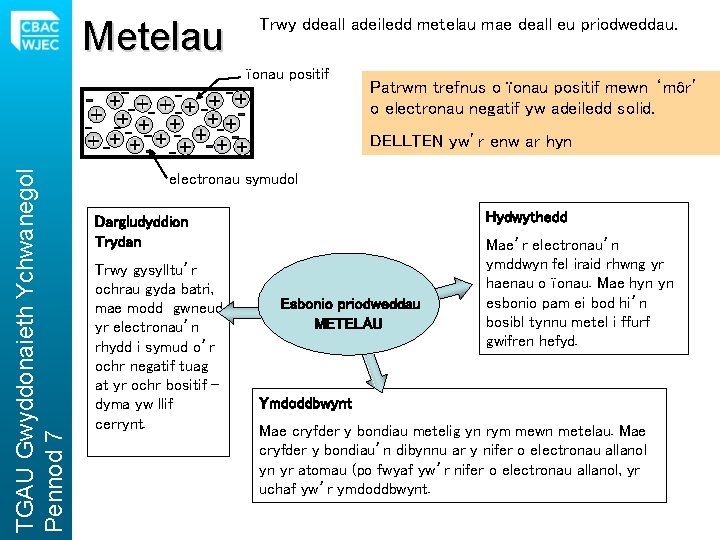
Metelau Trwy ddeall adeiledd metelau mae deall eu priodweddau. ïonau positif Patrwm trefnus o ïonau positif mewn ‘môr’ o electronau negatif yw adeiledd solid. TGAU Gwyddonaieth Ychwanegol Pennod 7 DELLTEN yw’r enw ar hyn electronau symudol Hydwythedd Dargludyddion Trydan Trwy gysylltu’r ochrau gyda batri, mae modd gwneud yr electronau’n rhydd i symud o’r ochr negatif tuag at yr ochr bositif – dyma yw llif cerrynt. Esbonio priodweddau METELAU Mae’r electronau’n ymddwyn fel iraid rhwng yr haenau o ïonau. Mae hyn yn esbonio pam ei bod hi’n bosibl tynnu metel i ffurf gwifren hefyd. Ymdoddbwynt Mae cryfder y bondiau metelig yn rym mewn metelau. Mae cryfder y bondiau’n dibynnu ar y nifer o electronau allanol yn yr atomau (po fwyaf yw’r nifer o electronau allanol, yr uchaf yw’r ymdoddbwynt.

TGAU Gwyddonaieth Ychwanegol Pennod 7 Aloion Mae dur gwrthstaen yn enghraifft o aloi a ddefnyddir i wneud sosbenni, cyllyll, ffyrc a llwyau. Mae rhai aloion yn gallu adfer eu siâp ar ôl eu plygu. Defnyddir y rhain mewn fframiau sbectol. Mae’r aloi modern hwn yn cael ei alw yn aloi cof-siâp ac yn cael ei ystyried yn ‘aloi smart’. Gwydr Metelig Fel y dywedir eisoes, mae gan y rhan fwyaf o solidau adeiledd sy’n dangos patrwm, ond mae’n bosib ffurfio metelau sy’n dangos llai o batrwm – dyma’r gwydrau metelig. Mae gwydrau metelig dair gwaith yn gryfach na dur a deg gwaith yn fwy ystwyth, sy’n eu gwneud yn ddelfrydol ar gyfer pen ffyn golff!
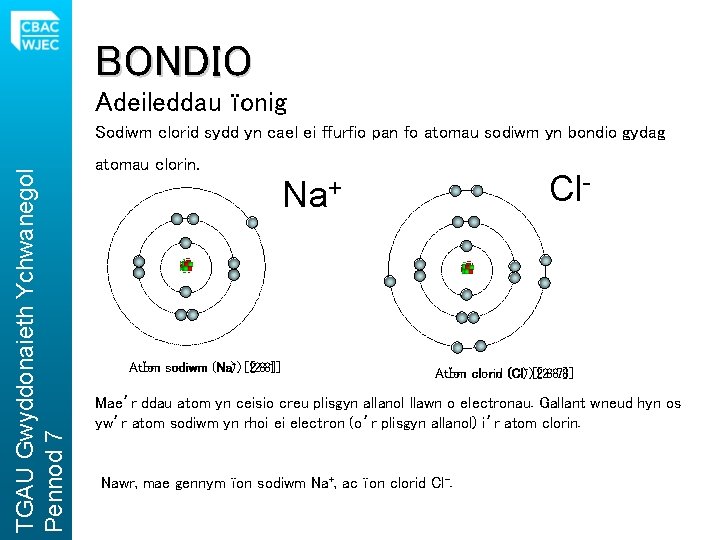
BONDIO Adeileddau ïonig TGAU Gwyddonaieth Ychwanegol Pennod 7 Sodiwm clorid sydd yn cael ei ffurfio pan fo atomau sodiwm yn bondio gydag atomau clorin. Cl- Na+ Atom Ïon sodiwm (Na) (Na+) [2. 8. 1] [2. 8] Ïon clorid (Cl) (Cl-)[2. 8. 7] [2. 8. 8] Atom Mae’r ddau atom yn ceisio creu plisgyn allanol llawn o electronau. Gallant wneud hyn os yw’r atom sodiwm yn rhoi ei electron (o’r plisgyn allanol) i’r atom clorin. Nawr, mae gennym ïon sodiwm Na+, ac ïon clorid Cl-.
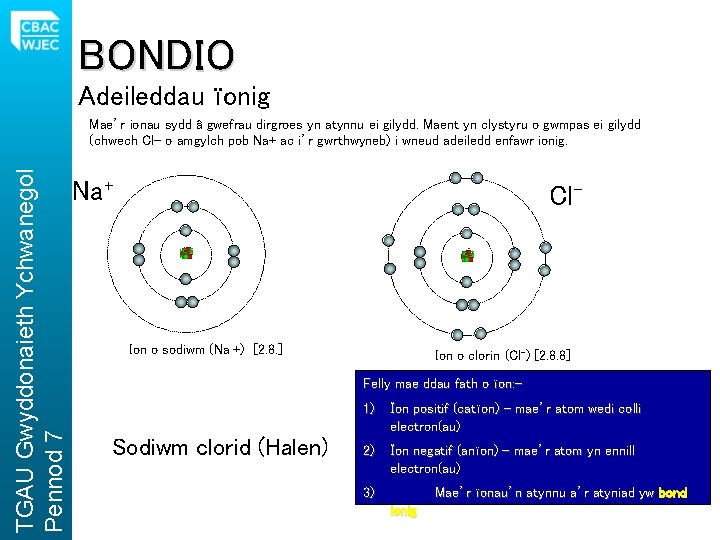
BONDIO Adeileddau ïonig TGAU Gwyddonaieth Ychwanegol Pennod 7 Mae’r ionau sydd â gwefrau dirgroes yn atynnu ei gilydd. Maent yn clystyru o gwmpas ei gilydd (chwech Cl- o amgylch pob Na+ ac i’r gwrthwyneb) i wneud adeiledd enfawr ionig. Na+ Cl- Ion o sodiwm (Na +) [2. 8. ] Ion o clorin (Cl-) [2. 8. 8] Felly mae ddau fath o ïon: - Sodiwm clorid (Halen) 1) Ïon positif (catïon)) – mae’r atom wedi colli electron(au) 2) Ïon negatif (anïon)) – mae’r atom yn ennill electron(au) 3) Mae’r ïonau’n atynnu a’r atyniad yw bond ionig.

BONDIO Adeileddau ïonig Felly mae dau fath o ïon: - 1) Ïon positif (catïon)) – mae’r atom wedi colli electron(au) 2) Ïon negatif (anïon)) – mae’r atom yn ennill electron(au) TGAU Gwyddonaieth Ychwanegol Pennod 7 Mae’r ïonau’n atynnu a’r atyniad yw bond ionig. Mae’r ionau sydd â gwefrau dirgroes yn atynnu ei gilydd. Maent yn clystyru o gwmpas ei gilydd (chwech Cl- o amgylch pob Na+ ac i’r gwrthwyneb) i wneud adeiledd enfawr ionig. Chwech ïon Clorid o amgylch un ïon Sodiwm Adeiledd moleciwlaidd Sodiwm Clorid (Cliciwch er mwyn chwarae’r animeiddiad) Chwech ïon Sodiwm o amgylch un ïon Clorid
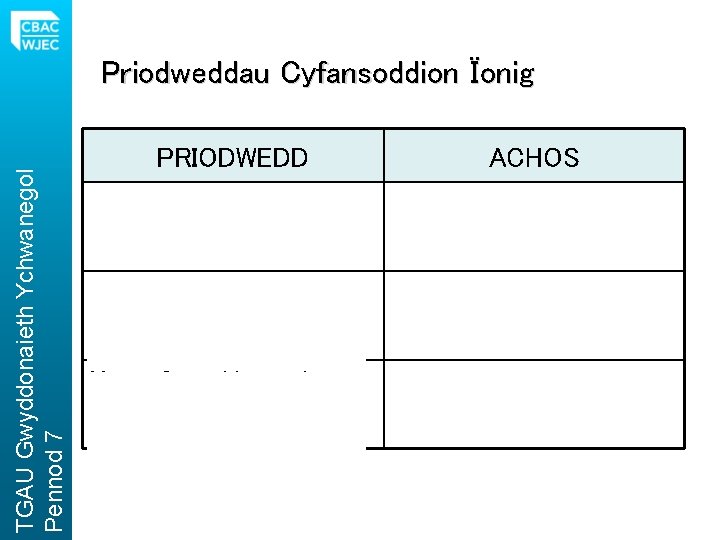
TGAU Gwyddonaieth Ychwanegol Pennod 7 Priodweddau Cyfansoddion Ïonig PRIODWEDD ACHOS Ymdoddbwyntiau uchel. Grymoedd electrostatig cryf rhwng yr ïonau. Mae angen llawer o egni i’w torri. Nid yw cyfansoddyn ïonig solet yn dargludo trydan. Mae’r ïonau wedi’u dal mewn safleoedd penodol, nid ydynt yn rhydd i symud. Mae cyfansoddyn ïonig tawdd yn dargludo trydan. Mae toddi yn gwahanu’r ionau fel y gallant symud heibio’i gilydd.

BONDIO TGAU Gwyddonaieth Ychwanegol Pennod 7 Bondio Cofalent Mae atomau anfetelau’n bondio gyda’i gilydd wrth rannu electronau’r plisgyn allanol. BONDIO COFALENT yw’r enw ar hyn. Gall bondio cofalent greu: • Moleciwlau bach o elfennau, e. e. H 2 • Moleciwlau bach o gyfansoddion, e. e. HCl • Moleciwlau enfawr o elfennau, e. e. diemwnt a graffit • Moleiwlau enfawr o gyfansoddion, e. e. Si. O 2
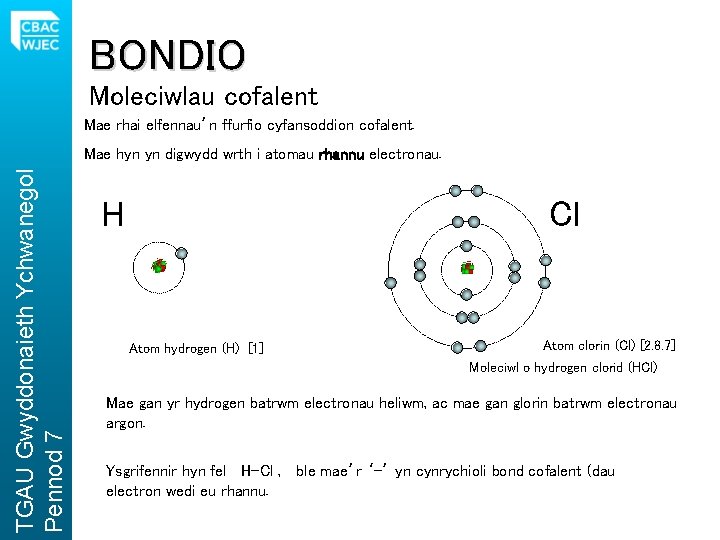
BONDIO Moleciwlau cofalent Mae rhai elfennau’n ffurfio cyfansoddion cofalent. TGAU Gwyddonaieth Ychwanegol Pennod 7 Mae hyn yn digwydd wrth i atomau rhannu electronau. H Cl Atom hydrogen (H) [1] Atom clorin (Cl) [2. 8. 7] Moleciwl o hydrogen clorid (HCl) Mae gan yr hydrogen batrwm electronau heliwm, ac mae gan glorin batrwm electronau argon. Ysgrifennir hyn fel H-Cl , ble mae’r ‘-’ yn cynrychioli bond cofalent (dau electron wedi eu rhannu.
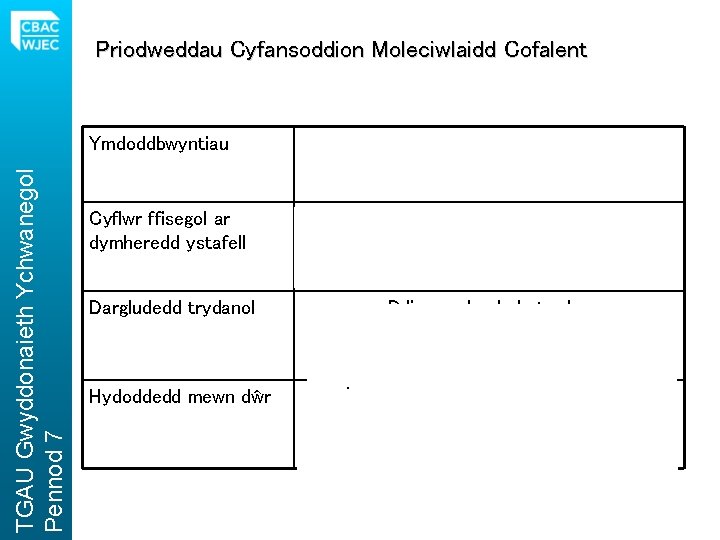
Priodweddau Cyfansoddion Moleciwlaidd Cofalent TGAU Gwyddonaieth Ychwanegol Pennod 7 Ymdoddbwyntiau Isel (atyniad rhwng y moleciwlau’n wan) Cyflwr ffisegol ar dymheredd ystafell Nwyon neu hylifau sydd â berwbwyntiau isel neu solidau ag ymdoddbwyntiau isel (grymoedd atyniad gwan rhwng y moleciwlau) Dargludedd trydanol Ddim yn dargludo trydan (nid oes gwefr gan y moleciwlau) Hydoddedd mewn dŵr Mae’r rhan fwyaf yn anhydawdd mewn dŵr
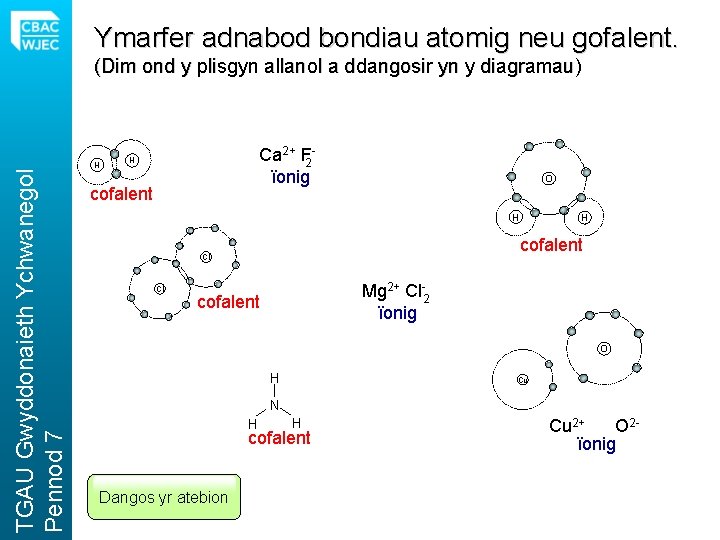
Ymarfer adnabod bondiau atomig neu gofalent. TGAU Gwyddonaieth Ychwanegol Pennod 7 (Dim ond y plisgyn allanol a ddangosir yn y diagramau) H Ca 2+ F 2ïonig H cofalent O H cofalent Cl Cl H Mg 2+ Cl-2 ïonig cofalent O H Cu N H H cofalent Dangos yr atebion Cu 2+ O 2ïonig

Adeileddau Cofalent Enfawr Cymharu priodweddau diemwnt a graffit TGAU Gwyddonaieth Ychwanegol Pennod 7 Mae rhai sylweddau cofalent yn bodoli fel adeileddau enfawr. Mae gan rain ymdoddbwyntiau uchel am fod yr atomau i gyd yn cael eu dal gan fondiau cofalent cryf. Mae diemwnt a graffit yn enghreifftiau o adeileddau cofalent enfawr a wneir o gasgliad o atomau carbon yn unig. PRIODWEDD Golwg Caledwch Diemwnt Crisialau tryloyw. Solid llwyd/du sgleiniog. Yn hynod o galed – fe’i ddefnyddir i dorri gwydr, ac ym mlaen ebillion dril ar gyfer torri trwy graig wrth chwilio am olew. Meddal iawn – gallu ei ddefnyddio fel iraid (lubricant). Defnyddir mewn pensiliau. Ynysydd trydan. Yn anfetel sy’n dargludo trydan. Cael ei ddefnyddio ar gyfer electrodau. Uchel iawn – dros 3500°C. Uchel iawn – dros 3600°C. Dargludedd Ymdoddbwynt Graffit
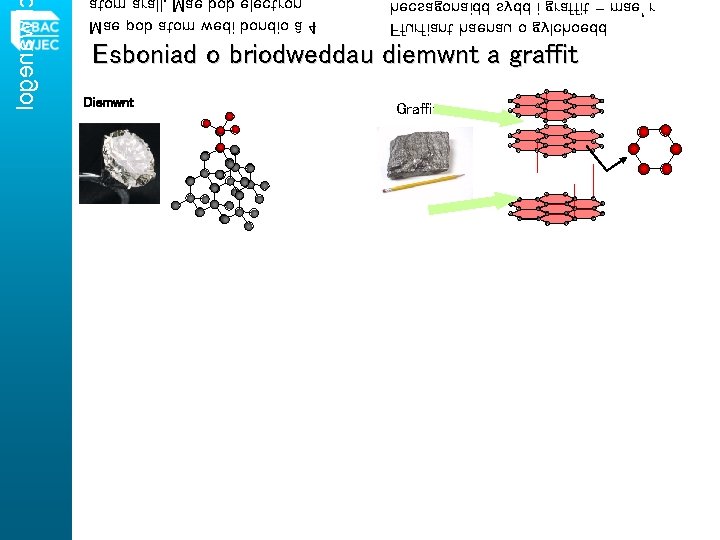
logenawhc Mae pob atom wedi bondio â 4 hecsagonaidd sydd i graffit – mae’r Ffurfiant haenau o gylchoedd Esboniad o briodweddau diemwnt a graffit Diemwnt Graffit
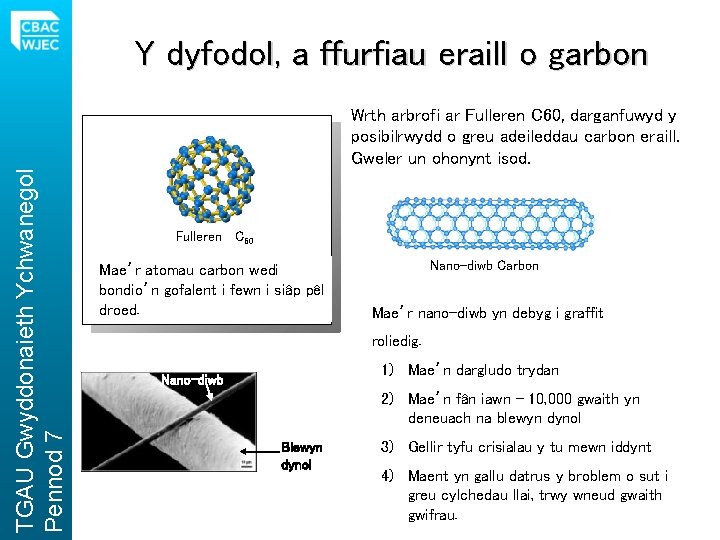
Y dyfodol, a ffurfiau eraill o garbon TGAU Gwyddonaieth Ychwanegol Pennod 7 Wrth arbrofi ar Fulleren C 60, darganfuwyd y posibilrwydd o greu adeileddau carbon eraill. Gweler un ohonynt isod. Fulleren C 60 Mae’r atomau carbon wedi bondio’n gofalent i fewn i siâp pêl droed. Nano-diwb Carbon Mae’r nano-diwb yn debyg i graffit roliedig. 1) Mae’n dargludo trydan Nano-diwb 2) Mae’n fân iawn – 10, 000 gwaith yn deneuach na blewyn dynol Blewyn dynol 3) Gellir tyfu crisialau y tu mewn iddynt 4) Maent yn gallu datrus y broblem o sut i greu cylchedau llai, trwy wneud gwaith gwifrau.
- Slides: 16