TERMOQUMICA Unidad 1 Contenidos 1 1 2 Sistemas











































- Slides: 45

TERMOQUÍMICA Unidad 1

Contenidos (1) 1. 2. - Sistemas, estados y funciones de estado. Primer principio de la Termodinámica. 3. - Energía interna y entalpía. Reacciones a volumen y a presión constante. 3. 1. 4. - Relación entre ambas. Entalpía estándar de reacción. 4. 1. Ecuaciones termoquímicas. 5. 6. - Entalpía estándar de formación. Cálculo de las entalpías de reacción. 7. - Ley de Hess. 2

Contenidos (2) 8. - 3 Energía o entalpía de enlace. 8. 1. Cálculo de la energía de reacción a partir de entalpías de enlace aplicando la ley de Hess. 8. 9. - Espontaneidad de las reacciones químicas. Entropía. 9. 1. Segundo principio de la Termodinámica. 9. 2. Tercer principio de la Termodinámica. 10. - Energía libre de Gibbs. 11. -Espontaneidad de las reacciones químicas. Influencia de la temperatura

4 Sistemas Parte pequeña del universo que se aísla para someter a estudio. n El resto se denomina ENTORNO. n Pueden ser: n – Abiertos (intercambia materia y energía). – Cerrados (no intercambia materia y sí energía). – Aislados (no intercambia ni materia ni energía). n En reacciones químicas. . . SISTEMAS = Sustancias químicas

5 Definición de Termoquímica. Es la parte de la Química que se encarga del estudio del intercambio energético de un sistema químico con el exterior. n Hay sistemas químicos que evolucionan de reactivos a productos desprendiendo energía. Son las reacciones exotérmicas. n Otros sistemas químicos evolucionan de reactivos a productos precisando energía. Son las reacciones endotérmicas. n

6 Variables de estado Magnitudes que pueden variar a lo largo de un proceso (por ejemplo, en el transcurso de una reacción química). n Ejemplos: n – Presión. – Temperatura. – Volumen. – Concentración.

7 Funciones de estado Tienen un valor único para cada estado del sistema. n Su variación solo depende del estado inicial y final y no del camino desarrollado. n SÍ son: Presión, temperatura, energía interna, entalpía. n NO son: calor, trabajo n

8 Primer principio de la Termodinámica n ENERGÍA INTERNA (U) es la energía total CALOR del sistema. Q>0 – Es imposible medir. – Su variación sí se mide. n TRABAJO W< 0 W>0 U=Q+W U es función de estado. Q<0 TRABAJO Q y W > 0 si se realizan a favor del sistema. n CALOR

9 Calor a volumen constante (Qv) Es el intercambio de energía en un recipiente cerrado que no cambia de volumen. n Si V= constante, es decir, V = 0 n W=0 Qv = U n

10 Calor a presión constante (Qp) La mayoría de los procesos químicos ocurren a presión constante, normalmente la atmosférica. n Si p = cte W = – p · V n U = Qp – p · V n U 2 – U 1 = Qp – p · (V 2 – V 1) n Qp + U 1 + p · V 1 = U 2 + p · V 2 n H 1 H 2 (entalpía)

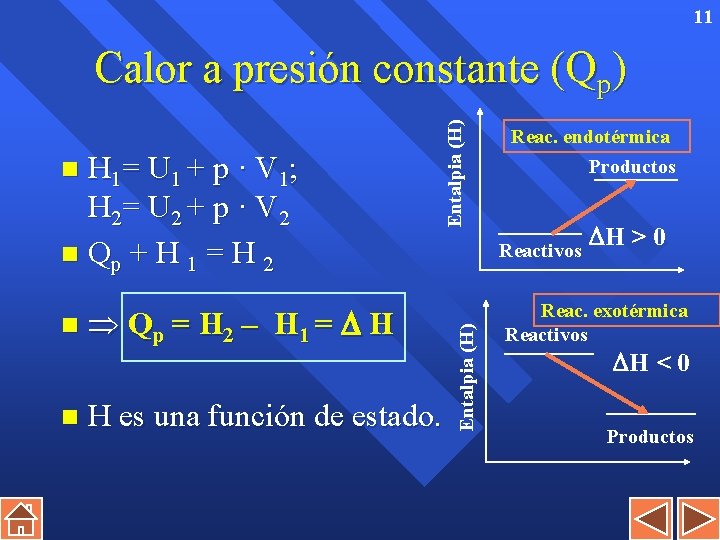
11 n n Qp = H 2 – H 1 = H H es una función de estado. Reac. endotérmica Productos Reactivos Entalpia (H) H 1= U 1 + p · V 1; H 2= U 2 + p · V 2 n Qp + H 1 = H 2 n Entalpia (H) Calor a presión constante (Qp) H > 0 Reac. exotérmica Reactivos H < 0 Productos

12 Relación Qv con Qp (gases). H= U+p· V Aplicando la ecuación de los gases: p·V=n·R·T n y si p y T son constantes la ecuación se cumplirá para los estados inicial y final: p· V= n·R·T n H= U+ n·R·T

Relación Qv con Qp (sólidos y líquidos) n En reacciones de sólidos y líquidos apenas se produce variación de volumen y. . . Qv Qp n es decir: U H 13

14 Ejercicio A: En termoquímica el valor de R suele tomarse en unidades del sistema internacional. Ya sabes que R = 0, 082 atm·l·mol-1·K-1. Determina el valor de R en el S. I con sus unidades. p=dgh 1 atm = 13546 kgxm-3 x 9, 8 mxs-2 x 0, 76 m = 10900 kgxm-1 xs-2

Ejemplo: Determinar la variación de energía interna para el proceso de combustión de 1 mol de propano a 25ºC y 1 atm, si la variación de entalpía, en estas condiciones, vale – 2219, 8 k. J. C 3 H 8 (g) + 5 O 2 (g) 3 CO 2 (g) + 4 H 2 O (l) H = – 2219, 8 k. J nreactivos = 1+5 = 6 ; nproductos = 3 n = – 3 Despejando en U = H – n · R · T = – 2219 k. J + 3 mol · (8, 3 J/mol. K) · 298 K = – 2214 k. J U = – 2212 k. J 15

16 Entalpía estándar de la reacción Es el incremento entálpico de una reacción en la cual, tanto reactivos como productos están en condiciones estándar (p = 1 atm; T = 298 K = 25 ºC; conc. = 1 M). n Se expresa como H 0 y como se mide en J o k. J depende de cómo se ajuste la reacción. n Así, H 0 de la reacción “ 2 H 2 + O 2 2 H 2 O” es el doble del de “H 2 + ½ O 2 H 2 O”. n H 0 = H 0 productos – H 0 reactivos

17 Ecuaciones termoquímicas Expresan tanto los reactivos como los productos indicando entre paréntesis su estado físico, y a continuación la variación energética expresada como H (habitualmente como H 0). n Ejemplos: n CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(l); H 0 = – 890 k. J H 2(g) + ½ O 2(g) H 2 O(g); H 0 = – 241’ 4 k. J

18 Ecuaciones termoquímicas n ¡CUIDADO!: H depende del número de moles que se forman o producen. Por tanto, si se ajusta poniendo coeficientes dobles, habrá que multiplicar H 0 por 2: n 2 H 2(g) + O 2(g) 2 H 2 O(g) ; H 0 = 2· (– 241’ 4 k. J) n Con frecuencia, suelen usarse coeficientes fraccionarios para ajustar las ecuaciones: n H 2(g) + ½ O 2(g) H 2 O(g) ; H 0 = – 241’ 4 k. J

Entalpía estándar de formación (calor de formación). 19 Es el incremento entálpico ( H) que se produce en la reacción de formación de un mol de un determinado compuesto a partir de los elementos en estado físico normal (en condiciones estándar). n Se expresa como Hf 0. Se trata de un “calor molar”, es decir, el cociente entre H 0 y el número de moles formados de producto. n Por tanto, se mide en k. J/mol. n Ejemplos: n C(s) + O 2(g) CO 2(g) Hf 0 = – 393’ 13 k. J/mol H 2(g) + ½ O 2(g) H 2 O(l) Hf 0 = – 285’ 8 k. J/mol

Cálculo de H 0 (calor de reacción) n Aplicando la ley de Hess podemos concluir que : H 0 = np Hf 0(productos)– nr Hf 0(reactivos) n 20 MU IM Y PO RT AN Recuerda que Hf 0 de todos los elementos en estado original es 0. TE

Ejemplo: Conocidas las entalpías estándar de formación 21 del butano (C 4 H 10), agua líquida y CO 2, cuyos valores son respectivamente – 124’ 7, – 285’ 8 y – 393’ 5 k. J/mol, calcular la entalpía estándar de combustión del butano. n n La reacción de combustión del butano es: C 4 H 10(g) +13/2 O 2(g) 4 CO 2(g) + 5 H 2 O(l) H 0 comb= ? H 0 = np Hf 0(product. ) – nr Hf 0(reactivos) = 4 mol(– 393’ 5 k. J/mol) + 5 mol(– 285’ 8 k. J/mol) – 1 mol(– 124’ 7 k. J/mol) = – 2878’ 3 k. J Luego la entalpía estándar de combustión será: H 0 combustión = – 2878’ 3 k. J/mol

Ley de Hess H en una reacción química es constante con independencia de que la reacción se produzca en una o más etapas. n Recuerda que H es función de estado. n Por tanto, si una ecuación química se puede expresar como combinación lineal de otras, podremos igualmente calcular H de la reacción global combinando los H de cada una de las reacciones. n 22 MU IM Y PO RT AN TE

Ejemplo: Dadas las reacciones (1) H 2(g) + ½ O 2(g) H 2 O(g) H 10 = – 241’ 8 k. J (2) H 2(g) + ½ O 2(g) H 2 O(l) H 20 = – 285’ 8 k. J calcular la entalpía de vaporización del agua en condiciones estándar. La reacción de vaporización es. . . (3) H 2 O(l) H 2 O(g) H 03 = ? (3) puede expresarse como (1) – (2), luego H 03 = H 01 – H 02 = – 241’ 8 k. J – (– 285’ 8 k. J) = 44 k. J H 0 vaporización = 44 k. J /mol 23

24 Esquema de la ley de Hess H H 2(g) + ½ O 2(g) H 10 = – 241’ 8 k. J H 20 = – 285’ 8 k. J H 2 O(g) H 30 = 44 k. J H 2 O(l)

Ejercicio B: Conocidas las entalpías estándar de formación 25 del butano (C 4 H 10), agua líquida y CO 2, cuyos valores son respectivamente – 124’ 7, – 285’ 8 y – 393’ 5 k. J/mol, calcular la entalpía estándar de combustión del butano. n Si utilizamos la ley de Hess, la reacción: n (4) C 4 H 10(g) +13/2 O 2(g) 4 CO 2(g) + 5 H 2 O(l) H 0 comb=? n Puede obtenerse a partir de: n (1) (2) (3) n n n H 2(g) + ½ O 2(g) H 2 O(l) C(s) + O 2(g) CO 2(g) 4 C(s) + 5 H 2(g) C 4 H 10(g) H 10 = – 285’ 8 k. J H 20 = – 393’ 5 k. J H 30 = – 124’ 7 k. J (4) = 4 · (2) + 5 · (1) – (3) 4 C(s) + 4 O 2(g) +5 H 2(g) + 5/2 O 2(g) + C 4 H 10(g) 4 CO 2(g) + 5 H 2 O(l) + 4 C(s) + 5 H 2(g) H 04 = 4 mol(– 393’ 5 k. J/mol) + 5 mol(– 285’ 8 k. J/mol) – 1 mol(– 124’ 7 k. J/mol) = – 2878’ 3 k. J

Ejercicio C: Determinar Hf 0 del eteno (C 2 H 4) a partir de los calores de reacción de las siguientes reacciones químicas: (1) H 2(g) + ½ O 2(g) H 2 O(l) H 10 = – 285’ 8 k. J (2) C(s) + O 2(g) CO 2(g) H 20 = – 393’ 13 k. J (3) C 2 H 4(g) + 3 O 2(g) 2 CO 2(g) + 2 H 2 O(l) H 30 = – 1422 k. J 26 La reacción de formación del eteno C 2 H 4(g) a partir de sus constituyentes en estado normal es: n (4) 2 C(s) + 2 H 2(g) C 2 H 4(g) n (4) se puede expresar como 2·(2) + 2·(1) – (3) n

Ejercicio C: Determinar Hf 0 del eteno (C 2 H 4) a partir de los calores de reacción de las siguientes reacciones químicas: 27 (1) H 2(g) + ½ O 2(g) H 2 O(l) H 10 = – 285’ 8 k. J (2) C(s) + O 2(g) CO 2(g) H 20 = – 393’ 13 k. J (3) C 2 H 4(g) + 3 O 2(g) 2 CO 2(g) + 2 H 2 O(l) H 30 = – 1422 k. J (4) 2 C(s) + 2 H 2(g) C 2 H 4(g) (4) = 2·(2) + 2·(1) – (3) luego H 40 = 2· H 20 + 2· H 10 – H 30 = = 2 · (– 393’ 13 k. J) + 2 · (– 285’ 8 k. J) – (– 1422 k. J) = = 64’ 14 k. J es decir Hf 0 (eteno) = 64’ 14 k. J/mol Se trata, pues, de una reacción endotérmica.

Ejercicio D: Las entalpías de combustión de la glucosa (C 6 H 12 O 6) y del etanol (C 2 H 5 OH) son – 2815 k. J/mol y – 1372 k. J/mol, respectivamente. Con estos datos determina la energía intercambiada en la fermenta– ción de un mol de glucosa, reacción en la que se produce etanol y CO 2. ¿Es exotérmica la reacción? n 28 Las reacciones de combustión son, respectivamente: (1) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O ; H 1 = – 2815 k. J (2) C 2 H 5 OH + 3 O 2 2 CO 2 + 3 H 2 O ; H 2 = – 1372 k. J n n n La reacción de fermentación de la glucosa es: (3) C 6 H 12 O 6 2 C 2 H 5 OH +2 CO 2 H 3 = ? (3) puede expresarse como (1) – 2· (2), luego H 3 = H 1 – 2· H 2 = – 2815 k. J – 2· (– 1372 k. J) = y la reacción es exotérmica. – 71 k. J

Energía de enlace. “Es la energía necesaria para romper un enlace de un mol de sustancia en estado gaseoso” n En el caso de moléculas diatómicas es igual que la energía de disociación: n A—B(g) A(g) + B(g) Hdis = Eenlace= Ee n Ejemplo: H 2(g) 2 H(g) H = 436 k. J n Es positiva (es necesario aportar energía al sistema) n Es difícil de medir. n Se suele calcular aplicando la ley de Hess. n 29

Ejemplo: Calcular la energía del enlace H—Cl n n n n 30 en el cloruro de hidrógeno conociendo Hf 0(HCl) cuyo valor es – 92, 3 k. J/mol y las entalpías de disociación del H 2 y del Cl 2 que son 436, 0 k. J/mol y 243, 4 k. J/mol, respectivamente. La reacción de disociación del HCl será: (4) HCl(g) H(g) + Cl(g) H 04= ? (1) ½H 2(g) + ½Cl 2(g) HCl(g) H 01 = – 92, 3 k. J (2) H 2(g) 2 H(g) H 02 = 436, 0 k. J (3) Cl 2(g) 2 Cl(g) H 03 = 243, 4 k. J (4) = –(1) + ½(2) + ½(3) H 04 = –(– 92, 3 k. J ) + ½(436, 0 k. J) + ½(243, 4 k. J) = = 432, 0 k. J Ee(HCl) = 432, 0 k. J/mol

Cálculo de H 0 a partir de las Energía de enlace IMMPUY OR TA (disociación). NT E 31 n Aplicando la ley de Hess en cualquier caso se obtiene la siguiente fórmula: H 0 = ni · Ee(enl. rotos) – nj · Ee(enl. formados) en donde ni representa el número de enlaces rotos y formados de cada tipo.

Ejemplo: Sabiendo que las energía de los siguientes 32 enlaces (k. J/mol): C=C : 611; C–C : 347; C–H : 413 y H–H : 436, calcular el valor de H 0 de la reacción de hidrogenación del eteno. n n n Reacción: CH 2=CH 2(g) + H 2(g) CH 3–CH 3(g) En el proceso se rompe un enlace C=C y otro H–H y se forman 2 enlaces C–H nuevos (el etano tiene 6 mientras que el eteno tenía sólo 4) y un enlace C–C. H 0 = Ee(enl. rotos) – Ee(enl. formados) = H 0 = 1 Ee(C=C) + 1 Ee(H–H) – 1 Ee(C–C) – 2 Ee(C–H) H 0 = 1 mol · 611 k. J/mol + 1 mol · 436 k. J/mol – (1 mol · 347 k. J/mol + 2 mol · 413 k. J/mol) = – 126 k. J

Ejercicio E: Calcula el calor de combustión de propano a partir de los datos de energía de enlace de la tabla. n C 3 H 8 + 5 O 2 3 CO 2 + 4 H 2 O n Enlaces rotos: 8 C–H, 2 C–C y 5 O=O n Enlaces formados: n 6 C=O y 8 O–H n H 0 = Ee(e. rotos) – Ee(e. form. ) n H 0 = 8 Ee(C–H) + 2 Ee(C–C) + 5 Ee(O=O) – [6 Ee(C=O) + 8 Ee(O–H)] n H 0 = 8· 413 k. J + 2· 347 k. J +5· 499 k. J – (6· 745 k. J + 8· 460 k. J) = – 1657 k. J H 0 comb(C 3 H 8) = – 1657 k. J/mol Enlace 33 Ee (k. J/mol) H–H 436 C–C 347 C=C 620 C C 812 O=O 499 Cl–C 243 C–H 413 C–O 315 C=O 745 O–H 460 Cl–H 432

Entropía (S) Es una medida del desorden del sistema que sí puede medirse y tabularse. S = Sfinal – Sinicial n Existen tablas de S 0 (entropía molar estándar) de diferentes sustancias. n En una reacción química: n S 0 = np· S 0 productos – nr· S 0 reactivos n La entropía es una función de estado. 34

Ejemplo: Calcula S 0 para las siguientes reacciones químicas: a) N 2(g) + O 2(g) 2 NO(g); b) 3 H 2(g) + N 2(g) 2 NH 3(g). Datos: S 0 (J·mol– 1·K– 1): H 2(g) = 130, 6; O 2(g) =205; N 2(g) = 191, 5; NO(g) = 210, 7; NH 3(g) =192, 3 35 S 0 = np· S 0 productos – nr· S 0 reactivos a) S 0 = 2 mol · 210, 7 J ·mol– 1 ·K– 1 – (191, 5 J·K– 1 + 205 J·K– 1 ) = 24, 9 J·K– 1 b) S 0 = 2· 192, 3 J·K– 1 – (3 mol · 130, 6 J· mol– 1·K– 1 + 191, 5 J·K– 1 ) = – 198, 7 J·K– 1

Segundo principio de la Termodinámica. n n n “En cualquier proceso espontáneo la entropía total del universo tiende a aumentar siempre”. Suniverso = Ssistema + Sentorno 0 A veces el sistema pierde entropía (se ordena) espontáneamente. En dichos casos el entorno se desordena. 36

Tercer principio de la Termodinámica “La entropía de cualquier sustancia a 0 K es igual a 0” (máximo orden). n Equivale a decir que no se puede bajar de dicha temperatura. n ¡CUIDADO! Las S de los elementos en condiciones estándar no son 0 sino que es positiva. n 37

En procesos reversibles y a temperatura constante se puede calcular S de un sistema como: Q S = — T n y si el proceso químico se produce a presión constante: n Hsistema – Hsistema Ssistema = ——— ; Sentorno= ———— T T n S 0 (entropía molar estándar) se mide en n J·mol– 1·K– 1. n Sreacción se mide en J·K– 1. 38

Energía libre de Gibbs (G) (energía libre o entalpía libre). 39 En procesos a T constante se define como: G=H–T·S G = H – T · S n En condiciones estándar: G 0 = H 0 – T· S 0 n Suniverso = Ssistema + Sentorno > 0 (p. espontáneos) Multiplicando por “–T” y como “–T Sentorno = Hsist n –T · Suniverso = – T · Ssist + Hsist = G < 0 n En procesos espontáneos: G < 0 n Si G. > 0 la reacción no es espontánea n Si G. = 0 el sistema está en equilibrio n

Incremento de energía libre de una reacción ( G) G es una función de estado. n Al igual que el incremento entálpico el incremento de energía libre de una reacción puede obtenerse a partir de Gf 0 de reactivos y productos: n G 0 = np Gf 0(productos)– nr Gf 0(reactivos) 40

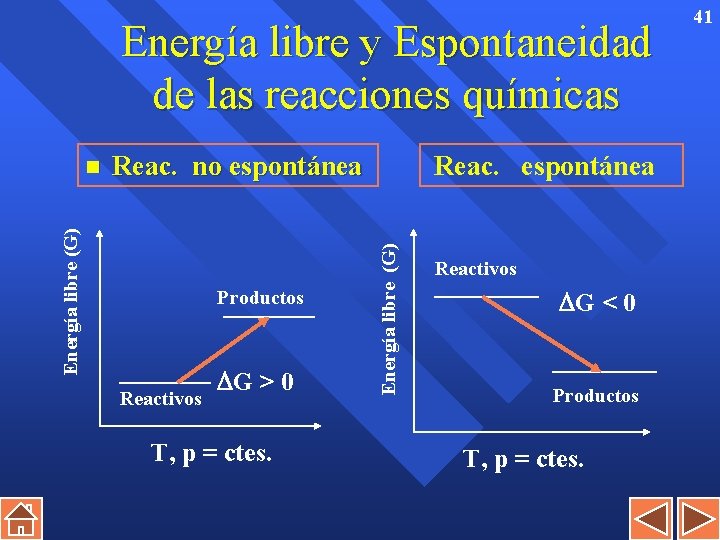
Energía libre y Espontaneidad de las reacciones químicas Reac. no espontánea Productos Reactivos G > 0 T, p = ctes. Reac. espontánea Energía libre (G) n Reactivos G < 0 Productos T, p = ctes. 41

Espontaneidad en las reacciones químicas. No siempre las reacciones exotérmicas son espontáneas. n Hay reacciones endotérmicas espontáneas: n n – Evaporación de líquidos. – Disolución de sales. . . Ejemplos de reacciones endotérmicas espontáneas: NH 4 Cl(s) NH 4+(aq) + Cl– (aq) H 0 = 14’ 7 k. J H 2 O(l) H 2 O(g) H 0 = 44’ 0 k. J 42

Espontaneidad de las reacciones químicas (cont). 43 Una reacción es espontánea cuando G ( H – T x S) es negativo. n Según sean positivos o negativos los valores de H y S (T siempre es positiva) se cumplirá que: n H < 0 y S > 0 G < 0 Espontánea n H > 0 y S < 0 G > 0 No espontánea n H < 0 y S < 0 G < 0 a T bajas G > 0 a T altas n H > 0 y S > 0 G < 0 a T altas G > 0 a T bajas n

44 MU IM Y PO RT AN Espontaneidad de las reacciones químicas (cont). H < 0 S > 0 S Espontánea a todas las temperaturas TE H > 0 S > 0 Espontánea a temperaturas altas H H < 0 S < 0 H > 0 S < 0 Espontánea a temperaturas bajas No Espontánea a cualquier temperaturas

Ejemplo: ¿Será o no espontánea la siguiente reacción 45 2 H 2 O 2(l) 2 H 2 O (l) + O 2(g) en condiciones estándar? Datos: H 0 f (k. J/mol) H 2 O(l) = – 285, 8; H 2 O 2(l) = – 187, 8 ; S 0 (J·mol 1 K· 1) H 2 O(l) = 69, 9; H 2 O 2(l) = 109, 6; O 2(g) =205, 0. H 0 = np Hf 0(productos)– nr Hf 0(reactivos) = = 2 Hf 0(H 2 O) + Hf 0(O 2) – 2 Hf 0(H 2 O 2) = 2 mol(– 285, 8 k. J/mol) – 2 mol(– 187, 8 k. J/mol) = – 196, 0 k. J S 0 = np· S 0 productos – nr· S 0 reactivos = 2 S 0(H 2 O) + S 0(O 2) – 2 S 0(H 2 O 2) = 2 mol(69, 9 J/mol·K) + 1 mol(205, J/mol·K) – 2 mol(109, 6 J/mol·K) = 126, 0 J / K = 0, 126 k. J / K G 0 = H 0 – T · S 0 = – 196, 0 k. J – 298 K · 0, 126 k. J/ K = G 0 = – 233, 5 k. J luego será espontánea