TERMOQUMICA A QUMICA DOS EFEITOS ENERGTICOS Valria Boechat

TERMOQUÍMICA A QUÍMICA DOS EFEITOS ENERGÉTICOS. Valéria Boechat

OS PRINCÍPIOS FUNDAMENTAIS DO CALOR E DO TRABALHO SE APLICAM, NO ESTUDO DE UMA REAÇÃO QUÍMICA E NAS MUDANÇAS DO ESTADO FÍSICO DE UMA SUBST NCIA.

OBSERVE OS FENÔMENOS

NELES, OCORREM TRANSFORMAÇÕES FÍSICAS E/OU QUÍMICAS ENVOLVENDO VÁRIOS TIPOS DE ENERGIA, INCLUSIVE ENERGIA TÉRMICA.

CONCEITOS IMPORTANTES Energia s. f. 1. Capacidade dos corpos para produzir um trabalho ou desenvolver uma força. 2. Modo como se exerce uma força. Conceito mais atual Energia é uma propriedade dos sistemas físicos que faz com que eles sofram (ou não) alterações com o tempo.

Qual ciência descreve os fenômenos que envolvem as alterações devidas a energia ? Termodinâmica !!!! Lei Zero da Termodinâmica Não se pode criar ou destruir energia Podemos interconvertê-la em várias formas Química Potencial Som Térmica Cinética Luz (radiação) Nuclear etc

Primeira Lei da Termodinâmica • Com uma unidade de energia é impossível obter duas unidades de energia Segunda Lei da Termodinâmica • Não se pode nem empatar • Com uma unidade de energia só é possível obter menos que uma unidade de energia

As inexoráveis Leis da Termodinâmica • A Benção da Primeira Lei Conservação de energia • A Maldição da Segunda Lei Degradação da energia. Energia nunca pode ser aproveitada a 100%

Energia Interna • A energia interna (U) é a energia total do sistema num dado estado (quando a temperatura, a pressão e a composição química permanecem constantes); • A variação de energia é a diferença entre o calor (Q) libertado para o meio ambiente e o trabalho (W) realizado pelo sistema; • À energia armazenada nas substâncias (reagentes e produtos) damos o nome de entalpia (H).

ENERGIA INTERNA ENERGIA ACUMULADA POR UMA SUBST NCIA SOB VOLUME CONSTANTE. ENTALPIA ENERGIA ACUMULADA POR UMA SUBST NCIA SOB PRESSÃO CONSTANTE, RESUMIDAMENTE, PODEMOS DIZER QUE É O CONTÉUDO DE ENERGIA DA SUBST NCIA.

Entalpia • Numa reação, a diferença entre as entalpias dos produtos e a dos reagentes é definida como variação de entalpia (ΔH); • Quando uma transformação se realiza a pressão constante, o calor libertado numa reação exotérmica ou o calor absorvido numa reação endotérmica é igual à variação de entalpia.
Fontes de energia Capacidade de realizar trabalho Elementos determinantes para produzir e/ou multiplicar trabalho Os músculos O Sol As águas correntes O vento A energia é um elemento básico para a sociedade moderna, pois é por seu intermédio que as máquinas e os motores funcionam ou que as luzes Os combustíveis Os minerais
Tipos de energia Renováveis Aquelas que, uma vez utilizados pelo homem, são susceptíveis de regeneração espontânea ou através de práticas conservacionista • Solos • Ar • Vegetação • Águas Correntes Não - renováveis Aqueles que, uma vez utilizados pelo homem NÃO são susceptíveis de regeneração espontânea ou mesmo pela intervenção adequada do homem Os Recurso naturais, ou seja, fontes de energia só adquirem valor em função de uma sociedade, de uma época e de técnicas de utilização. Ferro Manganês Combustíveis fósseis Petróleo Carvão Gás natural

O PROCESSO DE MEDIDA DOS CALORES DE REAÇÃO É DENOMINADO CALORIMETRIA. O APARELHO QUE MEDE A ENTALPIA DA REAÇÃO É DENOMINADO CALORÍMETRO.

CALORIA é a quantidade de energia necessária para aumentar de 1ºC a temperatura de 1 g de água. JOULE é a quantidade de energia necessária para deslocar uma massa de 1 kg, inicialmente em repouso, fazendo percurso de 1 metro em 1 segundo. 1 cal = 4, 18 J 1 kcal = 1000 cal 1 k. J = 1000 J

A temperatura pode alterar devido a um fluxo de CALOR (quando existe diferença de temperatura no sistema). Quando não há fluxo de calor pode ocorrer trabalho elétrico ou mecânico ou absorção de radiação, por exemplo.

RESPONDA !

Responda: 1 - Quando você esfrega suas mãos e elas ficam quentes: a) Fala-se de fluxo de calor ou aumento da temperatura? Temperatura

2 - Um ebulidor elétrico esquenta uma certa quantidade da água, numa panela. a) Houve alteração na temperatura? a) Sim b) Ocorreu fluxo de calor? b) Sim

3 - Você colocou duas panelas no fogão. Uma contendo 1, 0 L de água e outra 0, 5 L. a) Utilizando a mesma fonte de calor, qual ferve mais rápido? 0, 5 L b) Qual ferve a temperatura mais Igual elevada?

c) Qual necessita de maior quantidade de calor para ferver? c) 1, 0 L d) Se você deixar que elas esfriem, qual levará mais tempo para esfriar? d) 1, 0 L
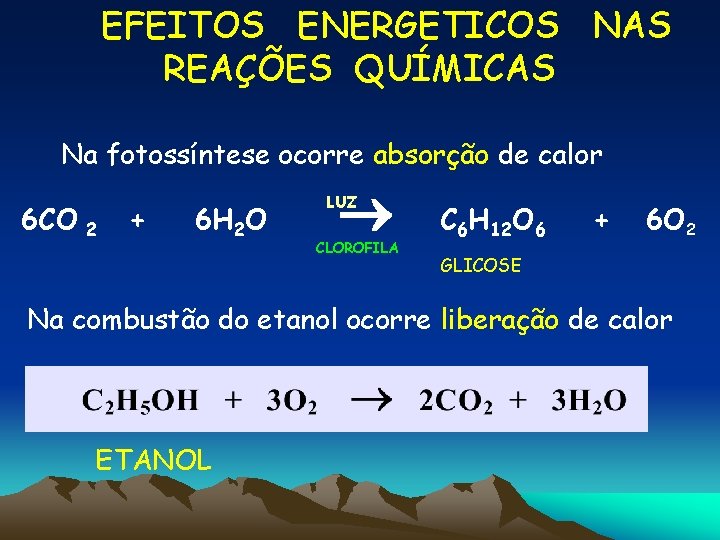
EFEITOS ENERGETICOS NAS REAÇÕES QUÍMICAS Na fotossíntese ocorre absorção de calor 6 CO 2 + 6 H 2 O LUZ CLOROFILA C 6 H 12 O 6 + 6 O 2 GLICOSE Na combustão do etanol ocorre liberação de calor ETANOL

A TERMOQUÍMICA ESTUDA AS MUDANÇAS TÉRMICAS ENVOLVIDAS NAS REAÇÕES QUÍMICAS E PROCESSOS FÍSICOS * quando envolve liberação de calor, denomina-se PROCESSO EXOTÉRMICO. * quando envolve absorção de calor, denomina-se PROCESSO ENDOTÉRMICO.

EQUAÇÃO TERMOQUÍMICA É a representação de uma reação química em que está especificado: * o estado físico de todas as substâncias. * o balanceamento da equação. * a variação de calor da reação ( H ). * variedade alotrópica quando existir. * as condições físicas em que ocorre a reação, ou seja, temperatura e pressão. ( 25ºC e 1 atm é o comum)

OBS. : * Convencionou-se entalpia zero para determinadas substâncias simples, em razão de não ser possível medir o valor real da entalpia de uma substância. * Foram escolhidas condições-padrão para estabelecer medidas relativas. * Terá entalpia zero qualquer substância simples que se apresente nos estados físico e alotrópico mais comum, a 25ºC e 1 atm de pressão.
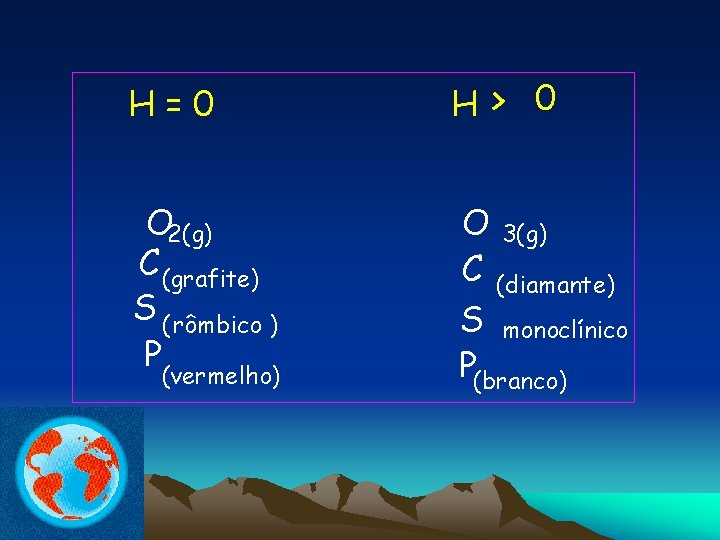
H=0 H> 0 O 2(g) C (grafite) S ( rômbico ) P O 3(g) C (diamante) S monoclínico P(branco) (vermelho)

I. Processos endotérmicos Ex. Quebra de ligações. • Fusão do gelo. • Fotossíntese. • Eletrólise • Cozimento de alimentos • Energia de ionização • Evaporação do álcool. • Dissolução do sal de cozinha em água. • Sublimação da naftalina.

EFEITOS ENERGÉTICOS NOS PROCESSOS FÍSICOS E QUÍMICOS Ex 1. Gelo derretendo : 25ºC gelo H 2 O 10ºC H 2 O

GELO DERRETENDO --- FUSÃO H 2 O (s) H 2 O(l) Processo físico Meio externo esfria Processo endotérmico Variação de entalpia H > O
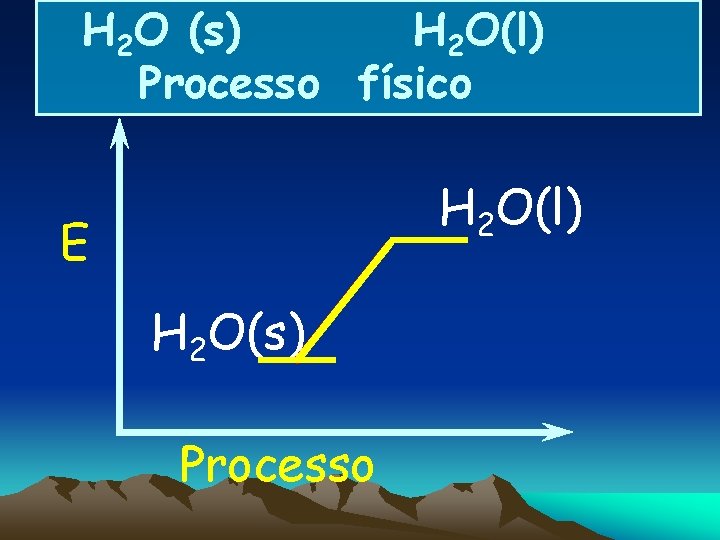
H 2 O (s) H 2 O(l) Processo físico H 2 O(l) E H 2 O(s) Processo
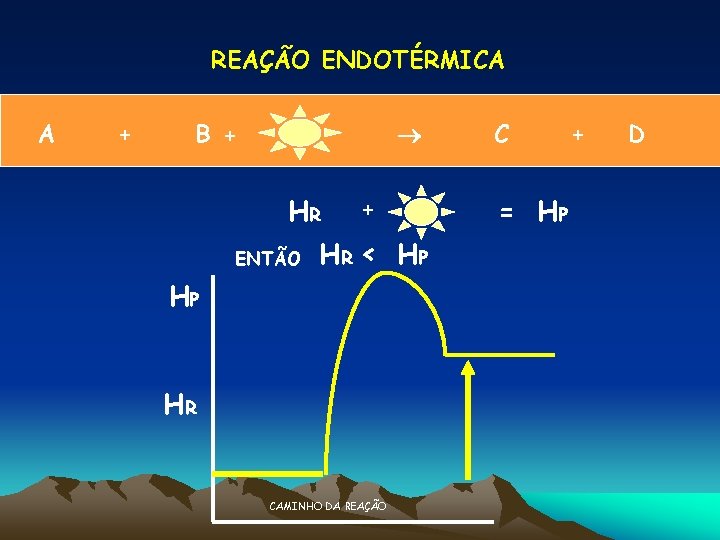
REAÇÃO ENDOTÉRMICA + B + HR ENTÃO HP HR HR CAMINHO DA REAÇÃO C = HP + > A HP + D
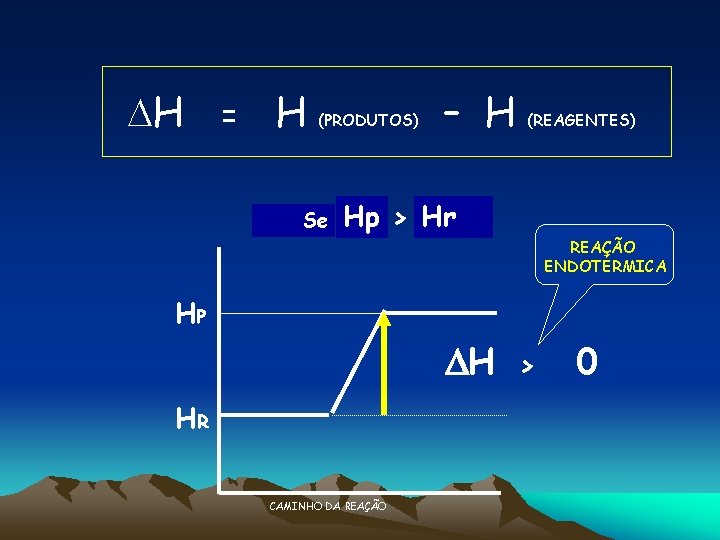
H = H (PRODUTOS) Se – H (REAGENTES) Hp > Hr REAÇÃO ENDOTÉRMICA HP H HR CAMINHO DA REAÇÃO > 0

Processos exotérmicos : Ex : Formação de ligações • Queimas (exceto a do N 2(g)) • Condensação do vapor de água • Solidificação. • Ionização de ácidos em água. • Digestão • Neutralização de uma sç de ácido forte por uma sç de base forte. • Respiração celular. • Reações que ocorrem em uma pilha

Ex 2: Dissolução da soda cáustica em água. 25ºC 30ºC Na. OH H 2 O
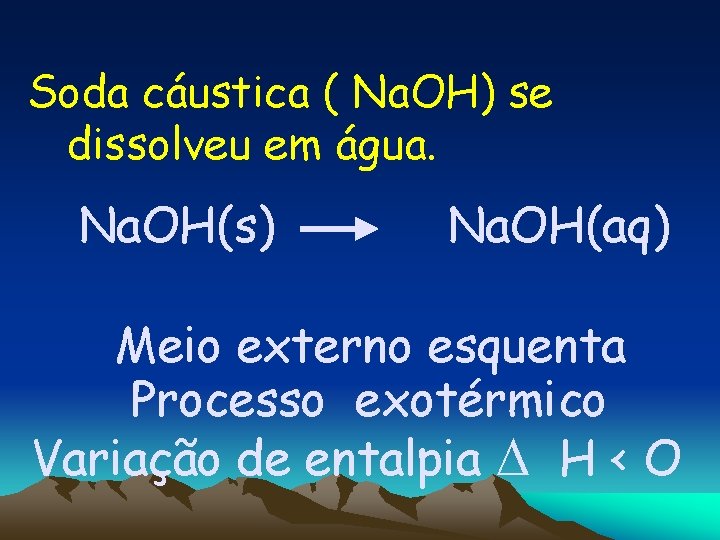
Soda cáustica ( Na. OH) se dissolveu em água. Na. OH(s) Na. OH(aq) Meio externo esquenta Processo exotérmico Variação de entalpia H < O
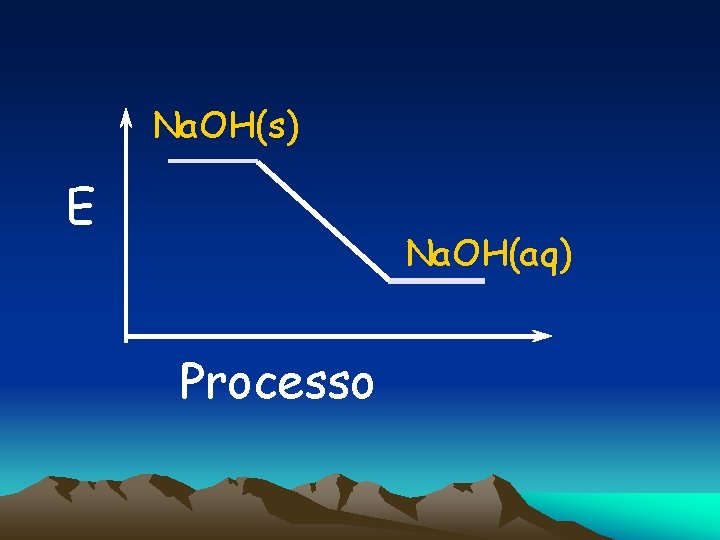
Na. OH(s) E Na. OH(aq) Processo
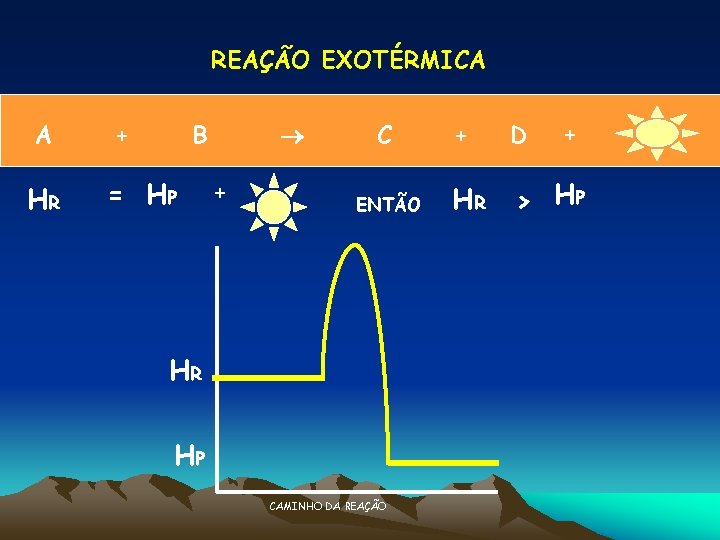
REAÇÃO EXOTÉRMICA A HR + B = HP + C ENTÃO HR HP CAMINHO DA REAÇÃO + + D HR > HP
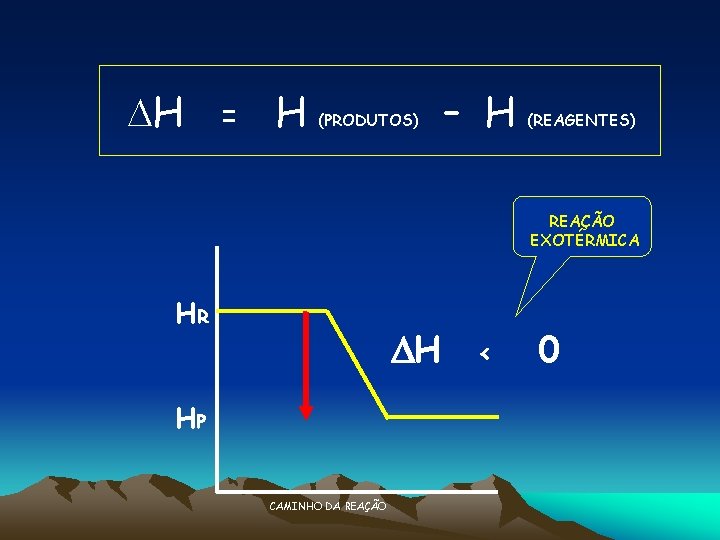
H = H (PRODUTOS) – H (REAGENTES) REAÇÃO EXOTÉRMICA HR H HP CAMINHO DA REAÇÃO < 0
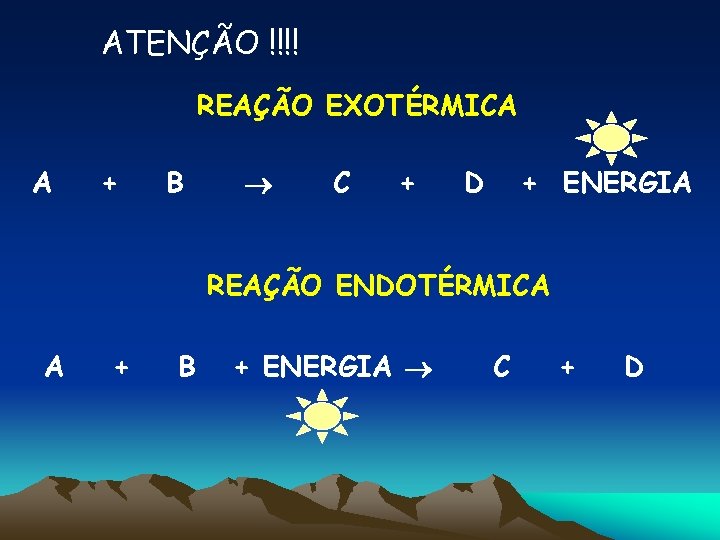
ATENÇÃO !!!! REAÇÃO EXOTÉRMICA A + B C + D + ENERGIA REAÇÃO ENDOTÉRMICA A + B + ENERGIA C + D

REAÇÃO EXOTÉRMICA OBSERVE OS SINAIS 2 C + 3 H C H (s) 2(g) 2 H = – 20, 2 kcal 6(g) 2 C(s) + 3 H C 2 H 6(g) + 20, 2 kcal 2(g) REAÇÃO ENDOTÉRMICA Fe 3 O 4(s) 3 Fe(s) + 2 O 2(g) +2 O 2(g) OBSERVE OS SINAIS H = + 267, 0 kcal - 267, 0 kcal

CÁLCULO DA VARIAÇÃO DE ENTALPIA A + B C + HR HP HR H ENTALPIA PRODUTO ENTALPIA REAGENTE D HP VARIAÇÃO DE ENTALPIA HP HR

Ex. A queima de carbono é um processo químico que libera uma quantidade de calor correspondente a 394 KJ Equação química correspondente: C(s) + O 2(g) CO 2 (g) + 394 KJ ou C(s) + O 2(g) CO 2 (g) H -394 KJ

C(s) + O 2(g) CO 2 (g) + 394 KJ A. O processo é exo ou endo? Exotérmico , libera calor B. Qual o valor de H H? = - 394 KJ C. O meio externo esquenta ou esfria? Esquenta
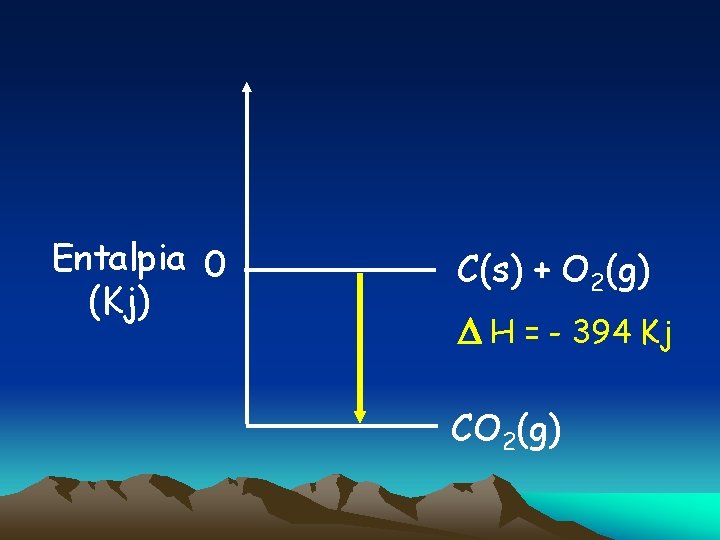
Entalpia 0 (Kj) C(s) + O 2(g) H = - 394 Kj CO 2(g)

CÁLCULOS DA VARIAÇÃO DE ENTALPIA LEI DE HESS A entalpia de uma reação depende apenas dos estados iniciais e finais da reação, não depende dos estados intermediários, ou seja a reação é a mesma para uma ou mais etapas. Ex. 1 - Cálculo da entalpia da reação de formação do gás carbônico: C(grafite)+ kcal/mol O 2(g) CO 2(g) H = ?

OBSERVE AS EQUAÇÕES: C(grafite)+ 1/2 O 2(g) CO(g) CO 2(g) H = – 26, 4 kcal/mol H = – 67, 6 kcal/mol

EFETUAMOS A SOMA ALGÉBRICA DAS MESMAS. Note que os termos semelhantes em membros opostos se anulam. 1ª etapa: C(grafite)+ 1/2 O 2(g) CO(g) H 1 = – 26, 4 kcal/mol 2ª etapa: CO(g) + 1/2 O 2(g) CO 2(g) Etapa final: H 2 = – 67, 6 kcal/mol C(grafite)+ O 2(g) CO 2(g) CONCLUINDO H = H 1 + H 2 H = – 94, 0 kcal/mol

PRINCÍPIO OU LEI DE HESS A quantidade de calor absorvida ou desprendida numa transformação qualquer depende apenas dos estados inicial e final.

EX 1 Escrever as equações correspondentes: Queima do carvão libera 94 K cal/mol C(s) +O 2(g) CO 2(g) H = -94 Kcal Queima do monóxido libera 68 Kcal/mol CO(g) + ½ O 2 CO 2(g) H = -68 Kcal Qual o H para a formação do CO(g)? C(s) + ½ O 2 CO(g) H = ?

RESOLUÇÃO Manipula-se as equações químicas como se fossem equações algébricas: C(s) + O 2(g) CO(g) + ½ O 2 C(s) + ½O 2(g) CO(g) H =- 94 Kcal H= + 68 Kcal H = -26 Kcal

Ex 2 Observe a equação correspondente o oxidação completa da glicose: C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + 2870 Kcal a) Qual o valor de H para a oxidação de 10 mols de Glicose? -28. 700 Kcal b)Qual o valor de H para oxidar 1, 8 g de Glicose? -28, 7 Kcal c) Qual o valor de H para formar 180 g de Glicose através do fenômeno da fotossíntese? H = +2870 Kcal

Exemplo 3 Observe o seguinte diagrama: 674 2 C(g) + 6 H(g) 312( quebra de 3 mols lig H-H ) Entalpia (Kcal) 0 2 C(g) + 3 H 2(g) 342 ( sublimação 2 mols C (grafita ) 2 C(grafita)+3 H 2(g) C 2 H 6(g) Formação de 1 mol de etano

EX 4 Qual o calor de sublimação de 12 g de carbono grafita? 2 C(g) + 6 H(g) 312 Entalpia (Kcal) 0 2 C(g) + 3 H 2(g) 342 674 2 C(grafita) +3 H 2(g) C 2 H 6(g) 342 ÷ 2 = 171 Kcal
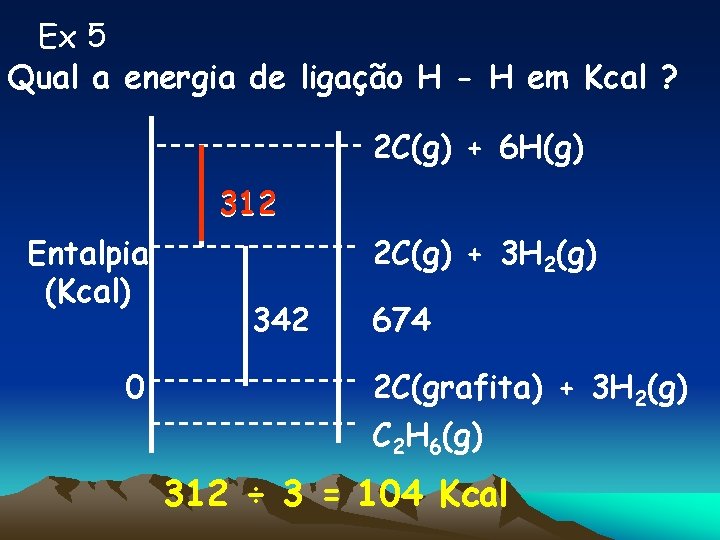
Ex 5 Qual a energia de ligação H - H em Kcal ? 2 C(g) + 6 H(g) 312 Entalpia (Kcal) 0 2 C(g) + 3 H 2(g) 342 674 2 C(grafita) + 3 H 2(g) C 2 H 6(g) 312 ÷ 3 = 104 Kcal

Exemplo 6 Qual a variação de entalpia para formação do etano em Kcal/mol? 2 C(g) + 6 H(g) 312 Entalpia (Kcal) 0 2 C(g) + 3 H 2(g) 342 674 2 C(grafita) + 3 H 2(g) C 2 H 6(g) = -20 Kcal 674 - (312 + 342)
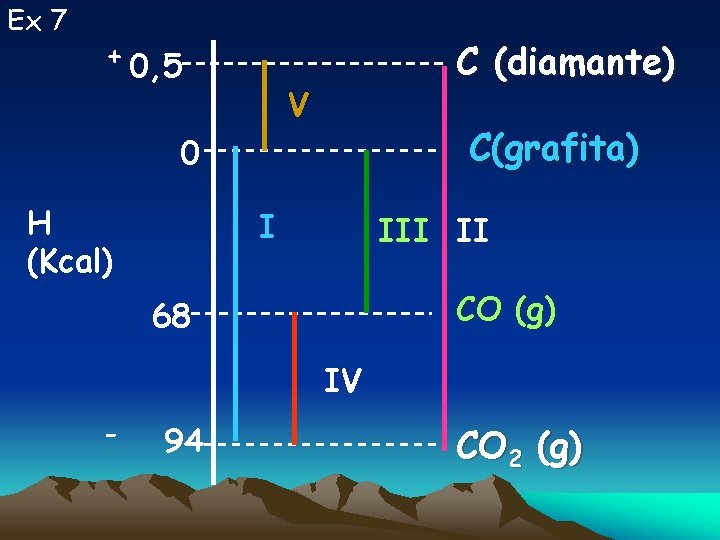
Ex 7 + 0, 5 C (diamante) V C(grafita) 0 H (Kcal) I II CO (g) 68 IV - 94 CO 2 (g)

NÃO SE ESQUEÇA !!!!!

Espontaneidade de um processo • Um processo tende a ser espontâneo quando leva a formação de um produto mais estável. • Numa reação espontânea , a troca de ligações TENDE ser um processo energeticamente favorável ( EXOTÉRMICO ) e que leve a um sistema de maior ENTROPIA ( desordem ) • Um sistema mais estável provavelmente terá : MENOR ENTALPIA E MAIOR ENTROPIA.

• Considere a equação de Gibbs ∆G=∆H-T∆S Onde: ∆ G = energia livre e o processo será espontâneo se ∆ G for menor que zero. T = temperatura ∆ S = variação de entropia. ∆ H = variação de entalpia

Além dos efeitos químicos não podemos nos esquecer dos efeitos que a combustão provoca no meio ambiente, contribuindo para a poluição ambiental, destruição da camada de ozônio e efeito estufa.
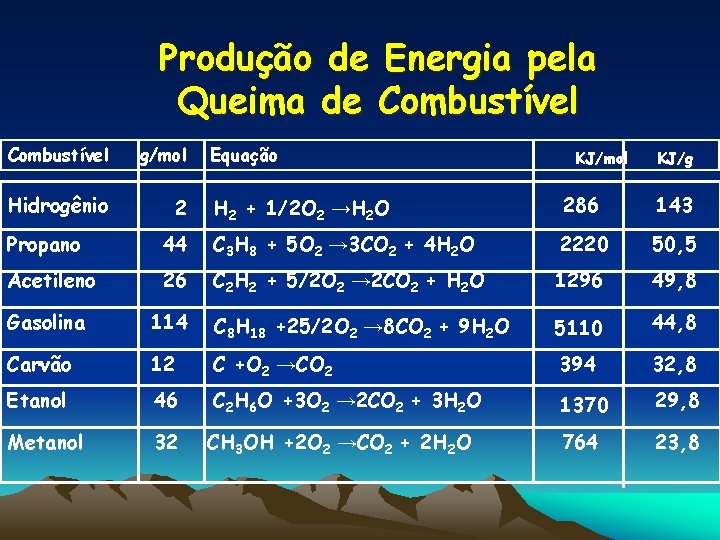
Produção de Energia pela Queima de Combustível g/mol Hidrogênio 2 Equação KJ/mol KJ/g H 2 + 1/2 O 2 →H 2 O 286 143 Propano 44 C 3 H 8 + 5 O 2 → 3 CO 2 + 4 H 2 O 2220 50, 5 Acetileno 26 C 2 H 2 + 5/2 O 2 → 2 CO 2 + H 2 O 1296 49, 8 Gasolina 114 C 8 H 18 +25/2 O 2 → 8 CO 2 + 9 H 2 O 5110 44, 8 Carvão 12 C +O 2 →CO 2 394 32, 8 Etanol 46 C 2 H 6 O +3 O 2 → 2 CO 2 + 3 H 2 O 1370 29, 8 Metanol 32 CH 3 OH +2 O 2 →CO 2 + 2 H 2 O 764 23, 8

1 - Levando-se em conta todos os aspectos, qual o melhor combustível da tabela apresentado? Hidrogênio 2 - Qual o calor liberado na queima de 224 litros de Propano a CNPT ? 22. 200 KJ 3 - Qual a energia liberada na queima de 5 moles de metanol ? 764 x 5 = 3820 KJ 4 - A queima de 6, 02 x 1025 átomos de carbono libera qual quantidade de calor? 100 mols x 394 = 39. 400 KJ

Ex 1. Dadas as equações: C(grafite )+ O 2(g) CO 2 H 2(g) H 1 = – 94, 0 kcal/mol + 1/2 O 2(g) H 2 O(l) H 2= – 68, 4 kcal/mol C(grafite)+ 2 H 2(g) CH 4(g) H 3= – 17, 9 kcal/mol Calcular a entalpia da reação da queima de um mol do metano:

Resolução: As equações dadas deverão ser arrumadas de tal modo que a sua soma resulte na equação-problema. Equação-problema: CH 4(g) + CO 2(g)+ H 2 O(l) CO 2(g) H 1 = – 94, 0 kcal/mol + 1/2 O 2(g) H 2 O(l) H 2 = – 68, 4 kcal/mol C(grafite )+ H 2(g) O 2(g) C(grafite)+ O 2(g) 2 H 2(g) CH 4(g) H 3 = – 17, 9 kcal/mol

Devemos manter a equação I pois dessa forma obteremos gás carbônico como produto. C(grafite )+ O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol Multiplicar por 2 a equação II para que os coeficientes fiquem ajustados. 2 (H + 1/2 O 2(g) H 2 O(l) 2(g) 2 H 2(g) + O 2(g) 2 H 2 O(l) ) H 2 = – 68, 4 kcal/mol H 2 = – 136, 8 kcal/mol O H 2 também é multiplicado Agora, invertemos a equação III de modo a obter o metano ( CH 4 ) como reagente. CH 4(g) C(grafite)+ 2 H 2(g) H 3 = + 17, 9 kcal/mol Observe a inversão de sinal do H 3

Finalmente aplica-se a soma algébrica das equações, inclusive das variações de entalpia. C(grafite )+ 2 H 2(g) O 2(g) CO 2(g) + O 2(g) 2 H 2 O(l) CH 4(g) C(grafite)+ 2 H 2(g) H 1 = – 94, 0 kcal/mol H 2 = – 136, 8 kcal/mol H 3 = + 17, 9 kcal/mol ___________________________

Observe os cortes: C(grafite )+ 2 H 2(g) CH 4(g) O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol + O 2(g) 2 H 2 O(l) H 2 = – 136, 8 kcal/mol C(grafite)+ 2 H 2(g) H 3 = + 17, 9 kcal/mol ____________________________ CH 4(g) + 2 O 2(g) CO 2(g)+ 2 H 2 O(l) H = – 212, 9 kcal/mol H = H 1 + H 2 + H 3

TIPOS DE H CALORES PADRÃO DE FORMAÇÃO OU ENTALPIA-PADRÃO DE FORMAÇÃO É o calor desenvolvido na formação de um mol de determinado composto, a partir das substâncias simples correspondentes no estado padrão. Representa-se por: O índice sobrescrito padrão. Hf º º significa estado O índice subscrito f significa formação. .
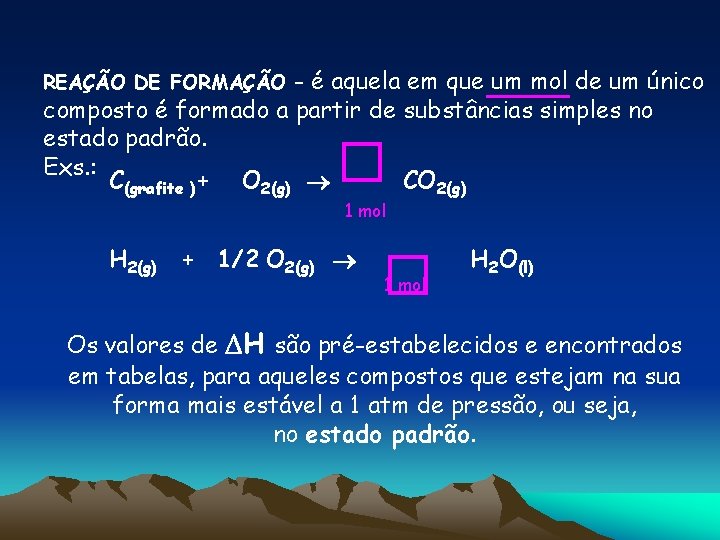
- é aquela em que um mol de um único composto é formado a partir de substâncias simples no estado padrão. Exs. : C(grafite )+ O 2(g) CO 2(g) � REAÇÃO DE FORMAÇÃO 1 mol + 1/2 O 2(g) � H 2(g) 1 mol H 2 O(l) Os valores de H são pré-estabelecidos e encontrados em tabelas, para aqueles compostos que estejam na sua forma mais estável a 1 atm de pressão, ou seja, no estado padrão.


CALOR PADRÃO DE COMBUSTÃO OU ENTALPIA-PADRÃO DE COMBUSTÃO É o calor liberado na combustão total de um mol de uma substância em que os componentes dessa reação estão no estado-padrão. H 2(g) + 1/2 O 2(g) H 2 O(l) H=– 68, 4 kcal/mol C 2 H 5 OH(l) + 3 O 2(g) 2 CO 2(g) + 3 H 2 O(l) H=– 325 kcal/mol COMBUSTÃO - reação de uma substância com o oxigênio (O 2) em que normalmente ocorre liberação de energia.

O PODER CALÓRICO DE ALGUMAS SUBST NCIAS A gasolina possui maior poder calorífico que o álcool. Para cada litro de gasolina queimado são produzidos aproximadamente 8000 quilocalorias, enquanto para cada litro de álcool queimado, temos a produção de aproximadamente 5000 quilocalorias. Veja a tabela de calorias de alguns alimentos, a seguir.
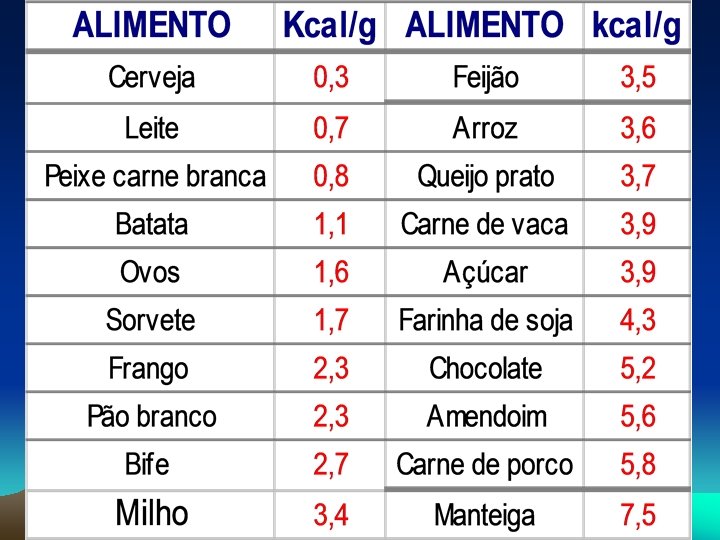

CALOR DE DISSOLUÇÃO OU ENTALPIA DE DISSOLUÇÃO É o calor desenvolvido ( liberado ou absorvido) provocado pela dissolução de um mol de substância, numa quantidade de água suficiente para se obter uma solução diluída, no estado padrão. H 2 SO 4(l) + aq H 2 SO 4(aq) H = KNO 3(s) + aq KNO 3(aq) – 22, 9 kcal/mol H = + 8, 5 kcal/mol

CALOR DE NEUTRALIZAÇÃO OU ENTALPIA DE NEUTRALIZAÇÃO É o calor liberado na neutralização de um equivalente-grama de um ácido por um equivalente-grama de uma base, ambos em soluções aquosas diluídas, no estado padrão. HCl(aq) + Na. OH(aq) Na. Cl(aq) + H 2 O(l) H = – 13, 8 kcal/eq-g HNO 3(aq) + Li. OH(aq) Li. NO 3(aq) + H 2 O(l) H = – 13, 8 kcal/eq-g OBS. : Para ácidos e bases fortes o H será sempre o mesmo.

Observe a equação: C 3 H 8(g) + 5 O 2(g) 3 CO 2(g) + 4 H 2 O(g) H = ? – kcal/mol Consultando a tabela de calores de formação: SUBST NCIAS C 3 H 8(g) CO 2(g) H 2 O (g) O 2(g) H -24, 8 kcal/mol -94, 1 kcal/mol -57, 8 kcal/mol zero

H = H(produtos) – H(reagentes) H = [3 HCO 2(g)+ 4 H H 2 O(g) ] - ( HC H 3 8(g) + 5 HO 2(g) ) H = [ 3(-94, 1) + 4(-57, 8)] - (-24, 8 + zero) H = - 488, 7 kcal/mol

ENERGIA DE LIGAÇÃO É A ENERGIA NECESSÁRIA PARA ROMPER UM MOL DE LIGAÇÕES NO ESTADO GASOSO. EX. Para romper um de ligação H – O são necessárias 110 kcal. Para romper um de ligação H – C são necessárias 100 kcal. Para romper um de ligação O = O são necessárias 118 kcal. .
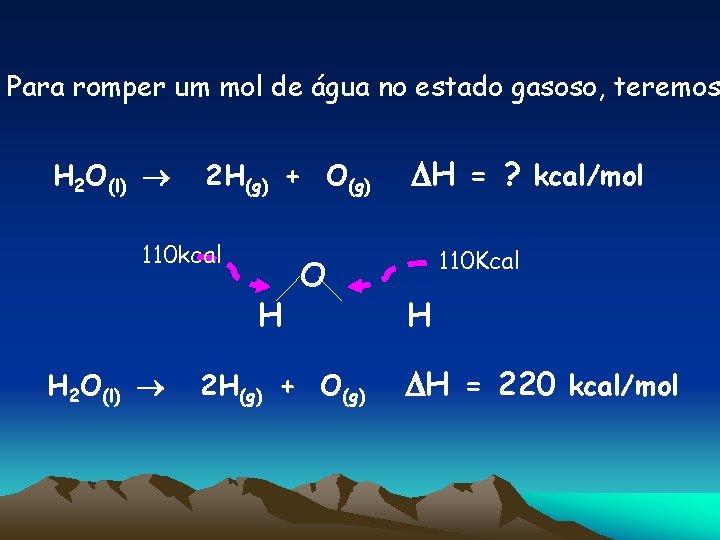
Para romper um mol de água no estado gasoso, teremos H 2 O(l) 2 H(g) + O(g) 110 kcal H H 2 O(l) O 2 H(g) + O(g) H = ? kcal/mol 110 Kcal H H = 220 kcal/mol

Observe a reação em que todos os participantes estão no estado gasoso: H | H— C— O — H | H + 3/2 O 2 O = C = O + 2 H 2 O Para romper as ligações intramoleculares do metanol e do oxigênio, serão absorvidos, para: 1 mol de O — H +464, 0 kj 1 mol de C — O +330, 0 kj 3 mols de C — H 3 (+413, 0 kj) 3/2 mols de O = O 3/2 (+493, 0 kj) TOTAL ABSORVIDO + 464, 0 kj + 330, 0 kj + 1239, 0 kj + 739, 5 kj + 2772, 5 kj

Cômputo dos produtos: H | H— C— O — H | H + 3/2 O 2 O = C = O + 2 H 2 O Para formar as ligações intramoleculares do CO 2 e da água, serão liberadas: 2 mols de C = O 2 (-7444, 0 kj) 2 mols de H — O 2 ( - 464, 0 kj) TOTAL LIBERADO -1 488, 0 kj - 928, 0 kj -2 416, 0 kj

O cálculo final será: H = H(reagentes) H = 2 772, 5 kj CALOR ABSORVIDO H = 356, 5 kj H(produtos) + + (- 2 416 kj) CALOR LIBERADO
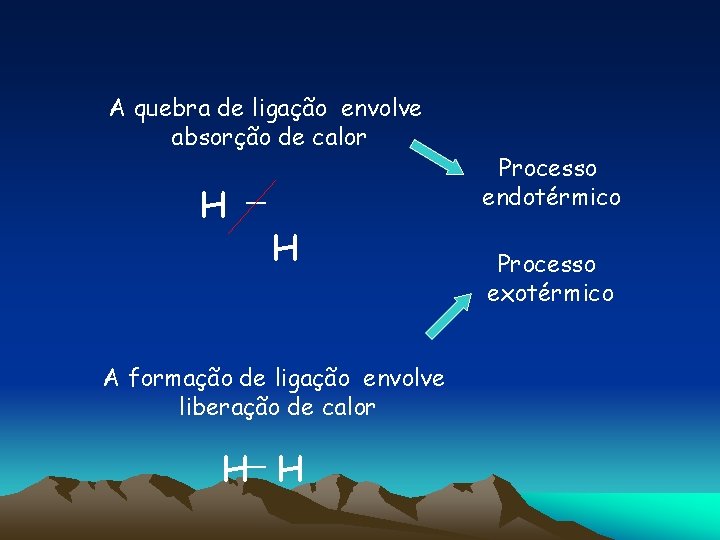
A quebra de ligação envolve absorção de calor H — H A formação de ligação envolve liberação de calor H— H Processo endotérmico Processo exotérmico

Lembre-se : Tipos de Calor de Reação Energia ou Calor de ligação: H 2(g) 2 H(g) Energia ou Calor de atomização ou dissociação: Br 2(l) 2 Br(g) Energia ou Calor de formação : C(s) +2 H 2(g) CH 4(g) Energia ou Calor de Combustão: C(s)+O 2(g) CO 2(g) Energia ou Calor de Sublimação: I 2(s) Energia ou Calor de fusão: H 2 O(s) Energia ou Calor de Vaporização: H 2 O(l) I 2(g) H 2 O(l) H 2 O(g)
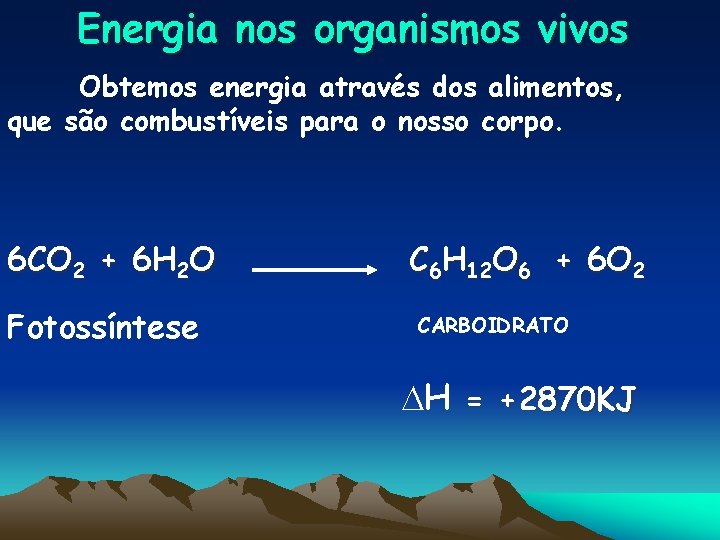
Energia nos organismos vivos Obtemos energia através dos alimentos, que são combustíveis para o nosso corpo. 6 CO 2 + 6 H 2 O Fotossíntese C 6 H 12 O 6 + 6 O 2 CARBOIDRATO H = +2870 KJ

A glicose possui alta energia que é liberada, em uma série de pequenas etapas, quando é degradada nono corpo humano. Trata-se da equação inversa da Fotossíntese. Esta energia é usada para realizar 3 tipos de principais trabalhos : anabolismo ou biossíntese, trabalho mecânico e transporte.

Fermentação da glicose C 6 H 12 O 6 2 C 2 H 5 OH + 2 CO 2 Fermentação de grãos e frutos, com ajuda de enzimas.

Lipídeos Fonte de reserva de energia. Eles existem como triglicerídios, melhor chamados de triacilglicóis, sendo o alimento que fornece energia mais concentrada: 38 KJ por grama, comparada com 17 KJ para carboidratos e proteínas. CH 2 OH CHOH +R -COOH CH 2 OH glicerol Ácido graxo CH 2 -O - CO - R CH -O-CO-R +3 H 2 O CH 2 -O - CO - R Triéster triacilglicerol

A maioria dos triacilglicerois da natureza (gorduras e óleos) contém ácidos graxos diferentes. Observe um ácido graxo SATURADO (ácido esteárico)e um ácido graxo INSATURADO (ácido oleico): H H CH 3 -(CH 2)7 -C = C -(CH 2)7 - COOH CH 3 - (CH 2)1 6 - COOH C 18 H 36 O 2 C 18 H 34 O 2 Na natureza existe o CIS

Principais diferenças entre óleos e gorduras GORDURAS Sólidos ÓLEOS Líquidos Maioria de origem animal Maioria de origem vegetal Maioria saturados Maioria insaturados Baixo índice de iodo Alto índice de iodo Índice de iodo: Massa de I 2, em gramas, que combina com 100 gramas de gordura ou óleo

EXERCÍCIOS 5 - Entre a manteiga que apresenta índice de iodo de 36 e o óleo de soja que apresenta índices de iodo 130, qual possui maior quantidade de ácidos graxos insaturados? Óleo de Soja 6 - Entre óleos e gorduras onde é maior o índice de iodo? Óleos 7 - No sebo predomina ácido esteárico, ao passo que no óleo de milho predomina ácido oleico. Qual apresenta maior número de ácidos graxos saturados? Sebo

Hidrólise dos Triacilgliceróis Quebra de uma gordura ou óleo pela água com catalisador, corpo degrada gordurante a digestão no intestino delgado. CH 2 - O - C 17 H 33 CH -O - CO- C 17 H 33 + 3 H 2 O CH 2 - O - C 17 H 33 H+ Glicerol+3 C 17 H 33 COOH Trioleína

Triacilgliceróis em contato com o ar ficam rançosos, desenvolvendo cheiro e odor desagradáveis. Isto por acontecer hidrólise ou por oxidação
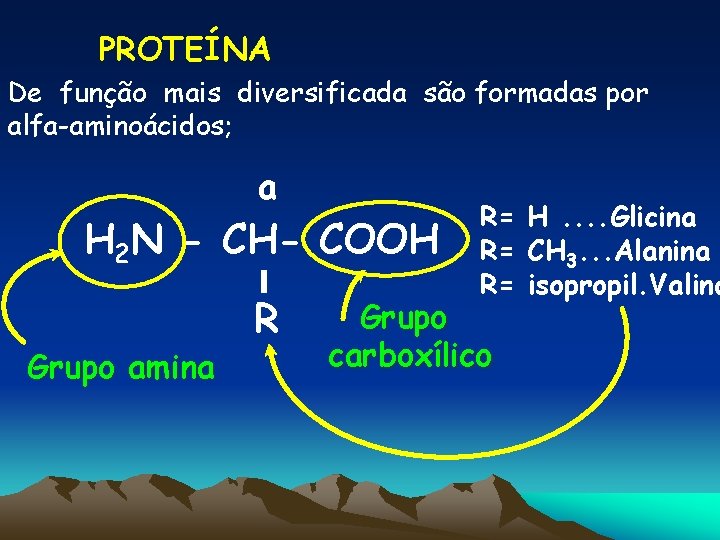
PROTEÍNA De função mais diversificada são formadas por alfa-aminoácidos; a H 2 N - CH- COOH Grupo amina R R= H. . Glicina R= CH 3. . . Alanina R= isopropil. Valina Grupo carboxílico

8 - O que seria uma margarina poliinsaturada? Várias insaturações. Ácidos graxos com várias ligações duplas. 9 - Qual a razão de aconselharem o uso de óleos ao invés de gorduras na culinárias? Pelas Insaturações 10 - Qual o único aminoácido que não apresenta carbono quiral? NH 2 H H 11 - Por que uma gordura sofrer rancidificação? C COOH = Glicina é mais difícil de Menos insaturações

UFLA Baseando-se na reação N 2(g) + 3 H 2 2 NH 3 (g) H = -22 Kcal Assinale a afirmativa FALSA (dados N = 14; H = 1) a) a reação é exotérmica. b) para se formar um mol de NH 3 são liberadas 11. 000 cal. c) para se formar 6, 02 x 1023 moléculas NH 3 são liberadas 11 kcal. d) 28 g de N 2 combinam com 6 g de H 2 formando 34 g de NH 3 e liberam 22. 000 cal. e) a decomposição de 17 g de NH 3 libera 11 Kcal.

PUC A tabela abaixo apresenta equações químicas de reações de formação de alguns óxidos metálicos e seus respectivos valores de H , a 25ºC e 1 atm. EQUAÇÃO QUÍMICA H (KCal/mol) Hg(l) + 1/2 O 2(g) Hg. O(s) - 22 2 Fe(s) + 3/2 O 2(g) Fe 2 O 3(s) - 197 Cu(s) + 1/2 O 2(g) Cu. O(s) - 38 2 Al(s) + 3/2 O 2(g) Al 2 O 3(s) - 400 Assinale a afirmativa INCORRETA: a) A formação desses óxidos é exotérmica. b) A reação de decomposição de dois Mols de óxido de mercúrio absorve 44 Kcal. c) A combustão de 5, 4 g de alumínio libera 40 Kcal. d) O metal mais fácil de ser obtido pelo aquecimento de seu óxido é o alumínio. e)Nas CNTP, o volume de O 2(g) necessário para reagir com um mol de Cu(s), para produzir 38 Kcal, é igual a 11, 2 L.

UFMG Combustíveis orgânicos liberam CO 2, em sua combustão. O aumento da concentração de CO 2 na atmosfera provoca um aumento do efeito estufa, que contribui para o aquecimento do planeta. A tabela abaixo informa o valor aproximado da energia liberada na queima de alguns combustíveis orgânicos, a 25ºC. COMBUSTÍVEL nome fórmula etanol C 2 H 5 OH metano CH 4 metanol CH 3 OH n-octano C 8 H 18 Energia liberada / k. J. mol-1' 1400 900 730 5600

COMBUSTÍVEL nome fórmula etanol C 2 H 5 OH metano CH 4 metanol CH 3 OH n-octano C 8 H 18 Energia liberada / k. J. mol-1' 1400 / 2 = 700 900 / 1 = 900 730 / 1 = 730 5600 / 8 = 700 O combustível que apresenta o maior quociente energia liberada/quantidade de CO 2 produzido é o: A) metano. B) etanol. C) n-octano. D) metanol. 32% acerto

UFMG A evaporação da água liquida é um processo que pode ocorrer como conseqüência de diversas ações. Dentre elas podem ser citadas o contato com um outro sistema de temperatura mais alta, a incidência de radiação eletromagnética e o arraste por um fluxo de gás. Considere três situações em que ocorre a evaporação da água liquida: I - na chama de um fogão a gás; II - em um forno de microondas em funcionamento; III - pela ação do vento. Sobre essas situações, pode-se afirmar que a evaporação ocorre devido a um fluxo de calor em A) I B) I, II e III C) I e II D) II e III 26% acerto
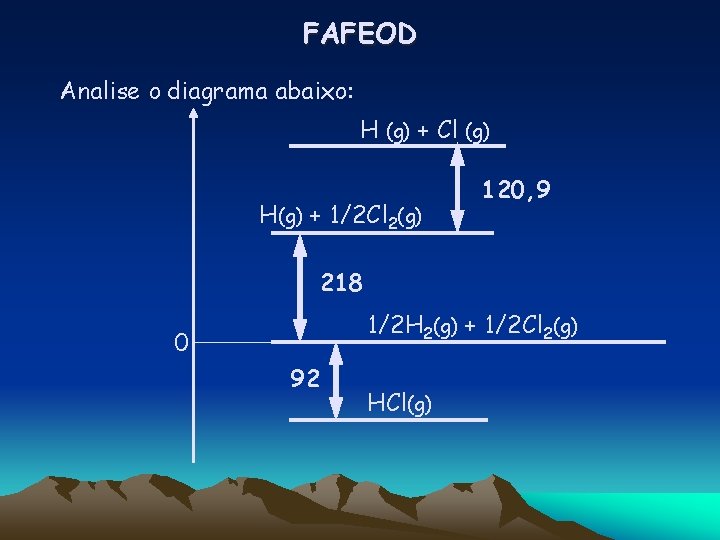
FAFEOD Analise o diagrama abaixo: H (g) + Cl (g) H(g) + 1/2 Cl 2(g) 120, 9 218 1/2 H 2(g) + 1/2 Cl 2(g) 0 92 HCl(g)

H (g) + Cl (g) 120, 9 H(g) + 1/2 Cl 2(g) 0 218 1/2 H 2(g) + 1/2 Cl 2(g) 92 HCl(g) Após essa análise, é INCORRETO afirmar que: A) a energia de ligação do hidrogênio é 436 k. J/mol. B) a energia de ligação do cloro é 120, 9 k. J/mol. C) a energia de formação do HCl (g) é -92 k. J/mol. D) a energia de ligação do HCl(g) é 430, 9 k. J/mol. E) a reação HCl(g) H( g) + 1/2 Cl 2 (g) absorve 310 k. J/mol.

A reação de combustão do metano pode ser abordada como um processo que envolve quebra e formação de ligações: H H—C—H + 2 O =O O =C = O + 2 O H H H Considerando o balanço energético dessa reação é correto afirmar que ocorre: A) absorção de energia na quebra das ligações do CH 4 e a reação tem H >0. B) absorção de energia na formação das ligações do CO 2 e a reação tem H < 0. C) liberação de energia na quebra das ligações do O 2 e a reação tem H >0. D) absorção de energia na quebra das ligações do CH 4 e a reação tem H < 0 E) liberação de energia na formação das ligações do H 2 O e a reação tem H > 0.

UFSJ Analise o diagrama. Energia (k. J) ½ N 2 (g) + 2 H 2 (g) + ½CI 2 (g) 46, 1 NH 3 (g) + ½ H 2 (g) + ½ CI 2 (g) 314, 4 92, 3 NH 3 (g) + HCI NH 4 CI (s) (g)

½ N 2 (g) + 2 H 2 (g) + ½CI 2 (g) 46, 1 NH 3 (g) + ½ H 2 (g) + ½ CI 2 (g) 314, 4 92, 3 NH 3 (g) + HCI A analise desse diagrama permite concluir que o calor envolvido NH 4 CI (s) na formação de um mol de NH 4 CI(s), a partir de NH 3(g) e HCI(g), e o calor de decomposição de um mol de NH 3(g), em N 2(g) e H 2(g), são, em k. J, respectivamente, 314, 4 - (46, 1 + 92, 3) 314, 4 - 138, 4 = 176, 0 A) 314, 4 e 46, 1 B) 176, 0 e 46, 1 C) 314, 4 e 92, 3 D) 268, 3 e 138, 4 (g)

UNAERP Energia Analisando atentamente o gráfico abaixo pode-se afirmar que a variação energética ocorrida Corresponde a uma reação de: H+ aq + OH- aq 13, 7 Kcal H 2 O(l) Caminho da reação a) oxidação de uma base pela adição de um ácido; b) neutralização de uma base por um ácido; c) combustão de hidrogênio: d) decomposição eletrolítica da água; e) decomposição térmica dda água

PASSO FUNDO A alternativa que identifica um sistema produtor de energia é: a) a ebulição da água. b) queima de um cigarro. c) o movimento veloz de um atleta. d) o cozimento de um alimento. e) o crescimento de um arbusto.

ITAÚNA Analisando o gráfico ao lado, todas as afirmativas são corretas, EXCETO: 2 NO 2(g) 67, 6 9, 6 0 N 2(g) + 2 O 2 (g) N 2 O 4(g) A) síntese do dióxido de nitrogênio (NO 2), a partir de N 2 e O 2, é uma reação de óxi-redução. B) a decomposição de um mol de N 2 O 4 em N 2 e O 2 libera 9, 6 k. J de energia. C) a conversão de NO 2 em N 2 O 4 é um processo exotérmico. D) a produção de um mol de NO 2, a partir de N 2 e O 2, libera 33, 8 k. J

Considere os seguinte processos: I - Combustão da gasolina no motor de um automóvel. II - Fusão do minério de ferro em um alto-forno. III- Evaporação da água de uma piscina por ação da luz do sol IV- Queima do gás de cozinha em um fogão. Representam reações exotérmica os processos: A) I e III b) II e III c) II e IV d) I e IV

PUC MG A cabeça de palito de fósforo contem uma substância chamada trissulfeto de tetrafósforo. Esse composto inflama na presença de oxigênio, ocorrendo, à pressão normal, a liberação de uma grande quantidade de calor. A reação referente ao processo está representada abaixo: P 4 S 3(s) + 8 O 2(g) P 4 O 10(s) + 3 SO 2(g) Dadas as entalpias de formação das seguintes substâncias, todas a 25ºC e 1 atm de pressão: P 4 O 10(s) = -2940, OKJ/mol P 4 S 3(s) = -153, 4 KJ / mol SO 2(s) = -296, 8 KJ / mol a entalpia de combustão do trissulfeto de tetrafósforo é, em KJ /mol, + 153, 4 a) -3. 677, 00 igual a: - 2940, 0 b) -3. 830, 40 + 153, 4 - 2940, 0 - 296, 8 x 3 = 890, 4 -3677, 0 c) -3. 390, 20 d) +3. 390, 20 e) +3. 667, 00

PUC MG Na comparação entre combustíveis, um dos aspectos a ser levado em conta A o calor liberado em sua queima. Seja dada a seguinte tabela: C 4 H 10 (g) + 13/2 O(g) = 4 CO 2(g) + 5 H 2 O(g) CH 3 OH (l) + 3/2 O(g) = CO 2 (g) + 2 H 2 O(g) C 2 H 5 OH (l) + 3 O(g) = 2 CO 2 (g) + 3 H 2 O(g) CH 4(g) + 2 O 2 = CO 2 (g) + 2 H 2 O(g) C 8 H 18(l) + 25/2 O 2 (g) =8 CO 2(g) + 9 H 2 O(g) H =-500 Kcal/mol H -57, 0 Kcal/mol H -66, 4 Kcal/mol H -212, 8 Kcal/mol H -1222, 5 Kcal/mol O combustível que possui maior poder calorifico por grama é: a) C 4 H 1 O 500 / 58 = 8, 6 b) CH 3 OH 57, 0 / 32 = 1, 8 c) C 2 H 5 OH 66, 4 / 46 = 1, 4 d) CH 4 212, 8 / 16 = 13, 25 e) C 8 H 18 1. 222, 5 / 114 = 10, 7

PUCMG Considere as seguintes transformações que envolvem o elemento potássio: K(s) I K(l) II K(g) III K+(g) + e- Ocorre transformação com absorção de energia em: a) I apenas b) II apenas c) III apenas d) I e II apenas e) I, II e III

UFMG Solicitado a classificar determinados processos como exotérmicos ou endotérmicos PROCESSO CLASSIFICAÇÃO Dissociação da molécula de hidrogênio em átomos Exotérmico Condensação de vapor de água Endotérmico Queima de álcool Exotérmico Considerando-se esse quadro, o número de erros cometidos pelso estudantes em sua classificação é A) 1 B) 3 C) 0 D)2

UFMG Considerando a ligação iônica do sal Na. Cl, pode-se prever as seguintes etapas: 1ª - Na (g) Na+(g) + 1 e H 1 2ª - Cl (g) + 1 e- Cl-(g) H 2 Observando os valores de prever que A B C D H 1 < 0 H 1 = 0 H 1 > 0 H das duas etapas, pode-se e H 2 < 0 e H 2 = 0 e H 2 < 0 e H 2 > 0

PUC Conhecem-se as seguintes equações termoquímicas: S(r) + O 2(g) S(m) + O 2(g) SO 2(g) H = - 71, 0 Kcal/mol H = - 71, 1 Kcal/mol Sobre elas são feitas as seguintes afirmativas: I - A formação do SO 2(g) é sempre exotérmica. II - A forma alotrópica estável do enxofre na temperatura da experiência é a rômbica. III- A conversão da forma rômbica na forma monoclínica é exotermica. A afirmativa está CORRETA em: a) I apenas b) II apenas. c) III apenas d) I e II apenas

Extra 1 : Localize os seguintes processos em um mesmo Diagrama. I- C(grafita) + O 2(g) → CO 2 (g) II- C (diamante) + O 2(g) →CO 2(g) III- C(s) + ½ IV - CO(g) + O 2(s) →CO (g) ½ O 2(g) →CO 2 (g) V-C(grafita) →C(diamante) H = - 94, 0 Kcal/mol H = - 94, 5 Kcal/mol H = - 26, 0 Kcal/mol H = - 68, 0 Kcal/mol H = + 0, 5 Kcal/mol
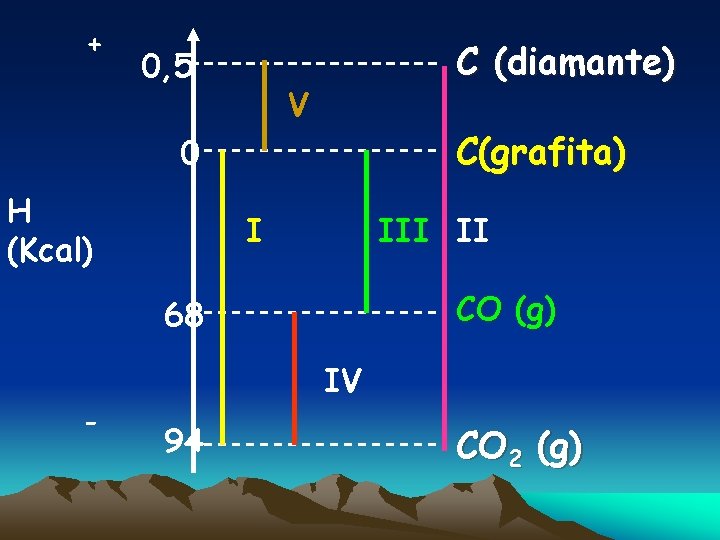
+ 0, 5 C (diamante) V C(grafita) 0 H (Kcal) I II CO (g) 68 - IV 94 CO 2 (g)
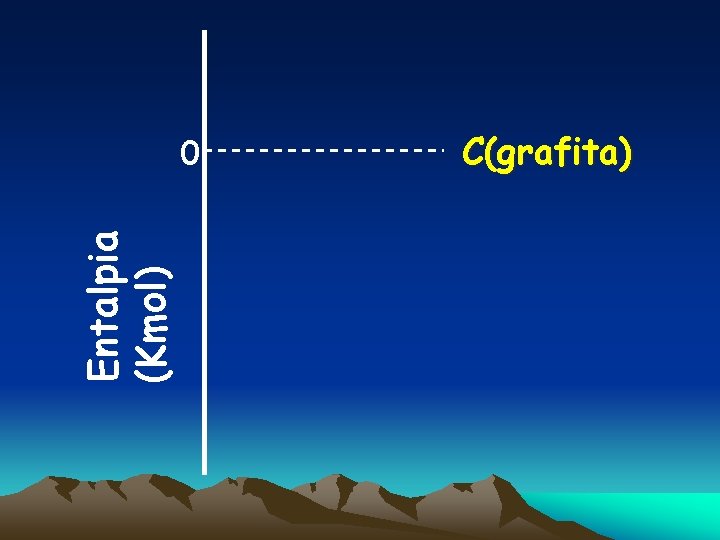
Entalpia (Kmol) 0 C(grafita)
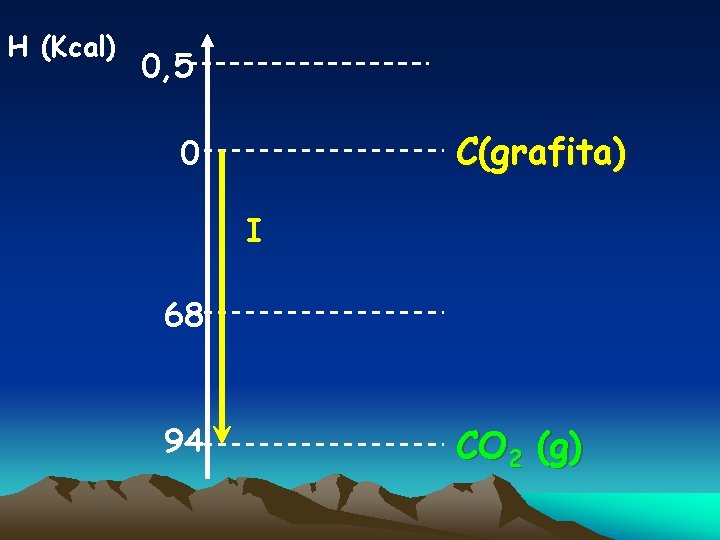
H (Kcal) 0, 5 C(grafita) 0 I 68 94 CO 2 (g)
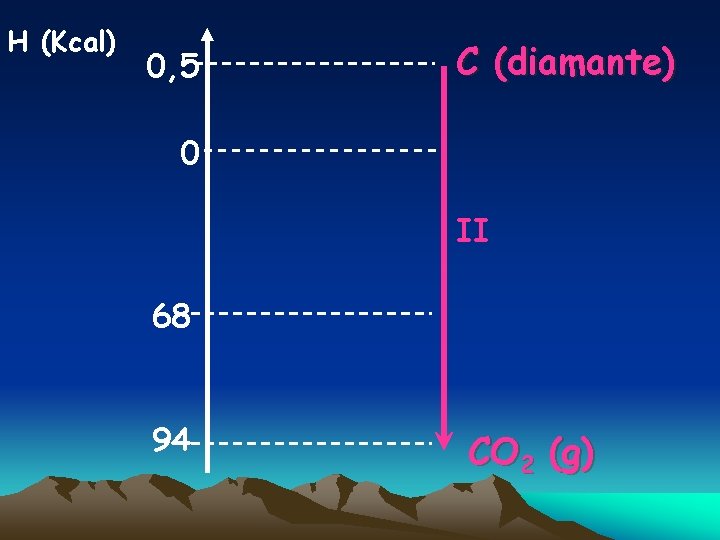
H (Kcal) 0, 5 C (diamante) 0 II 68 94 CO 2 (g)
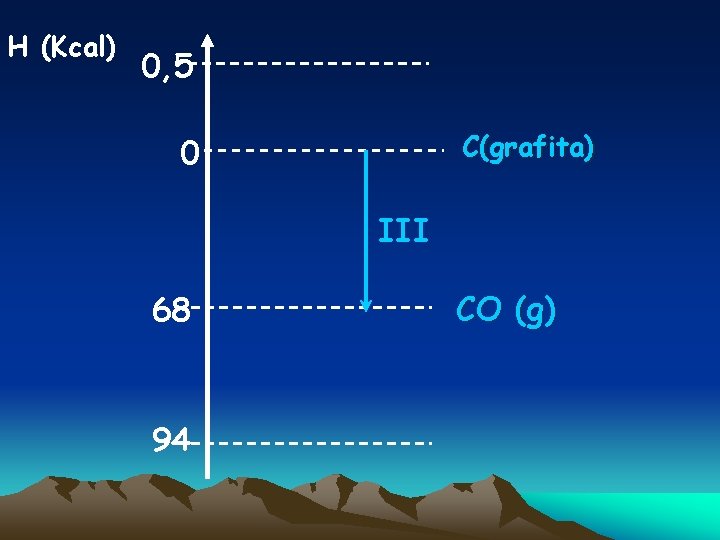
H (Kcal) 0, 5 C(grafita) 0 III 68 94 CO (g)
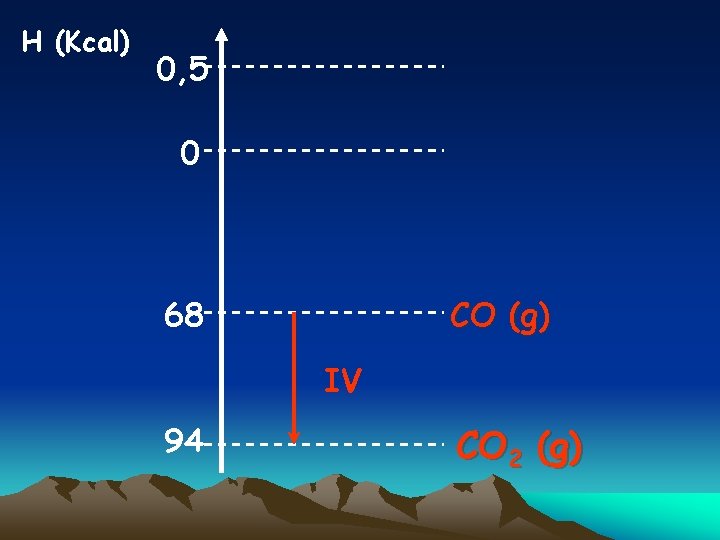
H (Kcal) 0, 5 0 68 CO (g) IV 94 CO 2 (g)
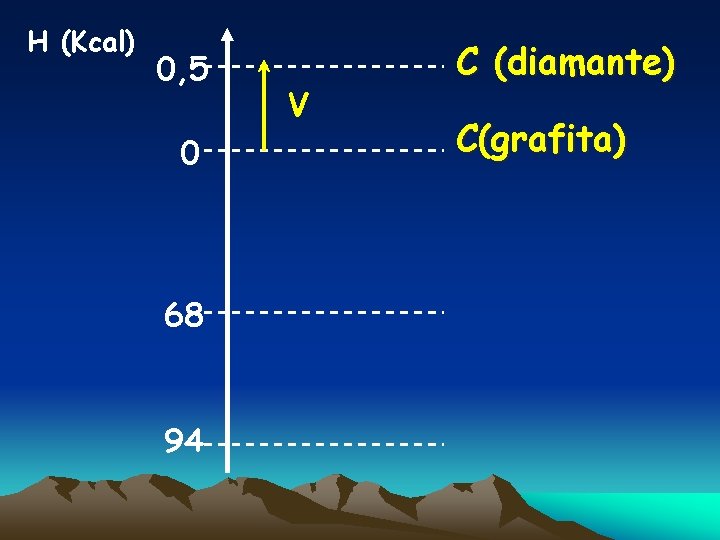
H (Kcal) 0, 5 0 68 94 V C (diamante) C(grafita)
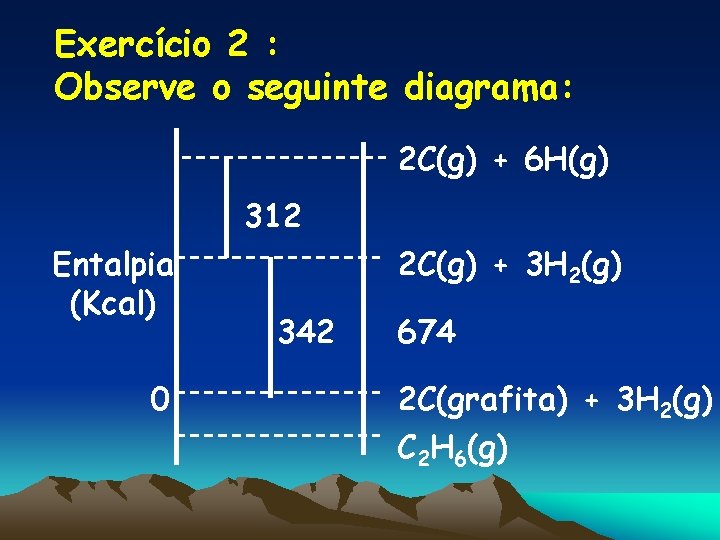
Exercício 2 : Observe o seguinte diagrama: 2 C(g) + 6 H(g) 312 Entalpia (Kcal) 0 2 C(g) + 3 H 2(g) 342 674 2 C(grafita) + 3 H 2(g) C 2 H 6(g)

Qual a energia de ligação H - H em Kcal 2 C(g) + 6 H(g) Entalpia (Kcal) 0 312 2 C(g) + 3 H 2(g) 2 C(grafita) + 3 H 2(g) C 2 H 6(g) 312 ÷ 3 = 104 Kcal

Qual o calor de sublimação de 12 g de carbono grafita? 2 C(g) + 6 H(g) Entalpia (Kcal) 2 C(g) + 3 H 2(g) 342 0 2 C(grafita) + 3 H 2(g) C 2 H 6(g) 342 ÷ 2 = 171 Kcal

Qual a variação de entalpia para formação do etano em Kcal/mol? 2 C(g) + 6 H(g) Entalpia (Kcal) 2 C(g) + 3 H 2(g) 674 0 2 C(grafita) + 3 H 2(g) C 2 H 6(g) 312 + 342 = 674 - 654 = 20 Kcal

2 C(g) + 6 H(g) Entalpia (Kcal) 0 2 C(g) + 3 H 2(g) 674 2 C(grafita) + 3 H 2(g) C 2 H 6(g)
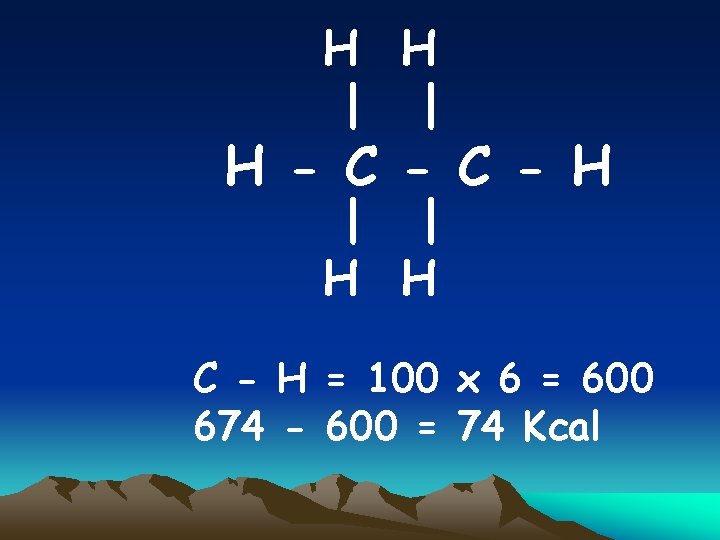
H H | | H - C - H | | H H C - H = 100 x 6 = 600 674 - 600 = 74 Kcal
- Slides: 129