TERMOQUMICA A QUMICA DOS EFEITOS ENERGTICOS OS PRINCPIOS









































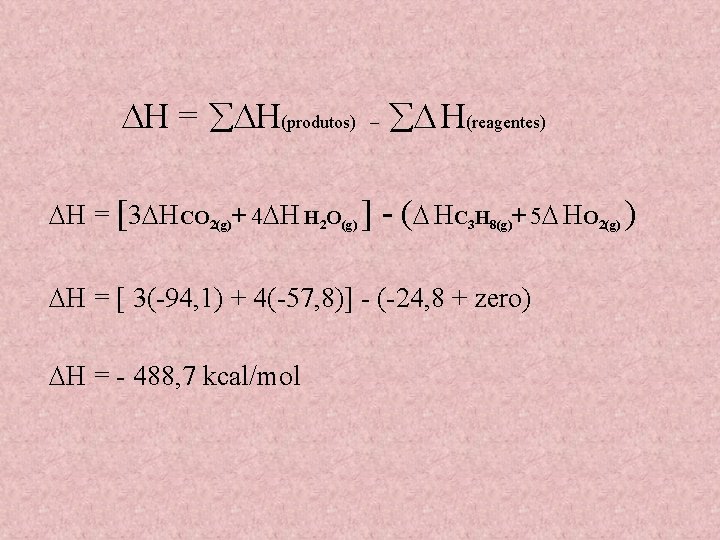



- Slides: 59

TERMOQUÍMICA A QUÍMICA DOS EFEITOS ENERGÉTICOS.

OS PRINCÍPIOS FUNDAMENTAIS DO CALOR E DO TRABALHO SE APLICAM, NO ESTUDO DE UMA REAÇÃO QUÍMICA E NAS MUDANÇAS DO ESTADO FÍSICO DE UMA SUBST NCIA.

pilha OBSERVE OS FENÔMENOS

NELES, OCORREM TRANSFORMAÇÕES FÍSICAS E (OU) QUÍMICAS ENVOLVENDO VÁRIOS TIPOS DE ENERGIA, INCLUSIVE ENERGIA TÉRMICA.

CONCEITOS IMPORTANTES SISTEMA - tudo aquilo que se reserva do universo para estudo. ENERGIA - resultado do movimento e da força gravitacional existentes nas partículas formadoras da matéria. ENERGIA QUÍMICA - trabalho realizado por um sistema através de reações químicas. CALOR - energia que flui de um sistema com temperatura mais alta para o outro com temperatura mais baixa. TRABALHO - deslocamento de um corpo contra uma força que se opõe a esse deslocamento.

ENERGIA INTERNA ENERGIA ACUMULADA POR UMA SUBST NCIA SOB VOLUME CONSTANTE. ENTALPIA ENERGIA ACUMULADA POR UMA SUBST NCIA SOB PRESSÃO CONSTANTE, RESUMIDAMENTE, PODEMOS DIZER QUE É O CONTÉUDO DE CALOR DA SUBST NCIA.

O PROCESSO DE MEDIDA DOS CALORES DE REAÇÃO É DENOMINADO CALORIMETRIA. O APARELHO QUE MEDE A ENTALPIA DA REAÇÃO É DENOMINADO CALORÍMETRO.

CALORIA é a quantidade de energia necessária para aumentar de 1ºC a temperatura de 1 g de água. JOULE é a quantidade de energia necessária para deslocar uma massa de 1 kg, inicialmente em repouso, fazendo percurso de 1 metro em 1 segundo. 1 cal = 4, 18 J 1 kcal = 1000 cal 1 k. J = 1000 J

EFEITOS ENERGETICOS NAS REACõES QUÍMICAS Na fotossíntese ocorre absorção de calor 6 CO 2 + 6 H 2 O LUZ CLOROFILA C 6 H 12 O 6 + 6 O 2 GLICOSE Na combustão do etanol ocorre liberação de calor ETANOL

A TERMOQUÍMICA ESTUDA AS MUDANÇAS TÉRMICAS ENVOLVIDAS NAS REAÇÕES QUÍMICAS * quando envolve liberação de calor, denomina-se REAÇÃO EXOTÉRMICA. * quando envolve absorção de calor, denomina-se REAÇÃO ENDOTÉRMICA.

EQUAÇÃO TERMOQUÍMICA É a representação de uma reação química em que está especificado: * o estado físico de todas as substâncias. * o balanceamento da equação. * a variação de calor da reação ( H ). * variedade alotrópica quando existir. * as condições físicas em que ocorre a reação, ou seja, temperatura e pressão. ( 25ºC e 1 atm é o comum) Segue alguns exemplos. . .

REAÇÃO EXOTÉRMICA 2 C(s) + 3 H 2(g) C 2 H 6(g) H= – 20, 2 kcal 2 C(s) + 3 H 2(g) C 2 H 6(g) + 20, 2 kcal REAÇÃO ENDOTÉRMICA Fe 3 O 4(s) 3 Fe(s) + 2 O 2(g) H= + 267, 0 kcal Fe 3 O 4(s) 3 Fe(s) + 2 O 2(g) - 267, 0 kcal

REAÇÃO EXOTÉRMICA 2 C(s) + 3 H 2(g) C 2 H 6(g) OBSERVE OS SINAIS H = – 20, 2 kcal 2 C(s) + 3 H 2(g) C 2 H 6(g) + 20, 2 kcal REAÇÃO ENDOTÉRMICA OBSERVE OS SINAIS Fe 3 O 4(s) 3 Fe(s) + 2 O 2(g) H = + 267, 0 kcal Fe 3 O 4(s) 3 Fe(s) + 2 O 2(g) - 267, 0 kcal

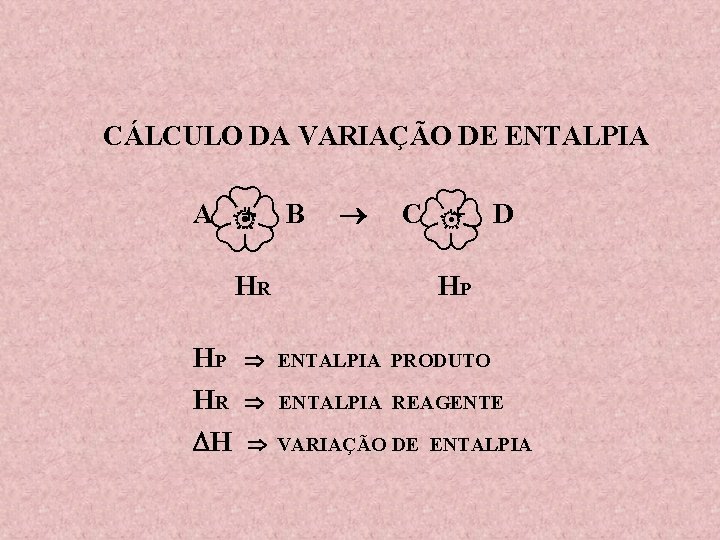
CÁLCULO DA VARIAÇÃO DE ENTALPIA A + HR HP HR H B C + D HP ENTALPIA PRODUTO ENTALPIA REAGENTE VARIAÇÃO DE ENTALPIA

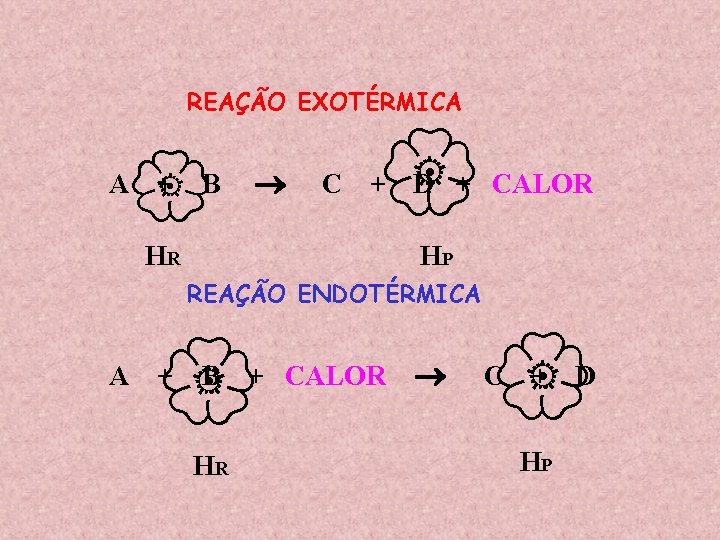
REAÇÃO EXOTÉRMICA A + B HR C + D + CALOR HP REAÇÃO ENDOTÉRMICA A + B HR + CALOR C + HP D

Não esqueça: HP ENTALPIA PRODUTO HR ENTALPIA REAGENTE H VARIAÇÃO DE ENTALPIA

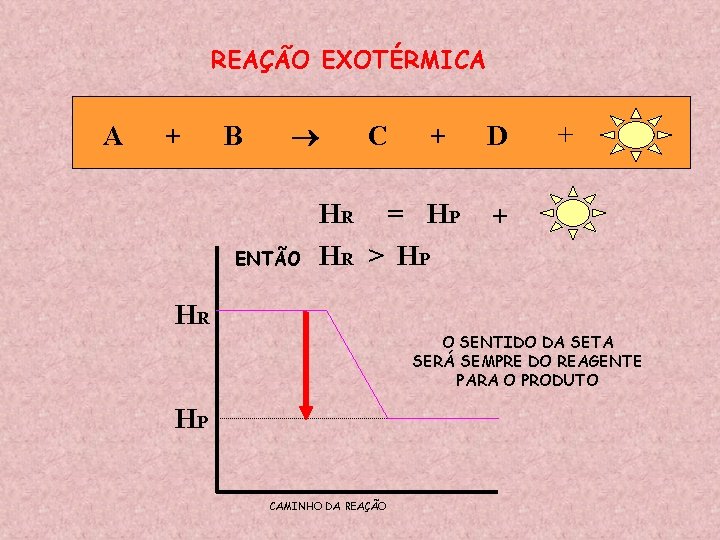
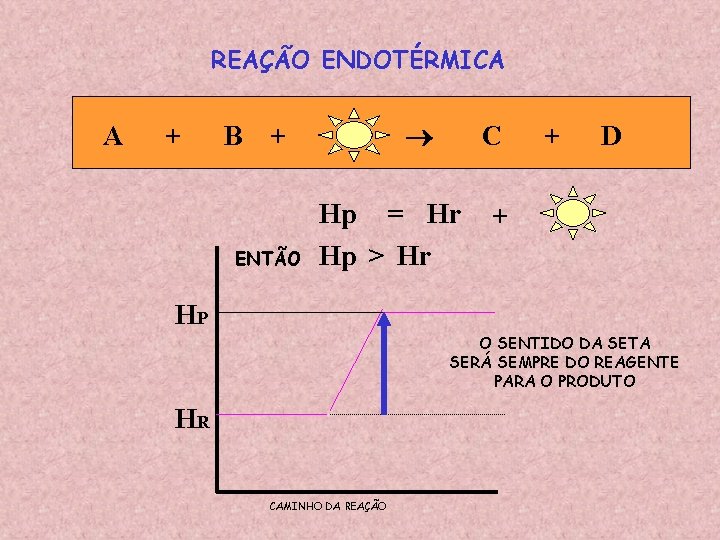
REAÇÃO EXOTÉRMICA A + B ENTÃO C + HR = HP HR > HP D + + HR O SENTIDO DA SETA SERÁ SEMPRE DO REAGENTE PARA O PRODUTO HP CAMINHO DA REAÇÃO

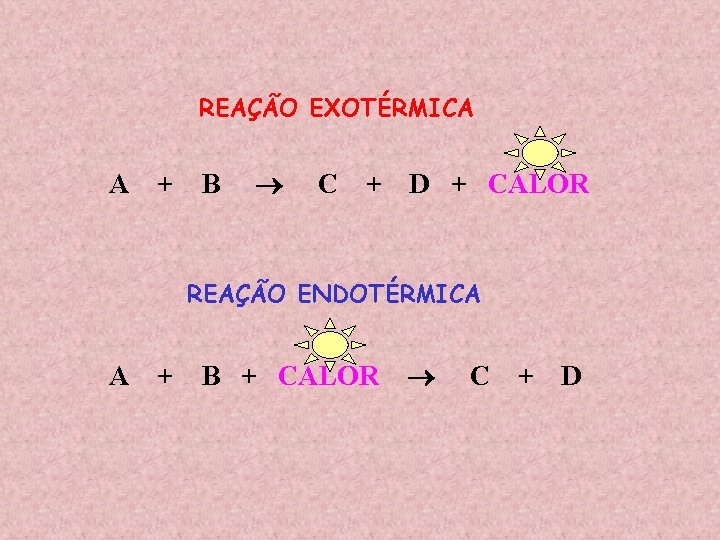
REAÇÃO EXOTÉRMICA A + B C + D + CALOR REAÇÃO ENDOTÉRMICA A + B + CALOR C + D

REAÇÃO ENDOTÉRMICA A + B + ENTÃO C Hp = Hr Hp > Hr + D + HP O SENTIDO DA SETA SERÁ SEMPRE DO REAGENTE PARA O PRODUTO HR CAMINHO DA REAÇÃO

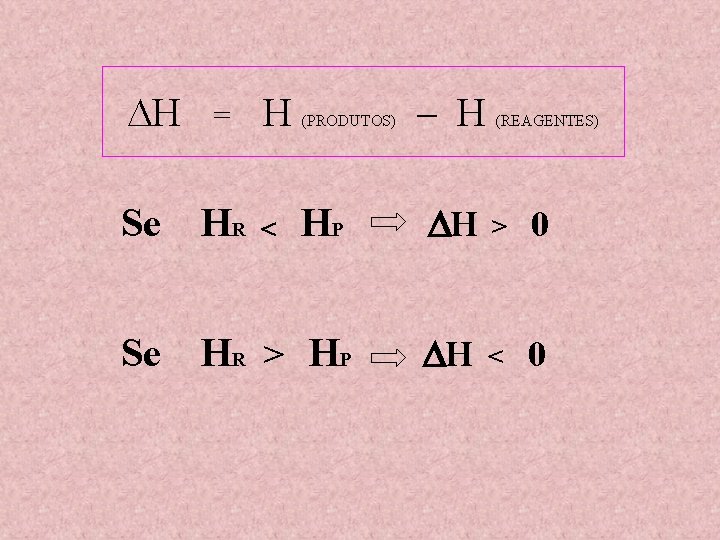
H = H (PRODUTOS) – H (REAGENTES) Se HR HP H > 0 Se H R > HP H < 0

H Se = HR H (PRODUTOS) HP – H H (REAGENTES) > 0 REAÇÃO ENDOTÉRMICA Se H R > HP H REAÇÃO EXOTÉRMICA < 0

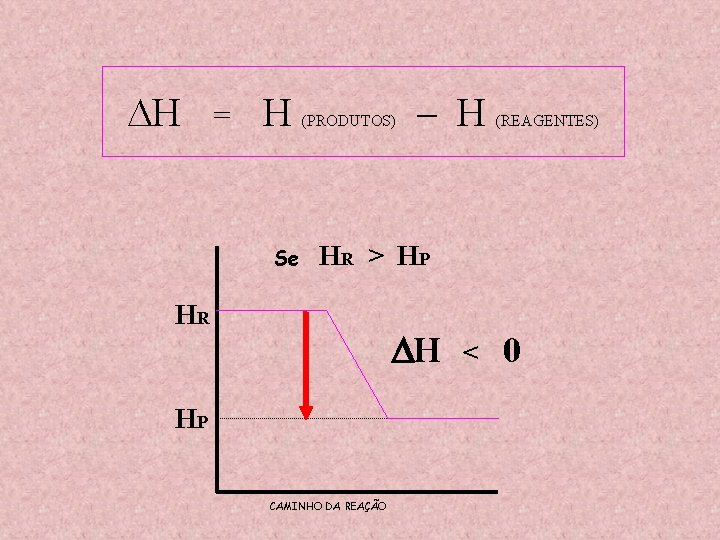
H = H Se (PRODUTOS) – H (REAGENTES) HR > HP HR H HP CAMINHO DA REAÇÃO < 0

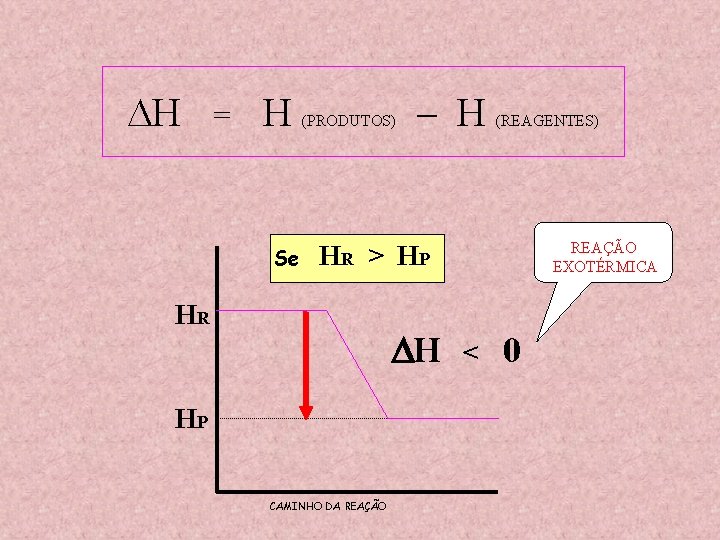
H = H Se (PRODUTOS) – H (REAGENTES) REAÇÃO EXOTÉRMICA HR > HP HR H HP CAMINHO DA REAÇÃO < 0

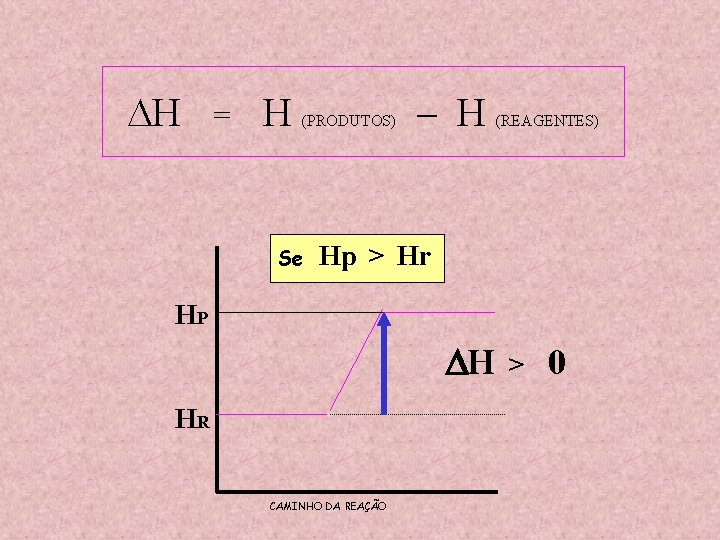
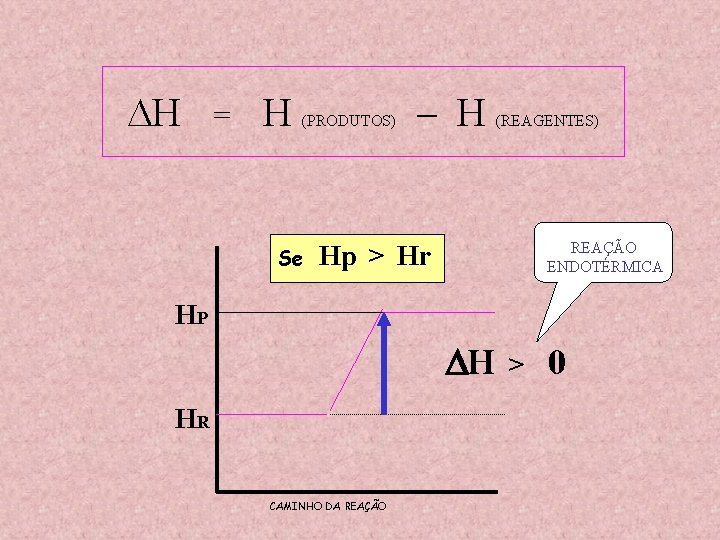
H = H (PRODUTOS) Se – H (REAGENTES) Hp > Hr HP H HR CAMINHO DA REAÇÃO > 0

H = H (PRODUTOS) Se – H (REAGENTES) REAÇÃO ENDOTÉRMICA Hp > Hr HP H HR CAMINHO DA REAÇÃO > 0

OBS. : * Convencionou-se entalpia zero para determinadas substâncias simples, em razão de não ser possível medir o valor real da entalpia de uma substância. * Foram escolhidas condições-padrão para estabelecer medidas relativas. * Terá entalpia zero qualquer substância simples que se apresente nos estados físico e alotrópico mais comum, a 25ºC e 1 atm de pressão.


* A forma alotrópica menos estável tem entalpia maior que zero.

Observe a reação de formação (síntese ) de um mol de água, a 25ºC e 1 atm de pressão. H 2(g) + 1/2 O 2(g) H 2 O(g) Cálculo da entalpia de formação: H = H(produtos) - H(reagentes)

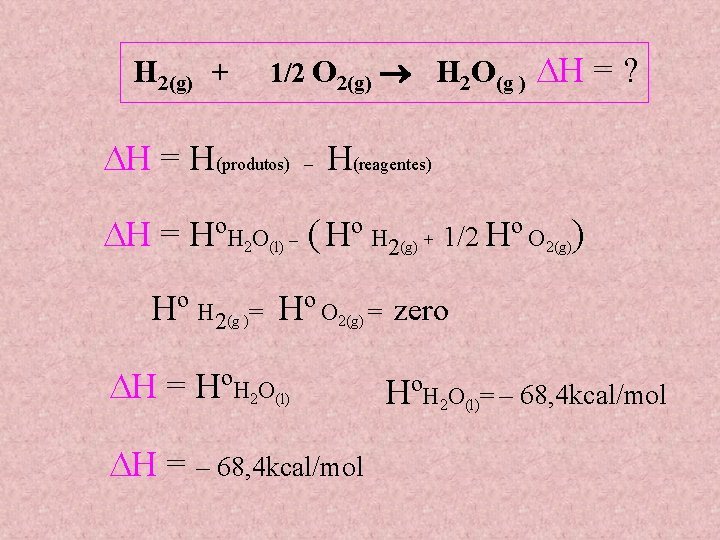
H 2(g) + 1/2 O 2(g) H 2 O(g ) H = H(produtos) – H = ? H(reagentes) H = HºH 2 O(l) – ( Hº H 2(g) + 1/2 Hº O 2(g)) COMO Hº H 2(g )= Hº O 2(g) = zero H = HºH 2 O(l) e ENTÃO H = – 68, 4 kcal/mol HºH 2 O(l)= – 68, 4 kcal/mol

H 2(g) + 1/2 O 2(g) H 2 O(g ) H = H(produtos) – H = ? H(reagentes) H = HºH 2 O(l) – ( Hº H 2(g) + 1/2 Hº O 2(g)) Hº H 2(g )= Hº O 2(g) = zero H = HºH 2 O(l) H = – 68, 4 kcal/mol HºH 2 O(l)= – 68, 4 kcal/mol

H 2(g) + 1/2 O 2(g) H 2 O(g ) H = H(produtos) – H = – 68, 4 kcal/mol H(reagentes) H = HºH 2 O(l) – ( Hº H 2(g) + 1/2 Hº O 2(g)) Hº H 2(g )= Hº O 2(g) = zero H = HºH 2 O(l) H = – 68, 4 kcal/mol HºH 2 O(l)= – 68, 4 kcal/mol

CÁLCULOS DA VARIAÇÃO DE ENTALPIA LEI DE HESS A entalpia de uma reação depende apenas dos estados iniciais e finais da reação, não depende dos estados intermediários, ou seja a reação é a mesma para uma ou mais etapas. Ex. 1 - Cálculo da entalpia da reação de formação do gás carbônico: C(grafite)+ O 2(g) CO 2(g) H = ? kcal/mol

OBSERVE AS EQUAÇÕES: C(grafite)+ 1/2 O 2(g) CO(g) H = – 26, 4 kcal/mol CO(g) + 1/2 O 2(g) CO 2(g) H = – 67, 6 kcal/mol

EFETUAMOS A SOMA ALGÉBRICA DAS MESMAS. Note que os termos semelhantes em membros opostos se anulam. 1ª etapa: C(grafite)+ 1/2 O 2(g) CO(g) H 1 = – 26, 4 kcal/mol 2ª etapa: CO(g) + 1/2 O 2(g) CO 2(g) H 2 = – 67, 6 kcal/mol Etapa final: C(grafite)+ CONCLUINDO O 2(g) CO 2(g) H = H 1 + H 2 H = – 94, 0 kcal/mol

Observe que o processo é puramente algébrico. 1ª etapa : C(grafite)+ 1/2 O 2(g) CO(g) H 1 = -26, 4 kcal/mol 2ª etapa : CO(g) + 1/2 O 2(g) CO 2(g) H 2 = -67, 6 kcal/mol Etapa final: C(grafite)+ O 2(g) CO 2(g) H = -94, 0 kcal/mol

Observe que o processo é puramente algébrico. 1ª etapa : C(grafite)+ 1/2 O 2(g) CO(g) H 1 = -26, 4 kcal/mol 2ª etapa : CO(g) + 1/2 O 2(g) CO 2(g) H 2 = -67, 6 kcal/mol Etapa final: C(grafite)+ O 2(g) CO 2(g) H = -94, 0 kcal/mol H = H 1 + H 2 = -94, 0 kcal/mol

Ex 2 - Dadas as equações: C(grafite )+ O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol H 2(g) + 1/2 O 2(g) H 2 O(l) H 2 = – 68, 4 kcal/mol C(grafite)+ 2 H 2(g) CH 4(g) H 3 = – 17, 9 kcal/mol Calcular a entalpia da reação: CH 4(g) + O 2(g) CO 2(g)+ H 2 O(l)

Resolução: As equações dadas deverão ser arrumadas de tal modo que a sua soma resulte na equação-problema. Agora vamos identificá-las com algarismos romanos. I) C(grafite )+ O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol II) H 2(g) + 1/2 O 2(g) H 2 O(l) H 2 = – 68, 4 kcal/mol III) C(grafite)+ 2 H 2(g) CH 4(g) H 3 = – 17, 9 kcal/mol Equação-problema: CH 4(g) + O 2(g) CO 2(g)+ H 2 O(l)

Devemos manter a equação I pois dessa forma obteremos gás carbônico como produto. C(grafite )+ O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol Multiplicar por 2 a equação II para que os coeficientes fiquem ajustados. ( 2 H 2(g) + 1/2 O 2(g) H 2 O(l) 2 H 2(g) + O 2(g) 2 H 2 O(l) ) H 2 = – 68, 4 kcal/mol H 2 = – 136, 8 kcal/mol O H 2 também é multiplicado Agora, invertemos a equação III de modo a obter o metano ( CH 4 ) como reagente. Observe a inversão de sinal do H 3 CH 4(g) C(grafite)+ 2 H 2(g) H 3 = + 17, 9 kcal/mol

Finalmente aplica-se a soma algébrica das equações, inclusive das variações de entalpia. C(grafite )+ O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol 2 H 2(g) + O 2(g) 2 H 2 O(l) H 2 = – 136, 8 kcal/mol CH 4(g) C(grafite)+ 2 H 2(g) H 3 = + 17, 9 kcal/mol _______________________________

Observe os cortes: C(grafite )+ O 2(g) CO 2(g) H 1 = – 94, 0 kcal/mol 2 H 2(g) + O 2(g) 2 H 2 O(l) H 2 = – 136, 8 kcal/mol CH 4(g) C(grafite)+ 2 H 2(g) H 3 = + 17, 9 kcal/mol _______________________________ CH 4(g) + 2 O 2(g) CO 2(g)+ 2 H 2 O(l) H = – 212, 9 kcal/mol H = H 1 + H 2 + H 3

CALORES PADRÃO DE FORMAÇÃO OU ENTALPIA-PADRÃO DE FORMAÇÃO É o calor desenvolvido na formação de um mol de determinado composto, a partir das substâncias simples correspondentes no estado padrão. Representa-se por: O índice sobrescrito padrão. Hfº º significa estado O índice subscrito f significa formação. .

- é aquela em que um mol de um único composto é formado a partir de substâncias simples no estado padrão. Exs. : C(grafite )+ O 2(g) CO 2(g) REAÇÃO DE FORMAÇÃO 1 mol H 2(g) + 1/2 O 2(g) H 2 O(l) 1 mol Os valores de H são pré-estabelecidos e encontrados em tabelas, para aqueles compostos que estejam na sua forma mais estável a 1 atm de pressão, ou seja, no estado padrão.


CALOR PADRÃO DE COMBUSTÃO OU ENTALPIA-PADRÃO DE COMBUSTÃO É o calor liberado na combustão total de um mol de uma substância em que os componentes dessa reação estão no estado-padrão. H 2(g) + 1/2 O 2(g) H 2 O(l) H=– 68, 4 kcal/mol C 2 H 5 OH(l) + 3 O 2(g) 2 CO 2(g) + 3 H 2 O(l) H=– 325 kcal/mol COMBUSTÃO - reação de uma substância com o oxigênio (O 2) em que ocorre liberação de energia. ( REAÇÃO EXOTÉRMICA )

O PODER CALÓRICO DE ALGUMAS SUBST NCIAS A gasolina possui maior poder clalorífico que o álcool. Para cada litro de gasolina queimado são produzidos aproximadamente 8000 quilocalorias, enquanto para cada litro de álcool queimado, temos a produção de aproximadamente 5000 quilocalorias. Veja a tabela de calorias de alguns alimentos, a seguir.


CALOR DE DISSOLUÇÃO OU ENTALPIA DE DISSOLUÇÃO É o calor desenvolvido ( liberado ou absorvido) provocado pela dissolução de um mol de substância, numa quantidade de água suficiente para se obter uma solução diluída, no estado padrão. H 2 SO 4(l) + aq H 2 SO 4(aq) H = – 22, 9 kcal/mol KNO 3(s) + aq KNO 3(aq) H = + 8, 5 kcal/mol

CALOR DE NEUTRALIZAÇÃO OU ENTALPIA DE NEUTRALIZAÇÃO É o calor liberado na neutralização de um equivalente-grama de um ácido por um equivalente-grama de uma base, ambos em soluções aquosas diluídas, no estado padrão. HCl(aq) + Na. OH(aq) Na. Cl(aq) + H 2 O(l) H = – 13, 8 kcal/eq-g HNO 3(aq) + Li. OH(aq) Li. NO 3(aq) + H 2 O(l) H = – 13, 8 kcal/eq-g OBS. : Para ácidos e bases fortes o H será sempre o mesmo.

A variação de entalpia de uma reação pode ser calculada, conhecendo-se apenas as entalpias de formação dos seus reagentes e produtos. H = H(produtos) – H(reagentes)

Observe a equação: C 3 H 8(g) + 5 O 2(g) 3 CO 2(g) + 4 H 2 O(g) H = ? – kcal/mol Consultando a tabela de calores de formação: SUBST NCIAS C 3 H 8(g) CO 2(g) H 2 O(g) O 2(g) H -24, 8 kcal/mol -94, 1 kcal/mol -57, 8 kcal/mol zero
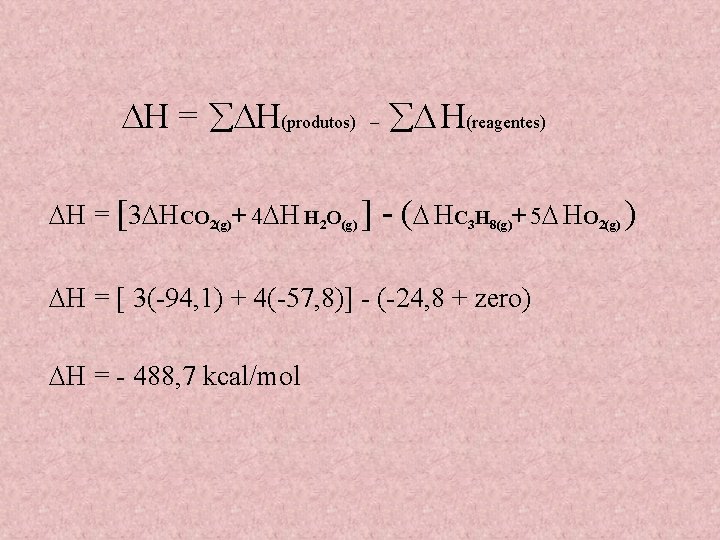
H = H(produtos) – H(reagentes) H = [3 HCO 2(g)+ 4 H H 2 O(g) ] - ( H C H 3 8(g) + 5 HO 2(g) ) H = [ 3(-94, 1) + 4(-57, 8)] - (-24, 8 + zero) H = - 488, 7 kcal/mol

ENERGIA DE LIGAÇÃO É A ENERGIA NECESSÁRIA PARA ROMPER UM MOL DE LIGAÇÃO DE UMA SUBST NCIA NO ESTADO GASOSO. EX. Para romper um de ligação H – O são necessárias 110 kcal. Para romper um de ligação H – C são necessárias 100 kcal. Para romper um de ligação O = O são necessárias 118 kcal. . * esses valores são tabelados

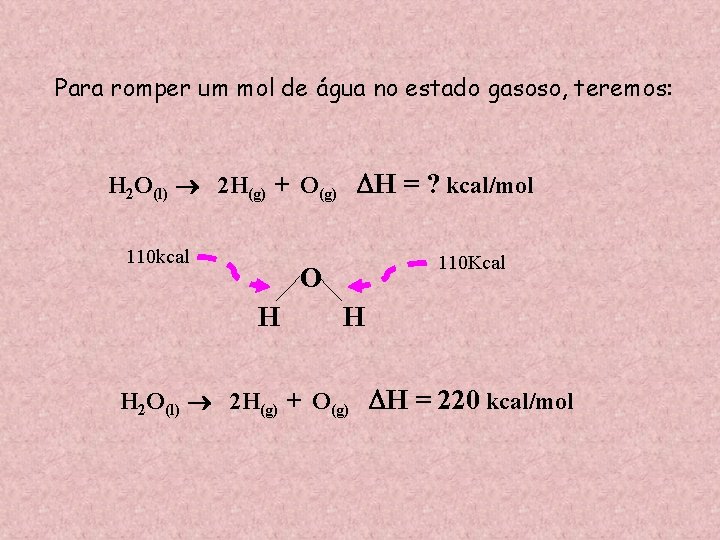
Para romper um mol de água no estado gasoso, teremos: H 2 O(l) 2 H(g) + O(g) H = ? kcal/mol 110 kcal 110 Kcal O H H H 2 O(l) 2 H(g) + O(g) H = 220 kcal/mol

Observe a reação em que todos os participantes estão no estado gasoso: H | H— C— O — H | H + 3/2 O 2 O = C = O + 2 H 2 O Para romper as ligações intramoleculares do metanol e do oxigênio, serão absorvidos, para: 1 mol de O — H +464, 0 kj + 464, 0 kj 1 mol de C — O +330, 0 kj + 330, 0 kj 3 mols de C — H 3 (+413, 0 kj) + 1239, 0 kj 3/2 mols de O = O 3/2 (+493, 0 kj) + 739, 5 kj TOTAL ABSORVIDO + 2772, 5 kj

Cômputo dos produtos: H | H— C— O — H | H + 3/2 O 2 O = C = O + 2 H 2 O Para formar as ligações intramoleculares do CO 2 e da água, serão liberadas: 2 mols de C = O 2 (-7444, 0 kj) 2 mols de H — O 2 ( - 464, 0 kj) TOTAL LIBERADO -1 488, 0 kj - 928, 0 kj -2 416, 0 kj

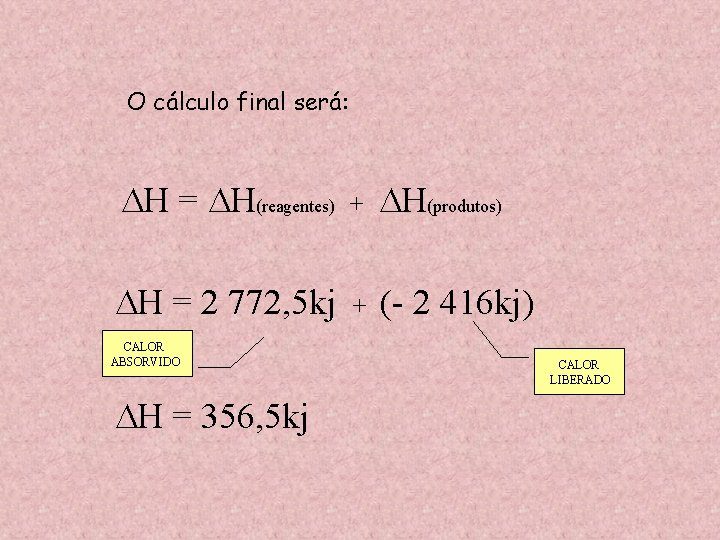
O cálculo final será: H = H(reagentes) + H(produtos) H = 2 772, 5 kj + (- 2 416 kj) CALOR ABSORVIDO H = 356, 5 kj CALOR LIBERADO

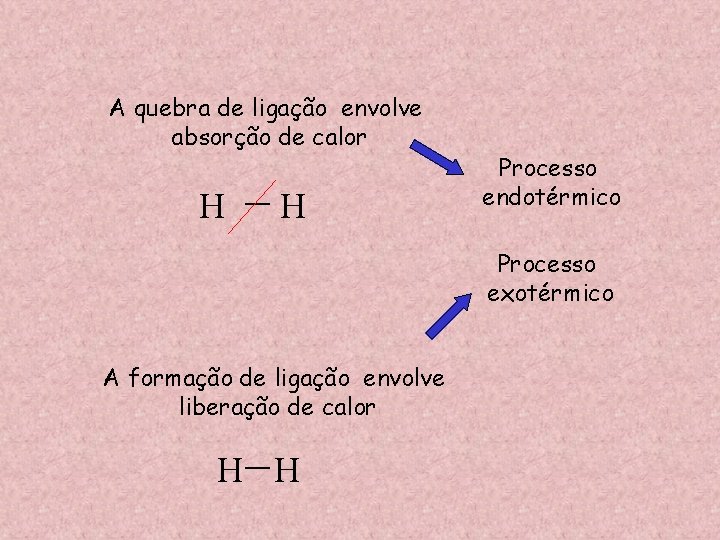
A quebra de ligação envolve absorção de calor H — H Processo endotérmico Processo exotérmico A formação de ligação envolve liberação de calor H— H