TERMOQUMICA 1 1 CONCEPTOS BSICOS 2 PRIMER PRINCIPIO

TERMOQUÍMICA 1

1 CONCEPTOS BÁSICOS 2 PRIMER PRINCIPIO DE LA TERMODINÁMICA Calor (Q) y trabajo (W) Qp y Q v Entalpías Ley de Hess Entalpías de enlace 3 SEGUNDO PRINCIPIO DE LA TERMODINÁMICA Entropía Energía Libre Espontaneidad
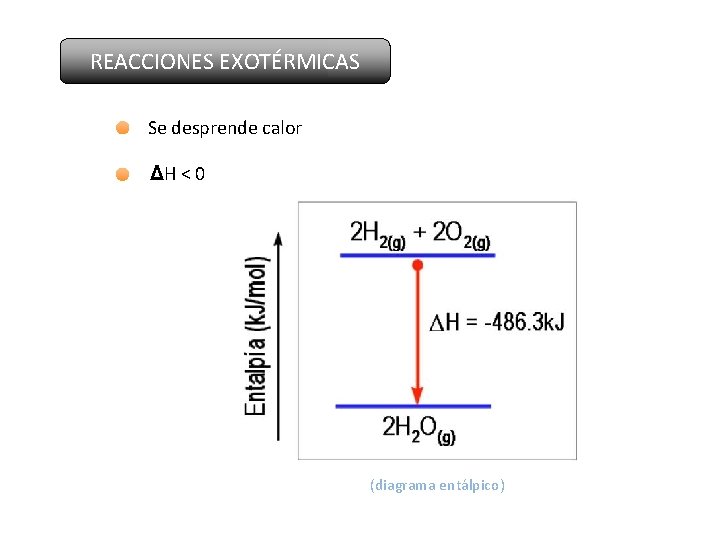
REACCIONES EXOTÉRMICAS Se desprende calor ΔH < 0 (diagrama entálpico)
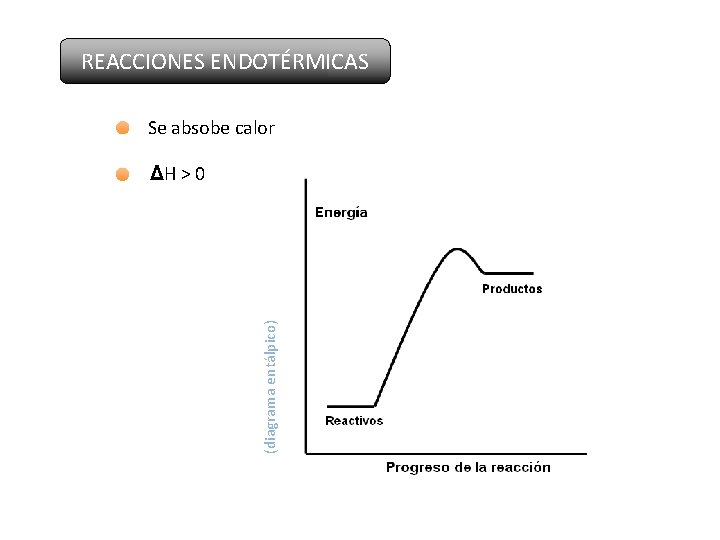
REACCIONES ENDOTÉRMICAS Se absobe calor (diagrama entálpico) ΔH > 0
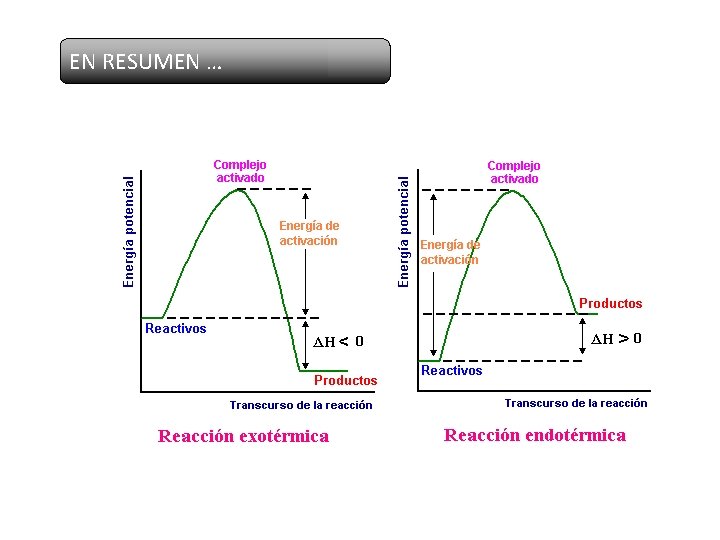
EN RESUMEN …

Ejercicio Sea la reacción: H 2 SO 4 (aq) + Zn (s) Zn. SO 4 (s) + H 2 (g) ΔH = -80 Kcal/mol a) ¿Qué calor se obtiene al consumir 800 m. L de disolución 0’ 35 M de H 2 SO 4 con zinc en exceso? b) ¿Qué masa de agua elevará 25 o. C su temperatura al consumir 143 g de H 2 SO 4 con zinc en exceso? Ce H 2 O = 4’ 18 k. J o. C Kg-1 ; S = 32 ; H = 1 ; O =16

Ejercicio: solución
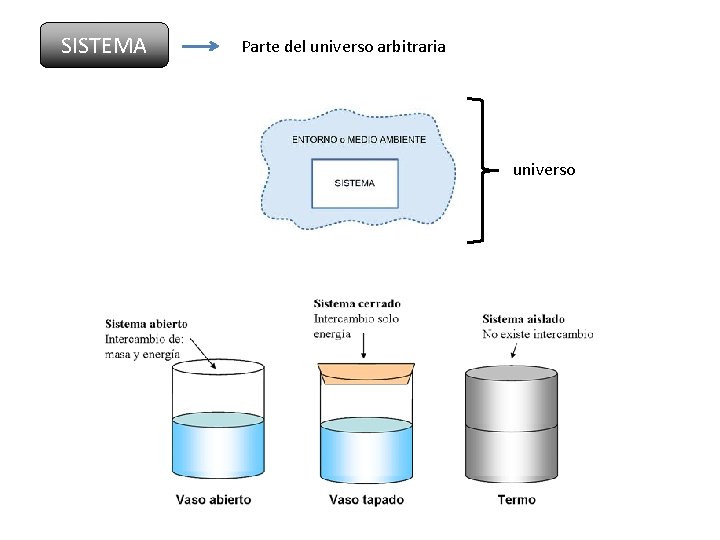
SISTEMA Parte del universo arbitraria universo
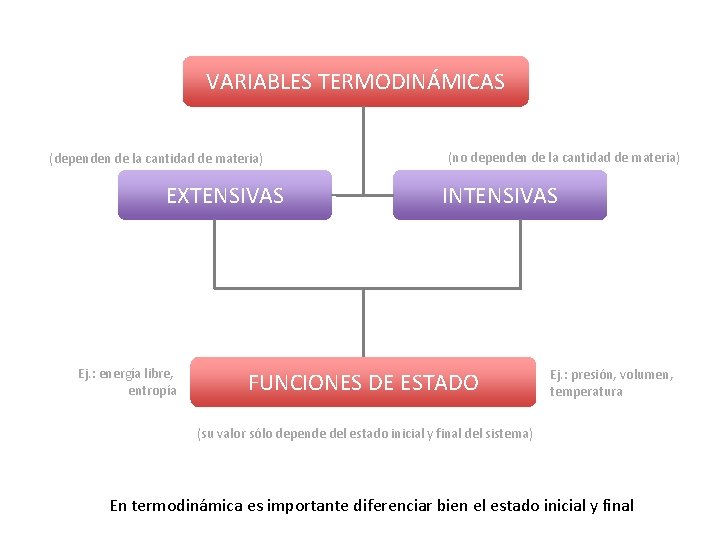
VARIABLES TERMODINÁMICAS (dependen de la cantidad de materia) EXTENSIVAS Ej. : energía libre, entropía (no dependen de la cantidad de materia) INTENSIVAS FUNCIONES DE ESTADO Ej. : presión, volumen, temperatura (su valor sólo depende del estado inicial y final del sistema) En termodinámica es importante diferenciar bien el estado inicial y final

PRIMER PRINCIPIO DE LA TERMODINÁMICA La energía total (Q + W) del universo en cualquier proceso termodinámico se mantiene constante. Esto significa que la energía se transfiere pero no se pierde. Para un sistema ΔU = Q + W U = ENERGÍA INTERNA DEL SISTEMA (cinética y potencial), inluye energía asociada al movimiento de las partículas, en los enlaces químicos, atracciones intermoleculares y la asociadad a los electrones de los átomos.
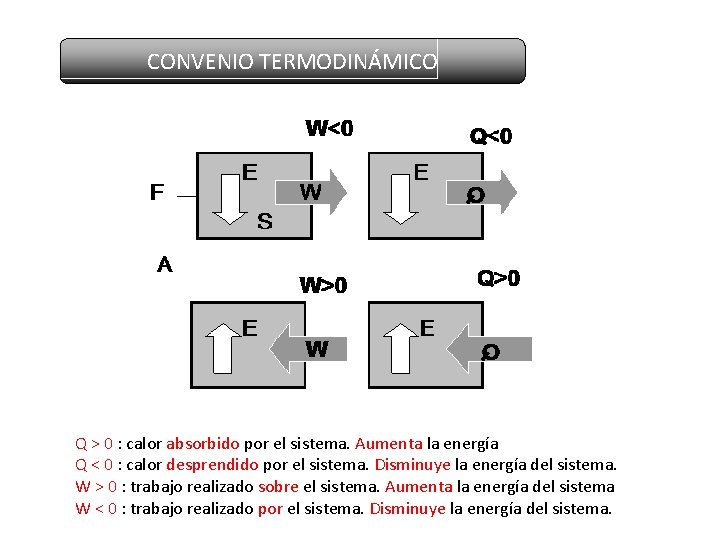
CONVENIO TERMODINÁMICO Q > 0 : calor absorbido por el sistema. Aumenta la energía Q < 0 : calor desprendido por el sistema. Disminuye la energía del sistema. W > 0 : trabajo realizado sobre el sistema. Aumenta la energía del sistema W < 0 : trabajo realizado por el sistema. Disminuye la energía del sistema.
Ejercicio Un sistema realiza un trabajo de 150 J sobre el entorno y absorbe 80 J de calor. Halla la variación de energía interna del sistema

Ejercicio solución

Trabajo en una reacción química Partimos de un recipiente de volumen variable ?

Consideraciones Si ΔV > 0, hay expansión del sistema y es él quien hace el trabajo. Por lo tanto W < 0 Si ΔV < 0, hay compresión del sistema y se hace un trabajo sobre él. Por lo tanto W > 0

Caso 1 PROCESO ISOCÓRICO ; V = cte (recipiente cerrado) ΔV = 0 W = - p. ΔV = 0 ΔU = Q + W ΔU = Qv + 0 ΔU = Qv El incremento de energía interna es igual al calor del proceso realizado a volumen constante.

Caso 2 • • PROCESO ISOBÁRICO ; P = cte (recipiente abierto) Concepto de ENTALPÍA p. V, tiene unidades de energía U, tiene unidades de energía, luego. . . U + p. V también. U + p. V es una energía que se define como ENTALPÍA = H El incremento de energía entalpía es igual al calor del proceso realizado a presión constante.

Caso 2 PROCESO ISOBÁRICO ; P = cte (recipiente abierto) Concepto de ENTALPÍA

Ejercicio nº 3 Para el proceso H 2 (g) + ½ O 2 (g) H 2 O (l) La variación de la energía interna a una temperatura de 25 o. C y una presión constante de 1 atm es ΔU = - 282 k. J. Determina ΔH a esa temperatura y presión. R = 8’ 31 J. o. K-1. mol-1

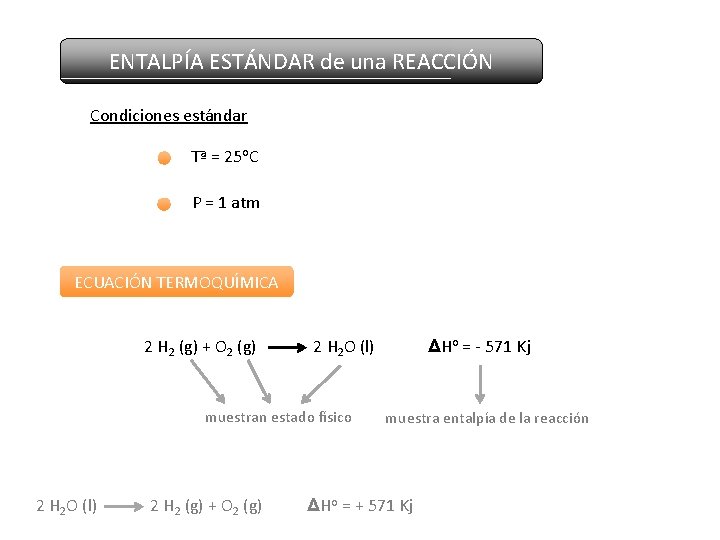
ENTALPÍA ESTÁNDAR de una REACCIÓN Condiciones estándar Tª = 25 o. C P = 1 atm ECUACIÓN TERMOQUÍMICA 2 H 2 (g) + O 2 (g) 2 H 2 O (l) muestran estado físico 2 H 2 O (l) 2 H 2 (g) + O 2 (g) ΔHo = - 571 Kj muestra entalpía de la reacción ΔHo = + 571 Kj
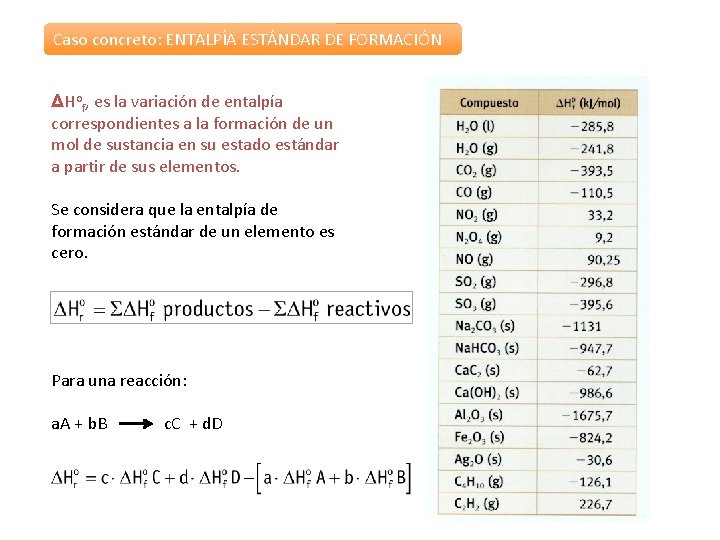
Caso concreto: ENTALPÍA ESTÁNDAR DE FORMACIÓN ΔHof, es la variación de entalpía correspondientes a la formación de un mol de sustancia en su estado estándar a partir de sus elementos. Se considera que la entalpía de formación estándar de un elemento es cero. Para una reacción: a. A + b. B c. C + d. D

Ejercicio nº 4 Dadas las entalpías de formación estándar: ΔHfo CO(g) = -110’ 5 k. J/mol ; ΔHfo CO 2(g) = -393’ 5 k. J/mol, halla ΔHfo para la reacción: CO (g) + ½ O 2 (g) CO 2 (g)


Caso concreto: ENTALPÍAS de ENLACE Una reacción química es, en realidad, una rotura de enlaces y la formación de otros. La entalpía estándar es un reacción es la suma de las entalpías de los enlaces rotos menos la suma de las entalpías d elos enlaces formados. consume energía produce energía

Actividad 22 Utilizando los valores de las entalpías de enlace que aparecen en la tabla, determina con carácter aproximado la entalpía estándar de cada una de las reacciones siguientes: a) Br 2 (g) + 3 F 2 (g) 2 Br. F 3 (g) b) CH 2 = CH 2 (g) + H 2 (g) CH 3 – CH 3 (g) c) C 2 H 5 OH (g) + 3 O 2 (g) 2 CO 2 (g) + 3 H 2 O (g)




Caso concreto: ENTALPÍAS de COMBUSTIÓN Una reacción de combustión es la reacción de un compuesto con el oxígeno. Si el compuesto sólo tiene O, C y H se producirá CO 2 y H 2 O Es la variación de energía que se produce cuando se quema un mol de sustancia en condiciones estándar Siempre son exotérmicas

Actividad 18 Formula la reacción de combustión del metano y calcula cuántos kilogramos de este gas deben quemarse en condiciones estándar para producir 2’ 7. 106 k. J de calor si se sabe que sólo se aprovecha el 75 % del calor obtenido en la combustión. (C = 12 ; H = 1) ΔHoc = -890 k. J. mol-1

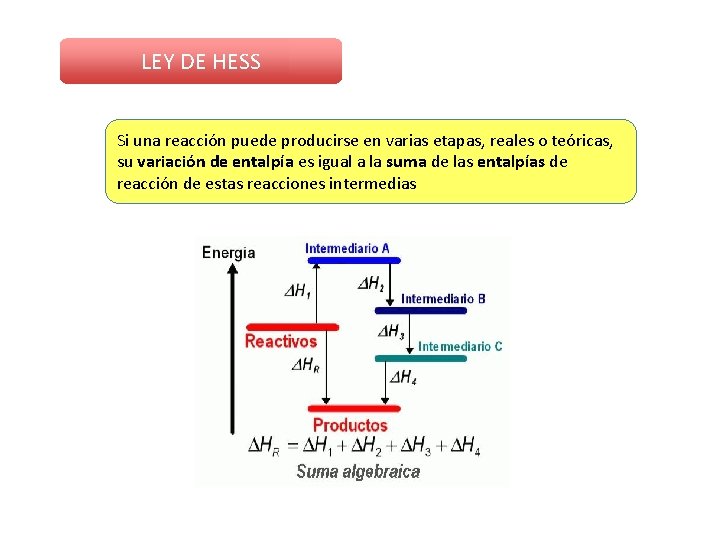
LEY DE HESS Si una reacción puede producirse en varias etapas, reales o teóricas, su variación de entalpía es igual a la suma de las entalpías de reacción de estas reacciones intermedias
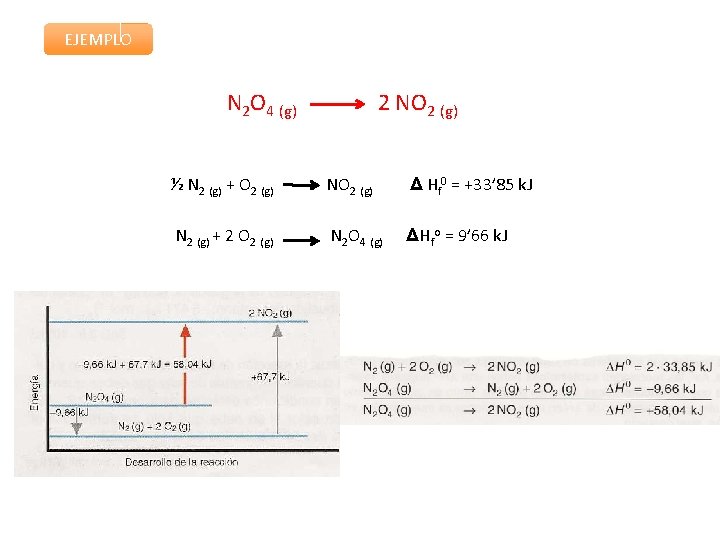
EJEMPLO N 2 O 4 (g) 2 NO 2 (g) ½ N 2 (g) + O 2 (g) NO 2 (g) Δ Hf 0 = +33’ 85 k. J N 2 (g) + 2 O 2 (g) N 2 O 4 (g) ΔHfo = 9’ 66 k. J

TQM - 2 Calcula el calor de reacción en el proceso: Zn. O (s) + CO (g) Zn (g) + CO 2 (g) ¿ ΔH? A partir de los siguientes datos: calor (entalpía) de formación del Zn. O(s) Δ H 1 = -83 Kcal/mol ; calor (entalpía) de vaporización del Zn, ΔH 2 = 32 Kcal/mol ; calor (entalpía) de combustión del CO, ΔH 3 = -68 Kcal


http: //about. me/profesorjano www. profesorjano. org www. profesorjano. com profesorjano@gmail. com
- Slides: 37