TERMOMETRIA CALORIMETRIA E TERMODIN MICA Aula 3 Maria




































- Slides: 44

TERMOMETRIA, CALORIMETRIA E TERMODIN MICA – Aula 3 Maria Augusta Constante Puget (Magu)

Temperatura e Calor (1) � Se tirarmos uma latinha de refrigerante da geladeira e a pusermos sobre a mesa da cozinha, sua temperatura aumentará, até que se iguale à do ambiente. Dizemos que, neste instante, foi atingido o equilíbrio térmico. � Da mesma forma, a temperatura de uma xícara de café quente, deixada sobre a mesa, cairá até atingir o mesmo valor da temperatura ambiente. � Generalizando, descrevemos o refrigerante ou o café como um sistema (com temperatura TS) e a cozinha como o ambiente (com temperatura TA) desse sistema. � Observa-se que se TS não for igual a TA, então TS variará (TA também pode variar um pouco) até que as duas temperaturas sejam iguais e, assim, o equilíbrio térmico seja alcançado. 2

Temperatura e Calor (2) � Tal variação na temperatura se deve à transferência de energia entre a energia interna do sistema e o ambiente que o cerca. � A energia transferida é chamada de calor e é simbolizada por Q. � Ou seja: Calor é a energia que um corpo transfere a outro como consequência exclusiva da diferença de temperatura entre eles. � O calor flui espontaneamente do corpo de maior para o de menor temperatura até que os dois atinjam o equilíbrio térmico. � Assim, calor é energia em trânsito. � Um corpo pode receber ou ceder calor, mas não pode contê-lo. O que o corpo contém é energia interna. 3

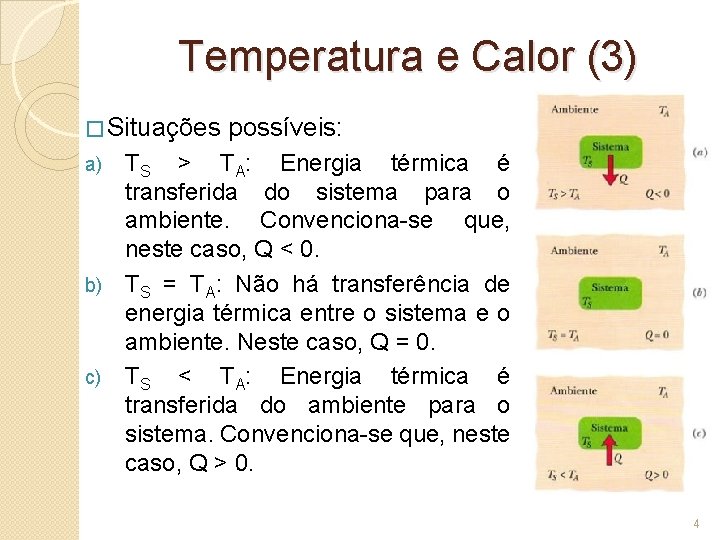
Temperatura e Calor (3) � Situações possíveis: TS > TA: Energia térmica é transferida do sistema para o ambiente. Convenciona-se que, neste caso, Q < 0. b) TS = TA: Não há transferência de energia térmica entre o sistema e o ambiente. Neste caso, Q = 0. c) TS < TA: Energia térmica é transferida do ambiente para o sistema. Convenciona-se que, neste caso, Q > 0. a) 4

Temperatura e Calor (4) � Vale lembrar que também podemos transferir energia entre um sistema e seu ambiente na forma de trabalho W, por meio de uma força atuando sobre o sistema. � Calor e trabalho, diferentemente da temperatura, da pressão e do volume, não são propriedades intrínsecas de um sistema. � Eles possuem significado apenas quando descrevem a transferência de energia para dentro ou para fora de um sistema. 5

Temperatura e Calor (5) �É apropriado dizer: Ø “Durante os últimos 3 minutos, foram transferidos 15 J de calor do ambiente para o sistema. ” Ø “Durante o último minuto, 12 J de trabalho foram realizados sobre o sistema pelo seu ambiente. ” � Não faz sentido dizer: Ø “Este sistema contém 450 J de calor. ” Ø “Este sistema contém 385 J de trabalho. ” 6

Calor (1) �O conceito de calor como uma forma de energia que flui de um corpo a outro devido a uma diferença de temperatura entre eles é recente. 7

Calor (2) � Antes de os cientistas se darem conta de que calor é energia em trânsito, o calor era definido em termos de sua capacidade de aumentar a temperatura da água. � Assim, a caloria (cal) foi definida como a quantidade de calor que elevaria a temperatura de 1 g de água de 14, 50 C para 15, 50 C. � No sistema britânico, a unidade correspondente era a unidade térmica britânica (Btu = British thermal unit), definida como a quantidade de calor que elevaria a temperatura de 1 lb de água de 630 F para 640 F. 8

Calor (3) � Em 1948, a comunidade científica decidiu que, já que o calor é energia transferida, a unidade SI para o calor deveria ser a mesma que é usada para energia, que é o joule. � A caloria atualmente é definida como sendo exatamente 4, 1860 J, sem qualquer referência ao aquecimento da água. � A caloria usada em nutrição é, na verdade, uma quilocaloria. � As relações entre as várias unidades de calor são: 1 cal = 3, 969 x 10 -3 Btu = 4, 1860 J 9

A Caloria Alimentar (1) �A quantidade de energia contida em um alimento é medida através da energia obtida pela sua queima. � Se queimarmos a mesma quantidade de pão e amendoim para aquecermos uma mesma quantidade de água, ao medirmos a temperatura da água no final da queima, perceberemos que ela ficará mais aquecida quando utilizamos o amendoim como combustível. � O amendoim libera mais energia na queima por ser constituído de menor quantidade de água e por possuir substâncias mais calóricas que o pão. 10

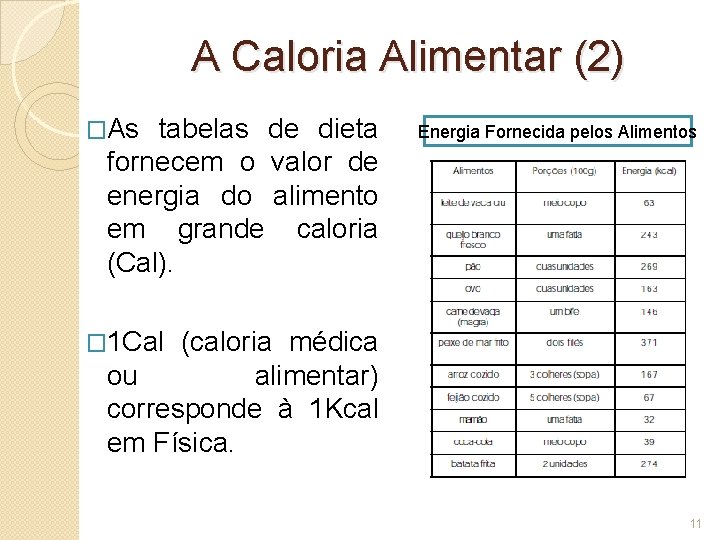
A Caloria Alimentar (2) �As tabelas de dieta fornecem o valor de energia do alimento em grande caloria (Cal). Energia Fornecida pelos Alimentos � 1 Cal (caloria médica ou alimentar) corresponde à 1 Kcal em Física. 11

A Caloria Alimentar (3) � Ao ingerirmos os alimentos, parte das substâncias entram na constituição celular e a outra parte fornece a energia necessária às nossas atividades. � Esse processo de liberação de energia se dá através da respiração: material orgânico + oxigênio => CO 2 + H 2 O + energia � Devido a diferenças no metabolismo, pessoas distintas absorvem quantidades variadas de energia ingerindo os mesmos alimentos. � A perda de energia ao realizar as mesmas atividades também é uma característica pessoal, dependendo do tamanho corporal e da eficiência dos movimentos. 12

Fontes de Calor (1) � Os fornos, fogões e aquecedores em geral têm seu funcionamento baseado na queima de um combustível. � Quando utilizamos combustíveis como gasolina, álcool, carvão, lenha, gás natural e outros, estamos transformando energia química em energia térmica. � O combustível mais utilizado nos fornos e fogões é o GLP (gás liquefeito de petróleo), contido em botijões de gás, que, ao ser liberado, entra em contato com o oxigênio do ar e, na presença de uma centelha, transforma energia química em energia térmica. Este processo recebe o nome de combustão. gás de cozinha + oxigênio -> CO 2 + H 2 O + calor 13

Fontes de Calor (2) �Os materiais queimam quando estão em contato com o ar e uma centelha são chamados combustíveis e o processo de queima é conhecido combustão. Calor de Combustão �A quantidade de calor liberada durante a queima completa de uma unidade de massa da substância combustível é denominada calor de combustão. 14

Absorção de Calor por Sólidos e Líquidos (1) Capacidade Calorífica ou Térmica �A capacidade calorífica (ou térmica) C de um objeto é a constante de proporcionalidade entre o calor Q que o objeto absorve ou perde e a variação de temperatura resultante T do objeto. Assim: Q = C T = C (Tf – Ti) onde: Tf, Ti: temperatura final e inicial do objeto, respectivamente. � A capacidade calorífica C possui unidade de energia por grau de temperatura. � A unidade usual é cal/°C. 15

Absorção de Calor por Sólidos e Líquidos (2) Calor Específico � Dois objetos feitos do mesmo material – por exemplo, o mármore – terão capacidades caloríficas proporcionais às suas massas. � Portanto, é conveniente definirmos uma “capacidade calorífica por unidade de massa” ou calor específico que se refere não a um objeto, mas a uma massa unitária do material do qual é feito o objeto. a equação Q = C T como: Q = c m T = c m (Tf – Ti) � Reescrevemos � Logo: C=mc 16

Absorção de Calor por Sólidos e Líquidos (3) Calor Específico � Do modo como a caloria e a Btu foram originalmente definidas, o calor específico da água é: c = 1 cal/(g∙ 0 C) = 1 Btu/(lb ∙ 0 F) = 4190 J/(kg∙K) �O calor específico de qualquer substância depende, de certa forma, da temperatura. Na tabela ao lado, tem-se os calores específicos para algumas substâncias à temperatura ambiente (os valores se aplicam bem a uma faixa de temperaturas próximas à temperatura ambiente). 17

Absorção de Calor por Sólidos e Líquidos (4) Calor Específico Molar � Em muitas situações a unidade mais conveniente para especificar a quantidade de uma substância é o mol, onde: 1 mol = 6, 02 x 1023 unidades elementares de qualquer substância. � Quando a quantidade da substância é expressa em mols, os calores específicos também devem envolver mols e são chamados de calores específicos molares. 18

Absorção de Calor por Sólidos e Líquidos (5) Calor Específico � Os gases possuem valores totalmente diferentes para os seus calores específicos sob condições de pressão constante e sob condições de volume constante, os quais são denominados, respectivamente, cp e cv. � As mudanças de volume de líquidos e sólidos, em virtude de aquecimento, são muito pequenas se comparadas às sofridas pelos gases. Por isso, os seus calores específicos a pressão e volume constante diferem em poucos por cento, de forma que, para eles, podemos considerar: c p = c v= c 19

Trocas de Calor (1) � Dois corpos A e B, colocados num recinto termicamente isolado, não trocam calor com o meio ambiente. � Se a temperatura de A é maior do que a de B, há transferência de calor do primeiro para o segundo, até que se estabeleça o equilíbrio térmico. � Como não há outros corpos trocando calor, se A perder, por exemplo, 50 cal nesse intervalo de tempo, B terá recebido exatamente 50 cal. � Pela convenção de sinais que se adota: QA = -50 cal QB = 50 cal 20

Trocas de Calor (2) � Sendo assim: QA = -QB ou QA + Q B = 0 �O princípio geral que descreve as trocas de calor pode ser então enunciado como: Se dois ou mais corpos trocam calor entre si, a soma algébrica das quantidades de calor trocadas pelos corpos, até o estabelecimento do equilíbrio térmico, é nula. 21

Calorímetros (1) � Geralmente, os corpos que trocam calor são colocados no interior de dispositivos especiais denominados calorímetros, isolados termicamente do meio exterior. � O calorímetro participa das trocas de calor, embora na maioria dos casos, essa participação seja pouco acentuada. � No entanto, quando o calorímetro absorve uma quantidade de calor considerável, deve-se levar em conta sua capacidade térmica C, expressa pela relação entre o calor absorvido Q e a variação de temperatura que ele sofre C = Q/ T. 22

Estados de Agregação (1) �No universo, a matéria pode se apresentar em diversos estados de agregação. �A tabela a seguir descreve as características macroscópicas e microscópicas dos estados sólido, líquido e gasoso. Sólido Líquido Gasoso Característic as Macroscópic as Volume próprio; Forma própria. Forma do recipiente. Volume do recipiente; Forma do recipiente. Característic as Microscópica s Arranjo denominado retículo cristalino; Forças de coesão intensas entre as partículas. Partículas muito distanciadas com grande liberdade de movimentação; Interações intensas apenas colisões. 23 Estrutura caótica; Forças menos intensas entre as partículas.

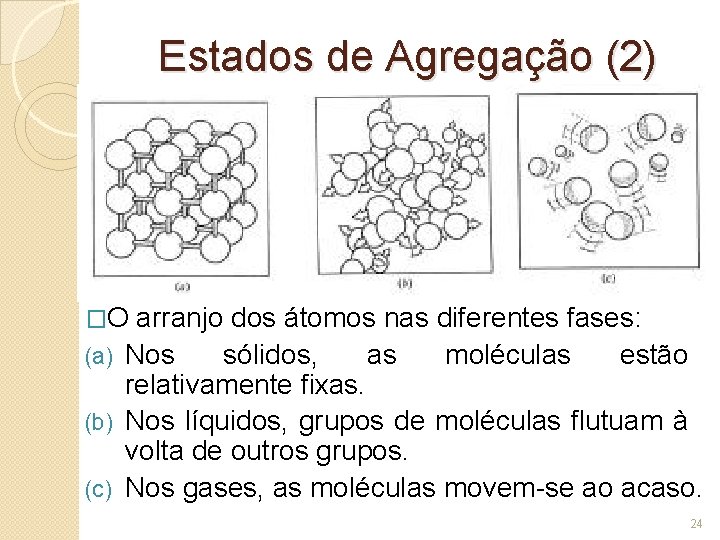
Estados de Agregação (2) �O arranjo dos átomos nas diferentes fases: (a) Nos sólidos, as moléculas estão relativamente fixas. (b) Nos líquidos, grupos de moléculas flutuam à volta de outros grupos. (c) Nos gases, as moléculas movem-se ao acaso. 24

Estados de Agregação (3) Ferro líquido: a fusão do ferro ocorre a 1535°C, sob pressão normal. Nitrogênio líquido: a condensação do nitrogênio ocorre a 195, 8°C, sob pressão normal. 25

E o vidro, o que é ? (1) �O vidro é um material inorgânico que possui a sílica como elemento básico. � Para ser considerado um sólido o vidro teria que apresentar estrutura cristalina definida, o que não é o caso, pois não possui estrutura microscópica periodicamente organizada. � É o que chamamos de sólido amorfo, ou um líquido com viscosidade muito elevada. � Há relatos de que o vidro escorre, feitos com base nos vitrais das catedrais antigas, onde existe uma diferença de grossura no topo e na base dos mesmos. Mas não existe uma confirmação científica sobre este acontecimento. 26

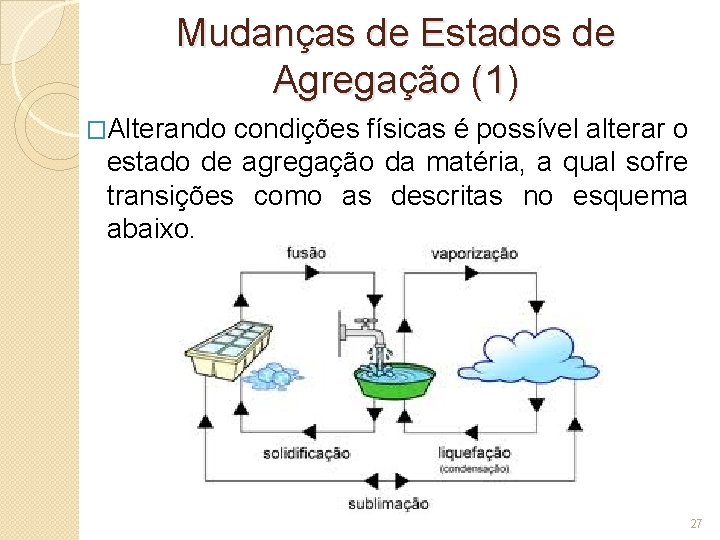
Mudanças de Estados de Agregação (1) �Alterando condições físicas é possível alterar o estado de agregação da matéria, a qual sofre transições como as descritas no esquema abaixo. 27

Mudanças de Estados de Agregação (2) � Quando um sólido ou um líquido absorve energia na forma de calor, a temperatura da amostra não se eleva necessariamente. � Ao invés disso, a amostra pode mudar de uma fase ou estado para outro. � Assim, por exemplo, se fornecemos calor a um sólido, aumentamos sua energia interna, a energia cinética das moléculas e, macroscopicamente, sua temperatura. � Em um dado instante, à temperatura de fusão, a energia fornecida passa a romper as ligações entre as moléculas. Enquanto isso ocorre, a energia fornecida não altera a energia cinética das moléculas, pois a temperatura permanece constante, mas há alteração na energia potencial de agregação (alteração das ligações). 28

Mudanças de Estados de Agregação (3) �Fundir um sólido significa mudá-lo do estado sólido para o estado líquido. O processo exige energia porque as moléculas precisam ser liberadas de sua estrutura rígida. Ex: Derreter um cubo de gelo para formar água líquida. �Solidificar um líquido é o processo inverso da fusão e exige que se remova energia do líquido, de modo que as moléculas possam se acomodar em uma estrutura rígida. 29

Mudanças de Estados de Agregação (4) �Vaporizar um líquido significa mudá-lo do estado líquido para o estado gasoso. Este processo exige energia, pois as moléculas do líquido precisam ser liberadas de seus agrupamentos. Ex: Ferver água líquida para transformá-la em vapor d’água. �Condensar um gás para formar um líquido é o processo inverso da vaporização e exige que se remova energia do gás, de modo que as moléculas possam se agrupar ao invés de se afastarem umas das outras. 30

Mudanças de Estados de Agregação (5) �Sublimação é a mudança do estado sólido para o estado gasoso, sem passar pelo estado líquido. �A sublimação à temperatura ambiente é característica de substâncias que possuem pressão de vapor no ponto de fusão maior que a pressão atmosférica. �A naftalina, assim como o iodo são bons exemplos de substâncias sublimáveis à 31 temperatura ambiente.

Calor de Transformação ou Latente (1) Calor latente L de uma mudança de fase é a quantidade de calor que a substância recebe (ou cede), por unidade de massa, durante a transformação, mantendo-se constante a temperatura. �Assim, quando uma amostra de massa m sofre completamente uma mudança de fase, a energia total transferida é: Q=Lm 32

Calor de Transformação ou Latente (2 ) � Para um corpo que recebe calor, a quantidade de calor trocado, por convenção, é positiva (Q > 0) e, para aquele que cede calor, a quantidade trocada é negativa (Q < 0). � Assim, o calor latente poderá ser positivo ou negativo, conforme a mudança de fase ocorra com ganho ou perda de calor. � Quando a mudança de fase é de líquido para gás ou de gás para líquido, o calor de transformação é denotado LV (calor latente de vaporização ou de liquefação, dependendo do sentido da mudança de fase). Por exemplo: q. Vaporização da água (a 1000 C) LV = 539 cal/g q. Condensação do vapor (a 1000 C) LV = -539 cal/g 33

Calor de Transformação ou Latente (3) �Quando a mudança de fase é de sólido para líquido ou de líquido para sólido, o calor de transformação é denotado LF (calor latente de fusão ou de solidificação, dependendo do sentido da mudança de fase). �Para a água, por exemplo, à sua temperatura normal de congelamento ou de liquefação: q. Fusão do gelo (a 00 C) LF = 80 cal/g q. Solidificação da água (a 00 C) LF = -80 cal/g 34

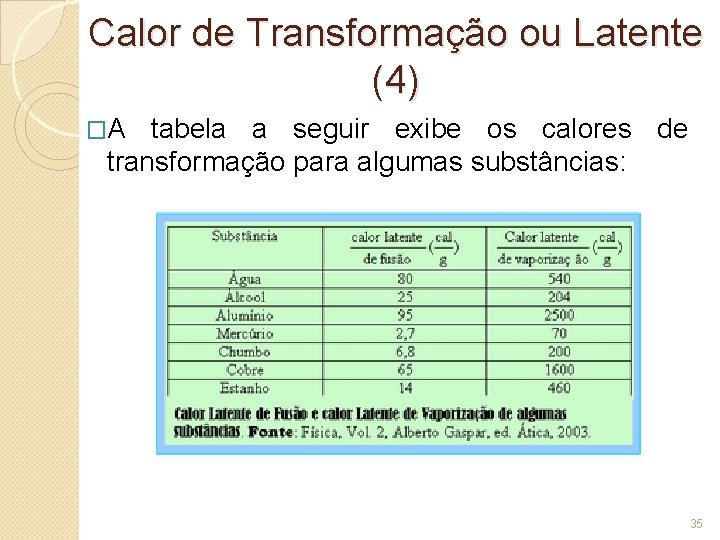
Calor de Transformação ou Latente (4 ) �A tabela a seguir exibe os calores de transformação para algumas substâncias: 35

Curvas de Aquecimento e de Resfriamento (1) � Suponhamos que temos, em um recipiente, uma certa massa de gelo inicialmente a -30 C, sob pressão normal. � Se levarmos este sistema ao fogo, acompanhando como varia a temperatura no decorrer do tempo, veremos que o processo todo pode ser dividido em cinco etapas distintas: A. Aquecimento do gelo de -30 C a 00 C. B. Fusão do gelo a 00 C. C. Aquecimento da água líquida de 00 C a 1000 C. D. Vaporização da água líquida a 1000 C. E. Aquecimento do vapor acima de 1000 C (possível somente se o confinarmos em um recipiente adequado). 36

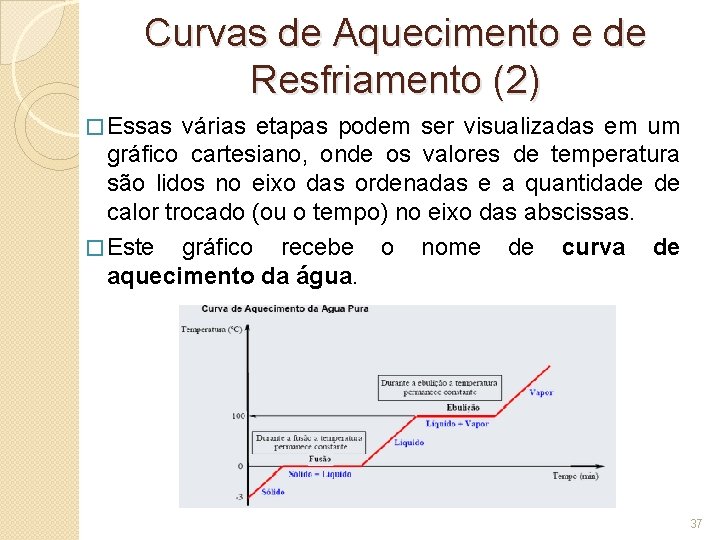
Curvas de Aquecimento e de Resfriamento (2) � Essas várias etapas podem ser visualizadas em um gráfico cartesiano, onde os valores de temperatura são lidos no eixo das ordenadas e a quantidade de calor trocado (ou o tempo) no eixo das abscissas. � Este gráfico recebe o nome de curva de aquecimento da água. 37

Curvas de Aquecimento e de Resfriamento (3) �É importante notarmos dois patamares de temperatura: ◦ Um corresponde ao ponto de fusão. ◦ Outro ao de ebulição. � Durante o processo de solidificação ou liquefação, assim como no de condensação ou vaporização, a temperatura permanece constante. � Em temperaturas inferiores ao ponto de fusão a amostra é sólida. � Em temperatura entre o ponto de fusão e o de ebulição é líquida. � Em temperaturas acima do ponto de ebulição a amostra é gasosa. � Exatamente no ponto de fusão coexistem as fases sólida e líquida. � Exatamente no ponto de ebulição coexistem as fases líquida e gasosa. 38

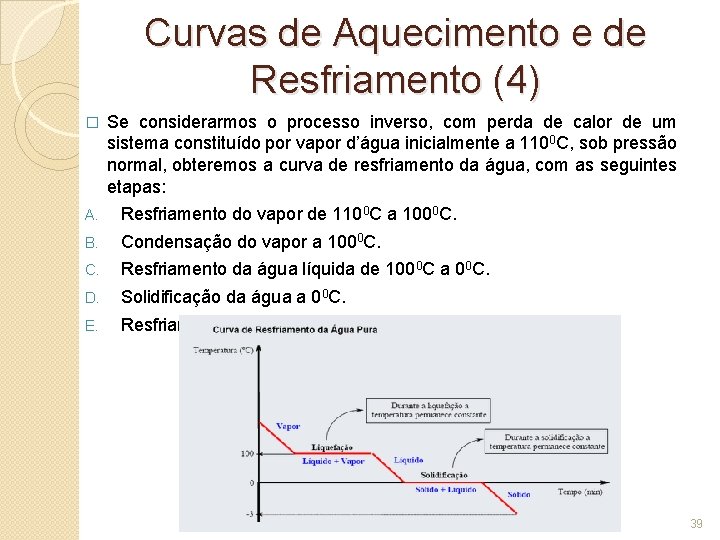
Curvas de Aquecimento e de Resfriamento (4) � Se considerarmos o processo inverso, com perda de calor de um sistema constituído por vapor d’água inicialmente a 1100 C, sob pressão normal, obteremos a curva de resfriamento da água, com as seguintes etapas: A. Resfriamento do vapor de 1100 C a 1000 C. B. Condensação do vapor a 1000 C. Resfriamento da água líquida de 1000 C a 00 C. D. Solidificação da água a 00 C. E. Resfriamento do gelo abaixo de 00 C. 39

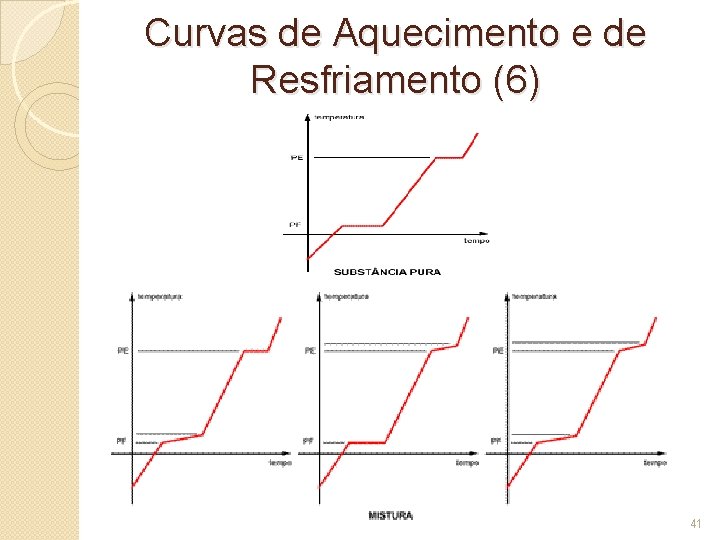
Curvas de Aquecimento e de Resfriamento (5) �O levantamento da curva de aquecimento (resfriamento) também nos dá outra informação importante: Nos diz se nossa amostra é uma substância pura ou uma mistura. � Como? Pela análise dos patamares que se formam no PF (ponto de fusão) e PE (ponto de ebulição): 1. Se ambos - PF e PE - apresentarem temperatura constante podemos afirmar que a amostra é uma substância pura. 2. Se um deles ou os dois apresentarem variação, trata -se de uma mistura. 40

Curvas de Aquecimento e de Resfriamento (6) 41

Curvas de Aquecimento e de Resfriamento (7) Classificando as misturas � Uma vez identificada que a amostra é uma mistura, analisando a curva de aquecimento podemos ainda classificá -la como: 1. Simples: Quando a mistura apresenta variação nos dois patamares, PF e PE. Quando a variação é em apenas um patamar, ou seja, apenas o PE ou o PF variam, a classificação é a seguinte: 2. Eutética: PF constante. 3. Azeotrópica: PE constante. �O exemplo mais comum de mistura eutética é a solda utilizada em eletrônica (37% chumbo e 63% estanho) e o de mistura azeotrópica é a mistura água e álcool (4% água e 96% álcool - álcool 96 GL). 42

Substância Pura X Mistura (1) �Substância pura: É uma substância que tem composição química fixa, homogênea e invariável (no entanto pode estar presente mais que um tipo de moléculas). �Pode existir em mais de uma fase, mas a composição química é a mesma em todas as fases. �O AR nessa definição é considerado uma substância pura. 43

Substância Pura X Mistura (2) Outros exemplos de substância pura: �Água (fases - sólida, líquida, e vapor). �Mistura de água líquida e vapor d’água. �Dióxido de Carbono (CO 2). �Nitrogênio (N 2). �Misturas homogêneas de gases, como o AR, desde que não ocorra mudança de fases. 44