TERMOKIMIA STANDAR KOMPETENSI Memahami perubahan energi dalam reaksi

TERMOKIMIA

STANDAR KOMPETENSI Memahami perubahan energi dalam reaksi kimia dan cara pengukurannya.

KOMPETENSI DASAR Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm, dan reaksi endoterm.

Indikator • Menjelaskan hukum/azas kekekalan energi • Membedakan sistem dan lingkungan • Membedakan reaksi eksoterm dan endoterm melalui percobaan • Menjelaskan macam-macam perubahan entalpi

AZAS KEKEKALAN ENERGI

1. Sistem dan Lingkungan ► Sistem ► Lingkungan ► Sistem terbuka ► Sistem tertutup ► Sistem terisolasi
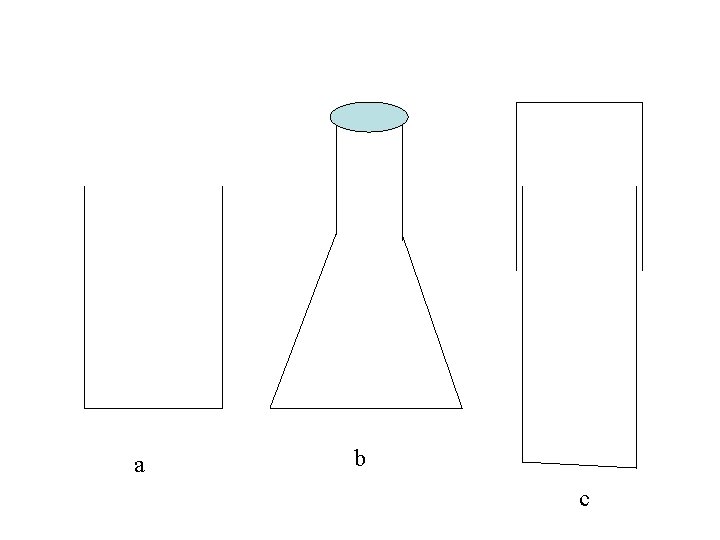
a b c

2. Energi Dalam (E) ► Energi kinetik ► Energi potensial ► Energi dalam ► Energi termal ► Energi kimia
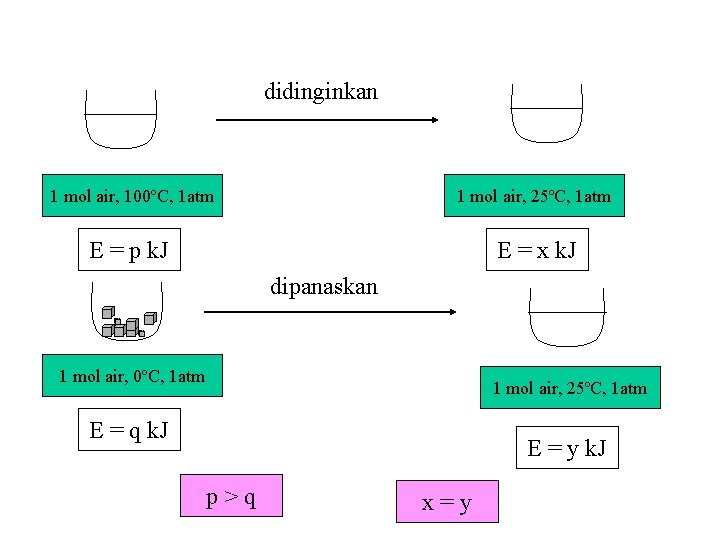
didinginkan 1 mol air, 100ºC, 1 atm 1 mol air, 25ºC, 1 atm E = p k. J E = x k. J dipanaskan 1 mol air, 0ºC, 1 atm 1 mol air, 25ºC, 1 atm E = q k. J E = y k. J p>q x=y

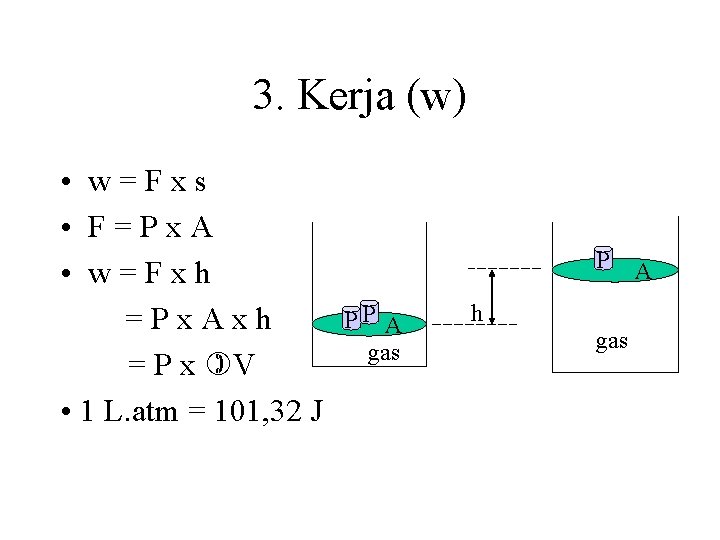
3. Kerja (w) • w=Fxs • F=Px. A • w=Fxh =Px. Axh = P x V • 1 L. atm = 101, 32 J P PP A gas h gas A
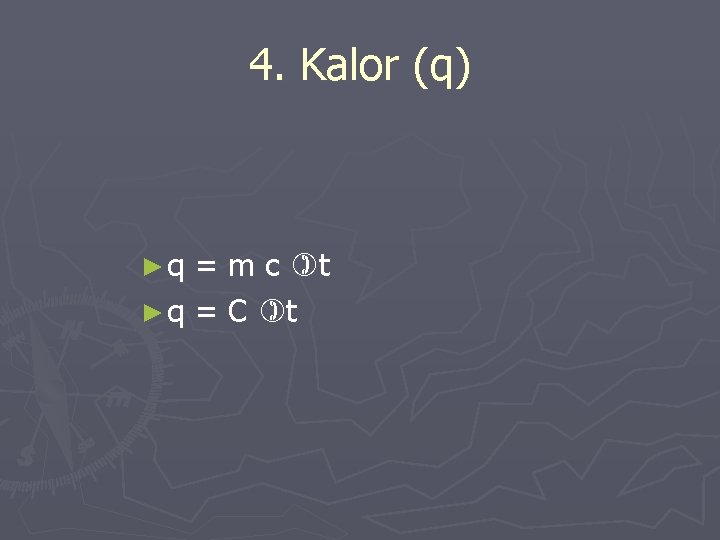
4. Kalor (q) ►q = m c t ► q = C t

5. Hukum Pertama Termodinamika (Azas Kekekalan Energi) ► Energi dapat diubah tetapi tidak dapat dimusnahkan atau diciptakan. ► E = q + w ► Sistem menerima kalor, q bertanda + ► Sistem membebaskan kalor, q bertanda – ► Sistem melakukan kerja, w bertanda – ► Sistem menerima kerja, w bertanda +
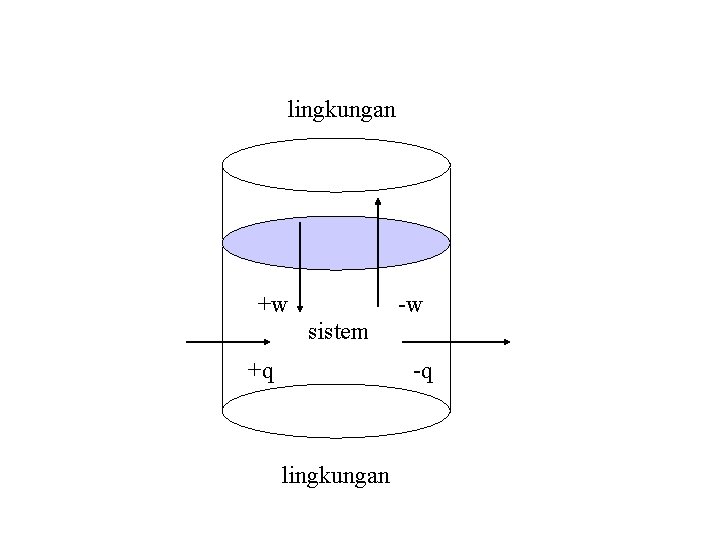
lingkungan +w -w sistem +q -q lingkungan
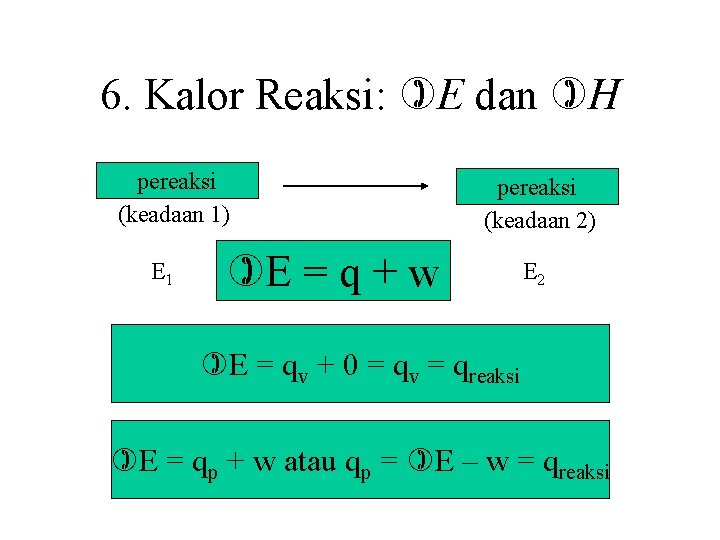
6. Kalor Reaksi: E dan H pereaksi (keadaan 1) E 1 pereaksi (keadaan 2) E = q + w E 2 E = qv + 0 = qv = qreaksi E = qp + w atau qp = E – w = qreaksi
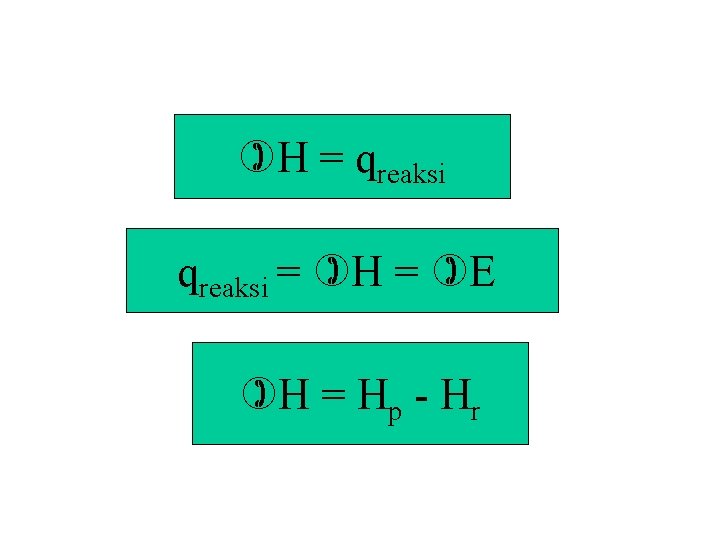
H = qreaksi = H = E H = Hp - Hr
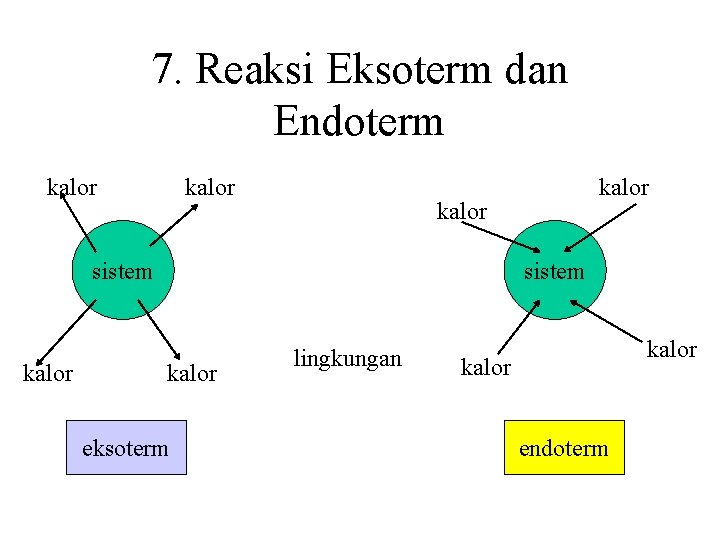
7. Reaksi Eksoterm dan Endoterm kalor sistem kalor eksoterm lingkungan kalor endoterm

Reaksi Endoterm: H = Hp – Hr > 0 Reaksi Eksoterm: H = Hp – Hr < 0
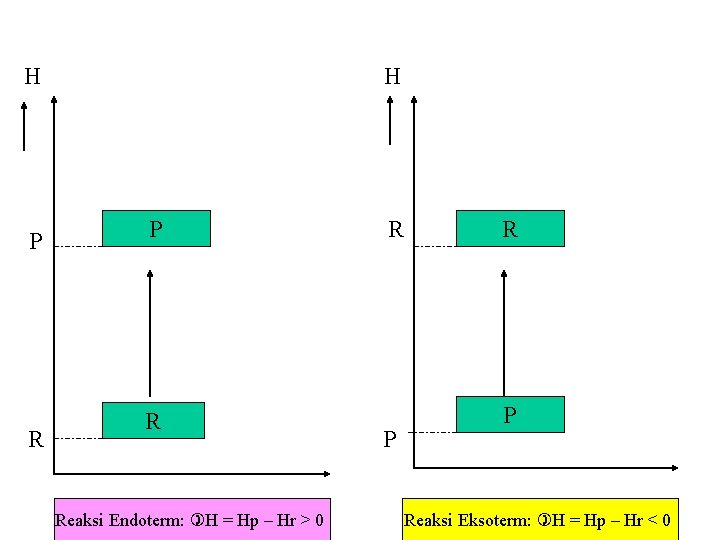
H P R Reaksi Endoterm: H = Hp – Hr > 0 R P Reaksi Eksoterm: H = Hp – Hr < 0

8. Persamaan Termokimia + 1/2 O 2(g) H 2 O(l) ► 2 H 2(g) + O 2(g) 2 H 2 O(l) ► H 2(g) H= -286 k. J H= -572 k. J 1/2 N 2(g) + 3/2 H 2(g) H= +46 k. J ► 2 NH 3(g) N 2(g) + 3 H 2(g) H= +92 k. J ► NH 3(g)
- Slides: 20