TERMOKIMIA Kimia SMK KELAS XI SEMESTER 2 SMKN




























- Slides: 32

TERMOKIMIA Kimia SMK KELAS XI SEMESTER 2 SMKN 7 BANDUNG

SK DAN KD Standar Kompetensi v Menentukan perubahan entalpi berdasarkan konsep termokimia Kompetensi Dasar v Menjelaskan entalpi dan perubahan entalpi v Menentukan perubahan entalpi reaksi v Menentukan kalor pembakaran berbagai bahan bakar Hal. : 2 Isi dengan Judul Halaman Terkait Adaptif

TUJUAN PEMBELAJARAN 1. Siswa mampu mendefinisikan pengertian istilah- istilah dalam reaksi termokimia beserta contohnya 2. Siswa mampu menjelaskan pengertian entalpi suatu zat dan perubahannnya. 3. Siswa mampu menentukan ΔH reaksi berdasarkan hukum Hess, data perubahan entalpi pembentukan standar, eksperimen data energi ikatan Hal. : 3 Isi dengan Judul Halaman Terkait Adaptif

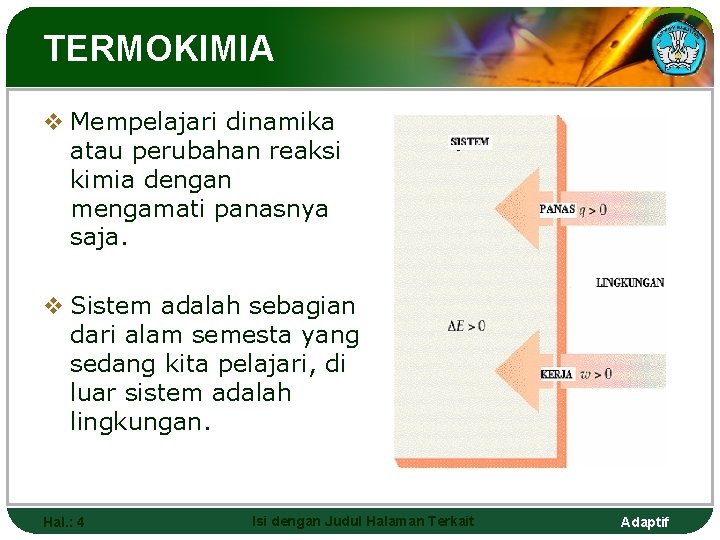
TERMOKIMIA v Mempelajari dinamika atau perubahan reaksi kimia dengan mengamati panasnya saja. v Sistem adalah sebagian dari alam semesta yang sedang kita pelajari, di luar sistem adalah lingkungan. Hal. : 4 Isi dengan Judul Halaman Terkait Adaptif

1. ENTALPI (H) DAN PERUBAHAN ENTALPI (ΔH) v. Nama lain dari entalpi adalah panas v. Panas reaksi pada tekanan tetap disebut perubahan entalpi dan reaksi dan diberikan dengan simbol ΔH. ΔH = H akhir – H mula Hal. : 5 Isi dengan Judul Halaman Terkait Adaptif

REAKSI EKSOTERM v Pada reaksi eksoterm terjadi perpindahan kalor dari sistem ke lingkungan atau pada reaksi tersebut dikeluarkan panas. v Pada reaksi eksoterm harga ΔH = negatif Contoh : C(s) + O(g) CO(g) + 393, 5 k. J ΔH = -393, 5 k. J Hal. : 6 Isi dengan Judul Halaman Terkait Adaptif

REAKSI ENDOTERM v Pada reaksi terjadi perpindahan kalor dari lingkungan ke sistem atau pada reaksi tersebut dibutuhkan panas. v Pada reaksi endoterm harga ΔH = positif Contoh : Ca. CO 3 (s) Ca. O (s) + CO 2 (g) -178, 5 KJ ΔH = +178, 5 KJ Hal. : 7 Isi dengan Judul Halaman Terkait Adaptif

3. PERUBAHAN ENTALPI STANDAR (ΔH 0) Perubahan entalpi reaksi diukur pada temperatur 298°K dan tekanan 1 atm disepakati sebagai entalpi standar, dinyatakan dengan simbol ΔH° Hal. : 8 Isi dengan Judul Halaman Terkait Adaptif

JENIS PERUBAHAN ENTALPI STANDAR 1. Perubahan Entalpi Pembentukan Standar (ΔHf ) (ΔHf = standar enthalpy of formation) v ΔH untuk membentuk 1 mol persenyawaan langsung dari unsurnya yang diukur pada 298 K dan tekanan 1 atm contoh : Hal. : 9 Isi dengan Judul Halaman Terkait Adaptif

2. Perubahan Entalpi Penguraian Standar (ΔHd)(ΔHd=standar enthalpy of decomposition) v ΔHd dari penguraian 1 mol persenyawaan langsung menjadi unsur-unsurnya (Kebalikan dari ΔH pembentukan) Contoh : Hal. : 10 Isi dengan Judul Halaman Terkait Adaptif

3. Perubahan Entalpi Pembakaran Standar ( ΔHc)(ΔHc = standar enthalpy Of combustion) v ΔH untuk membakar 1 mol persenyawaan dengan O 2 dari udara yang diukur pada 298 K dan tekanan 1 atm. Contoh : Hal. : 11 Isi dengan Judul Halaman Terkait Adaptif

4. ENTALPI REAKSI v ΔH dari suatu persamaan reaksi di mana zat-zat yang terdapat dalam persamaan reaksi dinyatakan dalam satuan mol dan koefisien persamaan reaksi bulat sederhana. Contoh : Hal. : 12 Isi dengan Judul Halaman Terkait Adaptif

5. ENTALPI NETRALISASI v ΔH yang dihasilkan (selalu eksoterm) pada reaksi penetralan asam atau basa. Contoh : Hal. : 13 Isi dengan Judul Halaman Terkait Adaptif

6. HUKUM LAVOISIER-LAPLACE "Jumlah kalor yang dilepaskan pada pembentukan 1 mol zat dari unsur-unsurnya sama dengan jumlah kalor yang diperlukan untuk menguraikan zat tersebut menjadi unsur-unsur pembentuknya. " Artinya : Apabila reaksi dibalik maka tanda kalor yang terbentuk juga dibalik dari positif menjadi negatif atau sebaliknya. Hal. : 14 Isi dengan Judul Halaman Terkait Adaptif

Contoh : Hal. : 15 Isi dengan Judul Halaman Terkait Adaptif

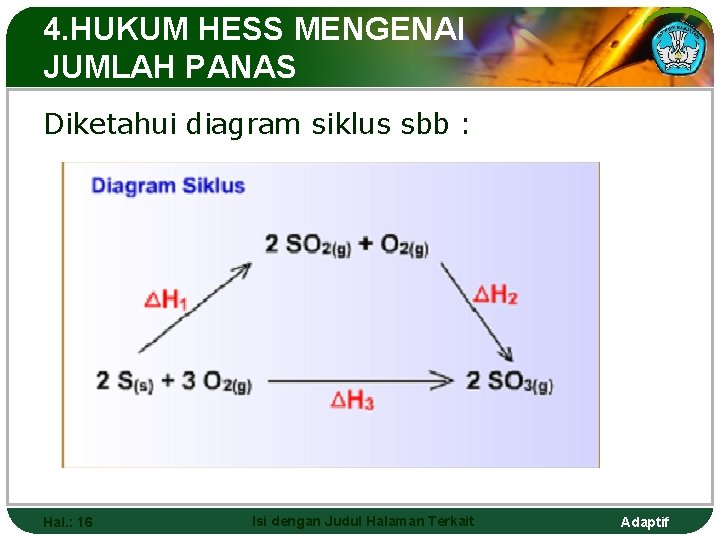
4. HUKUM HESS MENGENAI JUMLAH PANAS Diketahui diagram siklus sbb : Hal. : 16 Isi dengan Judul Halaman Terkait Adaptif

Maka reaksinya bisa digambarkan sbb : Hal. : 17 Isi dengan Judul Halaman Terkait Adaptif

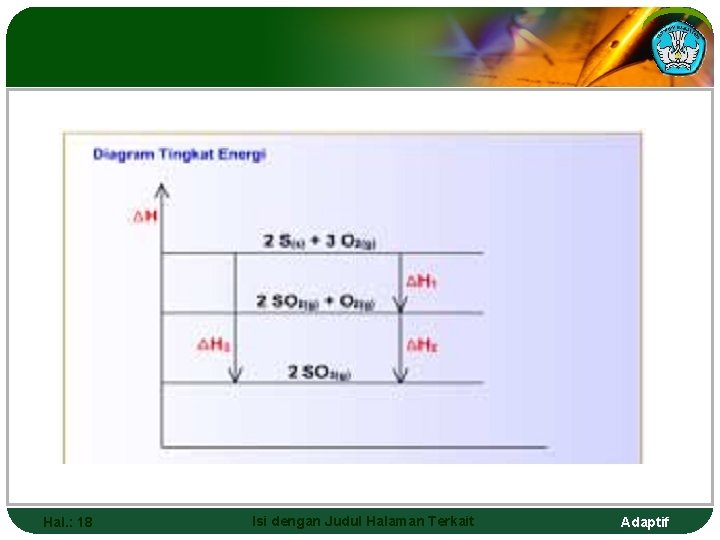
Hal. : 18 Isi dengan Judul Halaman Terkait Adaptif

v Entalpi adalah fungsi keadaan, maka besaran ΔH dari reaksi kimia tak tergantung dari lintasan yang dijalani pereaksi untuk membentuk hasil reaksi. Hal. : 19 Isi dengan Judul Halaman Terkait Adaptif

TAHAP-TAHAP REAKSI Hal. : 20 Isi dengan Judul Halaman Terkait Adaptif

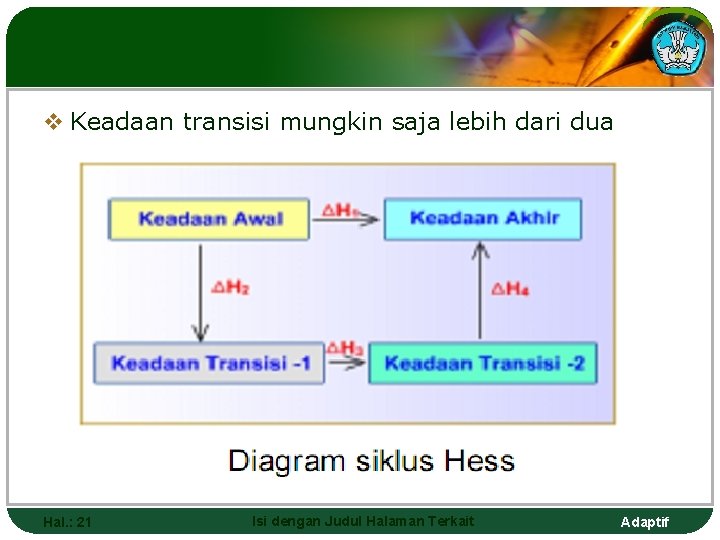
v Keadaan transisi mungkin saja lebih dari dua Hal. : 21 Isi dengan Judul Halaman Terkait Adaptif

CONTOH SOAL Buatlah diagram siklus dan diagram tingkat energinya! Hal. : 22 Isi dengan Judul Halaman Terkait Adaptif

Hal. : 23 Isi dengan Judul Halaman Terkait Adaptif

ENTALPI PEMBENTUKAN STANDAR Hal. : 24 Isi dengan Judul Halaman Terkait Adaptif

v Dalam mengerjakan perhitungan ini, kita anggap ΔH 0 f untuk setiap unsur pada keadaan murninya paling stabil pada suhu 250 C dan 1 atm = 0. Harga panas pembentukan standar untuk tiap elemen, ΔH 0 f = 0 Hal. : 25 Isi dengan Judul Halaman Terkait Adaptif

KAPASITAS PANAS DAN PANAS SPESIFIK v Kapasitas panas merupakan jumlah panas yang diperlukan untuk mengubah suhu temperatur suatu benda sebesar 10 C. v Panas spesifik merupakan jumlah panas yang diperlukan untuk menaikkan suhu 1 gram zat sebesar 10 C. v Contoh: panas spesifik (kalor jenis) air 4, 18 j/g 0 C, panas spesifik besi 0, 452 j/g 0 C Hal. : 26 Isi dengan Judul Halaman Terkait Adaptif

v. Rumus q = m. c. ΔT Keterangan q = jumlah kalor (joule) m = massa zat (gram) ΔT = perubahan suhu (takhir – tawal) c = kalor jenis Hal. : 27 Isi dengan Judul Halaman Terkait Adaptif

KALORIMETER v Kalorimeter adalah alat yang digunakan untuk mengukur panas reaksi Hal. : 28 Isi dengan Judul Halaman Terkait Adaptif

ENERGI IKATAN DAN ENTALPI REAKSI v Energi ikatan adalah energi yang diperlukan untuk memutuskan ikatan kimia dalam 1 mol senyawa Contoh : v Hitung energi ikatan jika entalpi pembentukan NH 3 adalah -46 k. J , energi ikatan H-H =436 k. J , energi ikatan N-H = 390 k. J , berapakah energi ikatan NΞN? Hal. : 29 Isi dengan Judul Halaman Terkait Adaptif

JAWAB Hal. : 30 Isi dengan Judul Halaman Terkait Adaptif

Hal. : 31 Isi dengan Judul Halaman Terkait Adaptif

Terimakasih Hal. : 32 Isi dengan Judul Halaman Terkait Adaptif