TERMOKIMIA ENTALPI PERUBAHANNYA REAKSI EKSOTERM REAKSI ENDOTERM DIANA

TERMOKIMIA ENTALPI & PERUBAHANNYA REAKSI EKSOTERM REAKSI ENDOTERM DIANA ANDRIANI MM. , MT 1

Termokimia Penerapan hukum pertama termodinamika terhadap peristiwa kimia disebut termokimia yang membahas perubahan kalor yang menyertai suatu reaksi kimia. 2

Energi Setiap sistem atau zat mempunyai energi yang tersimpan di dalamnya. Energi dibedakan menjadi 2 yaitu : 1. Energi kinetik adalah energi yang terdapat didalam materi yang bergerak. 2. Energi potensial adalah energi yang terdapat pada materi yang tidak bergerak. 3

Bentuk Energi Beberapa bentuk energi yang dikenal, yaitu energi kalor, energi kimia, energi listrik, energi cahaya, energi bunyi dan energi mekanik. Hukum kekekalan energi : energi tidak dapat diciptakan atau dimusnahkan. Artinya, suatu bentuk energi dapat diubah menjadi bentuk energi lain, tetapi tidak pernah ada energi yang hilang atau bertambah. 4

Entalpi (H) Entalpi atau kalor adalah jumlah dari semua bentuk energi dalam suatu zat, dinyatakan dengan H. Misalnya entalpi untuk uap air ditulis H H 2 O(g). Entalpi akan tetap konstan selama tidak ada energi yang masuk atau keluar dari zat. Besarnya entalpi tidak dapat ditentukan. 5

Perubahan Entalpi (ΔH) Perubahan entalpi (∆H) adalah perubahan kalor yang terjadi pada suatu rekasi kimia. ∆H merupakan selisih antara entalpi produk (HP) dan entalpi reaktan (HR). Rumus : ∆H = HP - HR 6

Ketentuan Entalpi (H) dan Perubahan Entalpi (ΔH) Jika H produk lebih kecil daripada H reaktan maka akan terjadi pembebasan kalor. Harga ∆H negatif atau lebih kecil daripada nol. 2 H 2 + O 2 2 H 2 O + kalor 2 H 2 + O 2 2 H 2 O ∆H = Jika H produk lebih besar daripada H reaktan maka akan terjadi penyerapan kalor. Harga ∆H positif atau lebih besar daripada nol. 2 H 2 O + kalor 2 H 2 + O 2 2 H 2 O 2 H 2 + O 2 - kalor 2 H 2 O 2 H 2 + O 2 ∆H = + 7

Reaksi Eksoterm dan Reaksi Endoterm Reaksi eksoterm adalah reaksi yang melepaskan kalor dari sistem ke lingkungan sehingga kalor dari sistem akan berkurang. Tanda reaksi eksoterm ∆H = Reaksi endoterm adalah reaksi yang menyerap kalor dari lingkungan ke sistem sehingga kalor dari sistem akan bertambah. Tanda reaksi endoterm ∆H = + 8
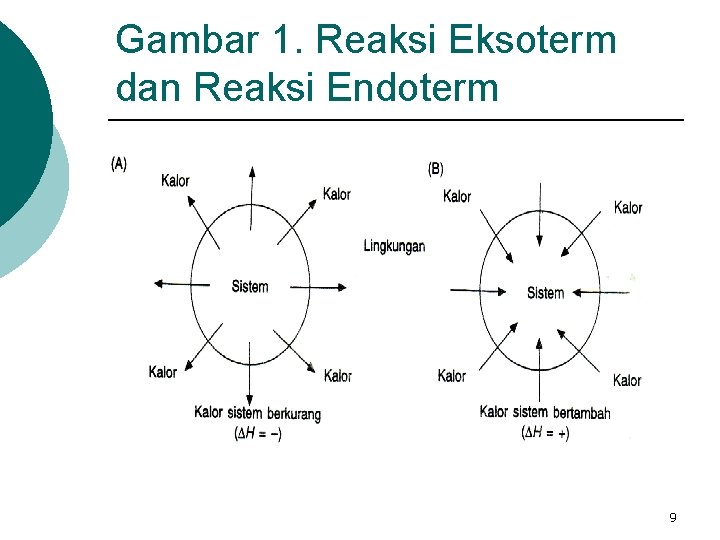
Gambar 1. Reaksi Eksoterm dan Reaksi Endoterm 9
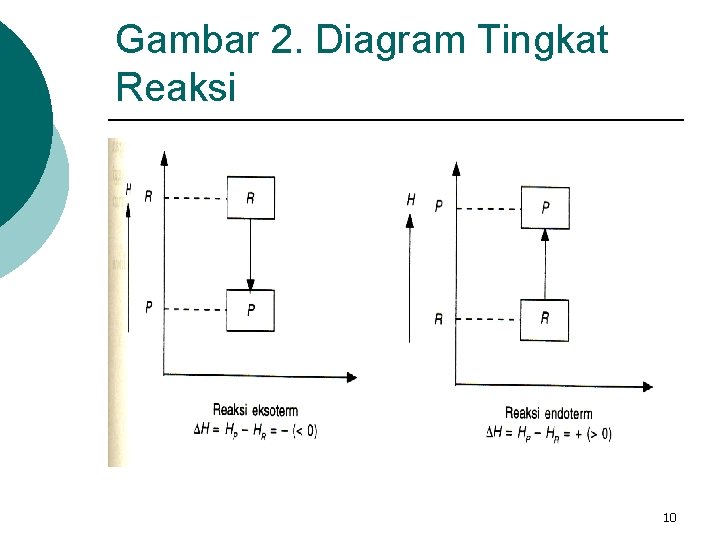
Gambar 2. Diagram Tingkat Reaksi 10

Perubahan Entalpi Standar (∆H˚) Perubahan entalpi reaksi yang diukur pada temperatur 298 K dan tekanan 1 atmosfer disepakati sebagai perubahan entalpi standar. Persamaan Termokimia. Persamaan termokimia adalah persamaan reaksi yang dilengkapi dengan harga perubahan entalpi (∆H). Persamaan termokimia selain menyatakan jumlah mol reaktan dan jumlah mol produk, juga menyatakan jumlah kalor yang dibebaskan atau diserap pada reaksi itu dalam satuan k. J atau dalam molar k. J/mol. 11

Contoh Soal Persamaan Termokimia 1. Reaksi 1 mol gas metana dengan 2 mol gas oksigen membebaskan kalor sebesar 802, 3 k. J pada temperatur 298 K dan tekanan 1 atm. Tentukan persamaan termokimianya! 2. Rekasi karbon dan gas hidrogen membentuk 1 mol C 2 H 2 pada temperatur 25° dan tekanan 1 atm membutuhkan kalor 226, 7 k. J/mol. Tentukan persamaan termokimianya! 12

Jenis-jenis Perubahan Entalpi Standar (∆H˚) 1. Perubahan entalpi pembentukan standar (ΔH˚f = standard entalphy of formation). 2. Perubahan entalpi penguraian standar (ΔH˚d = standard entalphy of decomposition). 3. Perubahan entalpi pembakaran standar (ΔH˚c = standard entalphy of combustion). 4. Perubahan entalpi pelarutan standar (ΔH˚s = standard entalphy of solubility). 13

Perubahan Entalpi Pembentukan Standar (ΔH˚f) Perubahan entalpi pembentukan standar adalah perubahan entalpi pada pembentukan 1 mol senyawa dari unsur-unsurnya pada keadaan standar. (temperatur 298, tekanan 1 atm). 1. Perubahan entalpi pembentukan gas CO 2 adalah – 393, 5 k. J/mol. Tentukan persamaan termokimianya! 2. Perubahan entalpi H 2 O (l) adalah -285, 8 k. J/mol. Tentukan persamaan termokiamianya! 14

Perubahan Entalpi Penguraian Standar (ΔH˚d) Perubahan entalpi penguraian standar adalah perubahan entalpi pada penguraian 1 mol senyawa menjadi unsur-unsurnya pada keadaan standar. 1. Perubahan entalpi penguraian gas NO adalah – 90, 4 k. J/mol. Tentukan persamaan termokimianya! 2. Perubahan entalpi penguraian H 2 O(l) adalah + 285, 8 k. J/mol. Tentukan persamaan termokimianya! 15

Perubahan Entalpi Pembakaran Standar (ΔH˚c) Perubahan pembakaran standar adalah perubahan entalpi pada pembakaran sempurna 1 mol unsur atau senyawa dalam keadaan standar. 1. Perubahan entalpi pembakaran gas CH 4 adalah -802 k. J/mol. Tentukan persamaan termokimianya! 2. Perubahan entalpi pembakaran CH 3 OH(l) adalah -638 k. J/mol. Tentukan persamaan termokimianya! 16
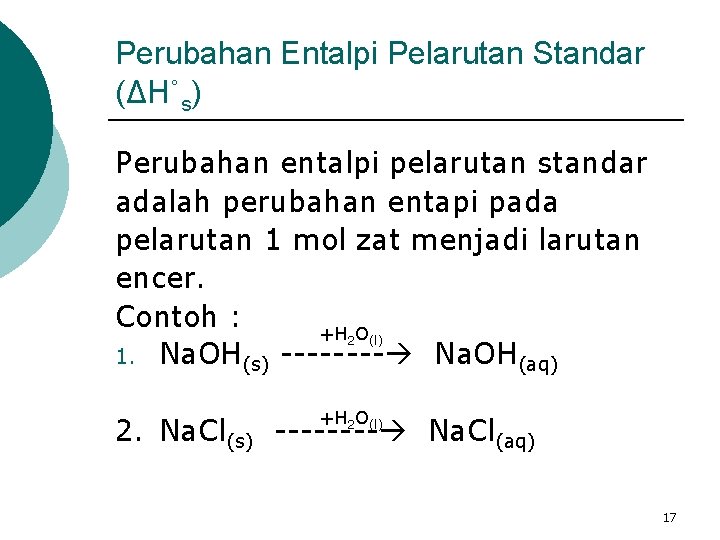
Perubahan Entalpi Pelarutan Standar (ΔH˚s) Perubahan entalpi pelarutan standar adalah perubahan entapi pada pelarutan 1 mol zat menjadi larutan encer. Contoh : +H 2 O(l) 1. Na. OH(s) ---- Na. OH(aq) +H 2 O(l) 2. Na. Cl(s) ---- Na. Cl(aq) 17

Menentukan Harga Perubahan Entalpi 1. Menentukan harga perubahan entalpi dengan kalorimeter. Kalorimeter adalah suatu alat untuk mengukur jumlah kalor yang diserap atau dibebaskan sistem. Q = m. c. ∆t Keterangan : Q = kalor yang diserap atau dikeluarkan m = massa zat ∆t = perubahan temperatur c = kalor jenis 18

Contoh Soal Dalam kalorimeter terdapat zat yang bereaksi secara eksotermik dan ternyata 0, 5 kg air yang mengelilinginya sebagai pelarut mengalami kenaikan temperatur sebesar 3˚C. Kalor jenis air = 4, 2 J/gram ˚C. Berapa kalor reaksi zat yang bereaksi itu? 19

Menentukan Harga Perubahan Entalpi 2. Menentukan harga perubahan entalpi dengan menggunakan hukum Hess. Hukum Hess “ perubahan entalpi reaksi hanya tergantung keadaan awal dan keadaan akhir sistem yang tidak tergantung pada jalannya reaksi. Kegunaan hukum Hess ialah untuk menghitung ∆H yang sukar diperoleh melalui percobaan. 20

Contoh Soal Ada 2 cara untuk memperoleh gas CO 2 yaitu : 1. Cara langsung. C(s) + O 2(g) CO 2(g) ∆H = -393, 5 k. J 2. Cara tidak langsung. C + ½O 2 CO ∆H = -110, 5 k. J CO + ½O 2 CO 2 ∆H = -283, 0 k. J + C + O 2 CO 2 ∆H = -393, 5 k. J 21
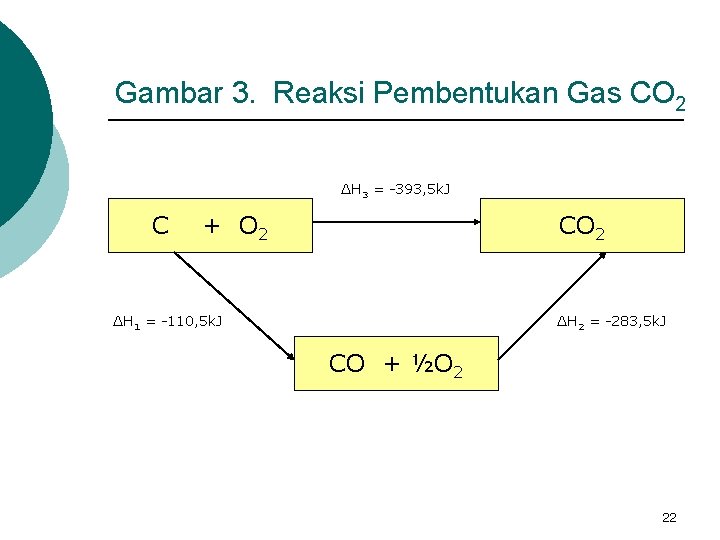
Gambar 3. Reaksi Pembentukan Gas CO 2 ∆H 3 = -393, 5 k. J C + O 2 CO 2 ∆H 1 = -110, 5 k. J ∆H 2 = -283, 5 k. J CO + ½O 2 22
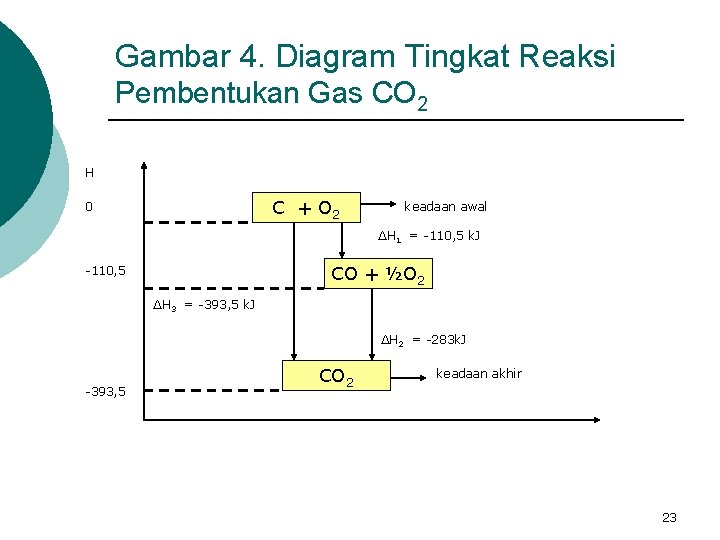
Gambar 4. Diagram Tingkat Reaksi Pembentukan Gas CO 2 H C + O 2 0 keadaan awal ∆H 1 = -110, 5 k. J CO + ½O 2 -110, 5 ∆H 3 = -393, 5 k. J ∆H 2 = -283 k. J -393, 5 CO 2 keadaan akhir 23

Menentukan Harga Perubahan Entalpi 3. Menetukan harga perubahan entalpi dengan menggunakan entalpi pembentukan. a PQ + b RS c PS + d QR reaktan produk ∆H = (c. ∆H˚f PS + d. ∆H˚f QR) – (a. ∆H˚f PQ + b. ∆H˚f RS) ∆H = ∑ ∆H˚f (produk) - ∑ ∆H˚f (produk) 24

Soal 1 Tentukan entalpi pembakaran gas etana, jika diketahui : ∆H˚f C 2 H 6 (g) ∆H˚f CO 2 (g) ∆H˚f H 2 O (l) = - 84, 7 k. J/mol-1 = -393, 5 k. J/mol-1 = -285, 8 k. J/mol-1 25

Soal 2 Tulislah persamaan termokimianya : a. Entalpi pembakaran C 2 H 5 OH(l) = -1. 234, 7 k. J/mol-1 b. Entalpi pembentukan NH 4 Cl = -317, 1 k. J/mol-1 26

Soal 3 Pada penguraian 1 mol gas amonia diperlukan kalor sebesar 46, 2 k. J/mol-1 a. Tulis persamaan termokimianya. b. Berapa harga ∆H pembentukan gas amonia? c. Pembentukan amonia tergolong reaksi eksoterm atau endoterm? d. Buatlah diagram tingkat energi untuk penguraian gas amonia. 27

Soal 4 Diketahui : ∆H˚f CO 2 (g) ∆H˚f H 2 O (l) ∆H˚f C 3 H 8 (g) ¡ ¡ = -393, 5 k. J/mol-1 = -285, 8 k. J/mol-1 = -103, 8 k. J/mol-1 Tentukan perubahan entalpi pembakaran C 3 H 8 (g) membentuk gas CO 2 dan air! Tentukan jumlah kalor yang dibebaskan pada pembakaran sempurna 4, 4 gram C 3 H 8 (g) 28

Soal 5 Diketahui reaksi-reaksi sebagai berikut : C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O ∆H= -2. 820 k. J/mol-1 C 2 H 5 OH + 3 O 2 2 CO 2 + 3 H 2 O ∆H= -1. 380 k. J/mol-1 Hitunglah perubahan entalpi untuk reaksi fermentasi glukosa C 6 H 12 O 6 fermen ------- 2 C 2 H 5 OH + 2 CO 2 29
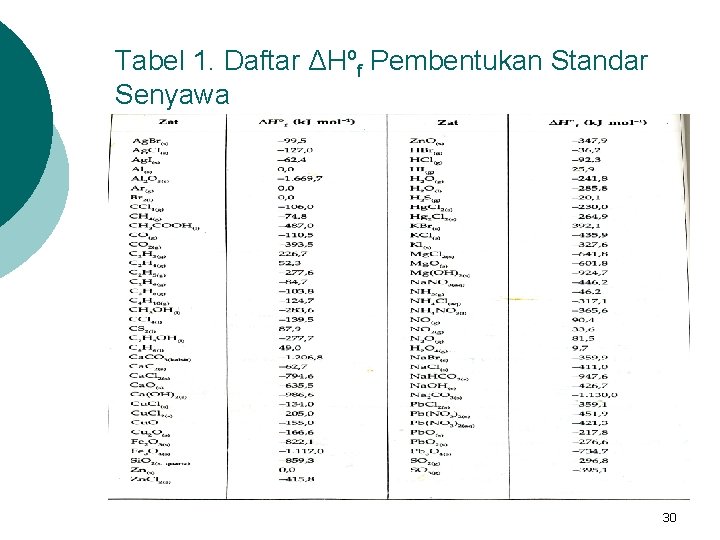
Tabel 1. Daftar ΔHºf Pembentukan Standar Senyawa 30

Energi Ikatan Energi ikatan adalah energi yang diperlukan untuk memutuskan ikatan kimia dalam 1 mol senyawa berwujud gas menjadi atom-atom gas pada keadaan standar. Energi ikatan diberi simbol D dan dinyatakan dalam satuan k. J/mol. 31

Contoh Soal 1 Tentukan energi ikatan dari : 1. Reaksi penguraian Cl 2(g). 2. Reaksi penguraian HBr(g). Catatan : Atom adalah partikel terkecil materi yang tidak dapat dibagi. Unsur adalah bentuk materi yang tidak dapat disederhanakan lagi dengan reaksi kimia. 32

Energi Ikatan Rata-rata Untuk molekul yang terdiri dari tiga atau lebih atom maka digunakan istilah energi ikatan rata-rata. Cara menghitung energi ikatan rata yaitu dengan menggunakan entalpi pembentukan standar dan entalpi atomisasi standar. 33

Contoh Soal 2 Diketahui data-data sbb : ΔH˚f CH 4(g) = -78, 8 k. J/mol ΔH˚f atom C(g) = +718, 4 k. J/mol ΔH˚f atom H(g) = 217, 9 k. J/mol Hitunglah energi ikatan C-H dalam molekul metana. 34

ΔH Reaksi Berdasarkan Energi Ikatan Reaksi kimia terjadi karena ada pemutusan ikatan dan pembentukan ikatan. Ikatanikatan pada reaktan akan putus dan terjadi ikatan baru pada produk. Oleh karena itu, perubahan entalpi dapat dicari dari selisih ΔH pemutusan ikatan dan ΔH pembentukan ikatan. ΔH = ΔH pemutusan ikatan – ΔH pembentukan ikatan 35

Contoh Soal 3 Dengan menggunakan tabel energi ikatan, hitunglah energi yang dibebaskan pada pembakaran 1 mol gas etana (C 2 H 6)! Catatan : Pada pemutusan ikatan diperlukan energi (ΔH = +). Pada pembentukan ikatan dilepaskan energi (ΔH = -) 36
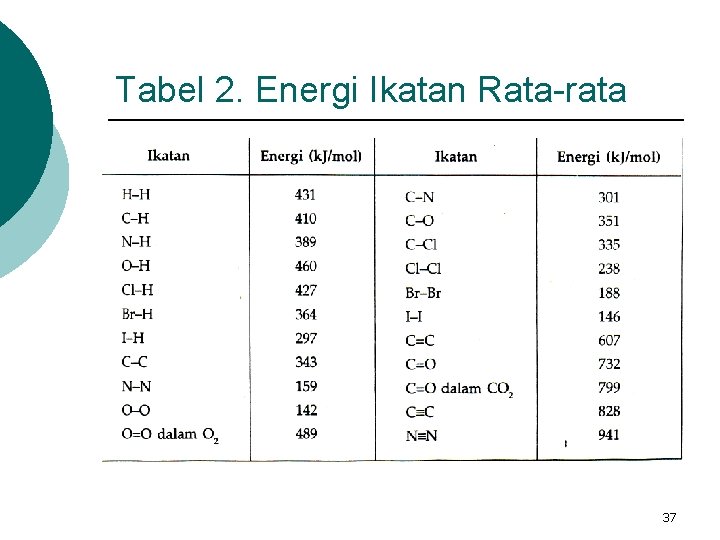
Tabel 2. Energi Ikatan Rata-rata 37
- Slides: 37