Termodinmica Aplicada AULA 4 Fernando Luiz Pellegrini Pessoa

















































- Slides: 53

Termodinâmica Aplicada AULA 4 Fernando Luiz Pellegrini Pessoa TPQBq ESCOLA DE QUÍMICA UNIVERSIDADE FEDERAL DO RIO DE JANEIRO EQ/UFRJ

Termodinâmica Aplicada As equações para propriedades extensivas na forma derivada: EQ/UFRJ

Termodinâmica Aplicada As equações para propriedades intensivas na forma derivada: EQ/UFRJ

Termodinâmica Aplicada Quais são as considerações utilizadas nas equações de Gibbs escritas anteriormente? • • sistema fechado composição constante Equações são inadequadas: Considere uma mistura de H 2 e O 2 num recipiente aberto (T e P constantes) com catalisador de Pt. O que acontece? EQ/UFRJ

Termodinâmica Aplicada As equações de Gibbs Formas integradas (P e T ctes): EQ/UFRJ

Termodinâmica Aplicada T e P são constantes, então: Como mudar estas equações de forma que sejam válidas para: – – Sistemas abertos? Misturas onde há mudança de composição? Equilíbrio de fases de misturas? Sistemas com reações químicas? EQ/UFRJ

Termodinâmica Aplicada A energia de Gibbs tem que depender do número de moles de cada espécie juntamente com T e P É necessário incluir esta dependência, o que é feito através do Potential Químico. C é o número de componentes. EQ/UFRJ

Termodinâmica Aplicada Teorema de Euler • “A derivada total de qualquer função homogênea de primeiro grau pode ser escrita como a soma de suas derivadas parciais primeiras” • Se f(x, y, z) for homogênea de grau 1, então : EQ/UFRJ

Termodinâmica Aplicada n constante • EQ/UFRJ

Termodinâmica Aplicada A derivada de n. G em relação ao número • de moles de i é a variável conhecida como: potencial químico, µi EQ/UFRJ

Termodinâmica Aplicada Relação fundamental das propriedades para sistemas abertos ou de composição variável A equação escrita na forma intensiva: Esta é a equação fundamental da TD de soluções, a partir da qual toda teoria é construída; ela é aplicada para fluido em fase simples de massa e/ou composição constante ou variável EQ/UFRJ

Termodinâmica Aplicada O que é o potencial químico? É o potencial para realizar trabalho químico. Por exemplo, um gradiente de temperatura significa que trabalho térmico pode ser realizado (ex. com um máquina térmica) Um gradiente de pressão significa que trabalho mecânico pode ser realizado (ex. , trabalho de eixo) Um gradiente de potential químico significa que trabalho químico pode ser realizado (ex. uma bateria, uma reação química, uma célula de combustível). EQ/UFRJ

Quais são as expressões corretas para as equações de Gibbs? Termodinâmica Aplicada • Entalpia: EQ/UFRJ

Termodinâmica Aplicada Derivadas com variáveis intensivas EQ/UFRJ

Termodinâmica Aplicada Derivadas com variáveis extensivas EQ/UFRJ

Termodinâmica Aplicada Equações na forma integrada (P e T ctes) EQ/UFRJ

Termodinâmica Aplicada EQUILÍBRIO DE FASES EQ/UFRJ

Termodinâmica Aplicada O Equilíbrio de Fases e a Engenharia de Processos Nós vivemos num mundo de MISTURAS: O ar que respiramos • A comida que comemos • A gasolina nossos automóveis • Nossas vidas estão intimamente ligadas a uma série de materiais que se constituem de uma variedade de substâncias químicas EQ/UFRJ

Termodinâmica Aplicada O Equilíbrio de Fases e a Engenharia de Processos Muitas coisas que fazemos dependem da transferência de substâncias de uma mistura para outra: Nos pulmões, o O 2 do ar se dissolve no sangue, enquanto o CO 2 do • sangue passa para o ar Na preparação do café, substâncias solúveis em água presentes nos grãos de café são extraídas Seja no nosso dia-a-dia, seja no meio-ambiente ou nas indústrias, há sempre a transferência de substâncias de uma para outra fase EQ/UFRJ •

Termodinâmica Aplicada O Equilíbrio de Fases e a Engenharia de Processos Quando 2 fases são colocadas em contato, elas tendem a transferir seus constituintes entre si até que a composição de cada uma fique constante (equilíbrio) As composições de equilíbrio de 2 fases são normalmente bastante diferentes entre si e é justamente essa diferença que nos permite separar as misturas por destilação, extração, adsorção, etc. EQ/UFRJ

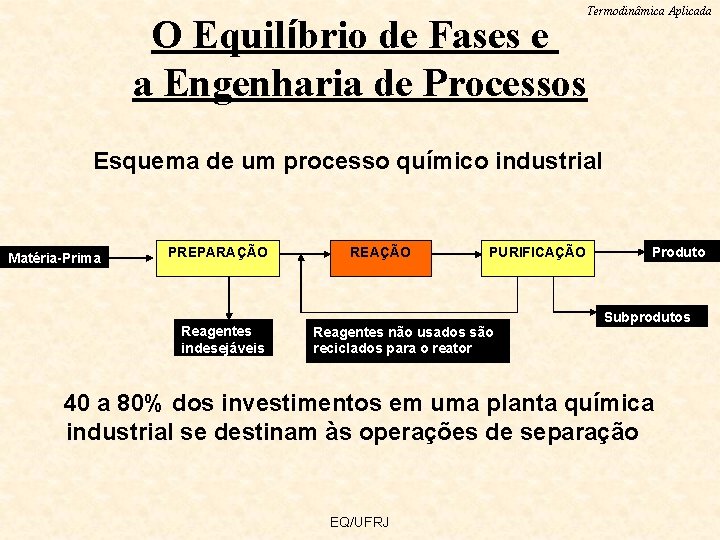
Termodinâmica Aplicada O Equilíbrio de Fases e a Engenharia de Processos Esquema de um processo químico industrial Matéria-Prima PREPARAÇÃO Reagentes indesejáveis REAÇÃO PURIFICAÇÃO Reagentes não usados são reciclados para o reator Produto Subprodutos 40 a 80% dos investimentos em uma planta química industrial se destinam às operações de separação EQ/UFRJ

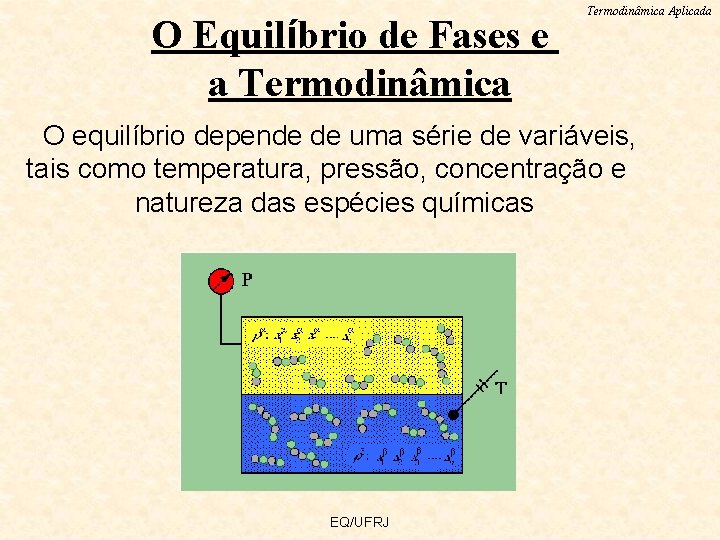
O Equilíbrio de Fases e a Termodinâmica Aplicada O equilíbrio depende de uma série de variáveis, tais como temperatura, pressão, concentração e natureza das espécies químicas EQ/UFRJ

O Equilíbrio de Fases e a Termodinâmica Aplicada Regra das Fases (sem reação química): F=C-P+2 Dado um sistema binário (C=2), com 2 fases em equilíbrio (P=2), tem-se F=2, ou seja, é necessário especificar 2 variáveis intensivas independentes para caracterizá-lo completamente. Por exemplo, dado T e P qual a seria a composição das fases em equilíbrio? EQ/UFRJ

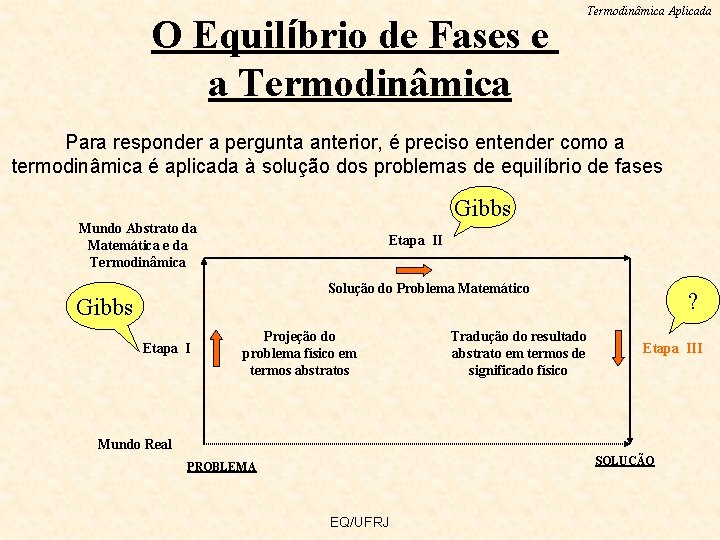
O Equilíbrio de Fases e a Termodinâmica Aplicada Para responder a pergunta anterior, é preciso entender como a termodinâmica é aplicada à solução dos problemas de equilíbrio de fases Gibbs Mundo Abstrato da Matemática e da Termodinâmica Etapa II Solução do Problema Matemático Gibbs Etapa I Projeção do problema físico em termos abstratos Tradução do resultado abstrato em termos de significado físico ? Etapa III Mundo Real SOLUÇÃO PROBLEMA EQ/UFRJ

Termodinâmica Aplicada Objetivo da Disciplina Estudar o equilíbrio de fases em sistemas de composição variável, através de conceitos da termodinâmica clássica e da modelagem do equilíbrio líquido-vapor, líquido-líquido, sólidolíquido e sólido-gás, com exemplos e aplicações a baixa e alta pressões, incluindo produtos naturais, fluidos do petróleo e polímeros EQ/UFRJ

Termodinâmica Aplicada TD Clássica do EF – – – Considere uma mistura pentano + hexano num recipiente. Supondo que as condições são tais que as fases líquida e vapor estão ambas presentes. Descreva o sistema em equilíbrio. Considere o vapor e o líquido como subsistemas abertos. Eles estão em contato e podem trocar calor e matéria entre si. Que variáveis podem ser usadas para especificar cada subsistema? Quais destas variáveis mostram que os subsistemas estão realmente em equílibrio? Quais são os critérios de equilíbrio de fases? Como calcular o equilíbrio de fases? EQ/UFRJ

Termodinâmica Aplicada Critérios do EF Primeira Lei TD • d(n. U) = d. Qrev + d. Wrev • d. Wrev = - Pd(n. V) • d. Qrev = Td(n. S) • d(n. U) = Td(n. S) – Pd(n. V) • d. Qrev = d(n. U) + Pd(n. V) EQ/UFRJ

Termodinâmica Aplicada Segunda Lei TD • d(n. S) ≥ d. Qrev / T • LOGO • Td(n. S) – d. Qrev ≥ 0 • d. Qrev = d(n. U) + Pd(n. V) • Td(n. S) – d(n. U) – Pd(n. V) ≥ 0 • d(n. U) + Pd(n. V) – Td(n. S) ≤ 0 • EQ/UFRJ

Termodinâmica Aplicada d(n. U) + Pd(n. V) – Td(n. S) ≤ 0 • S e V ctes • d(n. U) ≤ 0 → U 2 ≤ U 1 → U 2 = U 1 • U e V ctes • – Td(n. S) ≤ 0 • d(n. S) ≥ 0 → S 2 ≥ S 1 → S 2 = S 1 • EQ/UFRJ

Termodinâmica Aplicada • Definição das funções: • Este conjunto de equações é chamada Equações de Gibbs. EQ/UFRJ

Termodinâmica Aplicada d(n. U) + Pd(n. V) – Td(n. S) ≤ 0 • n. A = n. U – T(n. S) • d(n. A) = d(n. U) – Td(n. S) – n. Sd. T • d(n. U) = d(n. A) + Td(n. S) + n. Sd. T • d(n. A) + (n. S)d. T + Pd(n. V) ≤ 0 • T e V ctes • d(n. A) ≤ 0 → A 2 ≤ A 1 → A 2 = A 1 • EQ/UFRJ

Termodinâmica Aplicada d(n. U) + Pd(n. V) – Td(n. S) ≤ 0 • n. H = n. U + P(n. V) • d(n. H) = d(n. U) + Pd(n. V) + n. Vd. P • d(n. U) = d(n. H) - Pd(n. V) - n. Vd. P • d(n. H) - n. Vd. P – Td(n. S) ≤ 0 • P e S ctes • d(n. H) ≤ 0 → H 2 ≤ H 1 → H 2= H 1 • EQ/UFRJ

d(n. U) + Pd(n. V) – Td(n. S) ≤ 0 • P e T ctes • d(n. U) + d(Pn. V) – d(Tn. S) ≤ 0 • d(n. U + Pn. V – Tn. S) ≤ 0 • d(n. H – Tn. S) ≤ 0 • d(n. G) ≤ 0 • G 2 ≤ G 1 → G 2 = G 1 • EQ/UFRJ Termodinâmica Aplicada

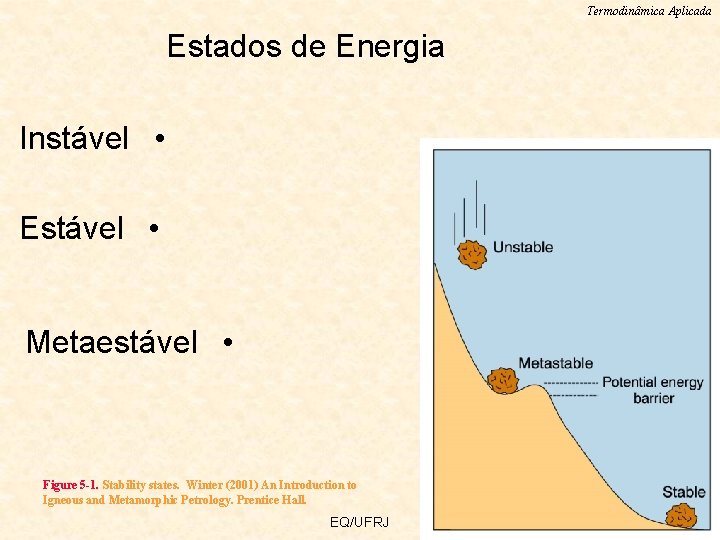
Termodinâmica Aplicada Estados de Energia Instável • Estável • Metaestável • Figure 5 -1. Stability states. Winter (2001) An Introduction to Igneous and Metamorphic Petrology. Prentice Hall. EQ/UFRJ

Termodinâmica Aplicada Potencial Químico como Critério de EF Considere um sistema fechado com duas • fases em equilíbrio Cada fase é um sistema aberto • Escrevendo d(n. G) para cada fase: • d(n. G)’=(n. V)’d. P – (n. S)’d. T + ∑μ’idn’i • d(n. G)’’=(n. V)’’d. P – (n. S)’’d. T + ∑μ’’idn’’i • EQ/UFRJ


Termodinâmica Aplicada O sistema global de duas fases é fechado então d(n. G) =(n. V)d. P – (n. S)d. T Logo com d(n. G) =(n. V)d. P – (n. S)d. T + ∑μ’idn’i + ∑μ’’idn’’i Obtém-se ∑μ’idn’i + ∑μ’’idn’’i = 0 EQ/UFRJ


Termodinâmica Aplicada Assumindo que o sistema (pentano + hexano) não está ainda em equilíbrio (note que o sistema leva um certo tempo para atingir o equilíbrio), O que acontecerá fisicamente no recipiente se ? EQ/UFRJ

Termodinâmica Aplicada Significado físico • • A igualdade de Temperatura indica que as fases estão em equilíbrio térmico. Não há gradientes de T para mover energia de uma fase para outra. A igualdade de Pressão faz com que haja equilíbrio mecânico entre as fases, isto é; não há gradientes de P para mover massa de uma fase para outra. A igualdade de Potencial Químico proporciona equílibrio químico ao sistema. A igualdade de potencial químico significa que não há forças motrizes de origem química que movam componentes preferencialmente de uma fase para outra. EQ/UFRJ

Termodinâmica Aplicada Condições para equilíbrio de fase Generalizando o resultado para cada fase contendo seus componentes e em equilíbrio entre si, as condições para o equilíbrio entre as fases são: EQ/UFRJ

Termodinâmica Aplicada Sistema de Duas Fases – Substâncias Puras Substâncias puras com duas fases em • equilíbrio tem os valores de V, U e H diferentes em cada fase, porém G tem o mesmo valor para as duas fases Como μ = G então G’ = G’’ • Neste caso d. G’ = d. G’’ • EQ/UFRJ


Termodinâmica Aplicada ELV Como Equação exata Logo Antoine ln. Psat = A - B/T ou EQ/UFRJ ln. Psat = A – B / (T + C)

Termodinâmica Aplicada Propriedades parciais molares • Potential químico : • Significado físico da derivada na equação acima: Variação na energia de Gibbs decorrente da adição de uma quantidade (moles) infinitesimal de um componente i à mistura, mantendo-se constantes a temperatura, a pressão e todos os números de moles dos demais componentes. EQ/UFRJ

Termodinâmica Aplicada Definição de Propriedades Parciais Molares M = U, H, A, S, V, G Pode-se calcular propriedades da solução a partir das propriedades parciais molares, bem como as propriedades parciais a partir das propriedades da solução EQ/UFRJ

Termodinâmica Aplicada Propriedades Parciais A contribuição de uma certa substância para uma • determinada propriedade de uma mistura é contabilizada através de uma função termodinâmica denominada PROPRIEDADE PARCIAL Para compreender o equilíbrio de fases em sistemas de • composição variável (misturas) é fundamental conhecer as relações entre as propriedades parciais e as propriedades das misturas. EQ/UFRJ

Termodinâmica Aplicada Propriedades Parciais As propriedades macroscópicas de um fluido • homogêneo em equilíbrio são funções da temperatura, pressão e composição, ou seja, onde M é uma propriedade intensiva, e por onde n. M é uma propriedade extensiva EQ/UFRJ

Termodinâmica Aplicada Propriedades Parciais M representa qualquer propriedade molar: V, U, H, Cv, • Cp, S, A e G. As seguintes propriedades também podem ser • representadas por M: (compressibilidade isotérmica) 4 (expansividade volumétrica) 4 (densidade) 4 Z (fator de compressibilidade) 4 EQ/UFRJ

Termodinâmica Aplicada Propriedades Parciais Fazendo-se a diferencial total de (n. M), tem-se • A derivada de n. M em relação ao número de moles de • cada componente, a P e T constantes, é denominada de PROPRIEDADE MOLAR PARCIAL, sendo escrita como EQ/UFRJ

Termodinâmica Aplicada Propriedades Parciais Combinando-se as 2 eqs. anteriores, tem-se • As propriedades das misturas e as propriedades parciais • molares se relacionam através das seguintes expressões: EQ/UFRJ

Termodinâmica Aplicada Significado físico da propriedade parcial molar A propriedade parcial molar é a taxa de • variação da propriedade (n. M) com o número de moles da espécie i (ni), a T, P e nj constantes, onde nj é o número de moles de todas as espécies presentes na solução, com exceção da espécie i. EQ/UFRJ

Termodinâmica Aplicada Observação: diferentes notações Propriedades Molares: • Propriedades da mistura M: – V, U, H, S, G, etc. • Propriedades da substância pura Mi: – Vi, Ui, Hi, Si, Gi, etc. • Propriedades parciais : – EQ/UFRJ