Termodinamika n n Napovedovanje ali bo stanje nekega

Termodinamika n n Napovedovanje ali bo stanje nekega makroskopskega sistema ostalo nespremenjeno ali pa bo spontano prešlo v novo stanje. Kinetika pove, koliko časa traja, da sistem doseže novo stanje. S termodinamiko najlažje razlagamo procese s takšno prostorsko razsežnostjo, da lahko zanemarimo posamezne atome, in s tako časovno, da lahko zanemarimo kinetiko. Vsi kinetični procesi potekajo hitreje ob povišani temperaturi, zato je termodinamika najbolj uporabna pri napovedovanju visokotemperaturnih

Definicije n Sistem je proučevano območje z dobro določenimi lastnostmi, da ga lahko ločimo od okolice. n n Faza je fizikalno homogen in mehanično ločljiv del sistema, npr. para, tekočina, trdna snov (mineral). n n n Izoliran – z okolico ne izmenjuje niti snovi niti energije Zaprt – z okolico izmenjuje energijo, a ne snovi Odprt - z okolico izmenjuje energijo in snov Homogen sistem – ena faza Heterogen sistem – več faz Komponenta je kemijska formula. Z njo izražamo spremembo sestave sistema ( H 2 O, Si. O 2, Fe). n Ne zamenjuj faze (voda, kremen) s komponento (H 2 O, Si. O ).

Ravnotežje je stanje v katerem se v času opazovanja makroskopske fizikalne lastnosti ne spreminjajo. n Mikroskopski procesi lahko potekajo, a je njihova hitrost enaka ustreznim reverzibilnim procesom. n Stabilno ravnotežje ima najnižjo možno potencialno energijo. Sistem na majhne spremebe odgovori z vrnitvijo v stabilno ravnotežno stanje. n Metastabilno ravnotežje je lokalni minimum potencialne energije. Pri večjih spremembah se premakne v smer nižje energije. n Nestabilno ravnotežje je točka, kjer spontano ne n
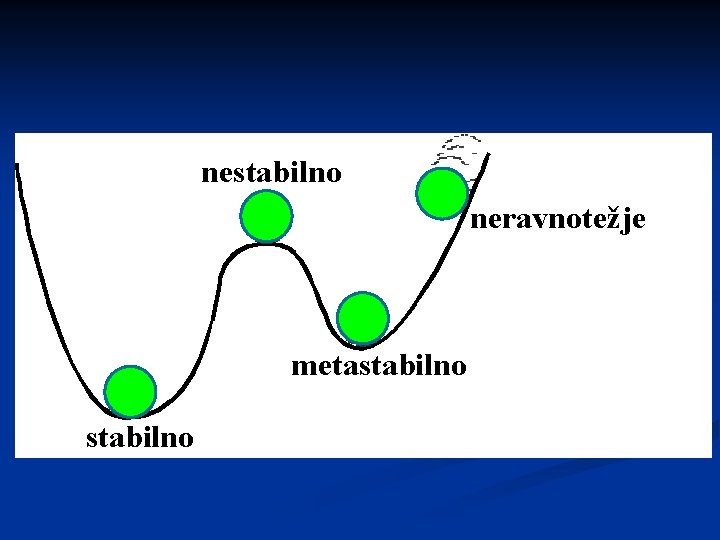
nestabilno neravnotežje metastabilno STABILNO

0. zakon termodinamike Če sta dva sistema v termičnem ravnotežju s tretjim, (med njimi ni toplotnega toka) sta v ravnotežju tudi med seboj. Vsi trije imajo enako temperaturo. n Absolutna ničla je temperatura, ko je prostornina idealnega plina enka nič. n n 0 o. C = 273 K n Pogoji ravnotežja (T, p, koncentracije)

U notranja energija n Q toplota n W delo n p tlak (pritisk) n V volumen (prostornina) n H entalpija n H 0 f formacijska entalpija n n S entropija T temperatura cp specifična toplota Gf standardna prosta energija formacije ali standardna Gibbsova prosta energija n G Gibbsova prosta energija n koncentracija n a, b. . . število ionov v reakciji n s topnost n Ksp topnostni produkt n E 0 standardni potencial n N število elektonov (e-) n

1. Zakon termodinamike ali zakon o ohranitvi energije n Celotna energija sistema je konstantna. Skupna sprememba notranje energije je enaka vloženemu delu in spremembi toplote. Sprememba energije sistema je neodvisna od njene poti. U = Q - W = Q - p V H = Q + V p W = p V

Termodinamika se ukvarja le z notranjo energijo sistema. Zanimajo nas le spremembe energije in ne absolutna energija sistema. n Sistem z okolico izmenjuje energijo na različne načine. V zaprtem sistemu sta najpomembnejša toplota in delo. n Spremembe entalpije (toplotne vsebnosti) posameznih procesov imajo svoja imena: izparilna toplota, reakcijska toplota, formacijska toplota. . . Toplota formacije neke komponente je sprememba toplote, ki nastane pri reakciji potrebnih elementov pod standardnimi pogoji (ss = 25 o. C, 1 bar). n

2. Zakon termodinamike Entropija podaja stopnjo (ne)urejenosti. Je mera za notranjo porazdelitev energije v ravnotežnem stanju. n Entropija vesolja se vedno viša. n Vrste reakcij: n n toplota se oddaja, urejenost se niža (viša se entopija) n primer: n gorenje premoga toplota se oddaja, urejenost se viša n primer: voda prehaja v led n možno Q>S možno toplota se sprejema, urejenost se niža n primer: voda prehaja v paro možno

2. zakon termodinamike: obstaja naravna smer poteka reakcije. n Določata jo toplotni tok in stopnja (ne)urejenosti - entropija. Oba faktorja povezuje Gibbsova funkcija. n Reakcija poteka, če je upadanje Gibbsove funkcije zaradi spremembe urejenosti večja kot njeno naraščanje zaradi absorbcije toplote. Toplote ne moremo 100% učinkovito pretvoriti v delo. n Pri obrnljivih (idealnih) procesih je absorbirana toplota enaka opravljenemu delu in produktu temperature in spremembe entropije. n

3. zakon termodinamike n Vsaka popolnoma urejena in kristalizirana snov ima pri absolutni ničli (-273 o. C) enako entropijo. Entropijo snovi pri drugi temperaturi lahko izračunamo s pomočjo specifične toplote. cp = d. Q/d. T ST = S 298 K + 298 Tcp/T d. T HT = H 298 K + 298 Tcp d. T

Gibbsova funkcija n Standardna prosta energija formacije je sprememba proste energije zaradi nastanka komponente iz njenih gradbenih elementov pod standardnimi pogoji. H = T S + V p G = V p - S T G = H - T S Gf = Gproduktov - Greaktantov

n Smer poteka reakcije ugotovimo z Gibbsovo prosto energijo: G < 0 reakcija poteka v desno G = 0 reakcija je v ravnotežju G > 0 reakcija poteka v levo

Ravnotežje in ravnotežna konstanta n Za idelano raztopino je pri dani temperaturi reakcije a. A + b. B c. C + d. D n ravnotežna konstanta (K): K = C c D d / A a B b n Pri realnih raztopinah koncentracijo nadomestimo z aktivnostjo (a). Aktivnosti trdnih snovi in navadno tudi vode so po dogovoru 1.

Topnost Koncentracije so podane v enotah teža/teža (mg/kg = ppm = mg/l), teža/volumen (mg/l = ppm), molarnost (m. M/l = (mg/l)/molska teža), m. Eq/l (upošteva količino naboja - npr. : SO 42 - 2 m. M/l = m. Eq/l). n Topnost določamo s pomočjo ravnotežne konstante, imenovane topnostni produkt. Topnost je enaka aktivnosti kationa ali aniona. Ag. Cl Ag+ Cl- Ksp = produkti/reaktanti = Ag+ Cl- s = Ag+ = Cl- = Ksp n

Kislost - p. H n p. H izraža aktivnost vodikovega iona. H 2 O H+ + OHp. H = -log H+ = 10 -p. H n Ravnotežna konstanta reakcije pri standardnem stanju: K = H+ OH- = 10 -14 n p. H je nevtralen (7), kadar je koncentracija (ali aktivnost) kationov eneka koncentraciji anionov.

Redoks potencial - Eh H 2 2 H+ + 2 e- E 0 = 0. 00 V Če neka snov reducira H+, je po dogovoru E 0 negativen, če pa H 2 reducira neko snov in pri tem prehaja v H+, je po dogovoru E 0 pozitiven. Reakcije z negativnim potencialom potekajo v levo, s pozitivnim pa v desno. n Pri standardnih pogojih za redoks reakcije velja: n G = -RTln. K = NE 0 F

n Redoks potencial je mera za tendenco raztopine, da dovoli nastop neke reakcije. Eh = E 0 + (RT/NF)ln. K n Pri standardnih pogojih velja: Eh = E 0 + (0. 059/N)log. K
- Slides: 18