Termodinamika Medicina 201718 1 Kratka povijest Stara Grka





















































- Slides: 71

Termodinamika Medicina 2017/18. 1

Kratka povijest �Stara Grčka – toplina mjera kvalitete � 1592. – Gallilei termoskop � 1620. – Bacon termometar � 1665. – Stalne točke �Niclolas Sadi Carnot – 1824. Reflections on the Motive Power of Fire ◦ Termodinamički kružni procesi �Joules - magnetoelektricitet 2

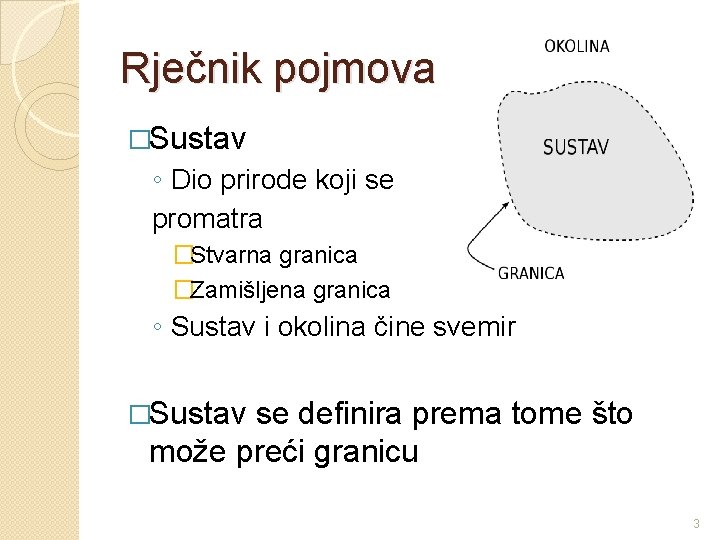
Rječnik pojmova �Sustav ◦ Dio prirode koji se promatra �Stvarna granica �Zamišljena granica ◦ Sustav i okolina čine svemir �Sustav se definira prema tome što može preći granicu 3

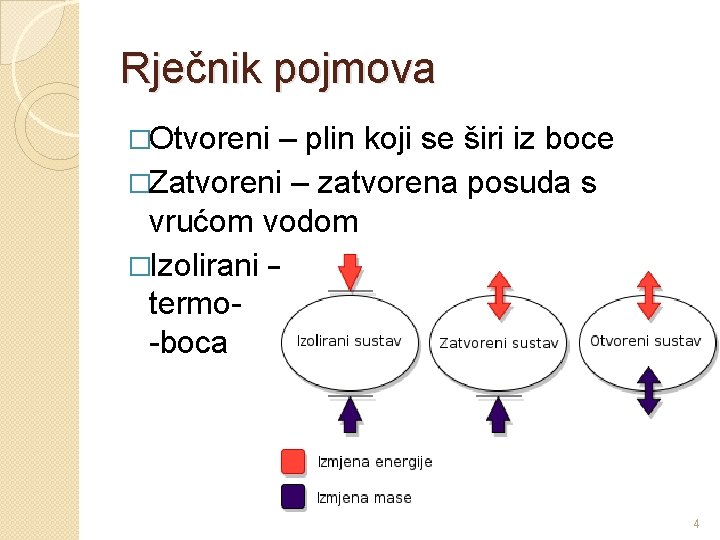
Rječnik pojmova �Otvoreni – plin koji se širi iz boce �Zatvoreni – zatvorena posuda s vrućom vodom �Izolirani – termo-boca 4

Rječnik pojmova �Sustav je od okoline odvojen granicom ◦ ◦ ◦ Adijabatska Dijatermalna Nepropusna Polu propusna 5

Termodinamički parametri �Intenzivni – čija fizička svojstva ne ovise o veličini sustava ◦ Temperatura ◦ Indeks loma ◦ Gustoća �Ekstenzivni – ovise o veličini sustava ◦ Unutarnja energija ◦ Volumen ◦ Masa 6

Termodinamička ravnoteža �Svojstva sustava u termodinamičkoj ravnoteži su nepromjenjena u vremenu ◦ Unutar sustava postoji izmjena energije �Staionarno stanje – parametri sustava se ne mijenjaju tijekom vremena iako sustav s okolinom izmjenjuje energiju 7

Funkcija stanja �Funkcija stanja – ovisi samo o parametria u konačnom i početnom stanju sustava ◦ Ne ovisi o putu ili načinu izvođenja procesa �Procesna funkcija – ovisi o načinu na koji je sustav došao iz početnog u konačno stanje 8

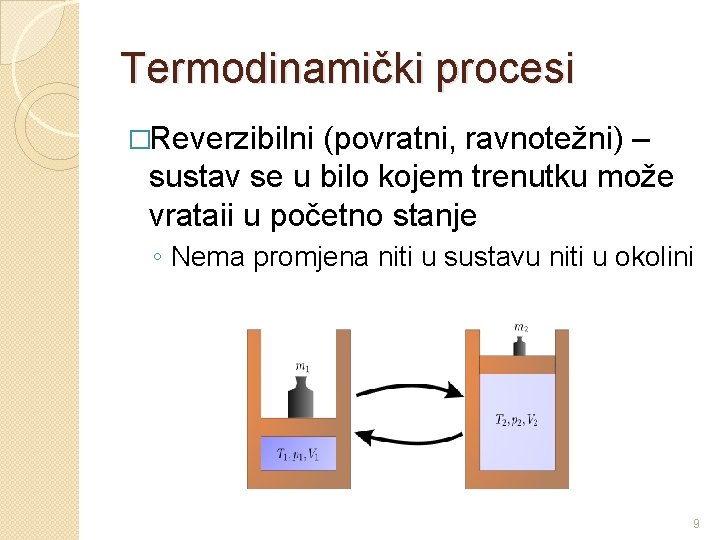
Termodinamički procesi �Reverzibilni (povratni, ravnotežni) – sustav se u bilo kojem trenutku može vrataii u početno stanje ◦ Nema promjena niti u sustavu niti u okolini 9

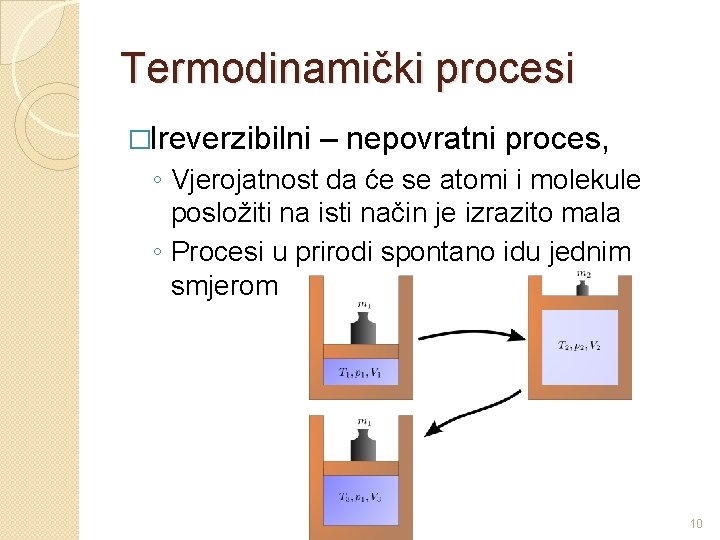
Termodinamički procesi �Ireverzibilni – nepovratni proces, ◦ Vjerojatnost da će se atomi i molekule posložiti na isti način je izrazito mala ◦ Procesi u prirodi spontano idu jednim smjerom 10

11

Unutarnja energija �Zbroj kinetičkih i potencijalnih energija svih molekula sustava �Može se promijeniti: ◦ Zagrijavanjem sustava ◦ Izvođenjem rada na sustavu ◦ Dodavanjem ili uzimanjem tvari 12

Sadržaj unutarnje energije monoatomni molekularni plin tekućina ili čvrstina ovaj doprinos jako varira za različite tvari jako velik za vodu translacijska kinetička energija rotacija i vibracija potencijalna energija intermolekularnih sila 13

Toplina i temperatura �Toplina - dio unutarnje energije tijela koju razmijenjuju sustavi međusobno ili s okolinom �Temperatura - određuje stanje termodinamičke ravnoteže sustava �Ako TMD sustav nije u ravnoteži (različite temperature), toplina prelazi sa zagrijanijih dijelova na hladnije dok se temperatune ne izjednače 14

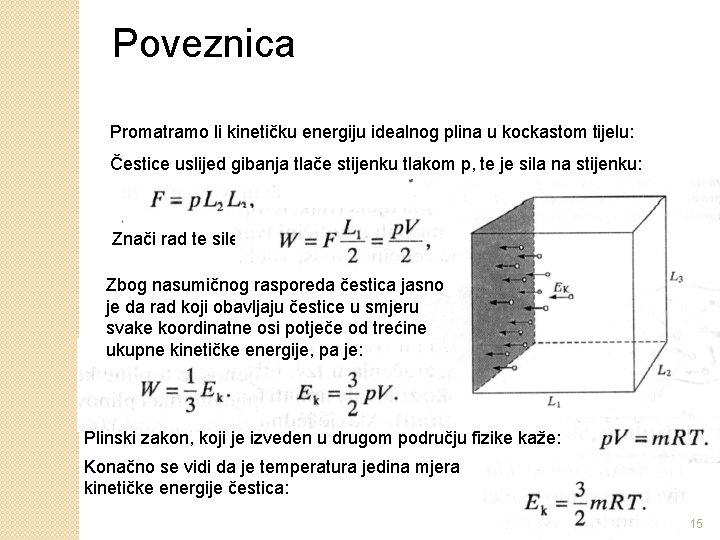
Poveznica Promatramo li kinetičku energiju idealnog plina u kockastom tijelu: Čestice uslijed gibanja tlače stijenku tlakom p, te je sila na stijenku: Znači rad te sile je: Zbog nasumičnog rasporeda čestica jasno je da rad koji obavljaju čestice u smjeru svake koordinatne osi potječe od trećine ukupne kinetičke energije, pa je: Plinski zakon, koji je izveden u drugom području fizike kaže: Konačno se vidi da je temperatura jedina mjera kinetičke energije čestica: 15

Dvije posude sadrže jednake količine vode. U jednoj je temperatura vode 20°C, a u drugoj 80°C. U kojoj posudi voda ima veću unutrašnju energiju? Rj, U posudi s vodom koja ima višu temperaturu 16

Što je jednako a što različito za 1 gram vode na 00 C i 1 g bakra na 00 C ? q jednaka temperatura - jednaka prosječna kinetička energija molekula q nisu jednake unutarnje energije q nisu jednaki toplinski kapaciteti c (vode) = 4186 J/kg K c (bakra) = 386 J/kg K Zašto? q unutarnja energija = translacijska kinetička energija + vibracijska i rotacijska kinetička energija + potencijalna energija od intermolekularnih sila 17

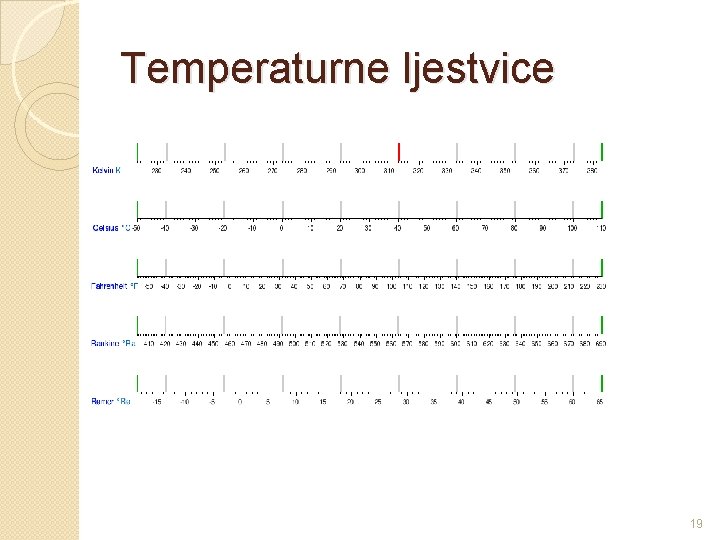
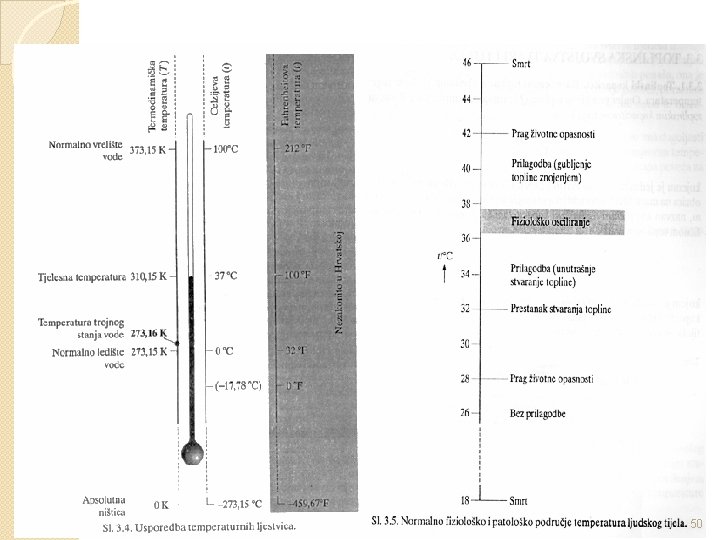
Temperaturne ljestvice � 18

Temperaturne ljestvice 19

Termometar �Uređaj kojim se mjeri temperatura 20

Termodinamički zakoni �Nulti – ako je sustav A u termičkoj ravnoteži sa sustavom C, i sustav B sa sustavom C, onda su i sustav A i B u termičkoj ravnoteži ◦ Potreban za matematičku formulaciju termodinamike 21

Prvi zakon termodinamike �Dovede li se sustavu neka količina topline (Q), sustavu se poveća unutarnja energija za ΔU i sustav izvrši rad W �Toplina je pozitivna ako se dovodi sustavu, a negativna ako se odvodi. �Rad je pozitivan ako sustav vrši rad, a negativan ako okolina vrši rad 22

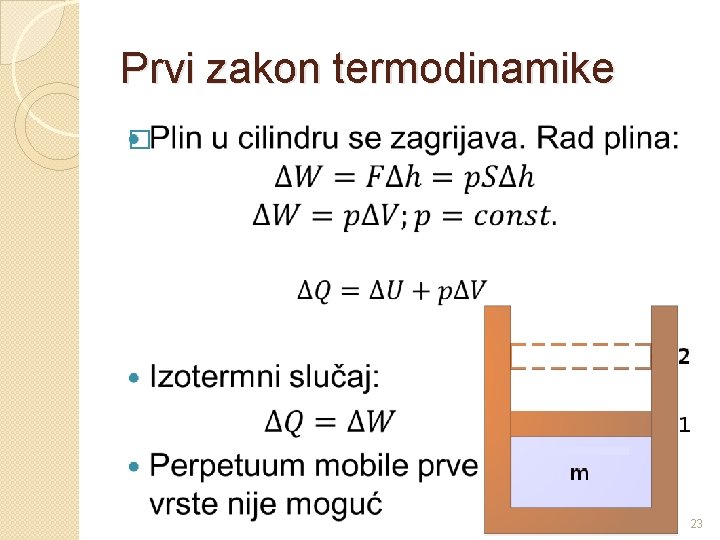
Prvi zakon termodinamike � 23

�Kolika je promjena unutrašnje energije sustava kojem predamo 1676 J topline i istodobno obavimo na njemu rad 838 J? Rj, 2, 514 k. J �Kolikoj toplini je ekvivalentan rad što ga u jednom satu obavi dizalica koja ima snagu 735 W? Rj, 2, 646 MJ 24

Drugi zakon termodinamike �Toplina ne može sama od sebe prelaziti s tijela niže na tijelo više temperature ◦ Entropija Svemira stalno raste ◦ Određuje smjer spontanih interakcija �U prirodi bilo koji uređeni sustav spontano teži neuređenosti, odnosno stanju s manjim stupnjem uređenosti 25

Drugi zakon termodinamike �There have been nearly as many formulations of the second law as there have been discussions of it. �Perpeetum mobile druge vrste – nije moguće svu dovedenu toplinu pretvoriti u mehanički rad 26

Treći zakon termodinamike �Pri apsolutnoj nuli nestaju razlike entropija između svih stanja koja su u unutrašnjoj termodinamičkoj ravnoteži �Nije moguće konačnim brojem procesa sniziti temperaturu bilo kojeg sustava na 0 K 27

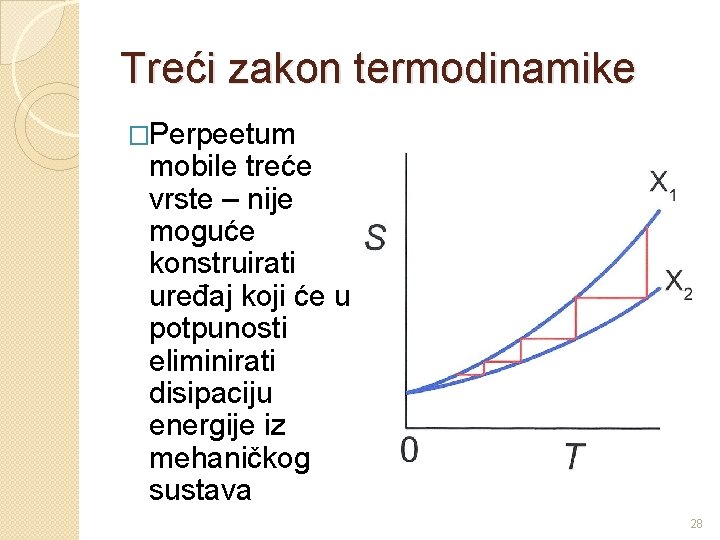
Treći zakon termodinamike �Perpeetum mobile treće vrste – nije moguće konstruirati uređaj koji će u potpunosti eliminirati disipaciju energije iz mehaničkog sustava 28

Entropija �Mjera stupnja uređenosti sustava ◦ Uređeni sustav – niska entropija ◦ d. Q – toplina dovedena sustavu; ◦ Tspr – temperatura spremnika �ΔS(reverzibilni kružni proces)=0 �ΔS(ireverzibilni kružni proces)>0 29

Entropija u kemijskoj termodinamici �Promjena entropije opisuje smjer i veličinu promjene u reakciji �Korisno je specificirati entropiju kao intenzivnu veličinu, odnosno karakteristiku proučavanog sustava (J/kg-1 K-1, J/mol-1 K-1) 30

31

Entalpija �Termodinamički potencijal koji se sastoji od promjene unutrašnje energije i volumnog rada �Budući su U, p i V funkcije stanja , i H je funkcija stanja 32

33

Gibbsova slobodna energija �Slobodna entalpija �Najveći iznos mehaničkog rada koji se može dobiti iz supstance u početnom stanju, bez povećavanja ukupnog volumena i prolaska topline �Maksimalni iznos rada koji se može dobiti iz zatvorenog sustava 34

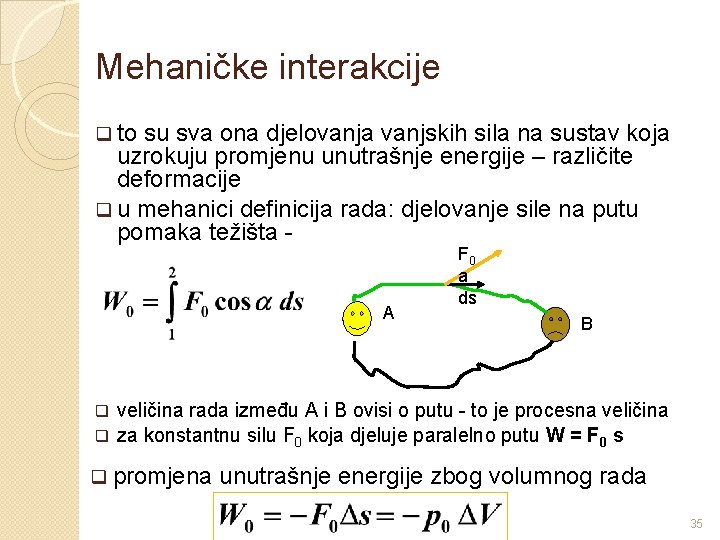
Mehaničke interakcije q to su sva ona djelovanja vanjskih sila na sustav koja uzrokuju promjenu unutrašnje energije – različite deformacije q u mehanici definicija rada: djelovanje sile na putu pomaka težišta - A F 0 a ds B veličina rada između A i B ovisi o putu - to je procesna veličina q za konstantnu silu F 0 koja djeluje paralelno putu W = F 0 s q q promjena unutrašnje energije zbog volumnog rada 35

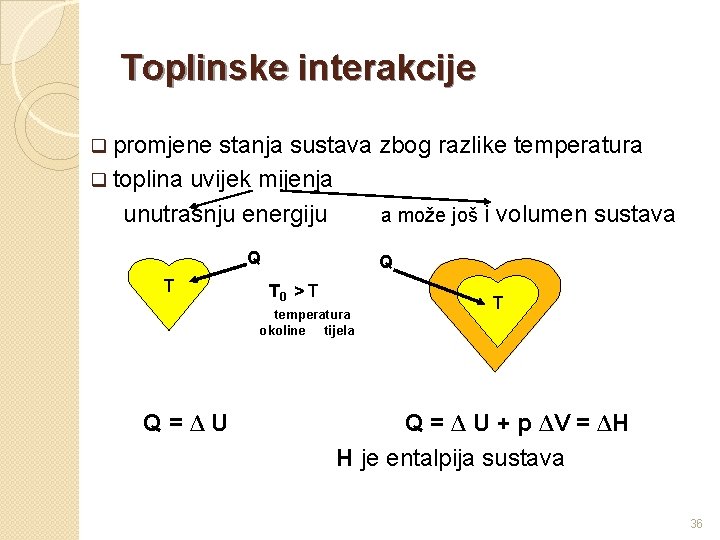
Toplinske interakcije q promjene stanja sustava zbog razlike temperatura q toplina uvijek mijenja unutrašnju energiju a može još i volumen sustava Q T 0 > T temperatura okoline tijela Q=ΔU T Q = Δ U + p ΔV = ΔH H je entalpija sustava 36

TOPLINSKO RASTEZANJE TVARI Promjenom temperature svim se tijelima mijenja obujam, ovisno o tvari. Primjer štapa. Ako se povišenjem temperature Δt duljina štapa poveća za Δl, ukupna duljina štapa je Rastezanje štapa će ovisiti o početnoj duljini i promjeni teperature, uz konstantu proporcionalnosti α, koji se naziva toplinska rastezljivost, te je: 37

�Štap od platine pri 20°C dugačak je 998 mm. Pri kojoj će temperaturi štap biti dugačak 1 m? Rj 243°C �Eiffelov toranj visok je 300 m pri 0°C. Pri kojoj će temperaturi toranj biti 10 cm viši? Rj 28°C 38

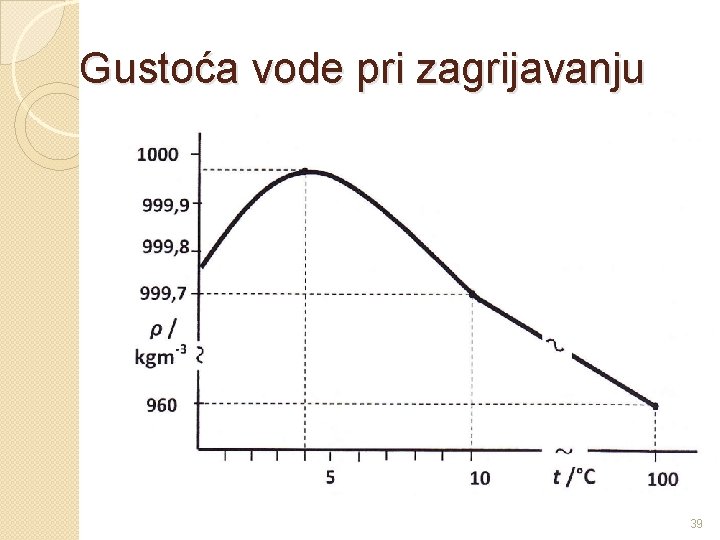
Gustoća vode pri zagrijavanju 39

40

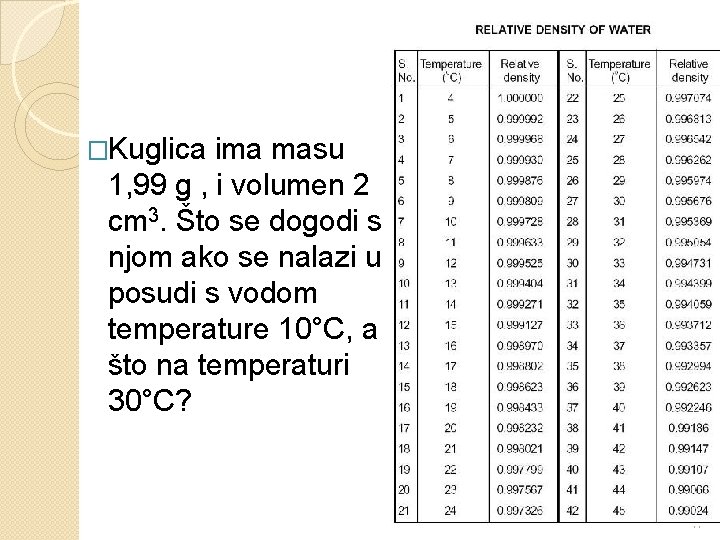
�Kuglica ima masu 1, 99 g , i volumen 2 cm 3. Što se dogodi s njom ako se nalazi u posudi s vodom temperature 10°C, a što na temperaturi 30°C? 41

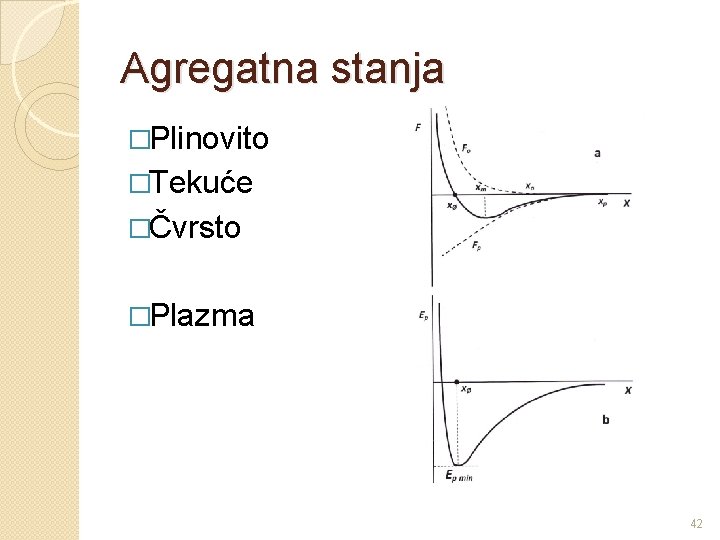
Agregatna stanja �Plinovito �Tekuće �Čvrsto �Plazma 42

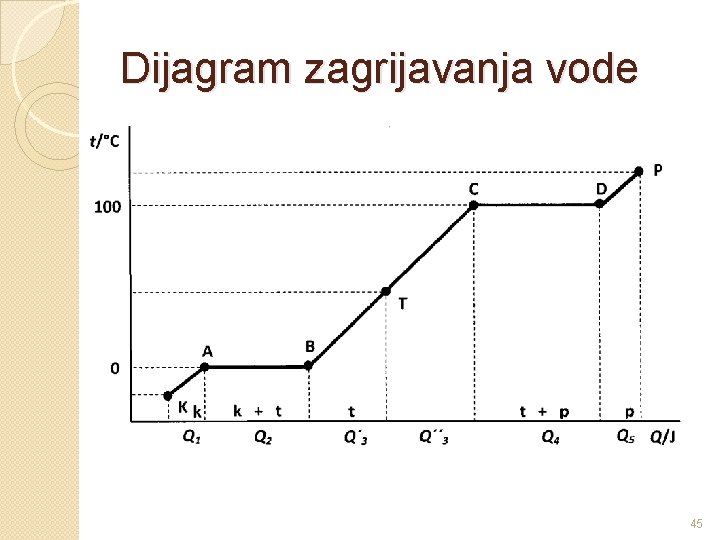
Posljedice toplinske interakcije 1. promjena q temperature sustava: Q = m c ΔT c – specifični toplinski kapacitet tvari – energija potrebna da se temperatura sustava mase od 1 kg promijeni za 1 stupanj 2. promjena agregatnog stanja: Q = q ΔH = Δm Lp, T- latentna toplina prijelaza – energija potrebna da masa 1 kg latentna toplina prijelaza promijeni fazu pri stalnom tlaku i na stalnoj temperaturi 3. kemijske reakcije – egzogene i endogene – toplina se oslobađa iz sustava ili ulazi u sustav ovisno o energiji stanja sudionika u reakciji 43

�Komadu bakra mase 3, 5 kg temperature 170°C hlađenjem snizimo unutrašnju energiju za 1, 6*105 J. Do koje se temperature ohladio komad bakra? Rj, t 50°C �Kolika energija je potrebna da 100 g alkohola na temperaturi 78. 3 °C ispari? Rj, Q = 85, 5 k. J 44

Dijagram zagrijavanja vode 45

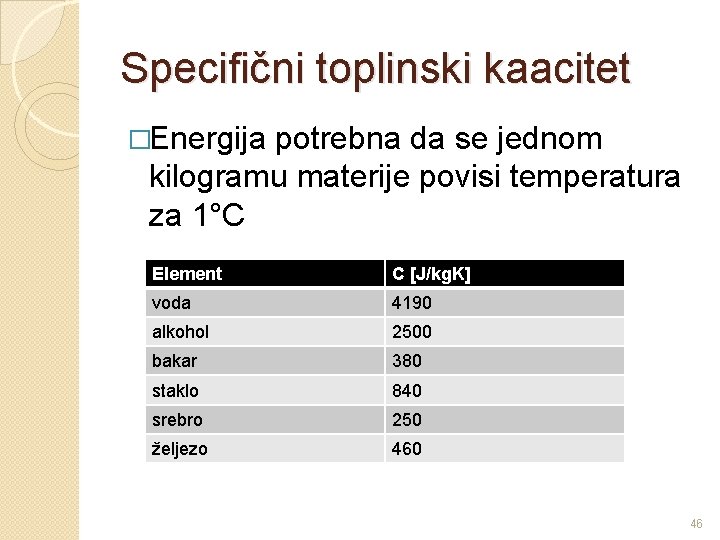
Specifični toplinski kaacitet �Energija potrebna da se jednom kilogramu materije povisi temperatura za 1°C Element C [J/kg. K] voda 4190 alkohol 2500 bakar 380 staklo 840 srebro 250 željezo 460 46

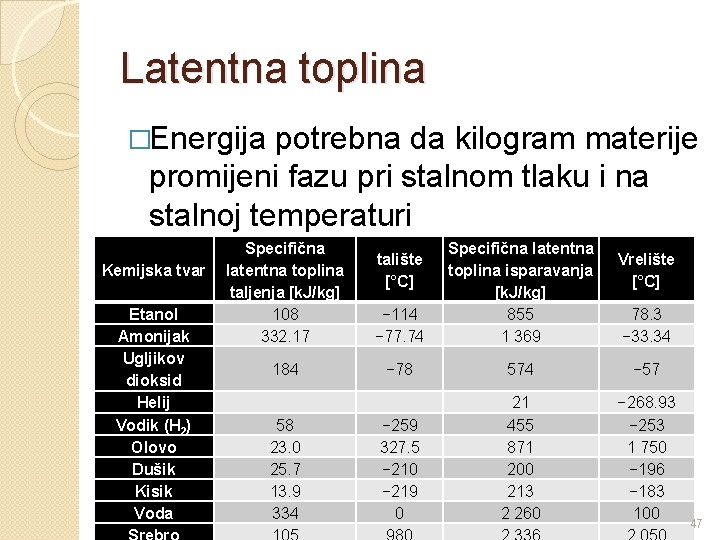
Latentna toplina �Energija potrebna da kilogram materije promijeni fazu pri stalnom tlaku i na stalnoj temperaturi Kemijska tvar Etanol Amonijak Ugljikov dioksid Helij Vodik (H 2) Olovo Dušik Kisik Voda Specifična latentna toplina taljenja [k. J/kg] 108 332. 17 − 114 − 77. 74 Specifična latentna toplina isparavanja [k. J/kg] 855 1 369 184 − 78 574 − 57 58 23. 0 25. 7 13. 9 334 − 259 327. 5 − 210 − 219 0 21 455 871 200 213 2 260 − 268. 93 − 253 1 750 − 196 − 183 100 talište [°C] Vrelište [°C] 78. 3 − 33. 34 47

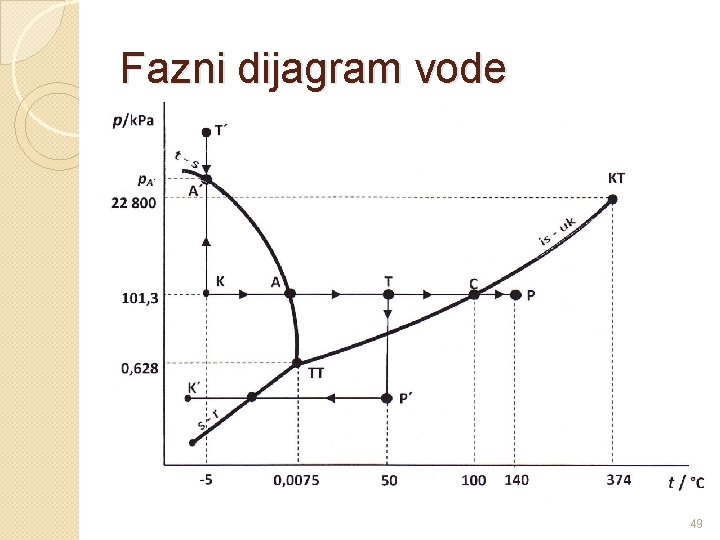
Dijagram stanja (fazni dijagram) �Pokazuje ravnotežno stanje zatvorenog sustava uz određene vrijednosti tlaka i temperature �Trojna točka određuje ravnotežu triju faza �Krivulje taljenja isparavanja i sublimacije 48

Fazni dijagram vode 49

50

Prijenos topline �Kondukcija ili vođenje �Konvekcija ili prenošenje �Iradijacija ili zračenje �Evaporacija ili isparavanje 51

Kondukcija �Prelazak topline u nekom tijelu s dijela tijela više temperature na dio tijela niže temperature �Količina prenesene enregije je veća što je veća razlika u temperaturama �Hvo – brzina prijenosa; S – presjek; l – duljina; T 1 i T 2 – temperature; kvo – konstanta toplinske vodljivosti 52

Konvekcija �Zagrijavanje -> širenje -> smanjenje gustoće =>konvekcijska cirkulacija �Hladni dijelovi nprekidno zamjenjuju toplije �tt i tf – temperature tijela i fluida; S – presjek; kpr – konstanta prijenosa 53

Radijacija �Tijelo više temperature predaje tijelu niže temperature energiju �Tijelo niže temperature tu energiju apsorbira �Sva tijela zrače energiju u obliku elektromagnetskih valova �e – koeficijent emisije; σ – Stefan- Boltzmannova konstanta 54

Isparavanje �Izlaskom molekula sa velikom kinetičkom energijom iz tekućine smanjuje se prosječna kinetička energija molekula koje ostaju, a time i temperatura �qi – specifična toplina isparavanja 55

Gibbsova energija i kemijski potencijal �Za ravnotežne izotermne i izobarne toplinske procese u zatvorenom sustavu vrijedi: �Iz toga slijedi �p, V = const. �Gibbsova energija 56

�Reverzibilne reakcije ΔG=0 �Promjena entalpije sustava kompenzirana promjenom entropije �Gibbsova energija je onaj dio entalpije koji se može iskoristiti za obavljanje rada 57

Ireverzibilni procesi �Neravnotežni spontani procesi idu u smjeru smanjenja Gibbsove energije do minimalne vrijednosti 58

Kemijski potencijal �Energija potrebna da se prenese 1 mol tvari 59

Mehaničke interakcije i Gibbsova slobodna energija �Spontani su samo oni procesi gdje je ΔS>0 pa je ΔG<0 i ΔW<0 �Sustav spontano izvodi rad prema okolini �U biološkim sustavima W=VΔp 60

�Pretpostavka p. V=n. RT G 0 – Standardna Gibbsova energija za homogeni sustav 61

�Kod razmatranja parcijalnih tlakova otopljnih čestica u razrijeđenim otopinama: 62

Difuzija �Proces prodiranja jedne tvari među čestice druge tvari �Nasumično translatorno gibanje molekula u fluidima �Sudaranje molekula => brzina difuzije ~ gradijent koncentracije (Δc/ Δx) ◦ Δc je razlika koncentracije na nekoj udaljenosti Δx �Fickov zakon: 63

�D – koeficijent difuzije S – presjek; ΔN – broj molekula �Negativan predznak => smjer difuzije je suprotan smjeru porasta koncentracije �Veća temperatura => više gibanja => brža difuzija �Brže se odvija u plinovima nego u tekućinama �https: //www. youtube. com/watch? v=Bz 02 z 4 GSS 0 k 64

�I. Fickov zakon se često piše u diferencijalnom obliku Δx → 0 Δt → 0 �Tok tvari: �I. Fickov zakon: 65

�Kod stacionarne difuzije prisutan je stalni tok čestica, a da se pritom ne mijenja gradijent koncentracije. �Potreban je proces izvan sustava koji će održavati gradijent koncentracije → aktivni trasport → biološki sustavi su otvoreni �aktivni transport je definiran kao pozitivni rad. �Kod nestacionarne difuzije koncentracija ovisi i o prostoru i o vremenu. Protok čestica dovodi do izjednačavanja koncentracija u sistemu. �II. Fickov zakon: 66

Koeficijent difuzije �Fickov zakon ne govori nista o ovisnosti brzine difuzije o temperaturi, veličini čestica ili svojstvima medija. �Te ovisnosti su sadržane u koeficijentu difuzije D (Stokes Einsteinova formula): ◦ Za slučaj kada su čestice kugle radijusa r, koje difundiraju kroz sredstvo viskoznosti η 67

Osmoza �Selektivna difuzija – kroz polupropusne menbrane �Voda 0, 38 nm; Glukoza 0, 88 nm �Efektivna osmotska koncentracija (o): �Osmotski tlak koji proizvodi čisto otapalo na membranu odjeljka u kojem se nalazi otopljena tvar: 68

�https: //www. youtube. com/watch? v=Sr ON 0 n. EEWmo 69

Vrste otopina �Razlika između osmotskih tlakova s unutarnje i vanjske strane membrane mjera je za količinu protokavode kroz membranu ◦ Izotonična otopina – vanjska i unutarnja koncentracija su jednake ◦ Hipertonična – vanjska koncentracija veća od unutarnje – stanica se isušuje ◦ Hipotpnične – vanjska manja od unutarnje – stanica bubri 70

Nernstova jednadžba c 1 i c 2 koncntracije iona unutar i izvan membrane; F – Faradejeva konstanta 71