Termodinamicamente estable Disolucin Microemulsin Termodinamicamente inestable Suspension Emulsion


• Termodinamicamente estable – Disolución – Microemulsión • Termodinamicamente inestable – Suspension – Emulsion Cuando algo es estable TD mantiene su forma física

• Disolución – Dispersión molecular clara – Agradable a la vista • Suspensión – Opaca – Cambios visibles con el tiempo • Emulsión – Grasosa y suave – Viscosa
• Disolución – Acción rápida • Suspensión – Acción lenta • Emulsión – Acción lenta


• Mezcla homogénea , < 1 nm • Moléculas del soluto dispersas entre las moléculas del solvente • Preparado líquido donde la sustancia activa esta disuelta en agua

– Estado físico: S-S, S-L, S-G, L-S, LL, L-G, G-S, G-L, G-G. – Tipo de disolvente: acuosos y no acuosos – Uso: oftálmicos, etc.

Solubilidad. - Definición. - ¿Cómo conocerla? . - Factores que la afectan: . - Estructura cristalina y tipo de molécula Modificación química (cambios en la actividad farmacológica y estudios de toxicidad y todos los de una molécula nueva). - Temperatura (Mov. browniano y Le Chatelier)

. - p. H (sustancias ácidas, básicas o sin propiedades ácidobase) Necesidad de buffer: debe ser biodisponible, su capacidad buffer, permitir c. o. l. aceptables, no afectar estabilidad del activo, ni su actividad . - Constante dieléctrica . - Cosolvencia: Deben ser bioaceptados (etanol, glicerina, sorbitol, propilenglicol, polietilenglicol). - Salting-in
. - Tensoactivos Ccm, humectación, toxicidad, HLB mayor de 15 son maravillosos solubilizantes. - Complejación (CDs, Kest, quien limita la solubilidad, via oral - constante, estequiometría). - Hidrotropía Aditivos cambian la solubilidad del fármaco (ejem. : altas [benzoato de Na] aumenta la solubilidad de la cafeína). - Otros Dispersiones sólidas y liposomas
Velocidad de disolución. - Definición. - ¿Cómo conocerla? . - Factores que la afectan: . - Estructura cristalina y tipo de molécula. - Temperatura . - p. H. - Disolvente
. - Factores que la afectan - Velocidad de agitación. - Tipo de agitación. - Superficie de contacto. - Tamaño de partícula

¿PORQUE USAR DISOLUCIONES EN FARMACIA? Ventajas 1. - Lo pueden tomar personas no capaces de deglutir sólidos 2. - Velocidad rápida de absorción (La absorción depende de la concentración de fármaco, volumen de líquido administrado, p. H, viscosidad, excipientes, transito intestinal, etc. )

Inconvenientes 1. - Inestabilidad del fármaco en disolución (se puede estabilizar de algún modo si las ventajas son mas que los inconvenientes? ) 2. -Fármacos de baja solubilidad en agua o baja velocidad de disolución 3. - Si la dosis es grande se dificulta la administración 4. - Debe ser farmacéuticamente elegante
Consideraciones a la hora de preparar una disolución 1. - Finalidad del fármaco 2. - Uso interno o externo 3. - Concentración del fármaco 4. - Selección del vehículo 5. - Estabilidad física y química 6. - Preservación de la preparación 7. - Uso de excipientes adecuados

Excipientes ØMantener la apariencia ØColor ØTransparencia ØConservadores ØTensoactivos ØProtección del fármaco ØBuffers ØAntioxidantes ØFavorecer las c. o. l. ØAzúcares ØSaborizantes

Disolventes farmacéuticos recomendados por la USP Agua Purificada, para inyección, estéril Alcoholes Etilico, butílico, isopropílico, metílico Polioles Glicerina, propilenglicol, hexilenglicol, PEG Cetonas Acetona, metilisobutilcetona Ésteres Benzilbenzoato, acetato de etilo, hidrato de amileno, diclorometano Aceites Maiz, algodón, cacahuate, sesamo, mineral

• Soluciones acuosas – Soluciones acuosas edulcoradas y otras soluciones viscosas • Soluciones no acuosas

Soluciones acuosas • Soluciones en las que el disolvente utilizado es el agua

Soluciones de lavado • Destinada a una parte o a una cavidad del cuerpo • Agentes limpiadores o antisépticos • Tipos: – Agua oxigenada – Solución de hipoclorito de sodio para uso quirúrgico – Soluciones de yodo
Enemas • Inyecciones rectales Evacuar el intestino (enemas de evacuación de Na. Cl, bicarbonato de sodio) • Propiedades. - Antihelmínticas – Contener sustancias radioopacas que posibilitan el examen radiológico del intestino grueso

Colutorios • Contienen antisépticos, antibióticos y/o agentes anestésicos • Uso: faringe y la nasofaringe. • Gargarismos

Enjuagues bucales • Cumplir 2 objetivos : terapéutico y cosmético Uso terapéutico • Reducir la formación de placas • La gingivitis • Las caries dentales • La estomatitis Uso cosmético • Combatir la halitosis (agentes antimicrobianos o aromatizantes)

Soluciones nasales • Introducidas en las fosas nasales • Forma de gotas o sprays – Nuevos estudios para la admón. de hormonas (luteinizante, insulina) Soluciones óticas • Principales fármacos: Analgésicos, Antibióticos Agentes antiinflamatorios • Líquidos viscosos, glicerina y/o PEG

Soluciones oftálmicas • Administrar un fármaco en el ojo • Desventaja principal: – Tiempo de contacto relativamente breve entre la medicación y las superficies absorbentes – Puede ser aumentado con la inclusión de un agente que aumente la viscosidad, como la metilcelulosa

Propiedades coligativas Presión osmótica Disminución de la presión de vapor Aumento del punto ebulloscópico Descenso del punto crioscópico

Presión osmótica. - Membrana semipermeable o selectiva. - Presión osmótica del líquido corporal= 0. 9% de Na. Cl Isotonicidad vs isoosmoticidad. - Ajuste de tonicidad. - Metodo de equivalentes de Na. Cl (E)

Planteamiento del problema • Se pretende desarrollar una disolución oftálmica, de acción duradera al 0. 1% de fosfato sódico de dexametasona. Dicha formulación debe de cumplir con una serie de requerimientos para evitar, en lo posible, una sensación desagradable en los ojos, éstos son p. H y tonicidad similares a los del líquido lacrimal. En función de lo anterior, propón una fórmula que cumpla con estos requisitos, así como un posible procedimiento de manufactura, considerando los factores de proceso a controlar. • Recuerda que el agua es un buen medio de cultivo para microorganismos.

Fosfato sódico de dexametasona al 0. 1% Agua purificada c. b. p. 30 ml 0. 9 % =. 270 g de Na. Cl en 30 ml E=0. 18 g de Na. Cl por 1 g de fármaco 0. 1% significa 0. 03 g y por 0. 18 es 0. 054 g de Na. Cl 0. 27 -0. 03= 0. 265 me da cuanto Na. Cl necesito Si tengo dextrosa y se que E=0. 16, también lo puedo usar
Soluciones acuosas edulcoradas y otras soluciones viscosas Melitos • Base utilizada: miel Mucílagos • Dispersión de gomas en agua • Viscosidad

Jarabes • Concentrados de azúcares (viscosas) • Agua u otro líquido acuoso • Enmascarar sabor de fármacos amargos o salados

• Preparación – Disolución con calor – Agitación sin calor (volatilidad o termolabilidad) – Agregado de un líquido medicinal al jarabe – Percolación. – Reconstitución

Factores importantes Jarabes de: en la Formulación - Efecto salting-out - Cosolvencia - p. H - Temperatura - Tipo de carbohidrato y concentración de
Posibles problemas de formulación • Inversión de azucares • Caramelización • Cristalización • Crecimiento microbiano
![Inversión [H+] T + Fermentación Alcohol Inversión [H+] T + Fermentación Alcohol](http://slidetodoc.com/presentation_image_h/aa695ed3bf3efebe9dea8f6c6daa6a39/image-35.jpg)
Inversión [H+] T + Fermentación Alcohol

Planteamiento del problema Se desea elaborar un Jarabe de Dextrometorfano cuya formulación sea estable al crecimiento microbiano, sin problemas de caramelización y/o precipitación, con una viscosidad de 80 cp, con bajo porcentaje de inversión.

Materia prima de la que dispone el alumno: • Principio Activo - Bromhidrato de Dextrometorfano • Carbohidratos - Glucosa - Sacarosa • Conservadores -Metilparabeno -Propilparabeno -Ac. Benzóico • Otros -Glicerina -Propilenglicol • Viscosantes -Sorbitol - Carboximetilcelulosa -Sacarina -Agua Purificada
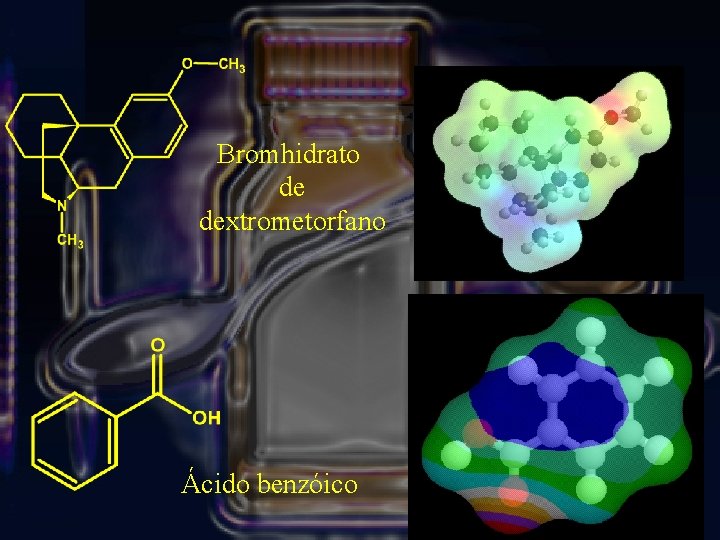
Bromhidrato de dextrometorfano Ácido benzóico
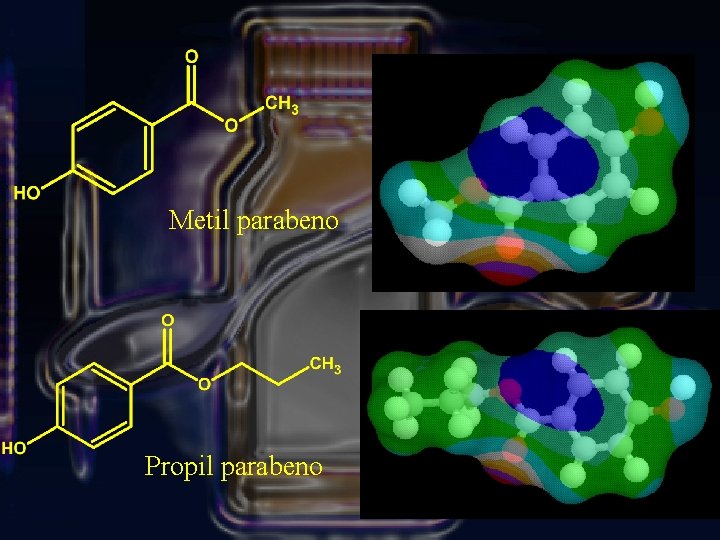
Metil parabeno Propil parabeno

Solubilidad El primer paso a realizar cuando se pretende formular un principio activo en una forma farmacéutica líquida es hallar la solubilidad del fármaco y de los excipientes a utilizar. Para ello, se plantea que el alumno realice estos estudios del siguiente modo: . - en un baño termostatado a 25°C y a una velocidad de agitación determinada se colocan cuatro tubos de ensayo con 5 m. L de agua purificada.

Solubilidad. - a cada uno de ellos se les adiciona un exceso de la molécula a ensayar (bromhidrato de dextrometorfano, metilparabeno, propilparabeno o ácido benzóico). . - se dejan en agitación hasta alcanzar el equilibrio (el próximo día de clase). . - se hace una curva de calibrado para cada una de las sustancias problema en espectroscopía UV-Visible. . - se filtran las muestras y se cuantifica la concentración disuelta por espectroscopía UV-Vis.

Velocidad de Disolución Para saber el tiempo que tardan en disolverse los diferentes componentes de una formulación es necesario conocer los datos de la velocidad de disolución (constantes cinéticas) de los mismos.

Velocidad de Disolución Para ello, el estudiante hará el siguiente estudio: . - en un espectrofotómetro HP 8452 A control de temperatura (25°C) y de agitación (100 r. p. m. ) realizará una cinética de disolución poeniendo en la celda un exceso de soluto. . . - se monitorearán dos longitudes de onda, la de máxima absorción de la molécula y una a la cual sepamos que la absorción es nula (700 nm) y posteriormente se graficará concentración vs tiempo. . - haciendo uso del programa Microcal Origin se obtendrán las constantes de velocidad.

Salting-out El alumno llevará a cabo estudios de solubilidad de las cuatro moléculas mencionadas anteriormente, pero ahora en presencia de diferentes concentraciones de azúcares. Así podrá observar el efecto salting-out de los mismos

Cosolvencia Para poder observar de manera experimental el efecto de cosolvencia, los alumnos harán estudios de la solubilidad de los parabenos en presencia de diferentes cantidades de propilenglicol. Se les propone a los estudiantes la formación de complejos de inclusión con b-ciclodextrina, de este modo conocerán otra manera de mejorar la solubilidad

Temperatura Un problema inherente a la fabricación de jarabes por esta metodología es el de caramelización. Para poder observarlo y controlarlo, así como relacionarlo con la temperatura, se propone realizar el jarabe con 80% de azúcares a altas temperaturas, ya que de este modo se mejora la solubilidad y se observa la problemática mencionada.

Cristalización Se hacen estudios de cristalización a diferentes tiempos (estabilidad) y concentraciones de azúcar, así como en presencia de diferentes cantidades de glicerina (0. 1%, 5%, 10%).

Estudio de crecimiento microbiano en función de los conservadores Se guardarán a temperatura ambiente y en refrigerador tres muestras con 30%, 55% y 80% de azúcares, en presencia y ausencia de estabilizantes (a elección del estudiante). Posteriormente se observará a simple vista si hay o no crecimiento microbiano.

Pruebas a realizarle a la forma terminada -Viscosidad - Crecimiento microbiano - Cristalización y Apariencia Uniformidad de contenido - Color - p. H - Inversión de azúcares Cuerpos extraños Densidad

Soluciones no acuosas Elixires • Hidroalcóholicos, sabor agradable y edulcorados de uso oral Glicerinas • Soluciones o mezclas de sustancias medicinales en no menos del 50% en peso de glicerina • Son muy viscosas y algunas son gelatinosas • Solución ótica de antipirina y benzocaína. (remoción del cerumen)

Linimentos • Disoluciones de varias sustancias en aceite • Estas preparaciones están destinadas al uso externo Oleovitaminas • Son aceites de hígado de pescado diluidos con aceite vegetal comestible o soluciones de las vitaminas indicadas • O los concentrados vitamínicos (Vit A y D) en aceite de hígado de pescado

Disoluciones Farmacéuticas (Composición) 1. –Disolvente Acuoso No acuoso Cosolventes 2. - Sales Buffers Isotonicidad Aumento de solubilidad 3. - Conservadores

3. - Otros Sustancias hidrotropizantes Azúcares etc. A. - ¿Y que importancia tiene en farmacia? B. - ¿Por qué tiene mal sabor? C. - Solucionar el problema

A. - ¿Y que importancia tiene en farmacia? Evitar conseguir una pauta posológica adecuada (niños y ancianos) B: - ¿Por qué el sabor? SABOR, FLAVOR: sensación mixta que relaciona los cinco sentidos (*) TIPOS DE SABORES: ácido, dulce, salado, amargo Resultado de efectos fisiológicos y psicológicos (**) ¿Quién los detecta? Papilas gustativas

a a b a d c a e f g a a a a: Receptores para todos los sabores b: dulce, salado, agrio c: salado y agrio d: ácido e: sin sensación gustativa f: dulce y ácido g: amargo, dulce y ácido Lengua Papilas Terminaciones nerviosas Reacción al sabor con la humedad de la boca Actividad fisicoquímica Impulsos eléctricos (percepción del sabor en el cerebro)

(*) Relación con otros sentidos: Cebolla, dulce si las fosas nasales están cerradas (**) Resultado de efectos fisiológicos y psicológicos Test de Paulov: segregación gástrica al oir sonidos (morder manzana) Sensación de asco por la textura: ostiones, caracoles, etc. Relación olor-color: cereza roja Fisiológicos: Catarro: disminuye el efecto del gusto

Bases estructurales del sabor Sabor dulce. - Relación con los grupos –OH, ¿qué pasa con la sacarina? . - Th de la unidad AH/B (Shallenberger y Acree), en la molécula sápida y en el receptor AH= protón unido a un átomo B=grupo electronegativo. - Th anterior más la presencia de grupos lipofílicos (zona g), en posiciones espaciales adecuadas para unirse al receptor Teoría tripartita del sabor dulce A más grupos hidrófobos, mayor dulzor hasta llegar al sabor amargo

Sabor amargo. - 1 a th: Presencia de un grupo polar y una parte hidrofóbica. - 2 da. Th: su estructura es como la de los azúcares, pero depende de la estructura que toma puede ser dulce o amargo. ej: aminoácidos, los D son dulces y los L amargos Sabor salado Muy complejo Mezclas psicológicas de los cuatro sabores Th: los cationes causan el sabor salado y los aniones lo inhiben (el sabor final dp de quien tiene un sabor más intenso) Sabor ácido Se desconoce su mecanismo. Se cree que es más importante el peso, tamaño y polaridad global que la [H+]

Otros sabores: Picante: irritante Astringente: sequedad y encogimiento (unión a las proteínas de la saliva y da precipitados, taninos) Refrescante: reacción endotérmica de disolución o evaporación ¿Cómo medimos el sabor? . - Umbral de reconocimiento: Conc. Mínima de una disolución de la sustancia a ensayar a la que se percibe el sabor. - Poder edulcorante relativo: conc. Sustancia patrón/conc. Sust. Problema (ambas con igual intensidad de sabor, ejem: sacarosa)

¿Y qué sabor predomina? Competencia de interacciones por el receptor C. Solucionar el problema. - Mezclado. - Enmascaramiento: uso de un sabor más intenso que el que se enmascara. - M. Físicos: compuestos insolubles emulsiones efervescencia aumento de la viscosidad recubrimiento: grageas, cápsulas, nano y microcápsulas

. - M. Químicos: adsorción del fármaco a un sustrato formación de complejos de inclusión (ciclodextrinas, dendrímeros, etc. ). - M. Fisiológicos: anestesiar las papilas con sabores fuertes (cepacol o graneodín) Saborizantes usados en productos farmacéuticos: ej. : glucosa, sacarosa, miel, jarabes de frutas, etc.

Aceptación del paciente=efecto psicológico Consideraciones: solubilidad inerte-no tóxico - no interacciona con otros componentes de la formulación Colorantes: Naturales. - Minerales = pigmentos, óxido férrico, negro de humo. - Vegetales: b-caroteno, clorofila, azafrán, etc. . - animales: rojo de la cochinilla (ac. carmínico), etc Los que se han caracterizado se hacen sintéticos

Sintéticos: 1856. - WH Perkin intentaba sintetizar quinina y obtuvo púrpura de Pekín, a partir de ahí todos los colorantes artificiales se llamaron colorantes de anilina Según FDA y para evitar toxicidad: . - FDC. Alimentos, medicamentos y cosméticos Habitualmente son aniónicos (sales de sodio), precipitan con cationes. - DC: medicamentos y cosméticos. - DC externos Concentraciones de uso . - Pequeñas, suficientes para dar color, pero no pintar piel o ropa . - Líquidos: 0. 0005%-0. 001% . - Polvos: 0. 1%
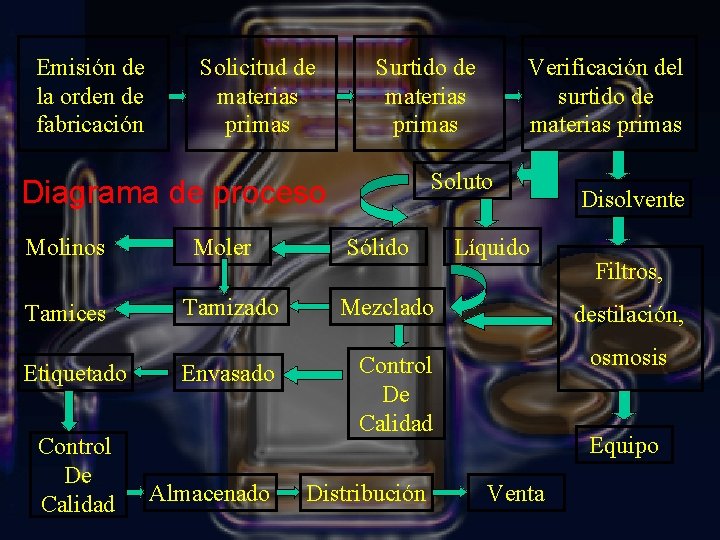
Emisión de la orden de fabricación Solicitud de materias primas Surtido de materias primas Soluto Diagrama de proceso Molinos Tamices Etiquetado Control De Calidad Moler Sólido Tamizado Mezclado Envasado Control De Calidad Almacenado Verificación del surtido de materias primas Distribución Líquido Disolvente Filtros, destilación, osmosis Equipo Venta

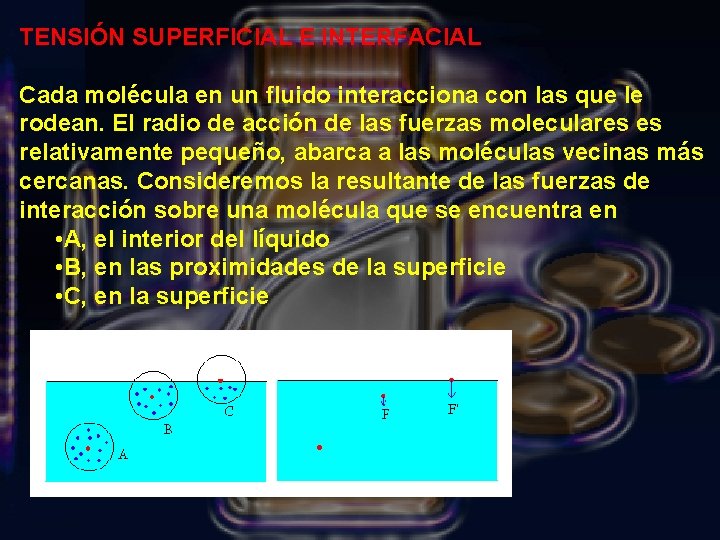
TENSIÓN SUPERFICIAL E INTERFACIAL Cada molécula en un fluido interacciona con las que le rodean. El radio de acción de las fuerzas moleculares es relativamente pequeño, abarca a las moléculas vecinas más cercanas. Consideremos la resultante de las fuerzas de interacción sobre una molécula que se encuentra en • A, el interior del líquido • B, en las proximidades de la superficie • C, en la superficie

Molécula A (lejos de la superficie). Por simetría, será nula la resultante de todas las fuerzas atractivas procedentes de las moléculas (en color azul) que la rodean. Molécula B, por existir en valor medio menos moléculas arriba que abajo, la molécula en cuestión estará sometida a una fuerza resultante dirigida hacia el interior del líquido. Molécula C, la resultante de las fuerzas de interacción es mayor que en el caso B. La fuerzas de interacción (cohesivas), hacen que las moléculas situadas en las proximidades de la superficie libre de un fluido experimenten una fuerza dirigida hacia el interior del líquido. Como todo sistema mecánico tiende a adoptar espontánea_ el estado de más baja energía potencial, se comprende que los líquidos tengan tendencia a presentar al exterior la superficie más pequeña posible.
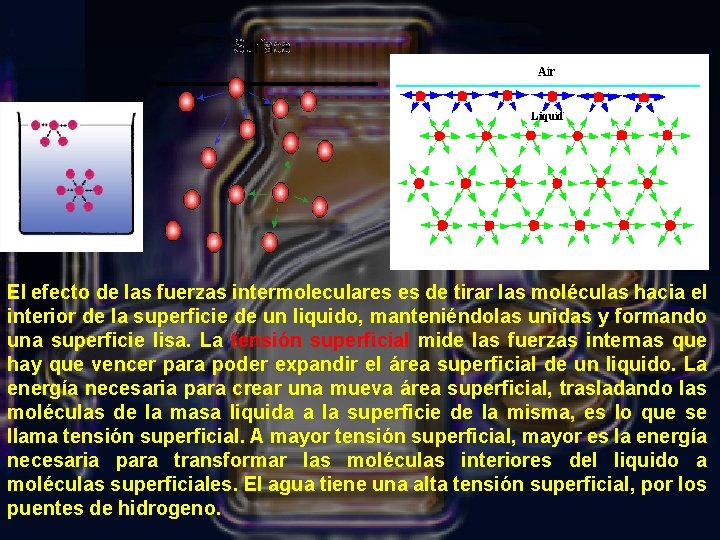
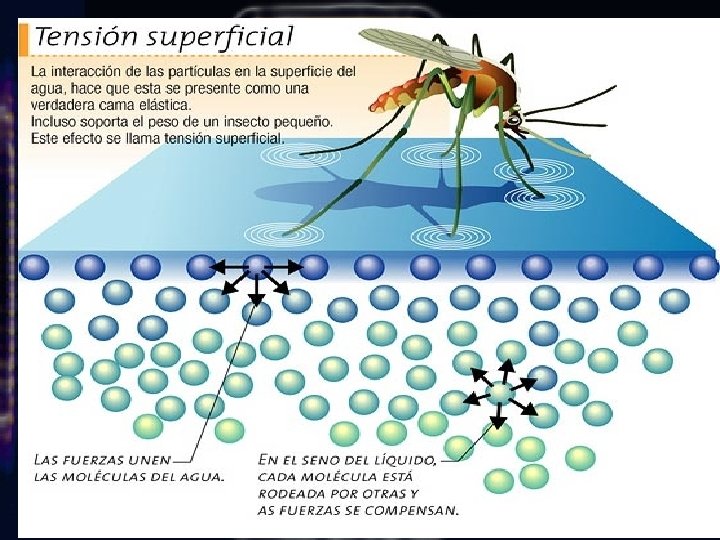
El efecto de las fuerzas intermoleculares es de tirar las moléculas hacia el interior de la superficie de un liquido, manteniéndolas unidas y formando una superficie lisa. La tensión superficial mide las fuerzas internas que hay que vencer para poder expandir el área superficial de un liquido. La energía necesaria para crear una mueva área superficial, trasladando las moléculas de la masa liquida a la superficie de la misma, es lo que se llama tensión superficial. A mayor tensión superficial, mayor es la energía necesaria para transformar las moléculas interiores del liquido a moléculas superficiales. El agua tiene una alta tensión superficial, por los puentes de hidrogeno.

EJEMPLOS • Agua • Puentes de hidrógeno intermoléculares • Tensión superficial a 20°C es 7. 29 x 10 -2 J/m 2 = 72. 8 m. N/m. • Mercurio • Enlaces intermoleculares metálicos • Tensión superficial a 20°C es 4. 6 x 10 -1 J/m 2

TENSIÓN INTERFACIAL Dos líquidos inmiscibles En la interfase hay un conjunto de fuerzas intermoleculares no balanceadas que da como resultante una fuerza dirigida al interior de su respectiva fase líquida Se produce una turbulencia en la superficie del líquido a escala molecular que tiene como resultado un tráfico de doble vía en el interior del líquido o fase de bulto y la superficie y entre la superficie y la fase vapor (tiempo de vida promedio de una molécula en la superficie de un líquido 10 -6 s)

FENÓMENO DE ADSORCIÓN Y TENSOACTIVOS Energía libre de superficie (DGs): trabajo que debe ser hecho para aumentar la superficie por unidad de área Las moléculas deben de llevarse del seno de la disolución a la superficie A mayor Ts mayor DGs Adsorción: fenómeno en el cual las moléculas dispersadas en un líquido son principalmente distribuidas en la superficie Menor DGs menor Ts

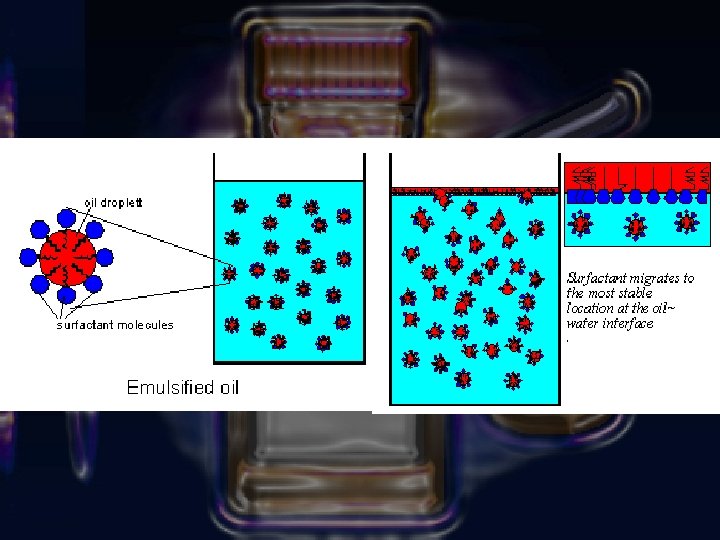
Moléculas que muestran adsorción positiva: TENSOACTIVOS (surfactantes o agentes de superficie activa) Definición: son moléculas que presentan una estructura polar-no polar (ampífilica), con tendencia a localizarse en la interfases formando una capa monomolecular adsorbida en la interfase. Las soluciones de tensoactivos resultan ser activas al colocarse en forma de capa monomolecular adsorbida en la superficie entre las fases hidrofílicas e hidrofóbicas. Esta ubicación "impide" el tráfico de moléculas que van de la superficie al interior de líquido en busca de un estado de menor energía, disminuyendo así , el fenómeno de tensión superficial.
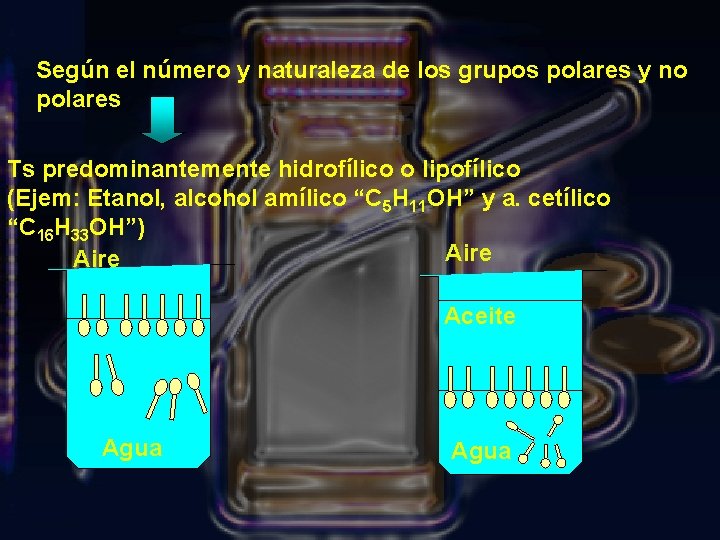
Según el número y naturaleza de los grupos polares y no polares Ts predominantemente hidrofílico o lipofílico (Ejem: Etanol, alcohol amílico “C 5 H 11 OH” y a. cetílico “C 16 H 33 OH”) Aire Aceite Agua
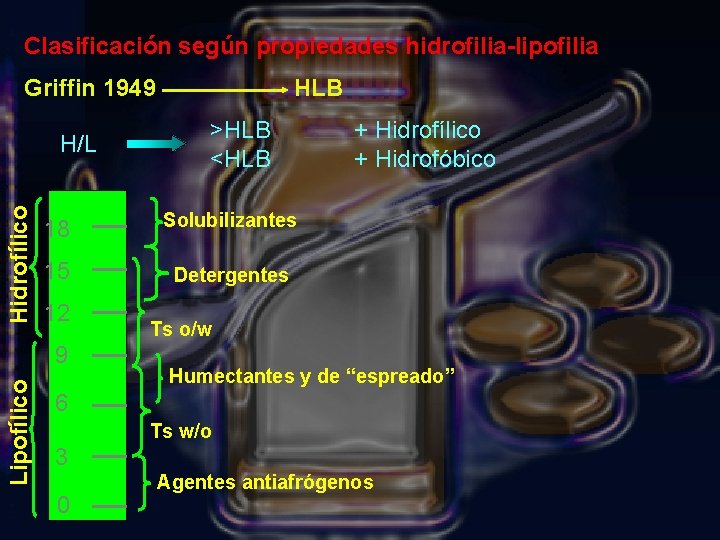
Clasificación según propiedades hidrofilia-lipofilia Griffin 1949 Hidrofílico H/L >HLB <HLB 18 Solubilizantes 15 Detergentes 12 9 Lipofílico HLB + Hidrofílico + Hidrofóbico Ts o/w Humectantes y de “espreado” 6 Ts w/o 3 0 Agentes antiafrógenos

Solubility and HLB • • Solubility HLB Range No dispersability in water 1 -4 Poor Dispersion in water 3 -6 Milky appearance 6 -8 Stable milky appearance 8 -10 Tanslucent to clear dispersion 10 -13 Clear solution 13+

HLB de algunos tensoactivos Tensocativo • A. Oleico • Monogliceridos acetilados • Sorbitan trioleato • Glicerol dioleato • Sorbitan tristearato • Propilenglycol monostearato • Glicerol Monoleato • Glicerol monostearato HLB 1. 0 1. 5 1. 8 2. 1 3. 4 3. 8
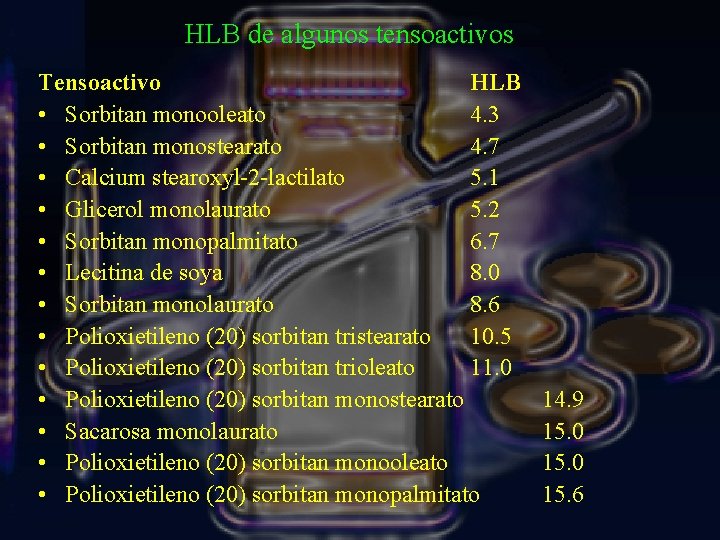
HLB de algunos tensoactivos Tensoactivo HLB • Sorbitan monooleato 4. 3 • Sorbitan monostearato 4. 7 • Calcium stearoxyl-2 -lactilato 5. 1 • Glicerol monolaurato 5. 2 • Sorbitan monopalmitato 6. 7 • Lecitina de soya 8. 0 • Sorbitan monolaurato 8. 6 • Polioxietileno (20) sorbitan tristearato 10. 5 • Polioxietileno (20) sorbitan trioleato 11. 0 • Polioxietileno (20) sorbitan monostearato • Sacarosa monolaurato • Polioxietileno (20) sorbitan monooleato • Polioxietileno (20) sorbitan monopalmitato 14. 9 15. 0 15. 6
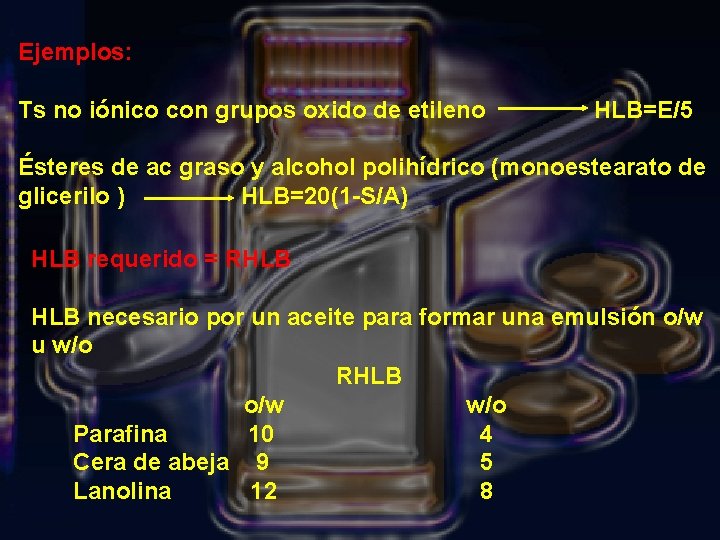
Ejemplos: Ts no iónico con grupos oxido de etileno HLB=E/5 Ésteres de ac graso y alcohol polihídrico (monoestearato de glicerilo ) HLB=20(1 -S/A) HLB requerido = RHLB necesario por un aceite para formar una emulsión o/w u w/o RHLB o/w w/o Parafina 10 4 Cera de abeja 9 5 Lanolina 12 8

Calculate the required HLB for the oil phase of the following o/w emulsion: cetyl alcohol 15 g. , white wax 1 g. Lanolin 2 g, emulsifier (q. s. ). water 100 g. Required HLB Fraction Cetyl alcohol White wax Lanolin (from reference) 15 x 12 x 10 x Total required HLB 15/18 12. 5 1/18 0. 7 2/18 1. 1 14. 3

What is the HLB of the mixture of 40 % Span 60 (HLB = 4. 7) and 60 % Tween 60 (HLB = 14. 9)? HLB of mixture: 4. 7 x 0. 4 + 14. 9 x 0. 6 = 10. 8 In what proportion should Span 80 (HLB = 4. 3) and Tween 80 (HLB = 15. 0) be mixed to obtain “required” HLB of 12. 0? 4. 3. (1 -x) + 15. x = 12 x = 0. 72 % Tween 80 and 28 % Span 80

Problema Ingrediente Cera de abeja lanolina parafina Cantidad 15 g 10 g 20 g RHLB (o/w) 9 12 10 Alc cetilico ts conservador color Agua 5 g 2 g 0. 2 g 15 100 g Total fase grasa=50 g Tween 80=15 Span 80=4. 3

Otra propiedad de los tensoactivos (“BULK” de la solución) En solución diluída se comportan como electrolitos normales A una concentración X ocurren cambios fisicoquímicos (cambio brusco de tensión superficial, de conductividad, de presión osmótica, etc. ) Mc. Bain : formación de agregados moleculares de tensoactivos llamados "micelas", (la parte hidrocarbonada de las moléculas se encuentra hacia adentro en el centro de la micela y los grupos hidrofílicos hacia afuera en contacto con el medio acuoso) La concentración a la cual se forman las micelas se le llama "concentración micelar crítica" y es la concentración a la cual, ocurren los cambios fisicoquímicos.
Mezclas anfifilo-agua Principio de las fuerzas opuestas (Tanford 1991) Interacción hidrofóbica Interacciones van der waals hidratación micelas
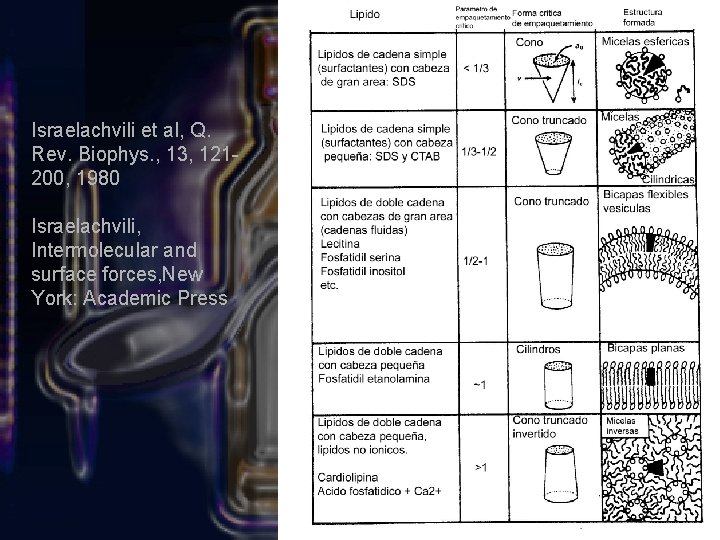
Israelachvili et al, Q. Rev. Biophys. , 13, 121200, 1980 Israelachvili, Intermolecular and surface forces, New York: Academic Press
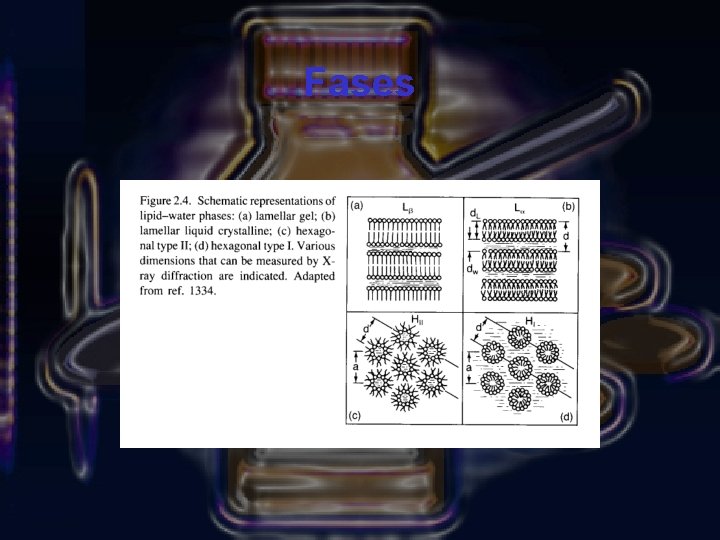
Fases
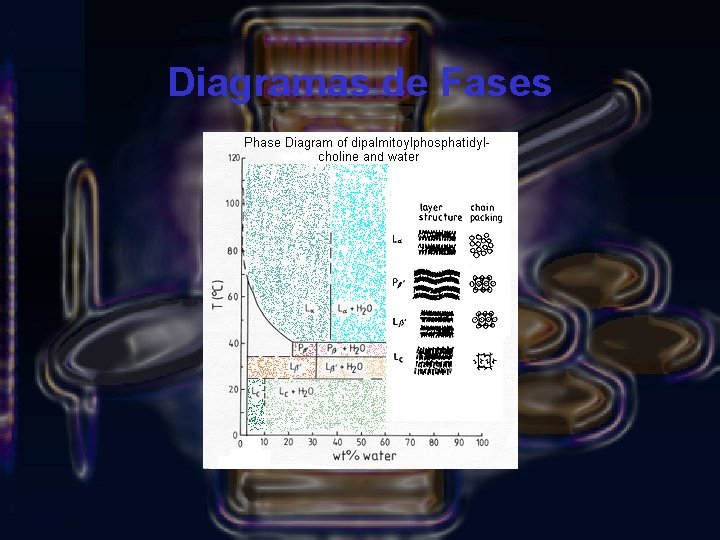
Diagramas de Fases

Estructuras cristalográficas

Dinámica de fosfolípidos en una fase micelar

Dinámica de una micela globular Figure 3. The 20 mer (top row) and 50 mer (bottom row) micelles after 1, 2, and 3 ns (left to right). Water molecules are omitted for clarity. Figure 10. Micelle interiors at 4 ns for the 10 mer (left), 34 mer (center), and 75 mer (right). Bottom views are created from 90° rotations about the horizontal. Only lipids whose centers of mass lie within 7 Å of the micelle midplane parallel to the plane of the page are included. For clarity, the radii of the tail carbons are reduced, and headgroup atoms for each lipid are replaced by a single sphere whose diameter is approximately that of the headgroup. The micelle centers are, in fact, densely packed; . Bogusz, et al. , J. Phys. Chem. B 2000, 104, 5462 -5470

Dinámica de una bicapa lipídica

Otra propiedad de los tensoactivos (INTERFASE) Mezcla de aceite crudo y agua Dos fases inmiscibles si se agita fuertemente multitud de pequeñas gotas. Pero la t. interfacial entre el agua y el aceite es muy grande, las gotas de aceite se reúnen para formar gotas mayores y al final se juntan todas en una sola fase Se introduce en la mezcla un tensoactivo La tensión interfacial disminuye y la velocidad de separación en capas es más lenta Si la tensión se disminuye al punto de que la separación sea imperceptible se logra una emulsión.

Otra propiedad de los tensoactivos (Ángulo de contacto) Ángulo entre una gota de líquido y la superficie sólida sobre la cual es colocado 180 ° 0° Al disminuir la tensión superficial de un líquido aumenta su poder humectante, ya que se extiende más. (HLB = 6 -9) A mayor d menor humectación

Clasificación de TS según grupos funcionales Grupo hidrofílico: aniónicos, catiónicos, anfotéricos y no iónicos Grupo hidrofóbico: cadena hidrocabonada, polidimetilsiloxano, perfluorocarbono
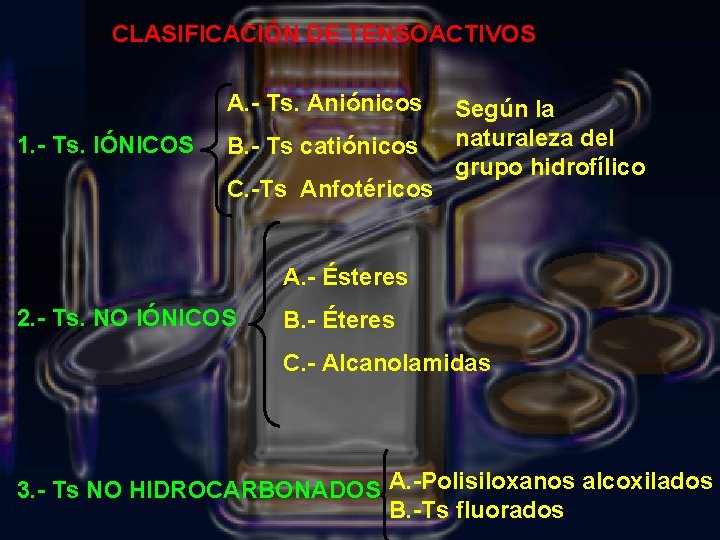
CLASIFICACIÓN DE TENSOACTIVOS A. - Ts. Aniónicos 1. - Ts. IÓNICOS B. - Ts catiónicos C. -Ts Anfotéricos Según la naturaleza del grupo hidrofílico A. - Ésteres 2. - Ts. NO IÓNICOS B. - Éteres C. - Alcanolamidas 3. - Ts NO HIDROCARBONADOS A. -Polisiloxanos alcoxilados B. -Ts fluorados

1 A. - Ts aniónicos. - Son los que se producen en mayor cantidad costo-eficacia abundantes en los limpiadores (gran acción detergente) No pueden limpiar suciedad cargada (-). - Carga negativa. - Son sensibles a los iones que le dan la dureza al agua

. - Grupo ionizado: 1 Aa. - carboxilato 1 Ab. - sulfato 1 Ac. - sulfonato 1 Ad. - fosfato. - Sulfatos son susceptibles de sufrir hidrólisis, mientras que sulfonatos son muy estables. - Algunos generan disoluciones muy viscosas Desventajas: Uso limitado a p. H = 9 o mayor (protonación) Forman sales insolubles con Ca, Mg o Al (aguas duras)

1 B. Catiónicos. - Compuestos que contienen por lo menos una cadena de 8 a 25 átomos de carbono, derivada de un ácido graso y un nitrógeno cargado (sales de amonio cuaternario o de alquilaminas) positivamente, el anión suele ser un Cl- Br- OH- , SO 42 -. . - Se unen con gran efectividad a sustratos negativos. . - Forman compuestos insolubles con compuestos aniónicos, son compatibles con no iónicos y anfotéricos

1 C. Anfotéricos (zwitteriones) . - Presentan en su molécula grupos aniónicos y catiónicos, . - Son productos completamente estables en sistemas ácidos y alcalinos, aunque su máxima actividad superficial es a p. H neutros. - A bajo p. H se comportan como catiónicos, a alto p. H como aniónicos y a p. H neutro exhiben ambas propiedades
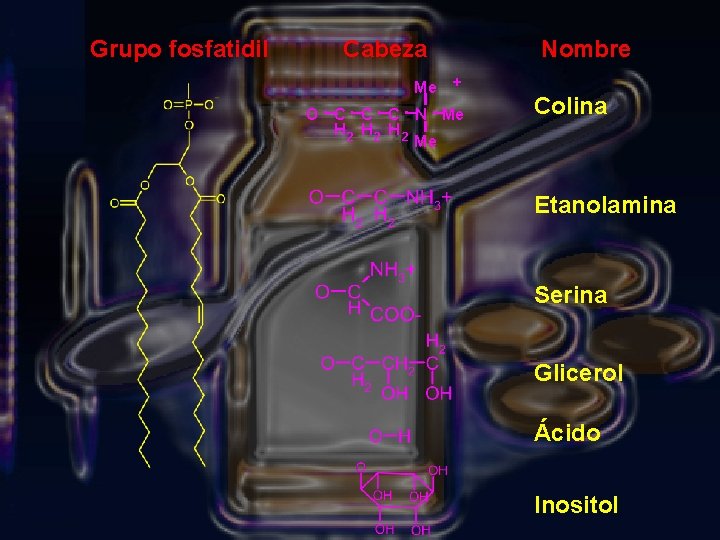
Grupo fosfatidil Cabeza Me Nombre + O C C C N Me H 2 H 2 Me Colina Etanolamina Serina Glicerol Ácido Inositol
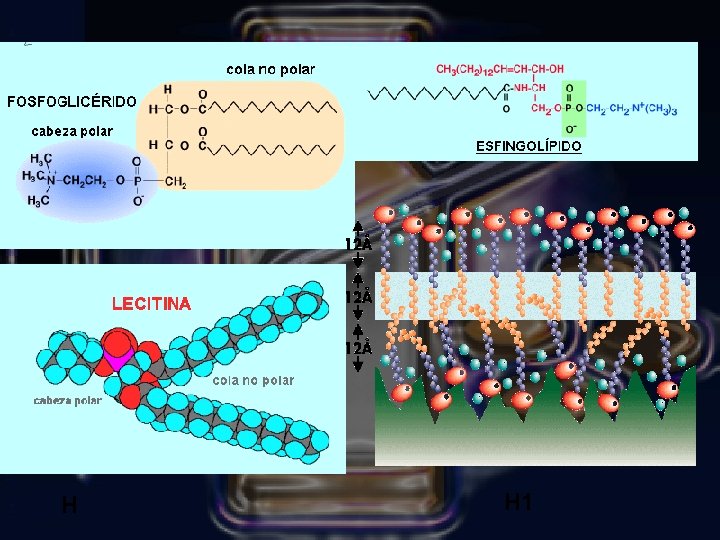
H H 1

2. - No iónicos. - Son principalmente dv polioxietilenados y polioxipropilados, . - Son estables con la mayoría de los productos químicos en las concentraciones usuales de empleo. . - Al no ionizarse en agua, no forman sales con los iones metálicos y son igualmente efectivos en aguas blandas y duras. Su naturaleza química los hace compatible con otros ts (-) y (+). - El grupo hidrofóbico está formado por una cadena larga que contienen una serie de grupos débilmente solubilizantes (hidrofílicos) tales como enlaces etéreos o grupos hidroxilos en sus moléculas. La repetición de estas unidades débiles tiene el mismo efecto que un hidrófilo fuerte, pero no hay ninguna ionización.

2 A. Ésteres. - Estables a p. H neutros, susceptibles de hidrólisis a p. H ácidos o básicos 2 Aa E. de etilenglicol. - Muy lipofílicos, poca actividad ts. - Ejem: Monoestearato de etilenglicol, dilaurato de etilenglicol, etc

2 Ab. E. de propilenglicol. - Imparten viscosidad. - Buenos emulsificantes w/o y o/w. - Ejem: Miristato de propilenglicol, etc. 2 Ac. E. de glicerol. - Ampliamente usado por su baja toxicidad. - Ejem: Estearato de glicerilo, etc. 2 Ad. E. de sorbitan. - Ampliamente usados en farmacia. - Ejem: acilato de sorbitan, span

2 Ae. E. de sacarosa. - Muy usados en farmacia. - Ejem: Acilato de sacarosa, etc. 2 Af. E. Etoxilados. - Dv de polímeros de etilen glicol (PEG o POE). - PEG (n=2 -100) + ácido graso. - Bastante estables, muchos enlaces éter y uno terminal éster (hidrolizable). - Ejem: Diestearato de PEG 150, polisorbato 40 (dv de sorbitan + ác graso + PEG), tween, brij, etc.

2 B. Éteres. - Dv de polietilen glicol o polipropilenglicol 2 Ba. - Alcoholes grasos etoxilados (éteres de polioxietileno). -Octoxinol 9, Ceteth 20, etc. - Usos. Solubilizantes, emolientes 2 Bb. - Alcoholes propoxilados. - Usos. Solubilizantes, emolientes 2 Bc. - Alcoholes etoxilados-propoxilados. - Poloxámeros (Pluronic) 2 C. Amidas (alcanolamidas). - Limpieza de la piel y del cuero cabelluedo

3. - No hidrocarbonados Polisiloxanos. - Son organosilicones. - Diferentes rangos de solubilidad (EO y PO). - Muy estables. - Gran uso en cosmética Fluorotensoactivos. - Excelente estabilidad térmica y química. - Usados a nivel industrial, poco uso a nivel humano

Aplicaciones de los tensoactivos en farmacia 1. - Emulsificantes 2. - Detergentes 3. - Humectantes 4. - Solubilizantes 5. - Promotores de la absorción 6. - Antimicrobianos (conservadores) 7. - Espumantes y antiespuma 5. - Promotores de la absorción. - Reducción de la ts interfacial entre la pared celular y el medicamento líquido. - Se facilita la adsorción y “espreado” del fármaco sobre la superficie del organismo
![Si la [ts] es > que cmc: la v. Penetración disminuye casi a 0 Si la [ts] es > que cmc: la v. Penetración disminuye casi a 0](http://slidetodoc.com/presentation_image_h/aa695ed3bf3efebe9dea8f6c6daa6a39/image-111.jpg)
Si la [ts] es > que cmc: la v. Penetración disminuye casi a 0 (fco disponible dividido entre interior y exterior de la micela) 6. - Antimicrobianos. -Los ts se adsorben en la pared de los m. o. Y aumentan la permeabilidad (pérdida de material celular esencial). - Gram – y Gram + sos susceptibles a los ts catiónicos. - Gram + más susceptibles a los ts aniónicos 7. -Espumantes. -Se forma una estructura estable a la mezcla con el aire (el líquido drena, colapsan los globulos y se rompe). - Problemas en proceso- Aceite de castor

Clasificación: Coloidales (0. 5 -1 mm) Gruesas (>1 mm) Dispersiones coloidales: Tipos: . - Liófilas. - Liófobas. - De agregación Propiedades: . - Ópticas: Efecto Tyndall. - Eléctricas: Potencial zeta Estabilidad: . - Eléctrica. - Adsorción de tensoactivos o polímeros

Dispersiones Gruesas • Suspensiones: Fármaco sólido en vehículo líquido • Emulsiones: Un líquido en vehículo líquido • (o/w) • (w/o)

Razones para usarlas • El p. a. es insoluble • El fármaco es más estable en suspensión o emulsión • Es necesario controlar la liberación • El fármaco tiene mal sabor (ví oral)

Vías de Administración • • • Oral Ocular Otica Rectal Parenteral Topica


Temario 1. Definición 2. Características de una suspensión 3. Ventajas y desventajas 4. Inestabilidad física 5. Ley de Stokes y Potencial Zeta 6. Formulación y proceso

1. Definición Farmacopea de los Estados Unidos Mexicanos Sistema disperso, compuesto de dos fases, los cuales contienen el o los principios activos y aditivos. Una de las fases, la continua o externa es generalmente un líquido o un semisólido y la fase dispersa o interna, está constituida de sólidos (principios activos) insolubles pero dispersables en la fase externa. En el caso de inyectables deben ser estériles. United States Pharmacopea (USP) Preparaciones líquidas que consisten en partículas sólidas dispersas a través de la fase líquida en la que las partículas no son solubles.

Una suspensión se define como una dispersión gruesa que contiene material insoluble, finamente dividido con un tamaño de partícula mayor de 0. 5 mm suspendido en un medio líquido (principalmente agua).

2. Características de una suspensión 1. Las partículas dispersas deben de ser de un tamaño tal que 1. no sedimenten de manera rápida. 2. En el caso de sedimentación no deben formar una pasta dura 1. (cake) que debe ser fácilmente resuspendible (mínimo esfuerz 3. Fácil de verter 4. Sabor agradable 5. Resistente al ataque microbiano

3. Ventajas y desventajas Ventajas 1. 2. 3. 3. 4. Se puede formular un fármaco insoluble. La cantidad de fármaco a formular puede ser mayor que en las otras formas farmacéuticas Se puede disminuir la velocidad de liberación del fármaco Puede protegerse al fármaco de la luz, el aire, etc Desventaja 1. Inestabilidad física (y química? )

4. Inestabilidad física Aumento de la superficie de interface entre las partículas y el medio dispersante 1. Incremento de energía libre de superficie 2. Presencia de una carga eléctrica sobre la superficie 3. de las partículas dispersas (Potencial de superficie)

1. Incremento de energía libre de superficie G 1 G 2 G 3 DG = g. DA G Energía libre, g tensión de interfase y A Cambio de superficie ¿Cómo solucionar el problema? 1. Agregando un agente humectante a. Permanecen las partículas dispersas
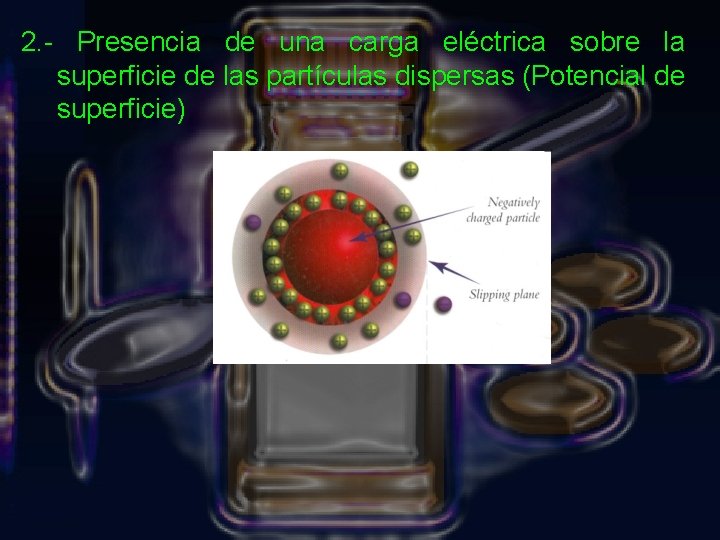
2. - Presencia de una carga eléctrica sobre la superficie de las partículas dispersas (Potencial de superficie)

Tipos de agregación Coagulación vs. Floculación • Coagulación, irreversible • Floculación, reversible, puede ser deseable o indeseable. • Teoría DLVO Siuperposición de repulsión electrostática y atracciones de Van der Waals
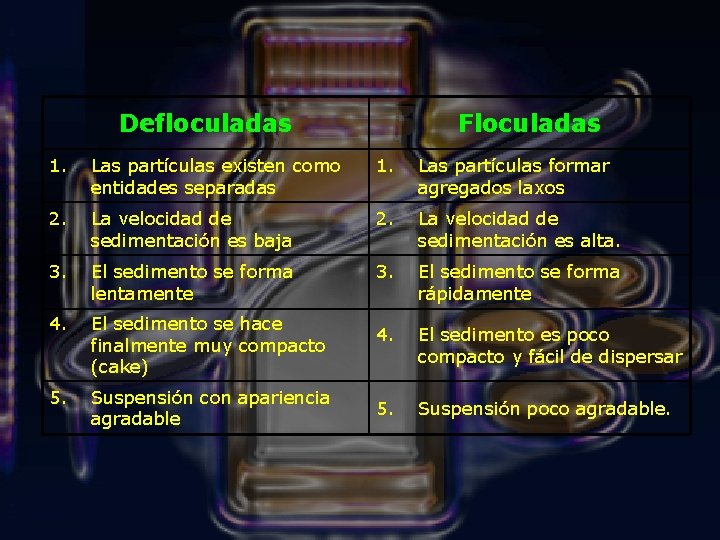
Defloculadas Floculadas 1. Las partículas existen como entidades separadas 1. Las partículas formar agregados laxos 2. La velocidad de sedimentación es baja 2. La velocidad de sedimentación es alta. 3. El sedimento se forma lentamente 3. El sedimento se forma rápidamente 4. El sedimento se hace finalmente muy compacto (cake) 4. El sedimento es poco compacto y fácil de dispersar 5. Suspensión con apariencia agradable 5. Suspensión poco agradable.
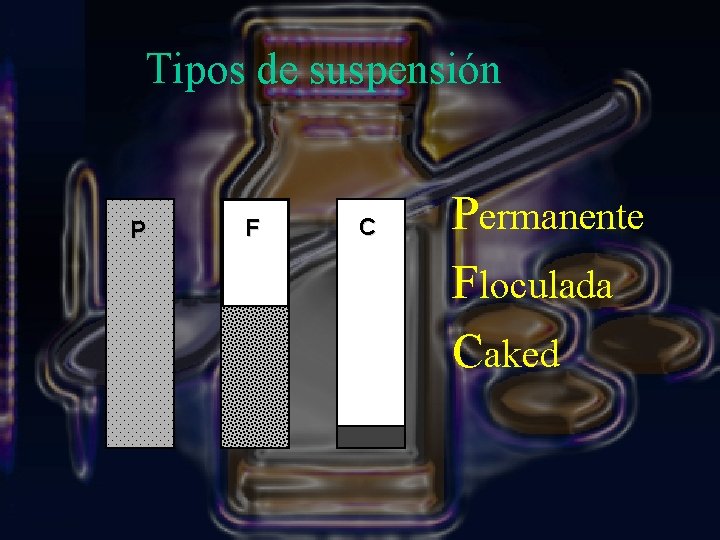
Tipos de suspensión P F C Permanente Floculada Caked
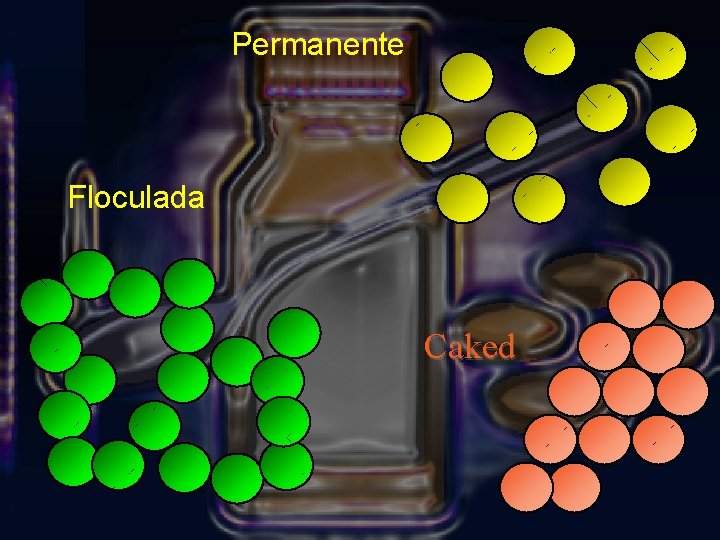
Permanente Floculada Caked

P. V. Farmacéutico • Buena – Suspension permanente – No hay separación ni sedimentación • Mala? – Algo de separación/sedimentación – Altos volumenes de flóculos son aceptables – Se reconstituye por agitación • Mal aspecto – Separación total – No se reconstituye por agitación

• “Una suspensión físicamente estable es la que se puede dispersar de manera uniforme con agitación moderada, sin haber cambios en el tamaño de partícula, la forma cristalina o las propiedades farmacológicas del activo.

5. Ley de Stokes La velocidad de sedimentación esta regida por la siguiente expresión: n velocidad final (cm/s) r radio de las partículas (cm) r 1 y r 2 densidad de la fase dispersa y del medio dispersante g aceleración de la gravedad (980. 7 cm/s 2) h viscosidad del medio dispersor (g/cm/s)
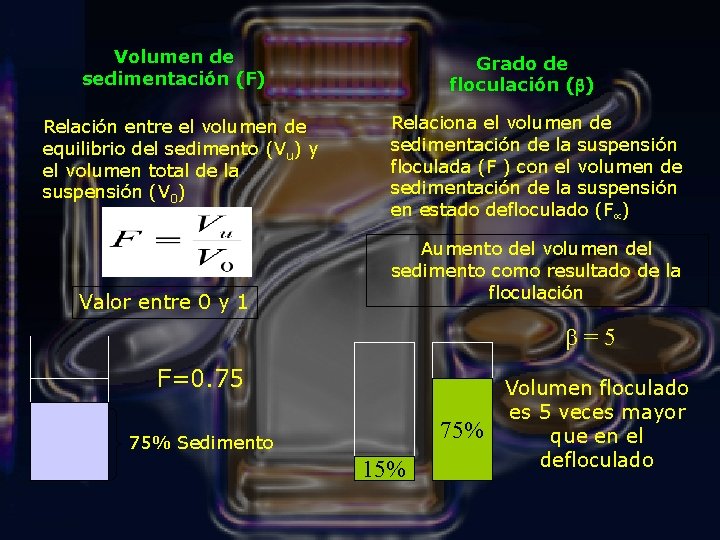
Volumen de sedimentación (F) Relación entre el volumen de equilibrio del sedimento (Vu) y el volumen total de la suspensión (V 0) Valor entre 0 y 1 Grado de floculación (b) Relaciona el volumen de sedimentación de la suspensión floculada (F ) con el volumen de sedimentación de la suspensión en estado defloculado (F ) Aumento del volumen del sedimento como resultado de la floculación b = 5 F=0. 75 75% Sedimento 15% Volumen floculado es 5 veces mayor que en el defloculado
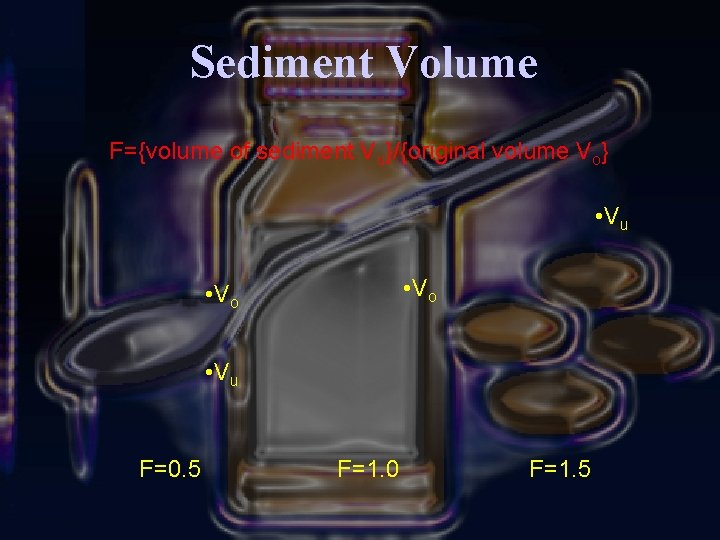
Sediment Volume F={volume of sediment Vu}/{original volume Vo} • V u • V o • V u F=0. 5 F=1. 0 F=1. 5
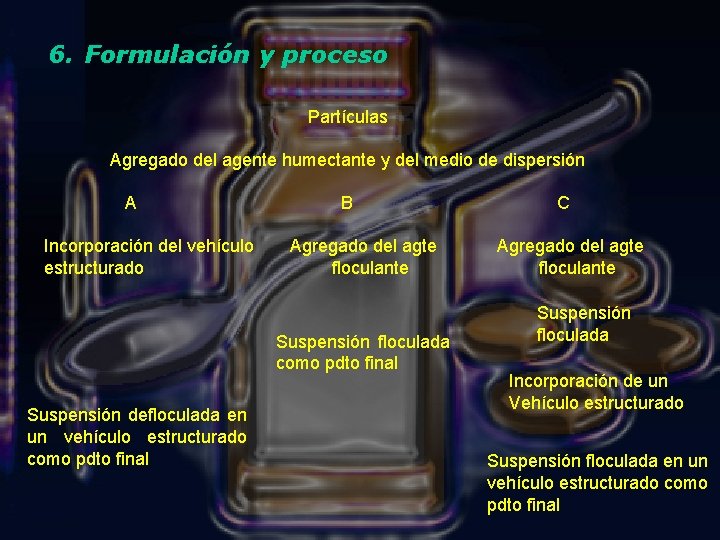
6. Formulación y proceso Partículas Agregado del agente humectante y del medio de dispersión A B C Incorporación del vehículo Agregado del agte estructurado floculante floculante Suspensión floculada como pdto final Suspensión defloculada en un vehículo estructurado como pdto final Suspensión floculada Incorporación de un Vehículo estructurado Suspensión floculada en un vehículo estructurado como pdto final
Humectación Humectante
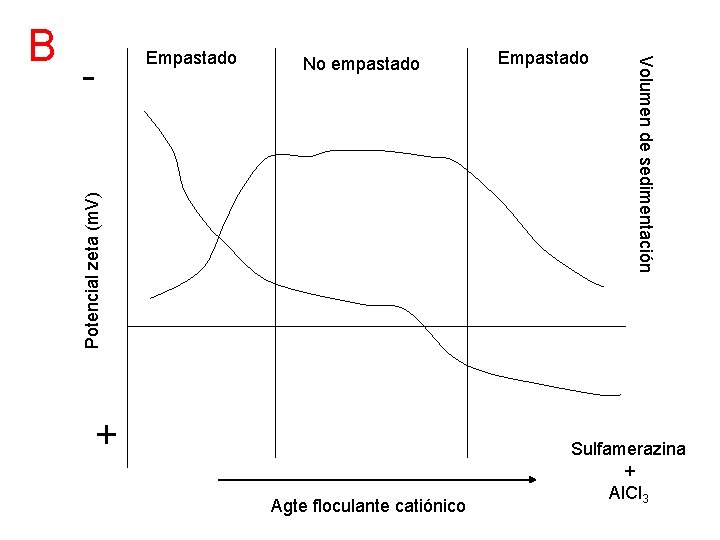
No empastado Potencial zeta (m. V) - Empastado + Agte floculante catiónico Empastado Volumen de sedimentación B Sulfamerazina + Al. Cl 3
Reología • Newtoniano • No Newtoniano – Pseudoplástico • Tixotropía – Dilatante
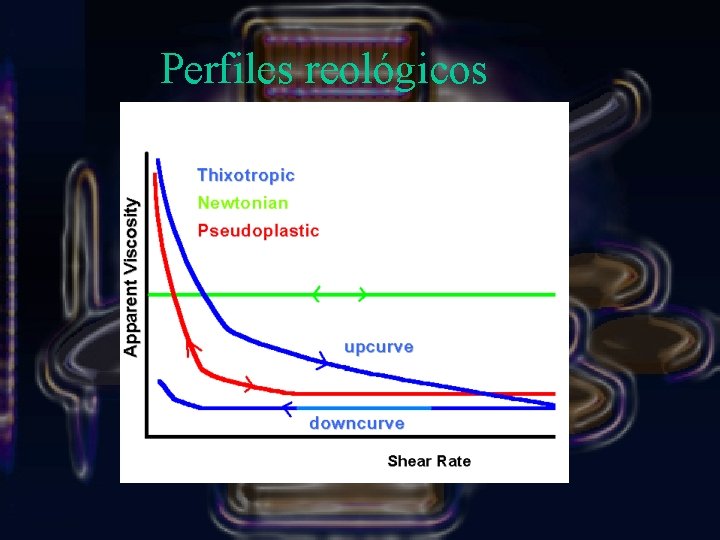
Perfiles reológicos
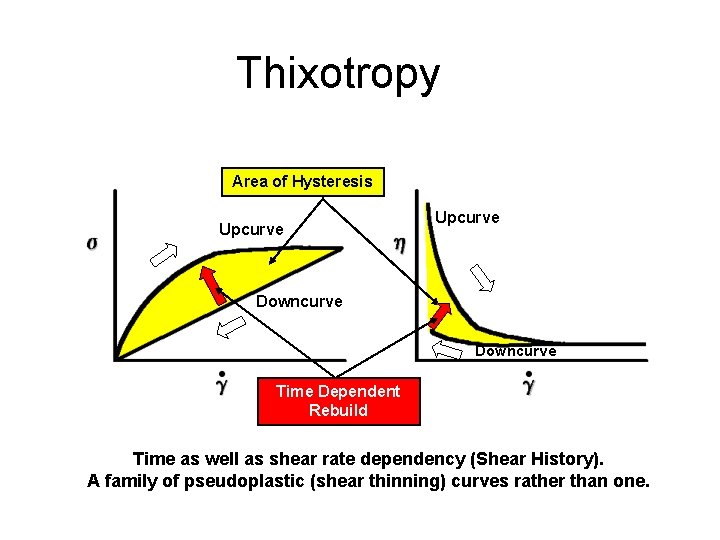
Thixotropy Area of Hysteresis Upcurve Downcurve Time Dependent Rebuild Time as well as shear rate dependency (Shear History). A family of pseudoplastic (shear thinning) curves rather than one.

PV Farmacéutico • Newtonian: No good Viscosity for permanent suspension = glass Pourable fluids will not suspend. • Pseudoplastic: No good High viscosity in bottle for permanent suspension. Will thin on shaking but instantly rethicken before pouring. • Thixotropic: Ideal High viscosity in bottle for permanent suspension. Will thin on shaking and remain pourable. Will rethicken on standing in the bottle. – Isothermal reversible sol-gel ideal for pharmaceutical permanent suspensions.

Formulación • Drug • Water • Suspending Agent • Dispersant (for hydrophobic drug)

Suspending Agents • Clays e. g. : Bentonite, Veegum, Antacids – Sensitive to electrolytes, p. H and high shear (Electrostatically stabilized) – Rheology less temperature sensitive • Water soluble Polymers e. g. : Carbomer, Xanthan, Carrageenan – Relatively insensitive to electrolytes, p. H and high shear – Temperature dependent thinning • Dispersible Cellulose • e. g. : Avicel RC/CL grades – Relatively insensitive to electrolytes, p. H and high shear – Rheology less temperature sensitive
Effect of Temperature on Viscosity

PLANTEAMIENTO DEL PROBLEMA En un laboratorio farmacéutico usted es el responsable del área de desarrollo, desea formular una suspensión de benzoilo de metronidazol al 4% ya que posee muy baja solubilidad en casi todos los disolventes permitidos para uso biológico. Para esto, hay que considerar que la velocidad de sedimentación viene regida por la ecuación de Stokes, siempre y cuando el tamaño y forma de las partículas en suspensión sea uniforme: V=d 2( 1 - 2)G 18 Donde V es la velocidad de sedimentación d es el diámetro de las partículas suspendidas 1 y 2 son la densidad de las partículas suspendidas y del medio respectivamente G es la gravedad (980. 7 cm/s 2) es la viscosidad del medio

Equipo: . - Pulverización. - Tamización . - Mezclado. - Llenado. - Acondicionamiento


Sistema disperso líquido-líquido dispersa y dispersante) (fase Generalmente entre 0. 1 a 100 mm Termodinamicamente inestables: floculación y coalescencia Excipiente emulsionante indispensable: agente
Emulsificación Emulsificador

Agente emulsionante Propiedades deseables. - Reducir la tensión superficial por debajo de 10 dinas/cm. - Ser adsorbidos rápidamente por la superficie de las gotas . - Impartir a las gotas un potencial zeta adecuado. - Aumentar la viscosidad de la emulsión. - Ser efectivos en una concentración razonablemente baja

Como actúan los emulsificantes: . - formando monocapa. -multicapas (polímeros como gelatina). - partículas sólidas (bentonita)

Estabilidad física Ley de Stokes Movimiento ascendente y descendente de las gotitas en la fase continua: sedimentación y cremado (densidad)

Viscosidad de las emulsiones 1. - Fase interna Concentración de volumen, viscosidad, tamaño 2. - Fase continua Viscosidad, estructura, p. H 3. - Emulsionante Estructura, concentración y solubilidad en cada fase, espesor del adsorbido 4. - Estabilizadores Hidrocoloides, etc

Estabilidad física Agregación (Potencial zeta) y coalescencia (espesor de la película) Inversión . - Presencia de sales, estearato de Mg o/w, mas Cl 2 Ca da estearato de Ca y forma w/o). - PIT (temperatura de inversión de fases), cambia la solubilidad del tensoactivo

Vías de administración. - Oral. - Transdérmica. - Parenteral Bancroft's Rule El tipo de emulsión (w/o o o/w) es dictada por el tensoactivo, éste debe de ser soluble en la fase continua.

Tipos de emulsión. - w/o . - o/w. - Múltiples . - Microemulsiones Métodos de detección. - Prueba de dilución. - Prueba de conductividad. - Prueba de solubilidad de un colorante

Preparación 1. - Determinar el tipo que debe de ser. - Seleccionar el emulsificante (HLB). - Evitar incompatibilidades 2. - Agrupar los componentes según su solubilidad y disolverlos donde proceda 3 a. - Adición de la fase interna sobre la externa 3 b. - Adición de la fase externa sobre la interna (Inversión de fases) 3 c. - Mezcla de las dos fases 3 d. - Adición alternada

Equipos. - Energía para formar la interfase. - Trabajo de mezclado. - Administración de calor. - Agitadores (Baja viscosidad). - Mezcladores mecánicos (A propulsión o de hélice y de turbina o de palas). - Molinos coloidales (estator y rotor). - Homogeneizadores de alta presión. - Dispositivos ultrasónicos

Ventajas. - Ocultan c. o. l. desfavorables. - Mayor estabilidad química. - Posible velocidad sostenida Inconvenientes. - Fabricación. - Inestabilidad física
LAS EMULSIONES EN EL MERCADO

GRUPOS TERAPÉUTICOS PRINCIPIOS ACTIVOS Antiulcerosos Cimetidina, ranitidina, famotidina, omeprazol. Antiagregantes plaquetarios Ticlopidina. Hipolipemiantes Gemfibrozilo, lovastatina Cardiotónicos Dobutamina Antagonistas del calcio Diltiazem, nifedipino, nimodipino, nitrendipino. Alfabloqueantes Doxazosina Inhibidores de la angiotensina convertasa Captoprilo, enalaprilo Asociaciones de IECA con diuréticos Captoprilo/Hidroclorotiazida Diuréticos Furosemida, Indapamida Vasodilatadores periféricos Pentoxifilina Betabloqueantes Atenolol Antifúngicos dermatológicos Clotrimazol Antivirales tópicos Aciclovir Antimicóticos de uso vaginal Clotrimazol Antiinfecciosos urinarios Norfloxacino
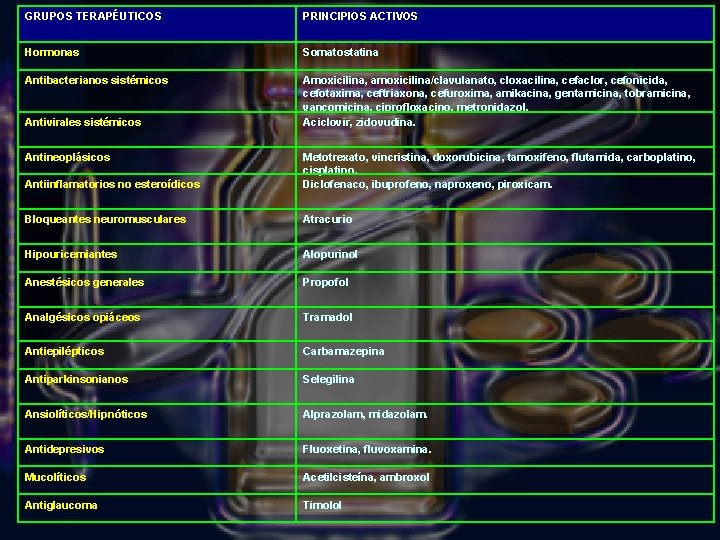
GRUPOS TERAPÉUTICOS PRINCIPIOS ACTIVOS Hormonas Somatostatina Antibacterianos sistémicos Amoxicilina, amoxicilina/clavulanato, cloxacilina, cefaclor, cefonicida, cefotaxima, ceftriaxona, cefuroxima, amikacina, gentamicina, tobramicina, vancomicina, ciprofloxacino, metronidazol. Aciclovir, zidovudina. Antivirales sistémicos Antineoplásicos Antiinflamatorios no esteroídicos Metotrexato, vincristina, doxorubicina, tamoxifeno, flutamida, carboplatino, cisplatino. Diclofenaco, ibuprofeno, naproxeno, piroxicam. Bloqueantes neuromusculares Atracurio Hipouricemiantes Alopurinol Anestésicos generales Propofol Analgésicos opiáceos Tramadol Antiepilépticos Carbamazepina Antiparkinsonianos Selegilina Ansiolíticos/Hipnóticos Alprazolam, midazolam. Antidepresivos Fluoxetina, fluvoxamina. Mucolíticos Acetilcisteína, ambroxol Antiglaucoma Timolol


Microemulsiones • Son sistemas que consisten en agua, solvente orgánico y anfifílico(s) que constituyen una solución líquida monofásica ópticamente isotrópica y termodinámicamente estable. Las microgotas tienen un tamaño entre 5 y 100 nm •

Ventajas generales • Facilidad de preparación • Transparencia • Estabilidad • Posibilidad de filtración • Vehiculización para drogas de diferentes lipofilicidades • Baja viscosidad • Ventajas farmacéuticas • Liberación sostenida de componentes solubles en la fase interna • Protección de la droga solubilizada en la fase dispersa • Aumento de la biodisponibilidad

• Fase apolar: aceites vegetales naturales y modificados, ésteres de ácidos grasos y sus derivados etoxilados, aceites de silicona. Componentes • Fase polar: buffers, soluciones salinas, glicerol, mezclas de solventes hidrofílicos. • Tensoactivos: • No iónicos: Brij 35, monooleato de sorbitan • Zwitteriónicos: Fosfolípidos, lecitinas, diacilfosfatidilcolina • Catiónicos: alquilamonio cuaternarios • Aniónicos: bis-2 -etilhexilsulfosuccinato (doble cola W/O)

Cosurfactantes • Cualquier componente que modifique las propiedades de empaquetamiento del surfactante. Ejs: Alcoholes de longitud de cadena media, aminas, propilenglicol, aminoalcoholes. • Funciones: • Disminuir la tensión interfacial • Aumentar la fluidez del film interfacial (aumento de S) • Aumentar la movilidad de la cola hidrocarbonada • Disminuir las interacciones repulsivas entre los grupos de cabeza cargados. • Particionarse entre ambas fases (mejora solubilidad mutua)

Etapas en la obtención de microemulsiones • Seleccionar los componentes • Definir la relación surfactante/cosurfactante • Titular a una relación definida de mezcla de componentes • Construir el Diagrama Pseudoternario de Fases.

Caracterización de microemulsiones • Nivel macroscópico: Viscosidad - Conductividad • Microscopía polarizante • Métodos de dispersión de luz estática y dinámica. • Distribución del tamaño de la fase interna: • RMN con gradiente de campo pulsado • Microscopía electrónica de crio-fractura

Aplicaciones • Administración transdérmica de fármacos: anestésicos locales, Aplicaciones antifúngicos. • Aumento de biodisponibilidad de drogas lipofílicas: corticoides y hormonas sexuales. • Fórmulas inyectables: drogas oncológicas • Administración de lípidos por vía intravenosa • Administración oral de péptidos: insulina, vasopresina, LHRH, ciclosporina. • Colirios: levobunolol y pilocarpina • Aerosol: salbutamol
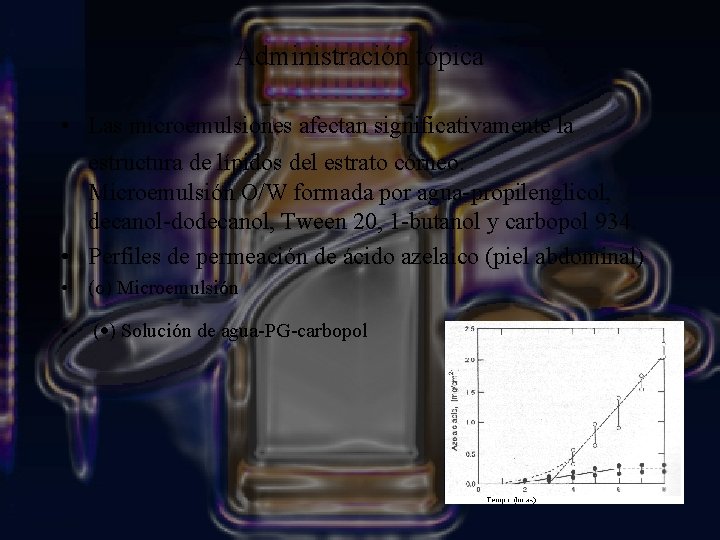
Administración tópica • Las microemulsiones afectan significativamente la estructura de lípidos del estrato córneo. Microemulsión O/W formada por agua-propilenglicol, decanol-dodecanol, Tween 20, 1 -butanol y carbopol 934. • Perfiles de permeación de ácido azelaico (piel abdominal) • (o) Microemulsión • ( ) Solución de agua-PG-carbopol

Miniemulsiones • Son soluciones azul-blancas casi opacas que contienen gotas dispersadas en un rango de diámetro entre 100 y 400 nm, que son obtenidas a través de la sonicación del sistema. • Principales diferencias con microemulsiones • Menor contenido de mezcla activa, del 1 al 3 % contra 15 al 30 %. • El cosurfactante es un alcohol de por lo menos 12 carbonos, mucho mas largo que el correspondiente a microemulsiones. • Obtención por sonicación.


¿Qué es un Conservador? ü Sustancia que previene crecimiento microbiano. o inhibe el ü Evitar la degradación de las preparaciones por acción de los microorganismos.

¿Porqué se emplean conservadores? ü La salud del consumidor puede afectarse. ü La estabilidad del producto puede verse disminuida. ü Farmacopeas; recomiendan evaluar a los productos para recuentos de microorganismos y la presencia de indicadores específicos de contaminación bacteriana Salmonella, E. coli, P. aeruginosa, S. aureus, ausencia de levaduras y hongos.

¿Cuáles son los criterios a considerar en la selección de un conservador? ü Debe ser efectivo frente a un amplio espectro de microorganismos. ü Estable durante toda su vida útil. ü Atóxico. ü No sensibilizante. ü Compatible con los componentes presentes en la forma farmacéutica.

ü Barato. ü Desprovisto de sabor y olor. ü Considerar el sitio de uso (externo, interno u oftálmico). ü El p. H del líquido, dado que este factor puede afectar la ionización y la estabilidad del conservador. ü La participación en la fase oleosa de una emulsión, lo que reduce la concentración en la fase acuosa en la que tiene lugar la acción conservadora.

ü La adsorción en la fase sólida de una suspensión lo que reduce la concentración en la fase acuosa. ü Variables del procesamiento y envasado (calor, orden del agregado de otros componentes, mezclado o materiales de envase). ü Tipo de forma farmacéutica por ejemplo: solución, emulsión o suspensión.

Para el caso de oftálmicos: ü Debe ser estable bajo una amplia gama de situaciones, incluidas las temperaturas de autoclave y los intervalos de p. H. ü Debe establecerse la estabilidad con otros componentes del preparado y con los sistemas de envasado. ü Debe establecerse la falta de toxicidad y de irritación con un margen de seguridad razonable.

¿De qué depende la acción de un conservador? ü De su actividad biológica intrínseca. ü De su disponibilidad en la fase acuosa. Dependiente del: Ø Ø Ø p. H. Distribución entre la fase oleosa y acuosa. Solubilidad verdadera. Solubilización micelar. Perdidas potenciales por los materiales de empaque.

Tipos de conservadores ü Pueden agruparse en diversos clases según su estructura molecular:

Agentes con actividad superficial ü Aniónicos. Ø Jabones. Ø Agentes tensoactivos aniónicos de síntesis. ü Catiónicos. . - Cloruro de benzalconio. ü Anfóteros (anfolitos, zwitteriones). ü No iónicos.

Alcoholes (Etanol) ü Para que sea eficaz se requiere una concentración relativamente alta (mayor del 10%). Propilenglicol) Puede actuar como conservador concentraciones del 15 al 30%. Potencia la actividad de los parabenos. en

Ácidos orgánicos (Ácido benzoico) ü Se ha usado por muchos años. ü Se acepta que es un conservador seguro. ü Tiene una baja solubilidad en agua (aprox. 0. 34% a 25°). ü El rango de concentración utilizado con fines inhibidores varia entre el 0. 1% y el 0. 5%. ü Sólo la forma no ionizada es efectiva. ü Por lo tanto su uso se limita a preparaciones con un p. H inferior a 4. 5.

Otros ácidos usados: ü Ácido Benzoico (p. Ka 4. 20) ü Ácido o-clorobenzoico (p. Ka 4. 0) ü Ácido Salicílico (p. Ka 2. 97) ü Ácido Sórbico (p. Ka 4. 7) ü Ácido Dihidroacético (p. Ka 6. 0) ü Ácido Propiónico (p. Ka 4. 8)

Ésteres del ácido p-hidroxibenzoico ü Llamados por lo común parabenos. ü Incluyen los derivados metílico, propílico y butílico. ü Son ampliamente usados en preparados farmacéuticos y cosméticos. ü La solubilidad en agua de estos compuestos disminuye a medida que el peso molecular aumenta (éster metílico 0. 25%, éster butílico 0. 02%).

ü Son efectivos y estables dentro de un espectro de p. H de 4 a 8. ü En soluciones alcalinas se produce la ionización, reduce la actividad de estos ésteres con perdida de la actividad. ü Se emplean en concentraciones de hasta aproximadamente el 0. 2%.
- Slides: 187