Termodinamica Equilibrio termico punti fissi temperatura e scale

Termodinamica Equilibrio termico, punti fissi, temperatura e scale termometriche 1

Quando due corpi diciamo A e B vengono posti a contatto tra loro si osserva che le grandezze fisiche li descrivono cambiano: Cambia il volume di un solido, di un liquido, di un gas Cambia la tensione superficiale di un liquido Cambia la resistenza elettrica di un resistore ………. Tale cambiamento prosegue fino a che i sistemi in interazione raggiungono una nuova situazione di equilibrio. Se uno di essi (ad esempio il corpo A) viene posto a contatto con un terzo corpo C di piccole dimensioni (al esempio il bulbo di un termometro) si vede che anche il copro C evolve verso una situazione di equilibrio. Una volta raggiunta questa situazione, se si pone il corpo C a contatto con l’altro dei due corpi intergenti, si osserva che esso è sempre in equilibrio con B. 2
A B 3
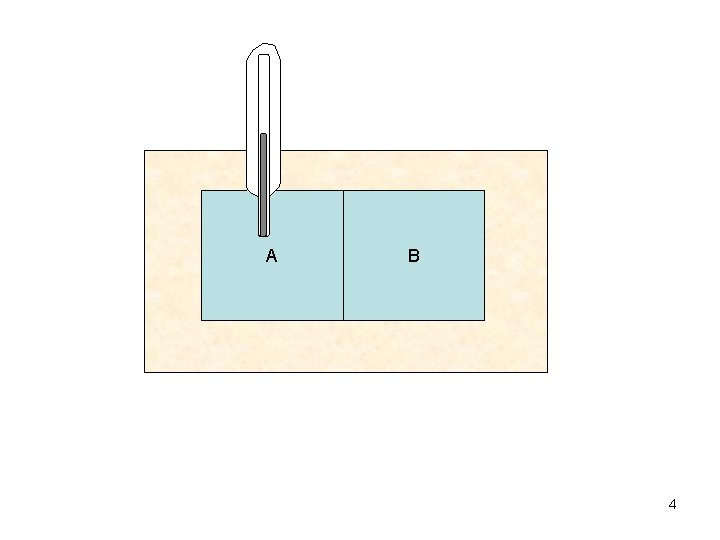
A B 4
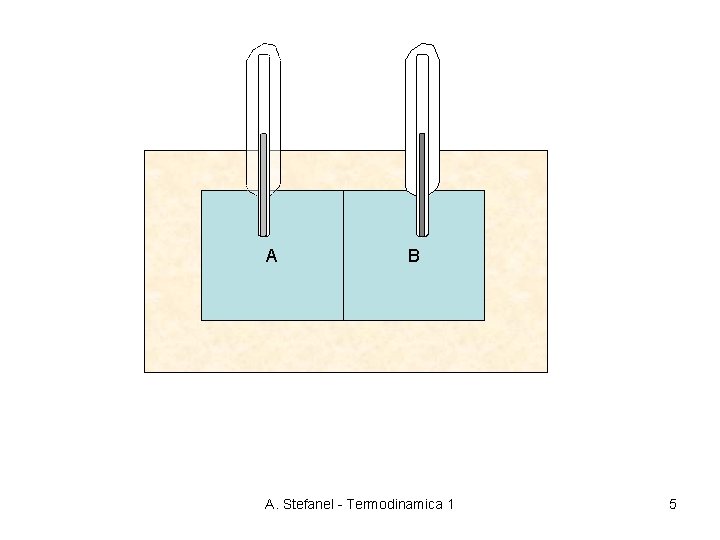
A B A. Stefanel - Termodinamica 1 5

Quando due sistemi in interazione tra loro hanno raggiunto l’equilibrio (ossia quando non cambiano più i valori delle grandezze che li caratterizzano) se si pone un termometro a contatto con ciascuno di essi si osserva che la colonnina raggiunge in entrambi i casi la stessa altezza. Questo ci autorizza ad introdurre una nuova grandezza fisica, che descrive l’equilibrio termico: La TEMPERATURA. Diremo allora che due sistema all’equilibrio termico hanno la stessa temperatura Due sistemi che hanno temperature diverse e vengono posti in interazione termica (a contatto tra loro, o anche semplicemente posti vicini in una ambiente isolato) evolvono verso un comune stato di equilibrio termico. A. Stefanel - Termodinamica 1 6
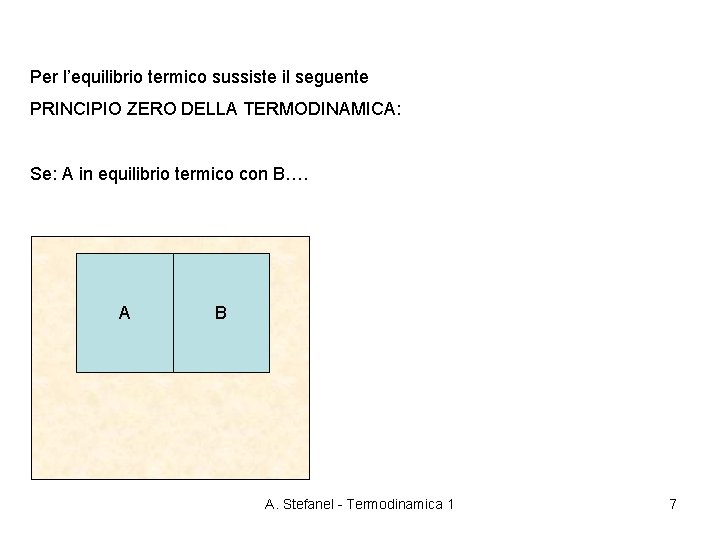
Per l’equilibrio termico sussiste il seguente PRINCIPIO ZERO DELLA TERMODINAMICA: Se: A in equilibrio termico con B…. A B A. Stefanel - Termodinamica 1 7
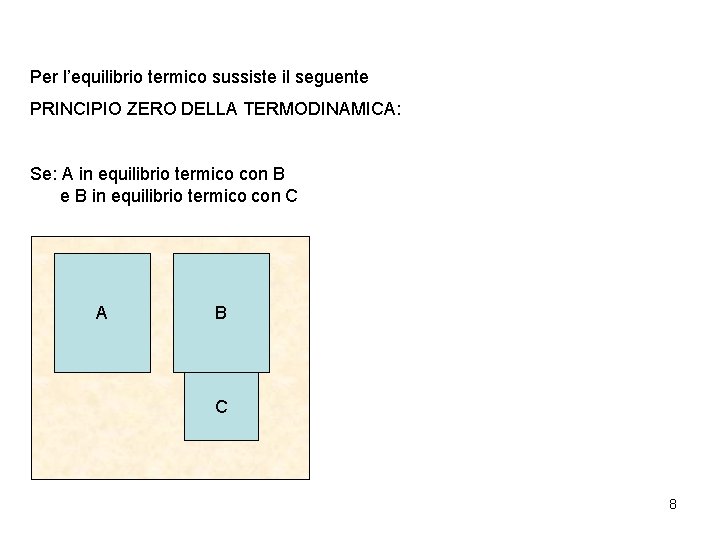
Per l’equilibrio termico sussiste il seguente PRINCIPIO ZERO DELLA TERMODINAMICA: Se: A in equilibrio termico con B e B in equilibrio termico con C A B C 8
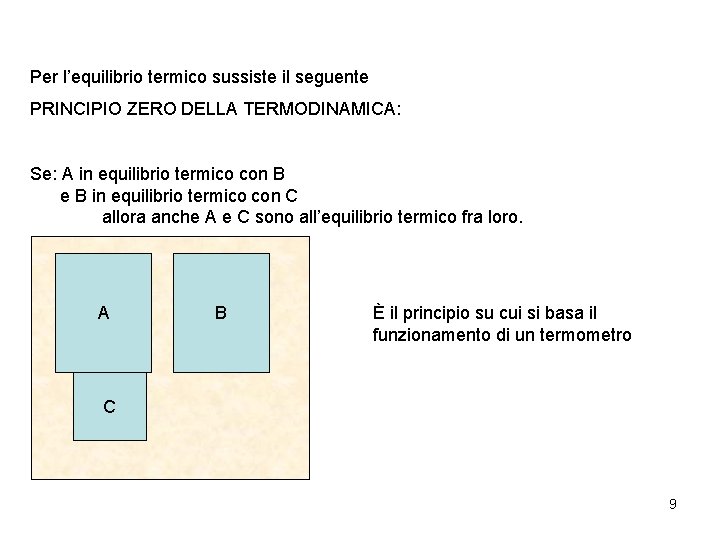
Per l’equilibrio termico sussiste il seguente PRINCIPIO ZERO DELLA TERMODINAMICA: Se: A in equilibrio termico con B e B in equilibrio termico con C allora anche A e C sono all’equilibrio termico fra loro. A B È il principio su cui si basa il funzionamento di un termometro C 9
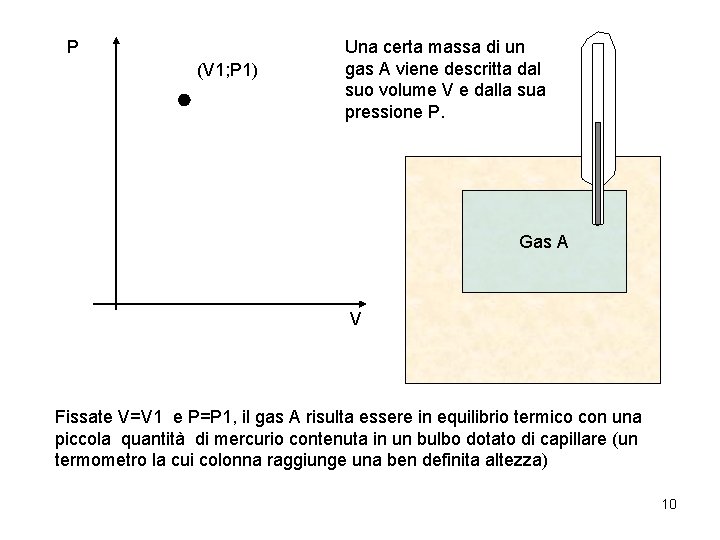
P (V 1; P 1) Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. Gas A V Fissate V=V 1 e P=P 1, il gas A risulta essere in equilibrio termico con una piccola quantità di mercurio contenuta in un bulbo dotato di capillare (un termometro la cui colonna raggiunge una ben definita altezza) 10
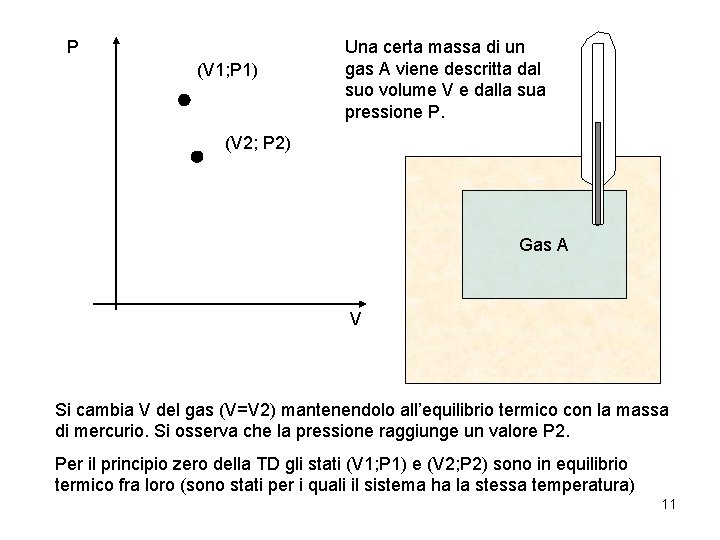
P (V 1; P 1) Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. (V 2; P 2) Gas A V Si cambia V del gas (V=V 2) mantenendolo all’equilibrio termico con la massa di mercurio. Si osserva che la pressione raggiunge un valore P 2. Per il principio zero della TD gli stati (V 1; P 1) e (V 2; P 2) sono in equilibrio termico fra loro (sono stati per i quali il sistema ha la stessa temperatura) 11
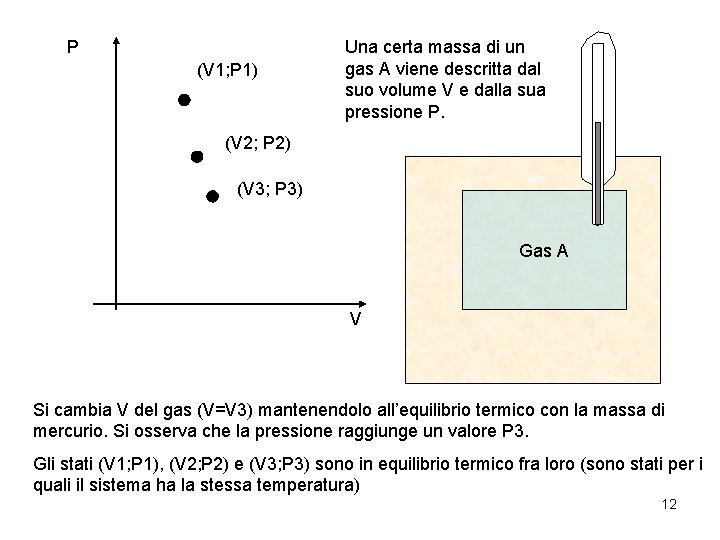
P (V 1; P 1) Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. (V 2; P 2) (V 3; P 3) Gas A V Si cambia V del gas (V=V 3) mantenendolo all’equilibrio termico con la massa di mercurio. Si osserva che la pressione raggiunge un valore P 3. Gli stati (V 1; P 1), (V 2; P 2) e (V 3; P 3) sono in equilibrio termico fra loro (sono stati per i quali il sistema ha la stessa temperatura) 12
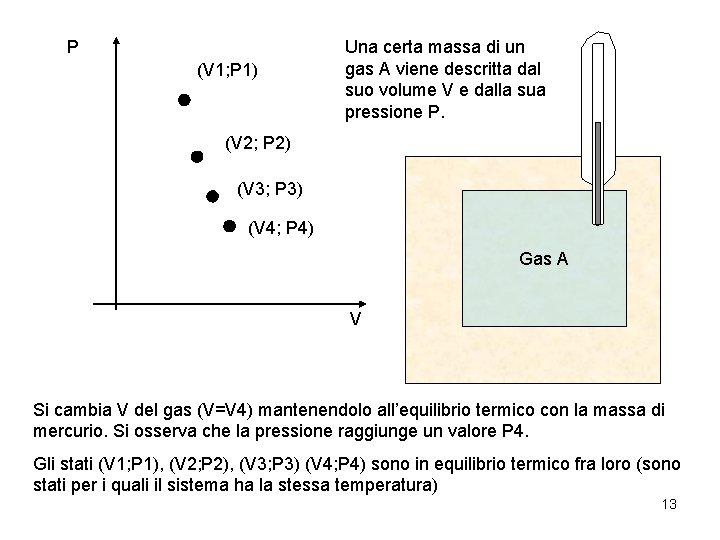
P (V 1; P 1) Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. (V 2; P 2) (V 3; P 3) (V 4; P 4) Gas A V Si cambia V del gas (V=V 4) mantenendolo all’equilibrio termico con la massa di mercurio. Si osserva che la pressione raggiunge un valore P 4. Gli stati (V 1; P 1), (V 2; P 2), (V 3; P 3) (V 4; P 4) sono in equilibrio termico fra loro (sono stati per i quali il sistema ha la stessa temperatura) 13
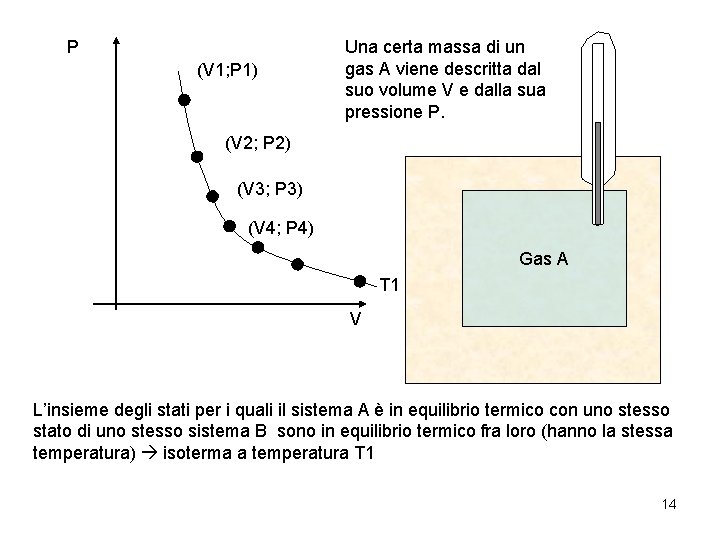
P (V 1; P 1) Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. (V 2; P 2) (V 3; P 3) (V 4; P 4) Gas A T 1 V L’insieme degli stati per i quali il sistema A è in equilibrio termico con uno stesso stato di uno stesso sistema B sono in equilibrio termico fra loro (hanno la stessa temperatura) isoterma a temperatura T 1 14
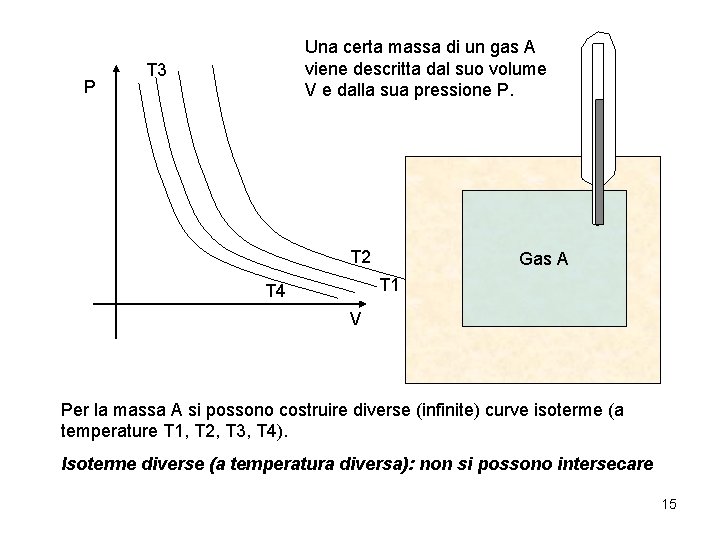
P Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. T 3 T 2 Gas A T 1 T 4 V Per la massa A si possono costruire diverse (infinite) curve isoterme (a temperature T 1, T 2, T 3, T 4). Isoterme diverse (a temperatura diversa): non si possono intersecare 15
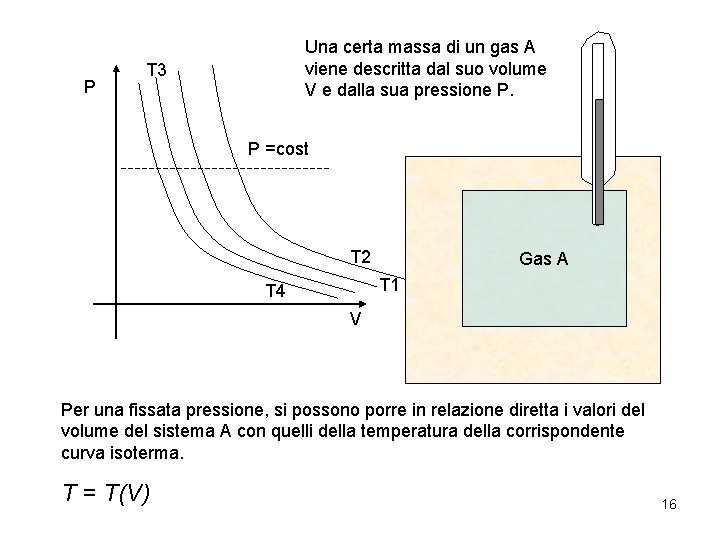
P Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. T 3 P =cost T 2 Gas A T 1 T 4 V Per una fissata pressione, si possono porre in relazione diretta i valori del volume del sistema A con quelli della temperatura della corrispondente curva isoterma. T = T(V) 16
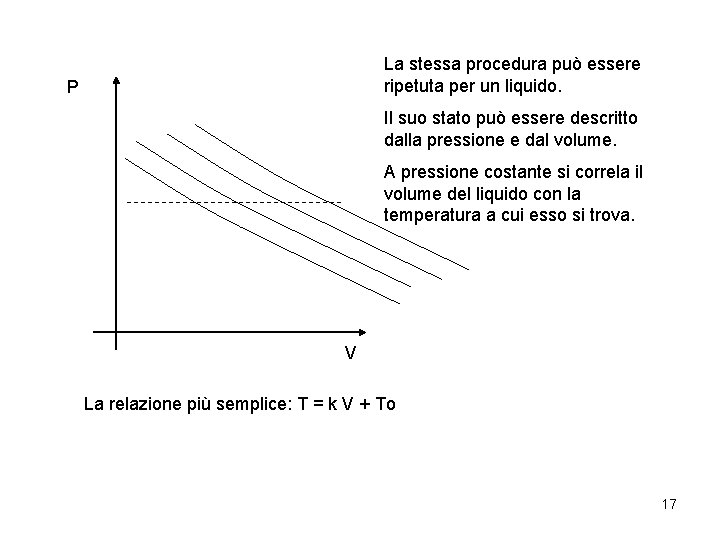
La stessa procedura può essere ripetuta per un liquido. P Il suo stato può essere descritto dalla pressione e dal volume. A pressione costante si correla il volume del liquido con la temperatura a cui esso si trova. V La relazione più semplice: T = k V + To 17
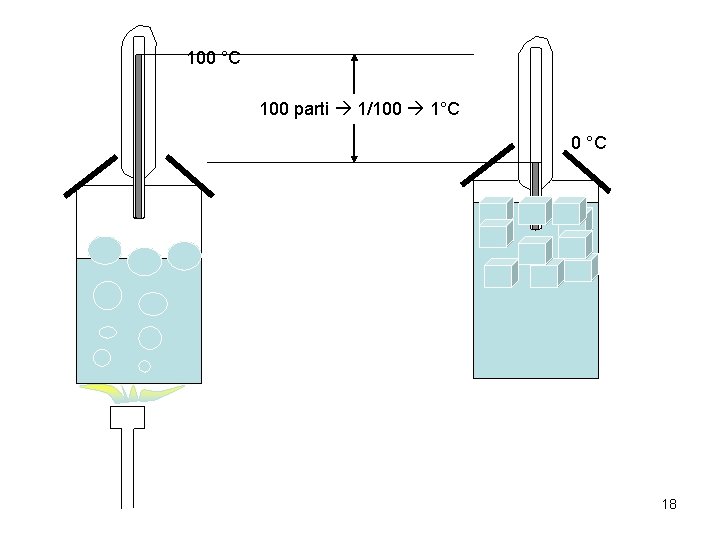
100 °C 100 parti 1/100 1°C 0 °C 18
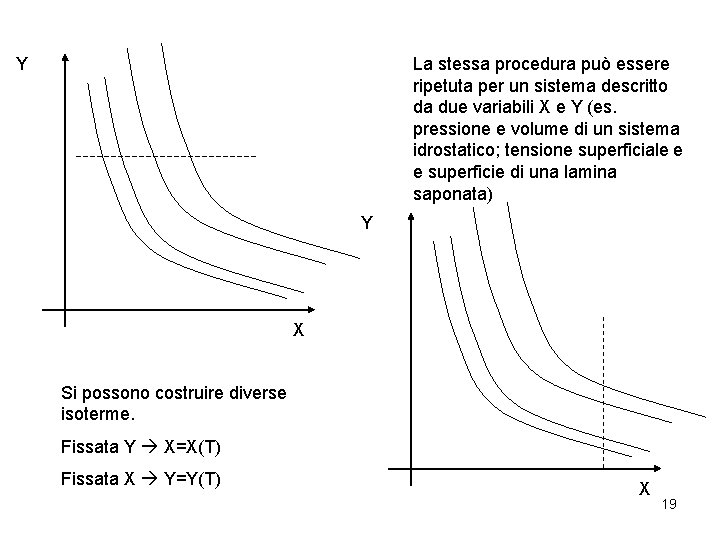
Y La stessa procedura può essere ripetuta per un sistema descritto da due variabili X e Y (es. pressione e volume di un sistema idrostatico; tensione superficiale e e superficie di una lamina saponata) Y X Si possono costruire diverse isoterme. Fissata Y X=X(T) Fissata X Y=Y(T) X 19
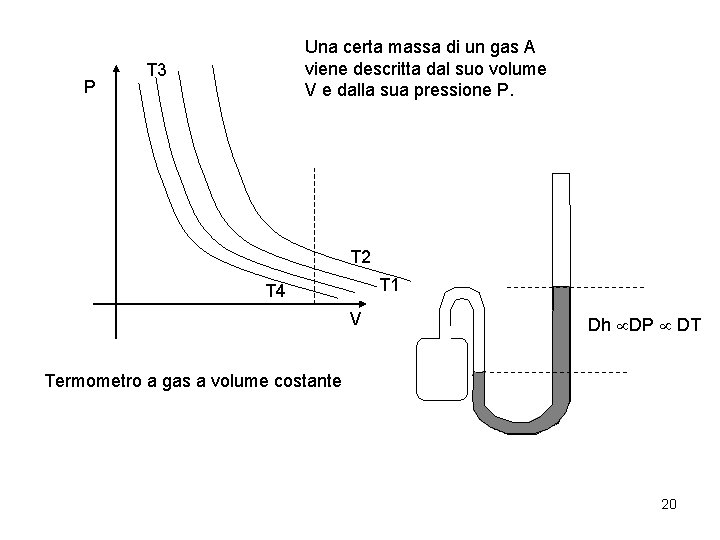
P Una certa massa di un gas A viene descritta dal suo volume V e dalla sua pressione P. T 3 T 2 T 1 T 4 V Dh DP DT Termometro a gas a volume costante 20

Il Termometro • Galileo nel 1610 descrive un “termoscopio” per misurare la temperatura. Tuttavia non vi era un valore standard di riferimento. • Nel 1641 viene costruito, per Ferdinando II Granduca di Toscana, il primo termometro ad alcool in vetro. Vi erano segnate 50 tacche arbitrarie • Nel 1702, Roemer suggerisce l’uso di due valori fissi standard su cui basare una scala di temperature 21

Scale di Temperatura • Gabriel Daniel Fahrenheit nel 1724 inventa il termometro a mercurio (che possiede una grande e regolare espansione termica) • I due punti fissi sono – 0: la temperatura di una miscela di cloruro d’ammonio e ghiaccio – 100: la temperatura di un corpo umano in salute – In seguito Fahrenheit modificò la scala in modo tale che la temperatura di fusione del ghiaccio fosse 32 °F e il punto di bollizione dell’acqua 212 °F 22
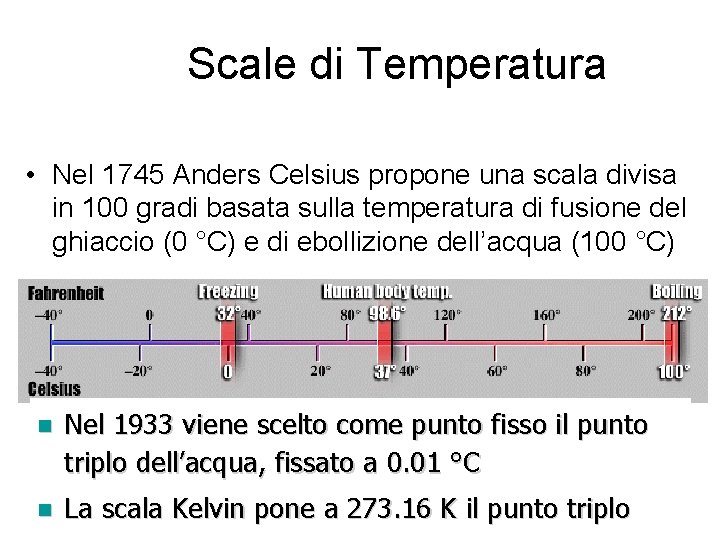
Scale di Temperatura • Nel 1745 Anders Celsius propone una scala divisa in 100 gradi basata sulla temperatura di fusione del ghiaccio (0 °C) e di ebollizione dell’acqua (100 °C) n n Nel 1933 viene scelto come punto fisso il punto triplo dell’acqua, fissato a 0. 01 °C A. Stefanel - Termodinamica 1 La scala Kelvin pone a 273. 16 K il punto triplo 23
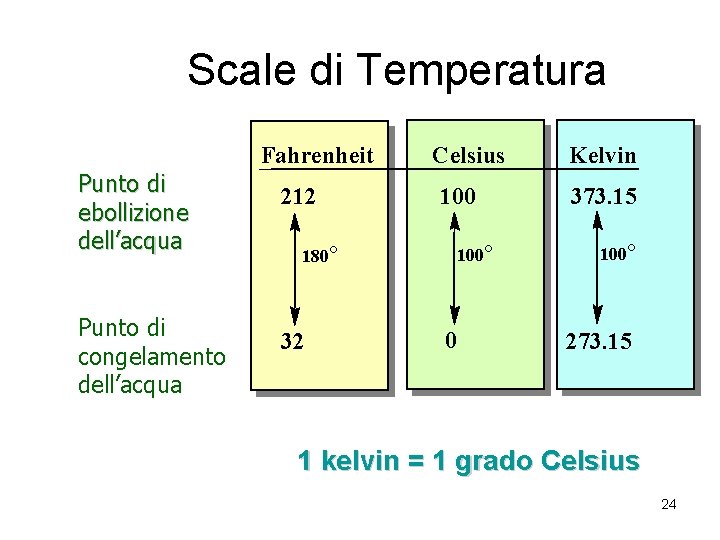
Scale di Temperatura Fahrenheit Punto di ebollizione dell’acqua Punto di congelamento dell’acqua 212 Celsius 100° 180° 32 0 Kelvin 373. 15 100° 273. 15 1 kelvin = 1 grado Celsius 24

Termometri • Si sfrutta una proprietà della materia • Nel nostro caso la dilatazione dei solidi e dei liquidi • Si definiscono due stati riproducibili • ad es. ghiaccio fondente ed acqua in ebollizione • Si danno delle temperature convenzionali ai due stati • ad es. 0°C e 100°C, ma anche 0°R e 80°R… 25

Termometri • Si divide l’intervallo in parti uguali • Si sceglie una scala lineare per semplicità • A questo punto si ha in mano un attrezzo per misurare • il solito termometro a bulbo, magari • Oggi – decine di sistemi diversi per misurare la temperatura – come si misurano temperature bassissime? E altissime? Ed in oggetti piccolissimi? Magari la temperatura di una zanzara o di una cellula? 26

Termoscopi e termometri • Legalmente ed internazionalmente si usa il termometro a gas perfetto 27
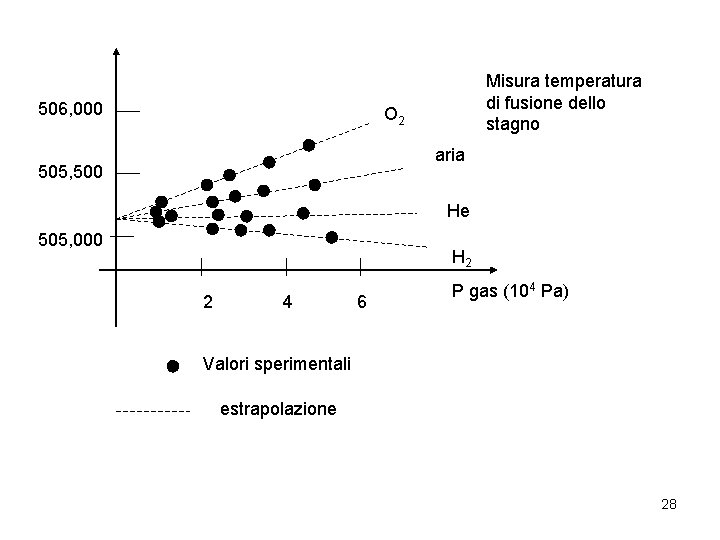
506, 000 Misura temperatura di fusione dello stagno O 2 aria 505, 500 He 505, 000 H 2 2 4 6 P gas (104 Pa) Valori sperimentali estrapolazione 28
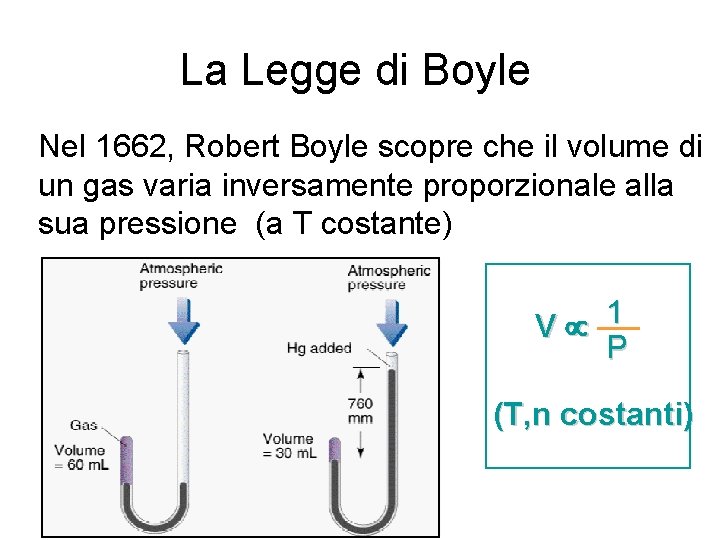
La Legge di Boyle Nel 1662, Robert Boyle scopre che il volume di un gas varia inversamente proporzionale alla sua pressione (a T costante) 1 V P (T, n costanti)
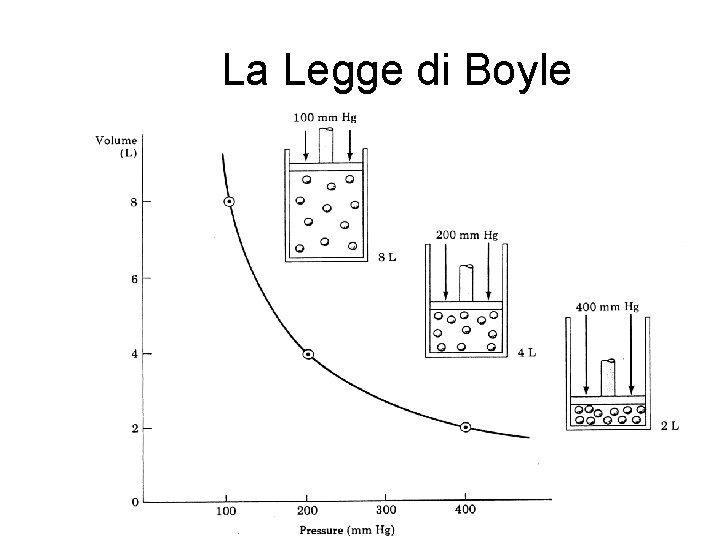
La Legge di Boyle A. Stefanel - Termodinamica 1 30

La Legge di Boyle · A Temperatura costante p. V = costante p 1 V 1 = p 2 V 2 Robert Boyle 1627 -1691. Figlio del Conte di Cork, Irlanda. 31
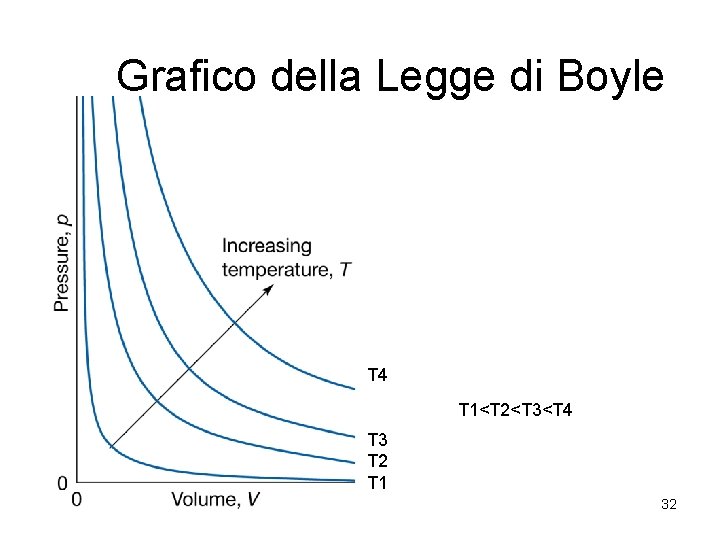
Grafico della Legge di Boyle T 4 T 1<T 2<T 3<T 4 T 3 T 2 T 1 32
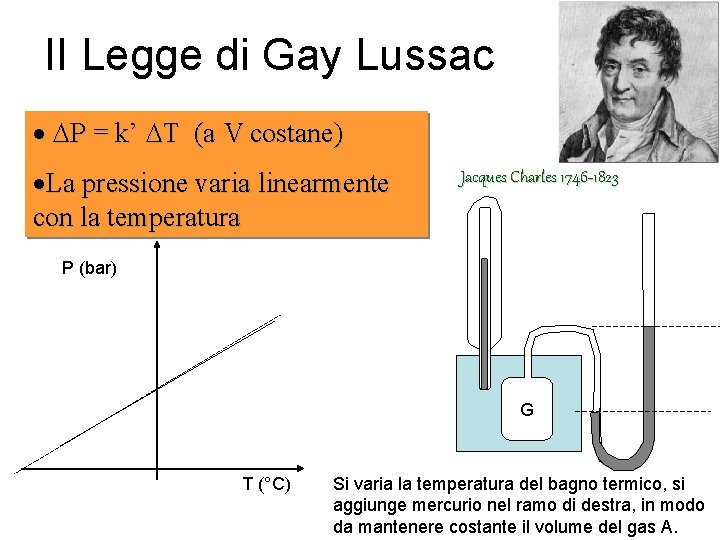
II Legge di Gay Lussac · P = k’ T (a V costane) ·La pressione varia linearmente con la temperatura Jacques Charles 1746 -1823 P (bar) G T (°C) Si varia la temperatura del bagno termico, si aggiunge mercurio nel ramo di destra, in modo da mantenere costante il volume del gas A.
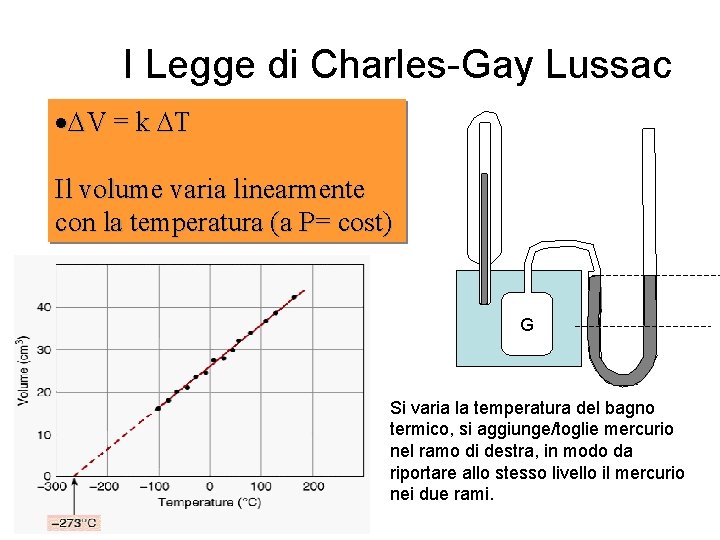
I Legge di Charles-Gay Lussac · V = k T Il volume varia linearmente con la temperatura (a P= cost) G Si varia la temperatura del bagno termico, si aggiunge/toglie mercurio nel ramo di destra, in modo da riportare allo stesso livello il mercurio nei due rami.
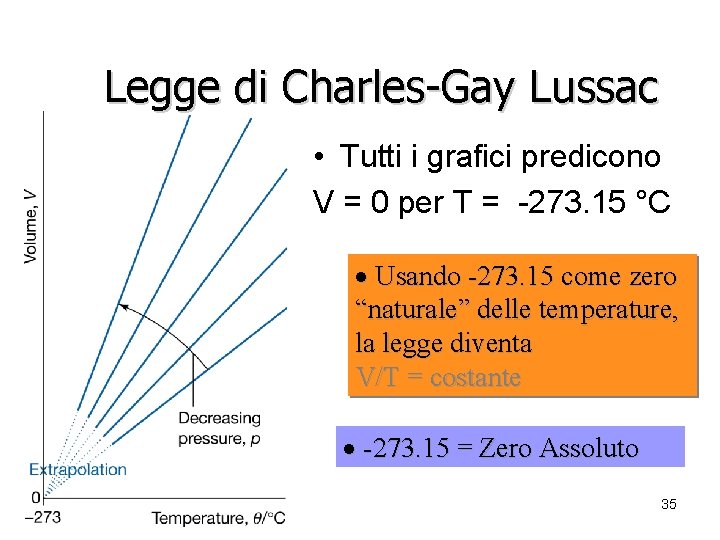
Legge di Charles-Gay Lussac • Tutti i grafici predicono V = 0 per T = -273. 15 °C · Usando -273. 15 come zero “naturale” delle temperature, la legge diventa V/T = costante · -273. 15 = Zero Assoluto 35

La Scala Kelvin di Temperatura • Dato che tutti i grafici della legge di Charles-Gay Lussac intersecano l’asse delle temperature a -273. 15°C, Lord Kelvin propose di usare questo valore come zero di una scala assoluta di temperature: la scala Kelvin. • 0 Kelvin (0 K) è la temperatura dove il volume di un gas ideale è nullo, e cessa ogni movimento molecolare. • 1 K = 1 °C 36

Condizioni Standard • Condizioni Ambientali Standard di T e P (SATP) – Temperatura: 25 °C = 298. 15 K – Pressione: 1 bar – Il volume molare di un gas e’ Vm = 24. 79 L n Condizioni Normali (vecchie STP, non piu’ usate) ´ Temperatura: 0 °C = 273. 15 K ´ Pressione: 1 atm ´ A. Stefanel - Termodinamica 1 37 Il volume molare di un gas ideale e’ Vm = 22. 41 L
- Slides: 37