Termodinamica ambiente sistema ambiente Sistemi Sistema aperto pu

Termodinamica

ambiente sistema ambiente

Sistemi • Sistema aperto = può scambiare energia e materia con l’ambiente • Sistema chiuso = può scambiare solo energia • Sistema isolato = non è in grado di scambiare né energia né materia

Calore, lavoro e energia interna • Lavoro, w = movimento contro una forza che vi si oppone. • Calore, q = trasferimento di energia per effetto di una differenza di temperatura. • Energia interna, U = l’energia interna di un sistema si accumula sotto forma di energia cinetica e di energia potenziale.

Variazione di energia interna Siamo interessati a trasformazioni di energia interna: DU = Ufin –U iniz Energia trasferita a un sistema per mezzo di lavoro = w Energia trasferita a un sistema come calore, per effetto di differenza di temperatura = q DU= w+q

Primo principio della termodinamica L’energia interna di un sistema isolato è costante. Il Primo Principio stabilisce l’equivalenza di calore e lavoro come mezzi di trasferire l’energia: DU = w + q

Le funzioni di stato • Le funzioni di stato dipendono soltanto dallo stato del sistema. • La variazione di una funzione di stato nel passare da uno stato all’altro è indipendente dal percorso fatto. • L’energia interna è funzione di stato; calore e lavoro non lo sono.
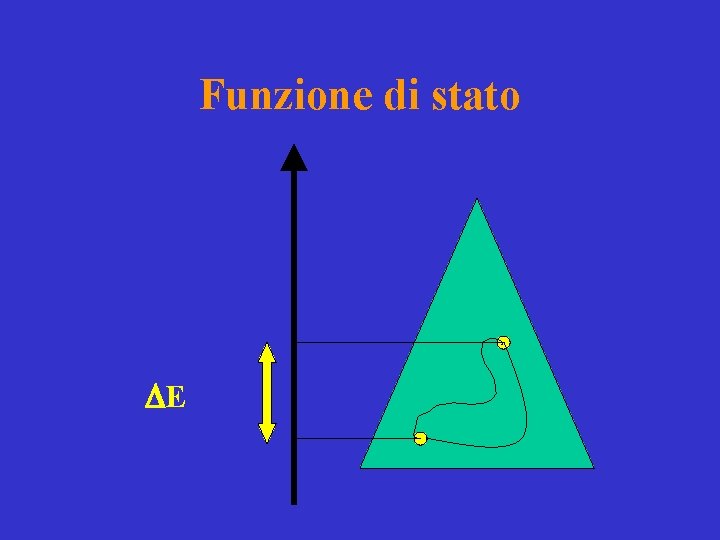
Funzione di stato DE

L’entalpia La funzione di stato che ci permette di seguire il calore scambiato a pressione costante è l’entalpia, H: H = Qp La variazione di entalpia uguaglia il calore ceduto o assorbito a P costante.

DH • L’entalpia di un sistema, che è una proprietà di stato, misura l’energia del sistema disponibile in forma di calore a P costante. • Per un processo endotermico DH > 0 • Per un processo esotermico DH < 0
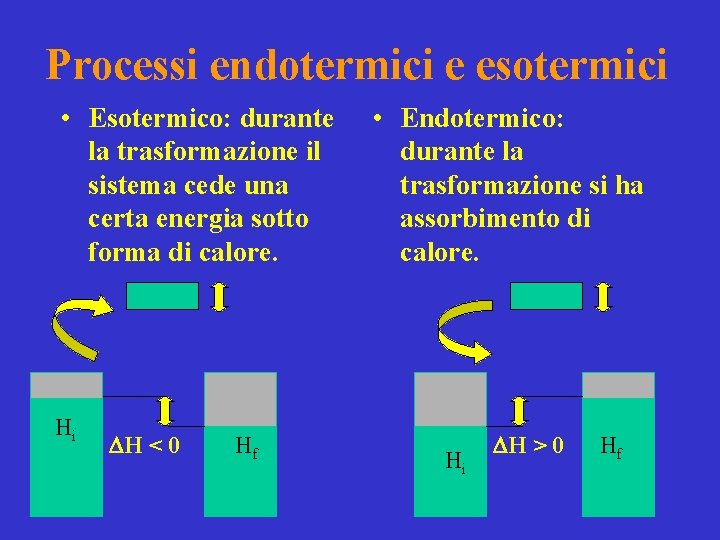
Processi endotermici e esotermici • Esotermico: durante la trasformazione il sistema cede una certa energia sotto forma di calore. Hi DH < 0 Hf • Endotermico: durante la trasformazione si ha assorbimento di calore. Hi DH > 0 Hf

L’entalpia nei cambiamenti di stato • Consideriamo cambiamenti di stato che avvengono a P costante: • Si può definire un’entalpia molare standard di vaporizzazione. Il processo sarà sempre endotermico: DHvap = Hvapore, m – H liquido, m • Lo stesso vale per il processo di fusione: DHfus = Hliquido, m – H solido, m • E per quello di sublimazione: DHsub = Hvapore, m – H solido, m
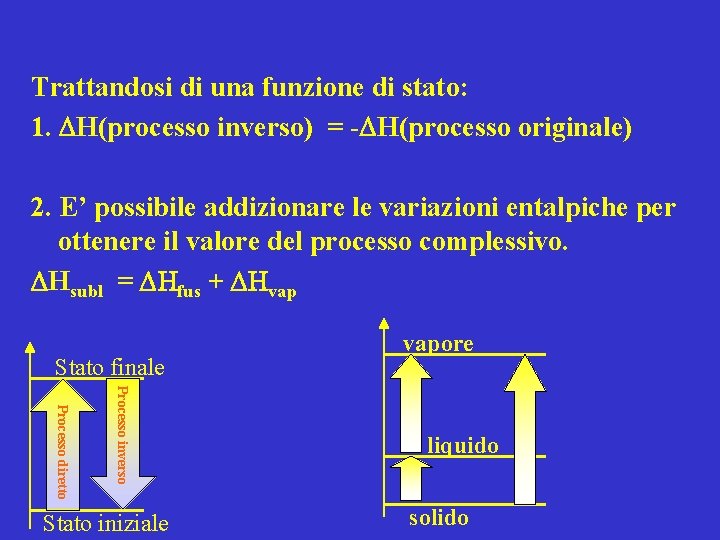
Trattandosi di una funzione di stato: 1. DH(processo inverso) = -DH(processo originale) 2. E’ possibile addizionare le variazioni entalpiche per ottenere il valore del processo complessivo. DHsubl = DHfus + DHvap Stato finale Processo inverso Processo diretto Stato iniziale vapore liquido solido

L’entropia e il secondo principio della termodinamica • L’entropia, S, è una funzione di stato che misura il disordine del sistema: bassa entropia vuol dire poco disordine; alta entropia corrisponde a grande disordine. • L’entropia di un sistema isolato aumenta nel corso di qualsiasi processo spontaneo. non spontaneo

DS DS = d. Q/T (si considerano piccole variazioni di Q in modo che il processo sia reversibile. Il sistema e l’ambiente hanno la possibilità di equilibrarsi, e quindi sono sempre in equilibrio tra loro) Intuitivamente: • se si trasferisce al sistema una certa quantità di calore, si promuove un considerevole disordine; • il disordine aumenta in misura maggiore quanto più la temperatura è bassa.

Terzo principio della termodinamica • In un cristallo perfetto allo zero assoluto l’entropia è uguale a zero.

Interpretazione molecolare dell’entropia S = k ln. W k = costante di Boltzmann W = numero dei modi in cui le particelle possono disporsi.

Interpretazione molecolare dell’entropia: Es. W = 24 2 numero di disposizioni 4 numero di molecole

L’equilibrio • Equilibrio equivale a mancanza di qualunque tendenza del sistema a evolvere nella direzione diretta o inversa. DStot = 0 Dove con “tot” si intende sistema + ambiente

Il cambiamento di entropia dell’ambiente DSamb = -DH/T L’entropia dell’ambiente aumenta se in esso viene rilasciato calore, e tale aumento è tanto maggiore tanto più la temperatura è bassa. DStot = DS + DSamb = DS -DH/T -TDStot = DH- TDS

L’energia libera di Gibbs G = H-TS DG = DH-TDS = -TDStot Un aumento dell’energia libera corrisponde ad una diminuzione dell’entropia totale. Quindi un processo è spontaneo quando corrisponde ad una diminuzione di energia libera. DG < 0

Spontaneità • La variazione dell’energia libera è una misura della variazione dell’entropia totale del sistema e del suo ambiente (a T e P costanti). • I processi spontanei (a T e P costanti) si accompagnano alla diminuzione dell’energia libera.

Processi spontanei Variazione di entalpia DH < 0 Esotermico DH > 0 Endotermico Variazione di entropia DS > 0 Aumento DS < 0 Diminuzione Spontaneo? DG < 0 SI SI se |TDS| < | DH| SI se |TDS| > | DH| DG > 0 NO

Termodinamica dei passaggi di stato • Passando dallo stato solido a quello liquido e a quello gassoso si passa da uno stato più ordinato a uno meno ordinato. Corrispondentemente l’entropia del sistema aumenta. • Transizione solido-liquido: DH > 0, DS >0 • Transizione liquido-gas: DH > 0, DS >0 • Transizione solido-gas: DH > 0, DS >0 DG può essere > o < 0, a seconda della T • Lungo le curve di equilibrio, DG = 0

Termodinamica del processo di dissoluzione DHsol = DHsoluto + DHsolvente +DHidratazione >0 <0 All’inizio del processo di dissoluzione DS > 0. Man mano che il processo di dissoluzione va avanti, DS diminuisce e può diventare anche negativo. Quando DHsol = TDS si ha l’equilibrio ed il numero di particelle che dal solido passano in soluzione è uguale al numero di particelle che dalla soluzione ritornano allo stato solido. Si dice che la soluzione è satura.

Termodinamica di reazione DG° = n DG° (prodotti) - n DG°(reagenti) • Condizioni standard (°): 1 atm e 298. 15 K. • Si parla sempre di valori molari. • Si possono scrivere formule analoghe per DH e DS.

Entalpia molare standard di formazione DHf° • Variazione di entalpia associata alla formazione di una mole di composto partendo dalle sostanze elementari che lo compongono, essendo tutti i reagenti e i prodotti alle condizioni standard. • Per convenzione DHf° di una qualunque sostanza elementare è uguale a zero. DH°= n. DHf°(prodotti)- n DHf°(reagenti)

Entropia molare standard Sm° • Entropia molare standard: cresce con la complessità della sostanza considerata. • A parità di temperatura l’entropia molare standard dei gas è superiore a quella dei solidi e dei liquidi corrispondenti. Sm° delle sostanze elementari è diversa da zero. DS°reazione = n. Sm° (prodotti) - n. Sm° (reagenti)

Energia libera molare standard di formazione DGf° • Variazione di energia libera associata alla formazione di una mole di composto partendo dalle sostanze elementari che lo compongono, essendo tutti i reagenti e i prodotti alle condizioni standard. In generale, qualsiasi: per una reazione • I valori di DH°(298) e DS°(298) permettono di stimare DG°(T) (sempre però alla P di 1 atm).

Legge di Hess Reazione complessiva Entalpia • L’entalpia di reazione è la somma delle entalpie di qualsiasi sequenza di reazioni (alla stessa T e alla stessa P) in cui la reazione generale può essere scomposta. e b a c prodotti d reagenti
- Slides: 30