TERMOCHEMIE REAKN TEPLO TERMOCHEMICK ZKONY RNDr Marta Najbertov

TERMOCHEMIE – REAKČNÍ TEPLO, TERMOCHEMICKÉ ZÁKONY RNDr. Marta Najbertová

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Název školy Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Adresa školy IČO Operační program Registrační číslo Označení vzdělávacího materiálu Vzdělávací oblast Vzdělávací obor Tematický okruh Sokolovská 1638 620 330 26 Operační program Vzdělávání pro konkurenceschopnost CZ. 1. 07/1. 1. 28/01. 0050 K_INOVACE_1. CH. 07 Člověk a příroda Chemie Termochemie – reakční teplo, termochemické zákony Zhotoveno Ročník Vyšší stupeň osmiletého gymnázia a čtyřleté gymnázium (RVP – G) Anotace Materiál je určen jako studijní materiál v předmětu chemie. Je zaměřen na energetické změny v průběhu chemické reakce a jejich popis pomocí termochemických zákonů. Primárně je koncipován pro seminář chemie, lze jej využít i v hodinách chemie.

Energetické změny v průběhu reakce V průběhu chemických reakcí dochází ke změnám vazebných poměrů, meziatomových vzdáleností, vazebných úhlů, vznikají nové elektronové konfigurace, nastávají změny skupenských stavů. To vše má za následek změny energie. K popisu těchto změn používáme: nestavové veličiny – jejich hodnota závisí na průběhu děje, při výpočtech nutný matematický aparát (integrace); mezi nestavové veličiny patří práce, teplo. stavové veličiny – jejich hodnota nezávisí na způsobu přechodu, je funkcí počátečního a konečného stavu; mezi stavové veličiny patří vnitřní energie (U), entalpie (H), entropie (S), Gibbsova energie (G), tlak (p), teplota (T)…. .

Energetické změny v průběhu reakce Celkový obsah energie soustavy se nazývá vnitřní energie. Podle prvního termodynamického zákona (1. věta termodynamiky) platí: 1. ∆U=Q+ Q teplo, A všechny druhy práce. Je-li konána pouze objemová práce, lze psát 2. ∆U=Q+ p. V je-li děj izobarický (konstantní tlak), lze psát 3. ∆U=Q+ p∆V úpravou vztahu dostaneme tvar 4. Q=∆U - p∆V je-li děj izochorický (konstantní objem), lze psát 5. Q=∆U

Energetické změny v průběhu reakce Protože teplo není stavová veličina, byla pro izobarické děje zavedena veličina entalpie a definována vztahem 6. ∆H=∆U+ p. V za předpokladu, že je děj izobarický, pak platí 7. ∆H=∆U+ p∆V a je-li děj izochorický, pak platí rovnost 8. ∆H=∆U z 5. a 8. rovnice pak platí rovnost 9. ∆H = Q kde ∆H – izobarické reakční teplo Absolutní hodnotu H nelze určit, proto se používá ∆ a tlaku 101325 Pa. - při teplotě 298, 15° K

Izobarické reakční teplo – teplo, které soustava přijme nebo odevzdá, jestliže v ní za konstantního tlaku proběhne daná chemická reakce v rozsahu jednoho molu základních reakčních přeměn vyjádřených chemickou rovnicí za předpokladu, že se teplota soustavy nezmění a reaktanty a produkty jsou ve stavech, udaných v chemické rovnici. Pro vyjádření stavů látek se používá označení: pevné skupenství (s) kapalné skupenství (l) Stav látek se doplní do rovnice za symboly látek. C(s, grafit) + O 2(g) CO 2(g) plynné skupenství (g)

Reakční teplo Hodnota ∆ se zjišťuje: ze standardních slučovacích tepel (∆ )sluč – takové reakční teplo reakce, kdyby jeden mol sloučeniny vznikl přímým sloučením z prvků, reaktanty a produkty jsou ve standardním stavu. Pro prvky je rovno nule. Pro teplo reakce platí vztah: ze standardních spalných tepel (∆ )spal – takové reakční teplo reakce, při níž se jeden mol sloučeniny spálí v nadbytku kyslíku, reaktanty a produkty jsou ve standardním stavu. Pro teplo reakce platí vztah: Reakční tepla většiny sloučenin byla experimentálně změřena a jsou uvedena v termochemických tabulkách.
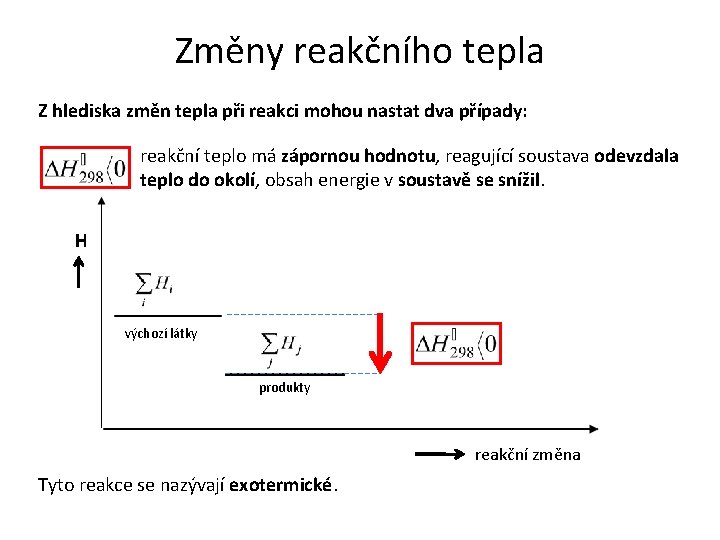
Změny reakčního tepla Z hlediska změn tepla při reakci mohou nastat dva případy: reakční teplo má zápornou hodnotu, reagující soustava odevzdala teplo do okolí, obsah energie v soustavě se snížil. H výchozí látky produkty reakční změna Tyto reakce se nazývají exotermické.
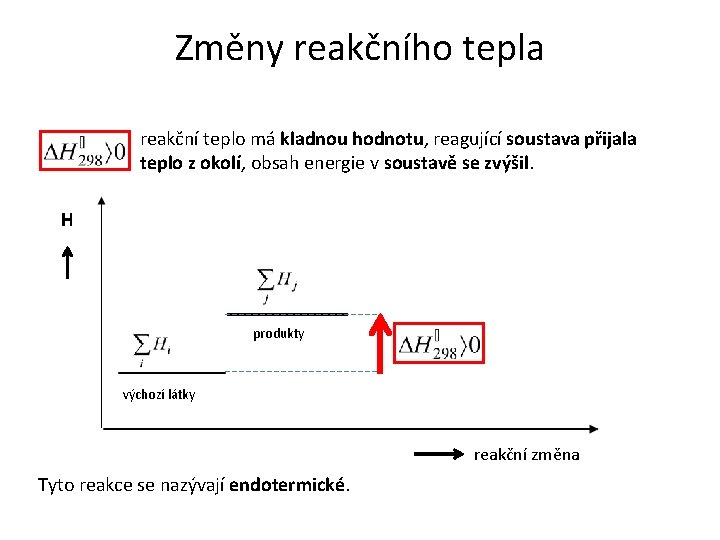
Změny reakčního tepla reakční teplo má kladnou hodnotu, reagující soustava přijala teplo z okolí, obsah energie v soustavě se zvýšil. H produkty výchozí látky reakční změna Tyto reakce se nazývají endotermické.

Zápis chemické reakce Definované stavy látek (skupenství, krystalografická modifikace) a reakční teplo se uvádí v termochemickém zápisu chemické rovnice. 2 moly vodíku v plynném skupenství reagují s 1 molem kyslíku v plynném skupenství, produktem reakce jsou 2 moly vody v plynném skupenství. Reakce je exotermická. 1 mol uhličitanu vápenatého v pevném skupenství zreaguje na 1 mol oxidu vápenatého v pevném skupenství a 1 mol oxidu uhličitého v plynném skupenství. Reakce je endotermická.

Termochemické zákony To, že je reakční teplo stavová veličina, umožňuje formulaci dvou termochemických zákonů. Laplace-Lavoisierův zákon – reakční teplo přímé a protisměrné reakce je až na znaménko stejné (1. termochemický zákon). Je-li přímá reakce exotermická, je opačná reakce endotermická a naopak. Hessův zákon – může-li probíhat reakce přímo nebo v několika mezistupních, je výsledné reakční teplo obou cest stejné (2. termochemický zákon). Součet reakčních tepel dílčích reakcí je roven reakčnímu teplu celkové reakce.
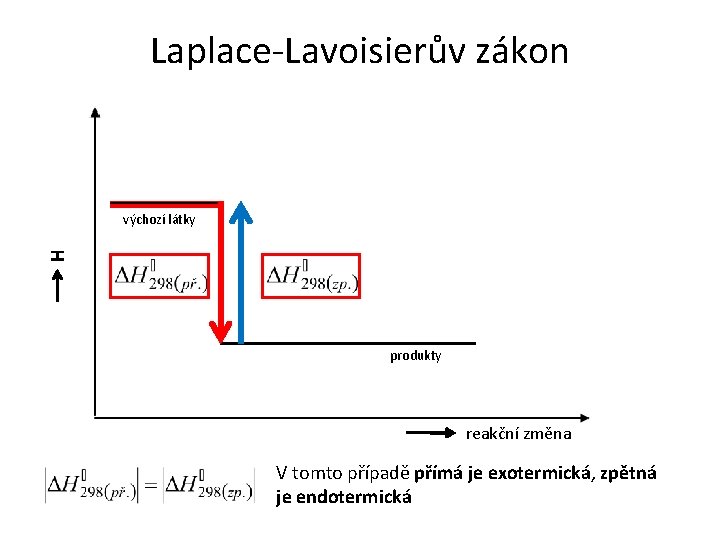
Laplace-Lavoisierův zákon H výchozí látky produkty reakční změna V tomto případě přímá je exotermická, zpětná je endotermická

Aplikace Laplace-Lavoisierova zákona Experimentálně lze obtížně zjistit reakční teplo tvorby benzenu z acetylenu: S využitím Hessova zákona lze pro výpočet využít cestu rozložení acetylenu na prvky a jejich následné sloučení na benzen: Reakční teplo rozkladu acetylenu lze snadno zjistit s využitím Laplaceova-Lavoisierova zákona. Až na znaménko je rovno slučovacímu teplu sloučení uhlíku a vodíku na acetylen. Slučovací teplo sloučení uhlíku a vodíku na benzen lze také bez problému určit:
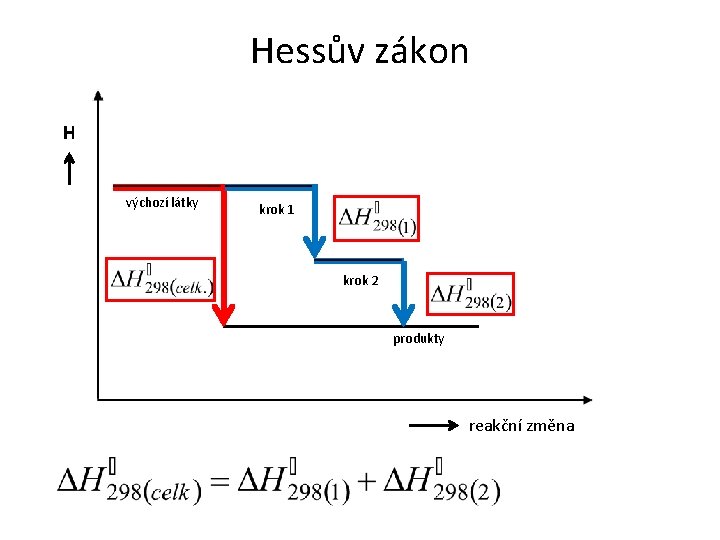
Hessův zákon H výchozí látky krok 1 krok 2 produkty reakční změna

Aplikace Hessova zákona Experimentálně lze těžko změřit reakční teplo přeměny uhlíku na oxid uhelnatý , vždy při reakci vzniká i oxid uhličitý. Toto reakční teplo lze spočítat ze snadno zjistitelných reakčních tepel přeměny uhlíku na oxid uhličitý a oxidu uhelnatého na oxid uhličitý. Přímá reakce Krok 1 Krok 2 Hledané reakční teplo

Termochemie a živé soustavy Živé objekty – otevřené systémy, existující ve stacionárně rovnovážném stavu – ustálený, dynamický stav, kdy je výměna hmoty a energie s okolím v rovnováze (může být porušeno). Anabolické reakce(asimilační) – složitější látky syntetizovány z jednodušších, využita energie rozkladem makroergních vazeb zásobních látek nebo látek přijatých v potravě. Katabolické reakce (disimilační) – rozklad složitějších látek na jednodušší, energie v přenašečích (ATP, GTP. . . ) využita na realizaci anabolických reakcí, část využita pro termoregulaci. Katabolické reakce Anabolické reakce

Termochemie a živé soustavy Přeměna glukózy (základní zdroj energie pro buňky) na oxid uhličitý a vodu: Glukóza primárně vzniká fotosyntézou podle zjednodušené rovnice: Při nedostatku energie se glukóza anaerobní glykolýzou (nedostatek kyslíku) jedenácti spřaženými reakcemi přemění na laktát. Vzniklý laktát je transportován do jater, kde je z něj reakcemi, které nejsou totožné s obráceným směrem glykolýzy (3 z reakcí musí probíhat jinak), opět vzniká glukóza. Reakční tepla obou cest jsou až na znaménka stejná.

Termochemie a živé soustavy Rozklad glukózy v živých organismech podle rovnice: Výsledné reakční teplo je stejné, jako kdybychom stejné množství glukózy (180 g) spálili v nadbytku kyslíku. K poškození buňky nedojde proto, že rozklad probíhá řadou dílčích reakcí, reakční teplo je uvolňováno postupně. Zapálit etanol není problém (lihové kahany, destiláty…). Jeho biologické odbourávání probíhá podle stejné rovnice: Při přímé oxidaci (reakční teplo uvolněno najednou) je teplota hoření etanolu 360 ◦C.

Předpověď průběhu reakce. Jestliže by reakční teplo bylo jediným kritériem průběhu reakce, probíhaly by pouze exotermické děje (systém se snaží dostat do stavu s minimem energie). K popisu změn v systému byla pro izobaricko-izotermický děj zavedena veličina Gibbsova energie G (volná entalpie, Gibbsova volná energie, Gibbsova funkce). Definiční vztah Platí: ∆G=∆H - T∆S ∆H – entalpie (tepelné zabarvení reakce) T – termodynamická teplota ∆S – entropie (míra neuspořádanosti systému) ∆G> 0 děje nepravděpodobné (nemožné) ∆G 0 děje reverzibilní ∆G< 0 děje pravděpodobné, ireverzibilní Gibbsova energie otevřeného systému se může zvyšovat, samozřejmě na úkor snížení Gibbsovy energie okolí (živé soustavy).

Předpověď průběhu reakce. Podmínka ∆G< 0 pro vztah ∆G=∆H - T∆S je splněna v případě: ∆H<0 a současně T∆S>0 exotermické rozkladné reakce, exotermické skladné za vysokých teplot, exotermické s přechodem produktu do kapalného nebo plynného skupenství ∆H<0 a současně T∆S<0, musí platit ∆H <T∆S exotermické skladné reakce při nízkých teplotách ∆H>0 a současně T∆S>0 , musí platit ∆H <T∆S endotermické reakce rozkladné nebo s přechodem produktu do kapalného nebo plynného skupenství ΔS› 0 – zvýšení neuspořádanosti systému, nastává u rozkladných reakcí (z 1 částice více částic) nebo při přechodu z pevného skupenství přes kapalné do plynného ΔS<0 – snížení neuspořádanosti systému, nastává u skladných reakcí (z více částic méně) nebo při přechodu z plynného skupenství přes kapalné do pevného

Gymnázium a Jazyková škola s právem státní jazykové zkoušky Svitavy Zdroje a použitá literatura 1. ATKINS, P. W. a DE PAULA, Julio. Fyzikální chemie. Vyd. 1. Praha: Vysoká škola chemicko-technologická v Praze, 2013. xxvi, 915 s. ISBN 978 -80 -7080 -830 -6. 2. RNDr. ČIPERA, Jan, CSc. Chemie pro IV. ročník gymnázií (2 díl). Praha: Státní pedagogické nakladatelství Praha, 1974. Učební texty pro gymnázia. 3. KLIKORKA, Jiří, VOTINSKÝ, Jiří a HÁJEK, Bohumil. Obecná a anorganická chemie: celost. vysokošk. učebnice pro vys. školy chemicko-technologické. 1. vyd. Praha: SNTL, 1985. 591 s. 4. Fotografie a vzorce z vlastní databáze autora. Vytvořeny programy ACD FREE 12, Snagit Materiál je určen pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízeních. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 21