Terdapat 4 probabilitas dalam peristiwa impregnasi logam pada
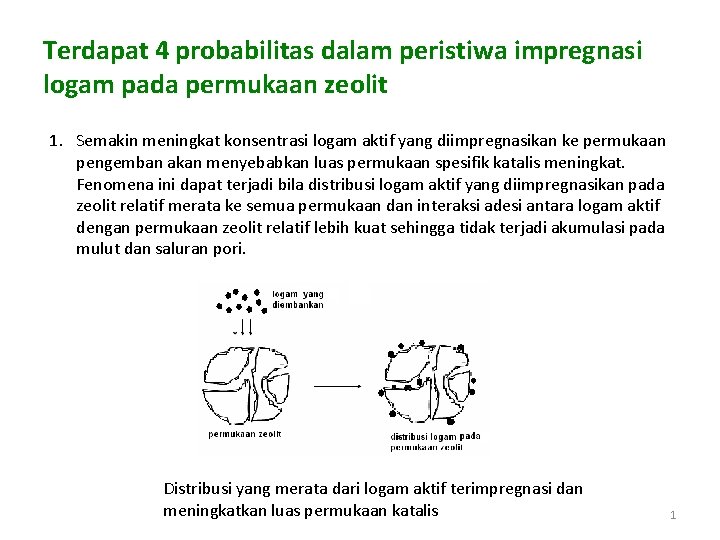
Terdapat 4 probabilitas dalam peristiwa impregnasi logam pada permukaan zeolit 1. Semakin meningkat konsentrasi logam aktif yang diimpregnasikan ke permukaan pengemban akan menyebabkan luas permukaan spesifik katalis meningkat. Fenomena ini dapat terjadi bila distribusi logam aktif yang diimpregnasikan pada zeolit relatif merata ke semua permukaan dan interaksi adesi antara logam aktif dengan permukaan zeolit relatif lebih kuat sehingga tidak terjadi akumulasi pada mulut dan saluran pori. Distribusi yang merata dari logam aktif terimpregnasi dan meningkatkan luas permukaan katalis 1
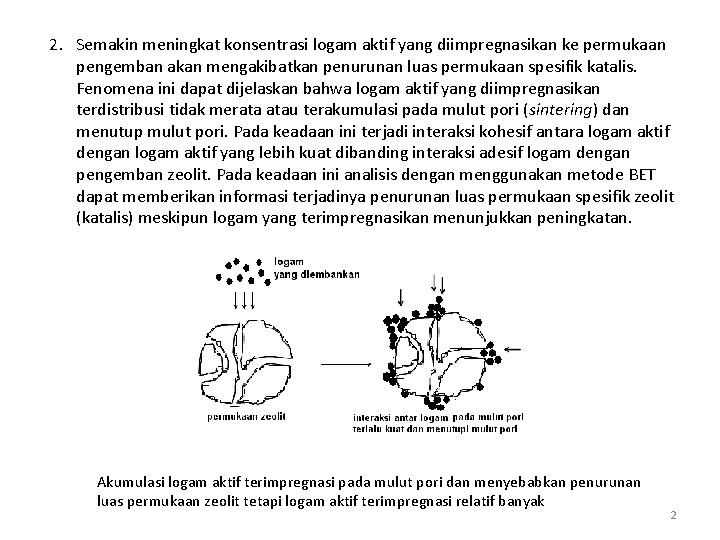
2. Semakin meningkat konsentrasi logam aktif yang diimpregnasikan ke permukaan pengemban akan mengakibatkan penurunan luas permukaan spesifik katalis. Fenomena ini dapat dijelaskan bahwa logam aktif yang diimpregnasikan terdistribusi tidak merata atau terakumulasi pada mulut pori (sintering) dan menutup mulut pori. Pada keadaan ini terjadi interaksi kohesif antara logam aktif dengan logam aktif yang lebih kuat dibanding interaksi adesif logam dengan pengemban zeolit. Pada keadaan ini analisis dengan menggunakan metode BET dapat memberikan informasi terjadinya penurunan luas permukaan spesifik zeolit (katalis) meskipun logam yang terimpregnasikan menunjukkan peningkatan. Akumulasi logam aktif terimpregnasi pada mulut pori dan menyebabkan penurunan luas permukaan zeolit tetapi logam aktif terimpregnasi relatif banyak 2
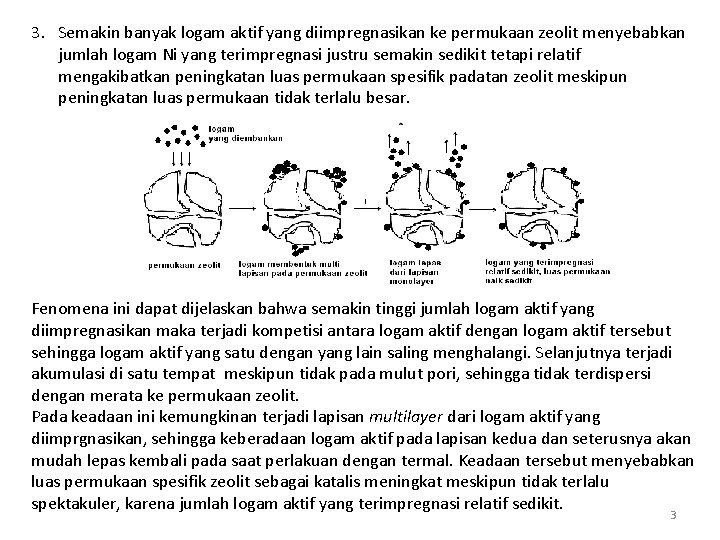
3. Semakin banyak logam aktif yang diimpregnasikan ke permukaan zeolit menyebabkan jumlah logam Ni yang terimpregnasi justru semakin sedikit tetapi relatif mengakibatkan peningkatan luas permukaan spesifik padatan zeolit meskipun peningkatan luas permukaan tidak terlalu besar. Fenomena ini dapat dijelaskan bahwa semakin tinggi jumlah logam aktif yang diimpregnasikan maka terjadi kompetisi antara logam aktif dengan logam aktif tersebut sehingga logam aktif yang satu dengan yang lain saling menghalangi. Selanjutnya terjadi akumulasi di satu tempat meskipun tidak pada mulut pori, sehingga tidak terdispersi dengan merata ke permukaan zeolit. Pada keadaan ini kemungkinan terjadi lapisan multilayer dari logam aktif yang diimprgnasikan, sehingga keberadaan logam aktif pada lapisan kedua dan seterusnya akan mudah lepas kembali pada saat perlakuan dengan termal. Keadaan tersebut menyebabkan luas permukaan spesifik zeolit sebagai katalis meningkat meskipun tidak terlalu spektakuler, karena jumlah logam aktif yang terimpregnasi relatif sedikit. 3

4. Semakin banyak logam aktif yang diimpregnasikan menyebabkan logam aktif yang terimpregnasi relatif sedikit dan luas permukaan spesifik zeolit sebagai katalis menjadi menurun. Kompetisi dan akumulasi logam aktif terimpregnasi pada mulut pori dengan LPS yang menurun Kejadian tersebut dapat disebabkan karena terjadinya kompetisi logam-logam aktif yang diimpregnasikan pada daerah mulut pori dan terjadi lapisan multilayer sehingga pada lapisan atau tumpukkan logam aktif yang berada diatas logam aktif yang lain kemungkinan mengalami interaksi yang lemah (adhesi logam aktif dengan permukaan pada mulut pori lebih kuat dibandingkan kohesi antar logam aktif), sehingga akan mengalami peristiwa desorpsi (pelepasan) dari logam aktif, dengan demikian jumlah logam aktif yang berada pada daerah mulut relatif sedikit dan menutupi mulut pori. Penutupan pori tersebut akan menyebabkan luas permukaan zeolit menjadi turun karena mulut pori tertutupi logam aktif yang diimpregnasikan. 4

Reaksi reversible dari alkohol pada beberapa temperatur 5
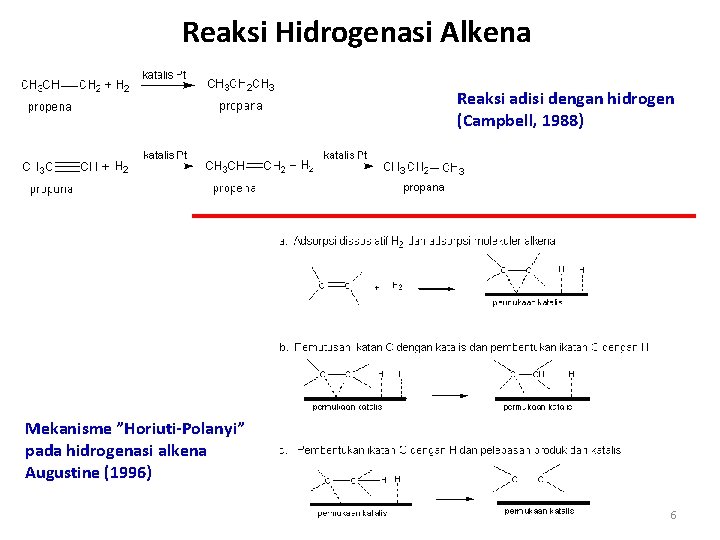
Reaksi Hidrogenasi Alkena Reaksi adisi dengan hidrogen (Campbell, 1988) Mekanisme ”Horiuti-Polanyi” pada hidrogenasi alkena Augustine (1996) 6
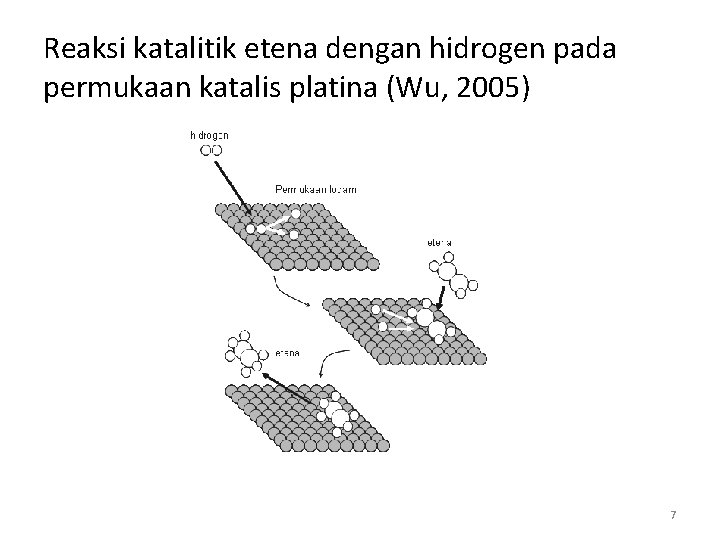
Reaksi katalitik etena dengan hidrogen pada permukaan katalis platina (Wu, 2005) 7

Pada tahun 1835, Berzelius menjelaskan suatu konsep katalis sebagai metode pengontrol terhadap laju suatu reaksi. Katalis didefinisikan sebagai suatu zat yang bila ditambahkan ke dalam sistem reaksi dapat meningkatkan laju reaksi atau mempercepat tercapainya keadaan setimbang dari sistem reaksi tersebut. Peran katalis tidak berpengaruh pada stoikiometri reaksi atau konstanta kesetimbangan reaksi. Katalis terlibat dalam suatu reaksi akan tetapi tidak bereaksi untuk menghasilkan produk dan pada akhir reaksi akan diperoleh kembali (Satterfield, 1980) Pengertian katalis adalah suatu substansi yang dapat mempercepat tercapainya keadaan kesetimbangan dari suatu reaksi tanpa katalis tersebut terlibat secara permanen dalam reaksi (Augustine, 1996). Oleh karena itu jika secara termodinamika suatu reaksi tidak dapat terjadi maka dengan adanya katalis dalam reaksi tersebut juga tidak akan menyebabkan terjadinya reaksi, sehingga dapat dikatakan bahwa katalis bukan suatu substansi yang memulai terjadinya reaksi. Katalis turut berperan aktif dalam proses reaksi tetapi tidak berubah menjadi senyawa produk. Peran aktif katalis tersebut terlihat dari interaksi antara katalis dengan reaktan selama reaksi berlangsung baik secara fisisorpsi maupun kemisorpsi (Satterfield, 1980). 8

Adsorpsi 1. Fisisorpsi 2. Kemisorpsi 3. Desorpsi Interaksi katalis dengan reaktan selalu mengacu pada kesetimbangan, yang artinya tidak seluruh reaktan dapat berubah menjadi produk reaksi (Satterfield, 1980). Interaksi katalis dengan reaktan secara garis besar meliputi proses fisisorpsi, kemisorpsi dan desorpsi. Interaksi antara katalis dengan reaktan dapat menghasilkan senyawa yang lebih aktif sebagai intermediet serta dapat meningkatkan laju, ketepatan dan konsentrasi tumbukan (encounter) akibat dari lokalisasi reaktan. Sebagai konsekuensi dari keadaan tersebut maka energi pengaktifan dari reaksi menjadi lebih rendah. 9
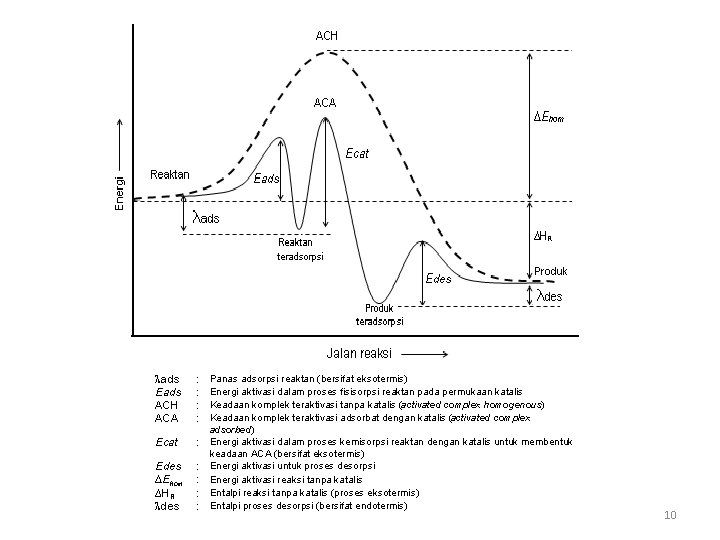
ads Eads ACH ACA : : Ecat : Edes ∆Ehom ∆HR des : : Panas adsorpsi reaktan (bersifat eksotermis) Energi aktivasi dalam proses fisisorpsi reaktan pada permukaan katalis Keadaan komplek teraktivasi tanpa katalis (activated complex homogenous) Keadaan komplek teraktivasi adsorbat dengan katalis (activated complex adsorbed) Energi aktivasi dalam proses kemisorpsi reaktan dengan katalis untuk membentuk keadaan ACA (bersifat eksotermis) Energi aktivasi untuk proses desorpsi Energi aktivasi reaksi tanpa katalis Entalpi reaksi tanpa katalis (proses eksotermis) Entalpi proses desorpsi (bersifat endotermis) 10

Energi pengaktifan adalah energi minimum yang diperlukan suatu reaktan untuk membentuk senyawa antara (keadaan kompleks teraktivasi), sebelum reaktan berubah menjadi produk. Secara kinetika energi pengaktifan dipengaruhi oleh adanya katalis. Reaksi dengan menggunakan katalis heterogen meliputi beberapa tahap utama, yaitu fisisorpsi, kemisorpsi dan desorpsi. Perbedaan jalan reaksi dengan menggunakan katalis dan tanpa katalis. Reaktan yang bereaksi tanpa menggunakan katalis memiliki energi aktivasi reaksi (∆Ehom) yang relatif besar untuk mencapai keadaan transisi (transition state complex, TSC) atau keadaan komplek teraktivasi tanpa katalis (activated complex homogenous, ACH), sehingga dengan ditambahkannya katalis ke dalam sistem reaksi akan menurunkan energi aktivasi reaksi yang diperlukan untuk reaksi tersebut. Besarnya energi aktivasi reaksi dengan menggunakan katalis (Ecat) nilainya lebih kecil dibandingkan dengan besarnya nilai energi aktivasi reaksi tanpa menggunakan katalis (∆Ehom). (sampai disini) 11

Menurut Gasser (1987), reaksi dengan menggunakan katalis melibatkan peristiwa fisisorpsi, kemisorpsi dan desorpsi. Peristiwa fisisorpsi merupakan keadaan molekul reaktan dalam fasa gas teradsorpsi pada permukaan katalis dan melibatkan gaya van der Waals. Peristiwa fisisorpsi bersifat eksotermis dan besarnya energi yang dilepaskan – 40 k. J/mol. Kemisorpsi merupakan peristiwa terjadinya pertukaran elektron serta pembentukan ikatan kimia antara molekul gas reaktan dengan permukaan katalis dan bersifat eksotermis. Besarnya energi yang dilepaskan pada peristiwa kemisorpsi adalah – 400 k. J/mol. Reaktan yang teradsorpsi pada permukaan katalis dapat bermigrasi sehingga memungkinkan terjadinya tumbukan antara reaktan yang satu dengan yang lain hingga terjadi reaksi dan menghasilkan produk antara pada permukaan katalis (activated complex adsorbed, ACA). Selanjutnya produk akan mengalami peristiwa desorpsi secara spontan, dimana energi yang diperlukan untuk peristiwa desorpsi (λdes) terpenuhi dari nilai energi yang dilepaskan dari peristiwa kemisorpsi. Peristiwa desorpsi pada reaksi katalitik bersifat endotermis. 12

Jenis, fungsi dan contoh katalis (Satterfield, 1980) No. Jenis Katalis 1 Logam 3 Oksida dan Sulfida Semikonduktif Oksida isolator 4 Asam 2 Fungsi Hidrogenasi, Dehidrogenasi Oksidasi, Desulfurisasi Contoh Fe, Ni, Pt, Ag Ni. O, Zn. O, Mg. O Bi 2 O 3, Mo. O 3 Dehidrasi Al 2 O 3, Si. O 2, Mg. O Polimerisasi, Isomerisasi, H 3 PO 4, H 2 SO 4, Alkilasi Si. O 2/Al 2 O 3 Tahapan dalam reaksi katalitik dengan katalis heterogen menurut Wu (2005) dan Augustine (1996), adalah sebagai berikut : 1. Difusi (transfer massa) reaktan dari fasa fluida menuju permukaan luar katalis. 2. Difusi reaktan dari mulut pori melalui pori-pori katalis menuju daerah sekitar permukaan bagian dalam katalis. 3. Adsorpsi reaktan pada permukaan katalis. 4. Reaksi pada permukaan katalis. 5. Desorpsi produk reaksi dari permukaan katalis. 6. Difusi produk dari permukaan bagian dalam melalui pori-pori katalis menuju mulut pori pada permukaan luar. 7. Difusi (transfer massa) produk dari permukaan katalis ke fasa fluida. 13

Proses adsorpsi reaktan pada permukaan katalis heterogen didasarkan pada tumbukan (collision) atau pertemuan (encounter) antara molekul reaktan dalam fasa fluida dengan permukaan katalis. Menurut Gasser (1987), terdapat beberapa tipe tumbukan yang mungkin terjadi pada permukaan padatan (katalis) yaitu : 1. Molekul reaktan yang menumbuk katalis dipantulkan dari permukaan padatan yang bersifat elastis sempurna atau sebagian. Pada proses ini tidak terjadi pertukaran energi (d. E = 0) atau terjadi pertukaran energi sebagian. Tumbukan molekul reaktan pada permukaan padatan akan dipantulkan kembali dengan energi yang sama saat molekul tersebut menumbuk atau dipantulkan dengan energi yang hampir sama. 2. Molekul reaktan diadsorpsi pada permukaan dan terjadi perpindahan atau pertukaran energi (d. E ≠ 0). Pada fenomena ini tumbukkan antara molekul reaktan dengan permukaan katalis akan dipantulkan sebagian dan berdasarkan besarnya energi yang dilepaskan maka fenomena adsorpsi ini dibedakan menjadi dua macam, yaitu : 14

Fisisorpsi merupakan proses penyerapan molekul gas pada permukaan padatan secara fisik yang diasosiasikan sebagai gaya tarik yang lemah (Van der Waals) dari molekul reaktan dan permukaan katalis. Dasar pemikiran dari proses fisisorpsi adalah gaya tarik-menarik elektrostatis antar molekul dan bila gaya ini terjadi antara atom atau molekul dengan permukaan maka yang terjadi adalah hanya gaya tarik-menarik secara fisik tanpa disertai perubahan kimia. Fisisorpsi mempunyai panas adsorpsi yang relatif kecil yaitu sekitar 40 k. J/mol (eksotermis). Pada fisisorpsi molekul gas yang teradsorpsi akan mudah dilepas kembali dengan cara menaikkan temperatur sistem. Kemisorpsi merupakan adsorpsi secara kimia yang diasosiasikan atau digambarkan dengan pertukaran elektron dan pembentukan ikatan kimia antara molekul reaktan yang teradsorp dengan permukaan padatan (interaksi antar orbital elektron). Kemisorpsi pada umumnya didahului dengan proses fisisorpsi, dan pada kemisorpsi energi yang dilepaskan cukup besar yaitu sekitar 400 k. J/mol (eksotermis). 15
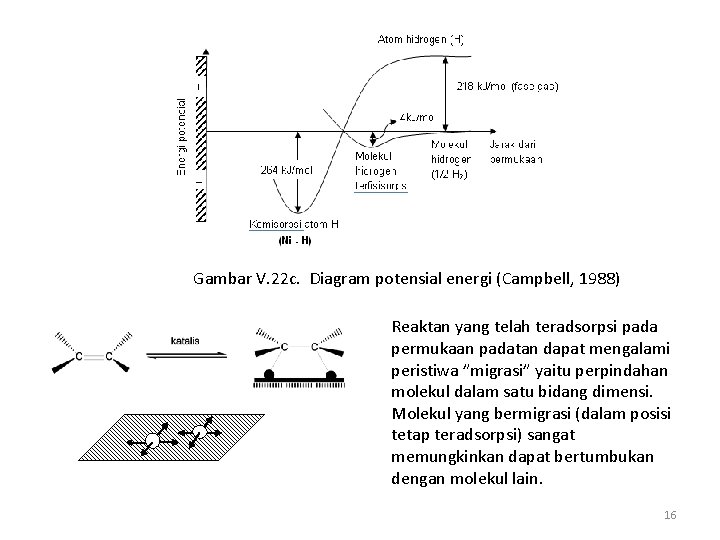
Gambar V. 22 c. Diagram potensial energi (Campbell, 1988) Reaktan yang telah teradsorpsi pada permukaan padatan dapat mengalami peristiwa ”migrasi” yaitu perpindahan molekul dalam satu bidang dimensi. Molekul yang bermigrasi (dalam posisi tetap teradsorpsi) sangat memungkinkan dapat bertumbukan dengan molekul lain. 16
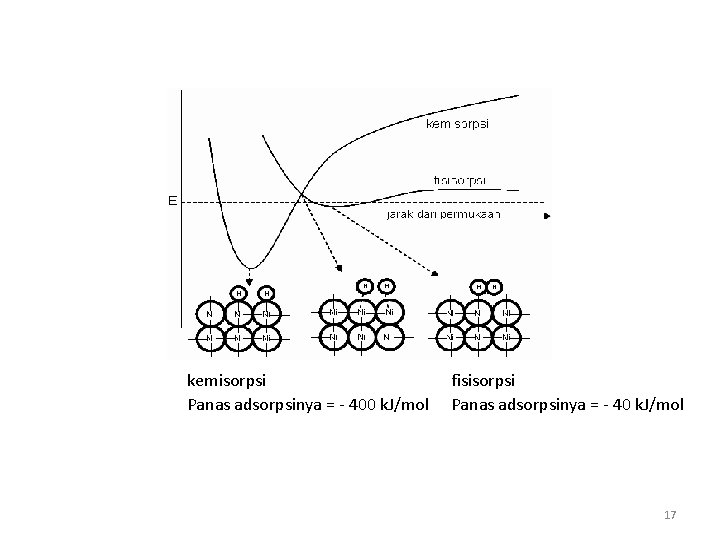
kemisorpsi Panas adsorpsinya = - 400 k. J/mol fisisorpsi Panas adsorpsinya = - 40 k. J/mol 17

Terima kasih atas perhatian anda 18
- Slides: 18