Teoria dos Orbitais Moleculares TOM TOM Importncia v

Teoria dos Orbitais Moleculares (TOM)

TOM - Importância v Elucidar alguns aspectos da ligação não explicados pelas estruturas de Lewis, pela teoria da RPENV e pela hibridização. v Exemplos: v Por que o O 2 interage com um campo magnético?

Teoria dos Orbitais Moleculares (TOM) v Nas moléculas, os elétrons encontram-se nos orbitais moleculares assim como nos átomos, os elétrons são encontrados nos orbitais atômicos. v Orbitais atômicos na molécula se combinam e se “espalham” por vários átomos ou até mesmo por toda a molécula. v “O número total de orbitais moleculares é sempre igual ao número de orbitais atômicos que os compõem”. v Os cálculos da mecânica quântica para a combinação dos OAs originais consistem em: 1) uma adição das funções de onda do AO; 2) uma subtração das funções de onda do AO. 3

Orbitais moleculares (OM) Características v Podem ser construídos como uma combinação linear de OA (CLOA); v Energias definidas; v Princípio de exclusão de Pauli: cada OM pode ser ocupado por até dois elétrons. v Se dois elétrons estão presentes, então seus spins devem estar emparelhados (↑↓). v Quando dois OA equivalentes se combinam (Ex: 1 s + 1 s), eles sempre produzem um orbital ligante e um antiligante. 4
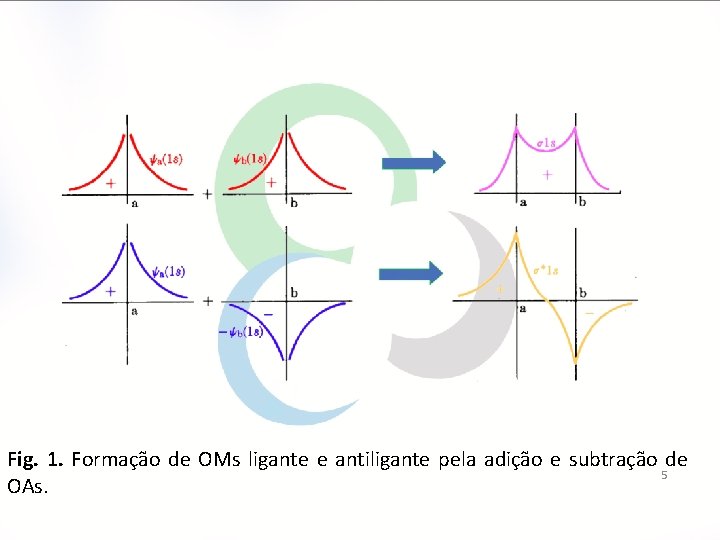
Fig. 1. Formação de OMs ligante e antiligante pela adição e subtração de 5 OAs.
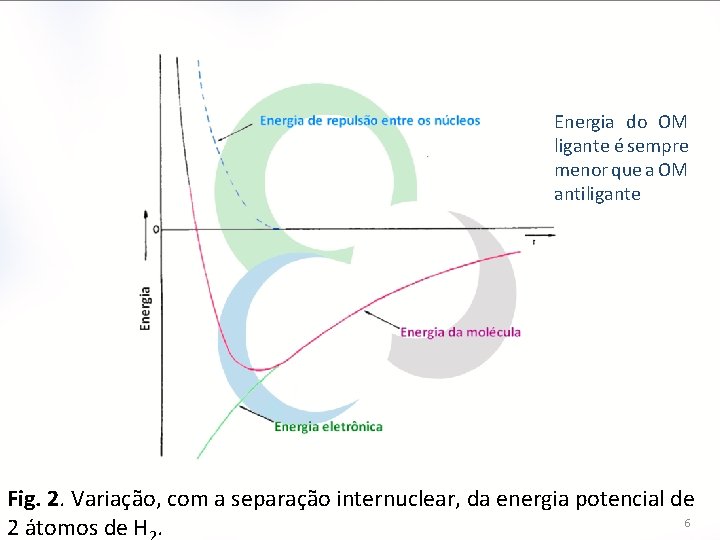
Energia do OM ligante é sempre menor que a OM antiligante Fig. 2. Variação, com a separação internuclear, da energia potencial de 6 2 átomos de H.
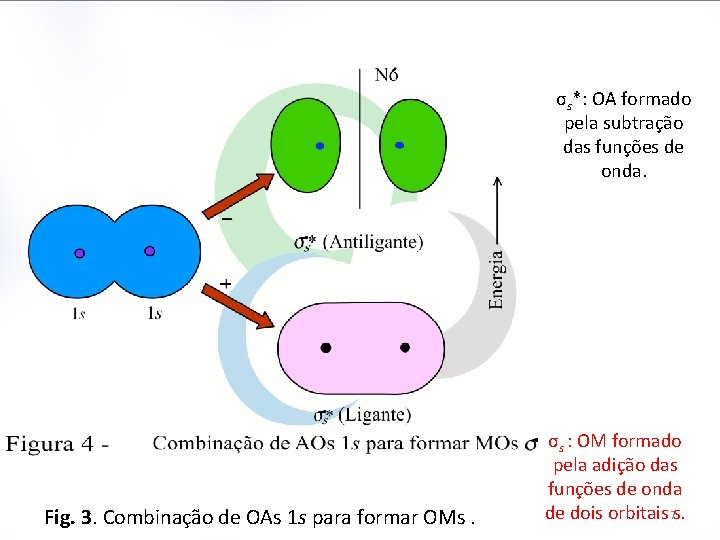
σs*: OA formado pela subtração das funções de onda. Fig. 3. Combinação de OAs 1 s para formar OMs. σs : OM formado pela adição das funções de onda de dois orbitais 7 s.
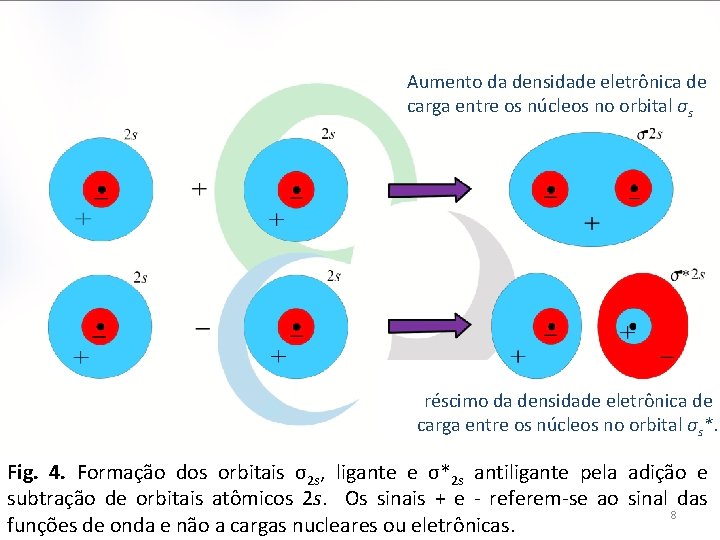
Aumento da densidade eletrônica de carga entre os núcleos no orbital σs réscimo da densidade eletrônica de carga entre os núcleos no orbital σs*. Fig. 4. Formação dos orbitais σ2 s, ligante e σ*2 s antiligante pela adição e subtração de orbitais atômicos 2 s. Os sinais + e - referem-se ao sinal das 8 funções de onda e não a cargas nucleares ou eletrônicas.
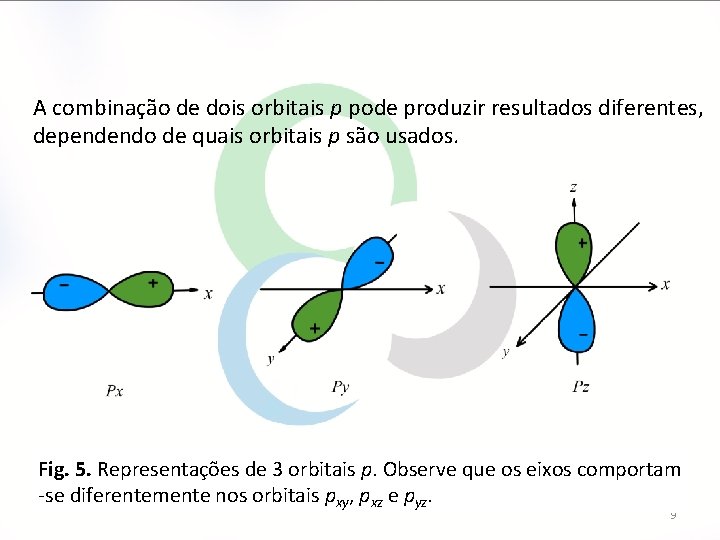
A combinação de dois orbitais p pode produzir resultados diferentes, dependendo de quais orbitais p são usados. Fig. 5. Representações de 3 orbitais p. Observe que os eixos comportam -se diferentemente nos orbitais pxy, pxz e pyz. 9
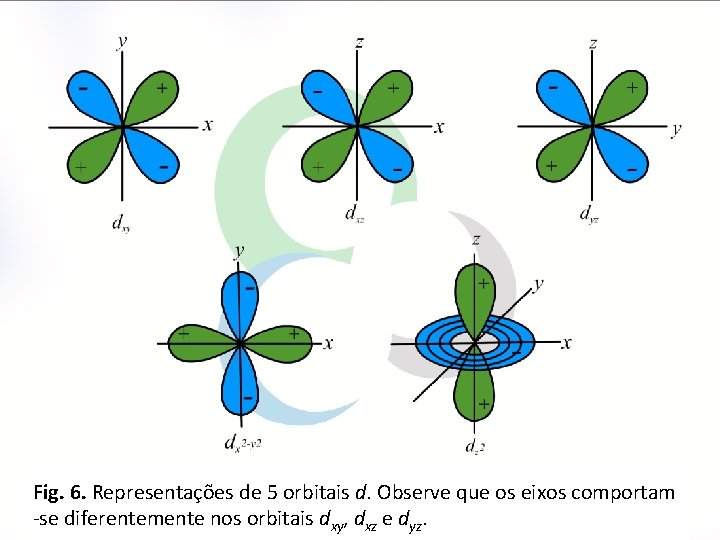
Fig. 6. Representações de 5 orbitais d. Observe que os eixos comportam 10 -se diferentemente nos orbitais dxy, dxz e dyz.
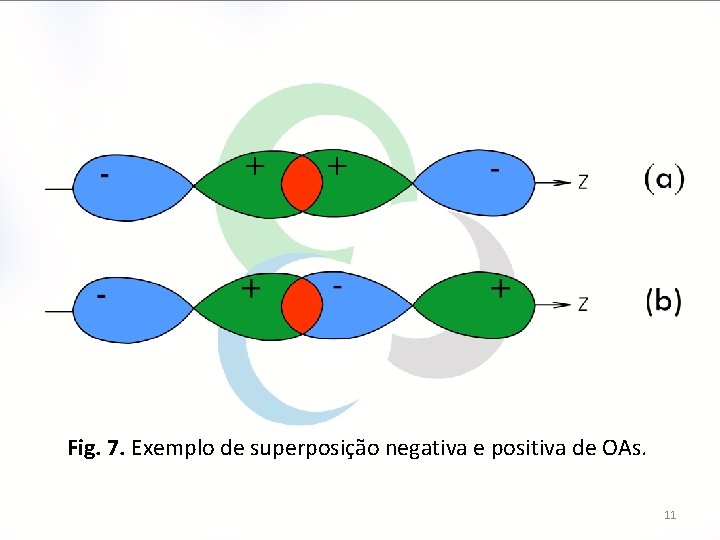
Fig. 7. Exemplo de superposição negativa e positiva de OAs. 11
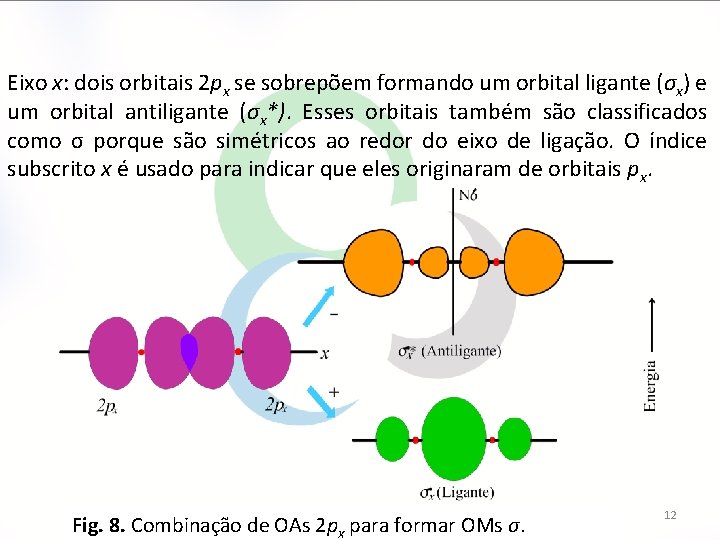
Eixo x: dois orbitais 2 px se sobrepõem formando um orbital ligante (σx) e um orbital antiligante (σx*). Esses orbitais também são classificados como σ porque são simétricos ao redor do eixo de ligação. O índice subscrito x é usado para indicar que eles originaram de orbitais px. Fig. 8. Combinação de OAs 2 px para formar OMs σ. 12
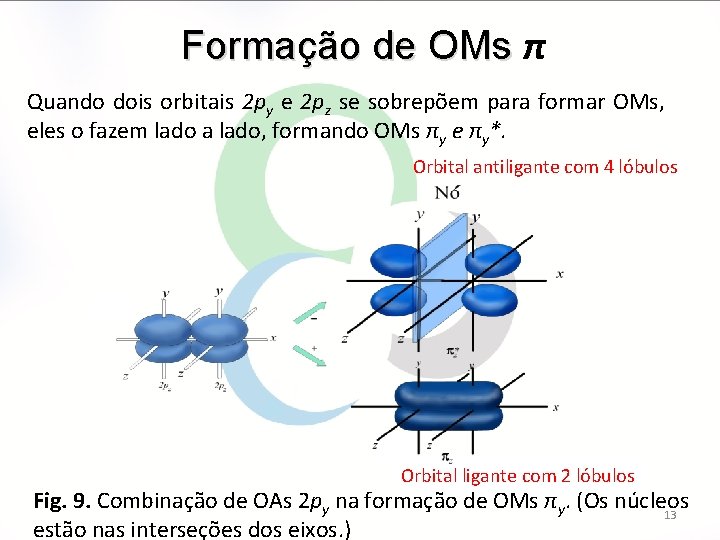
Formação de OMs π Quando dois orbitais 2 py e 2 pz se sobrepõem para formar OMs, eles o fazem lado a lado, formando OMs πy e πy*. Orbital antiligante com 4 lóbulos Orbital ligante com 2 lóbulos Fig. 9. Combinação de OAs 2 py na formação de OMs πy. (Os núcleos 13 estão nas interseções dos eixos. )
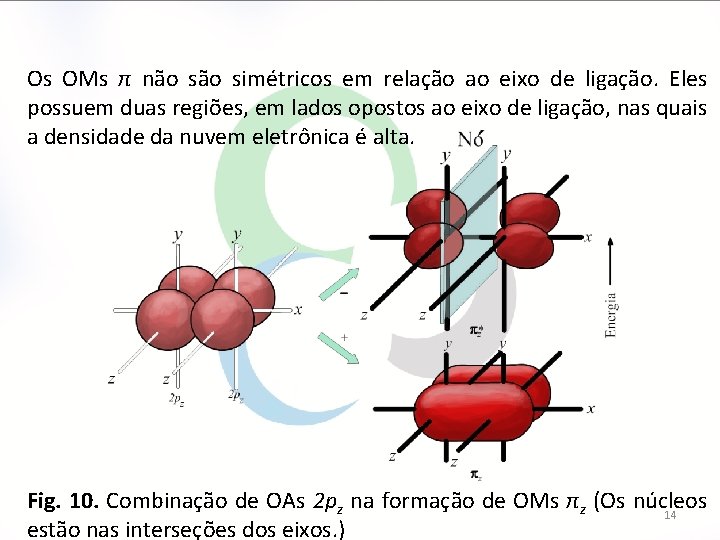
Os OMs π não simétricos em relação ao eixo de ligação. Eles possuem duas regiões, em lados opostos ao eixo de ligação, nas quais a densidade da nuvem eletrônica é alta. Fig. 10. Combinação de OAs 2 pz na formação de OMs πz (Os núcleos 14 estão nas interseções dos eixos. )
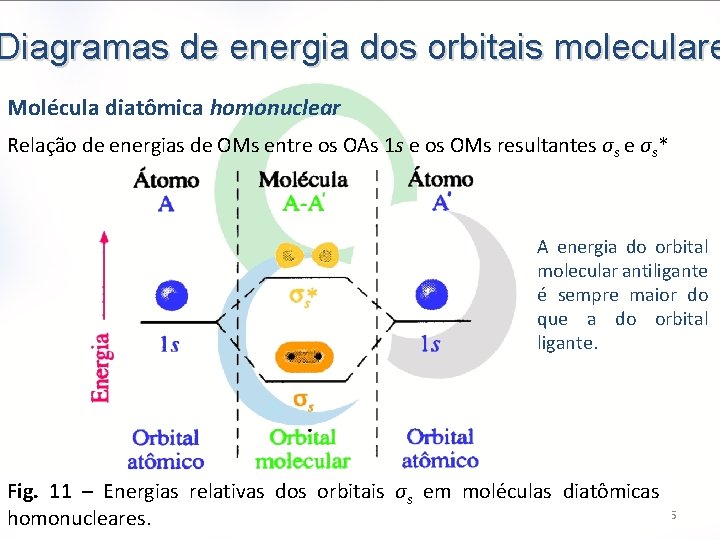
Diagramas de energia dos orbitais moleculare Molécula diatômica homonuclear Relação de energias de OMs entre os OAs 1 s e os OMs resultantes σs e σs* A energia do orbital molecular antiligante é sempre maior do que a do orbital ligante. Fig. 11 – Energias relativas dos orbitais σs em moléculas diatômicas 15 homonucleares.
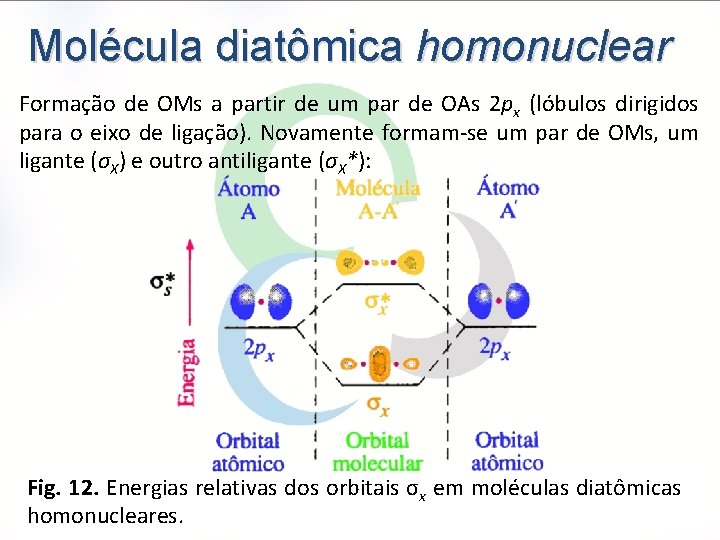
Molécula diatômica homonuclear Formação de OMs a partir de um par de OAs 2 px (lóbulos dirigidos para o eixo de ligação). Novamente formam-se um par de OMs, um ligante (σX) e outro antiligante (σX*): Fig. 12. Energias relativas dos orbitais σx em moléculas diatômicas homonucleares.
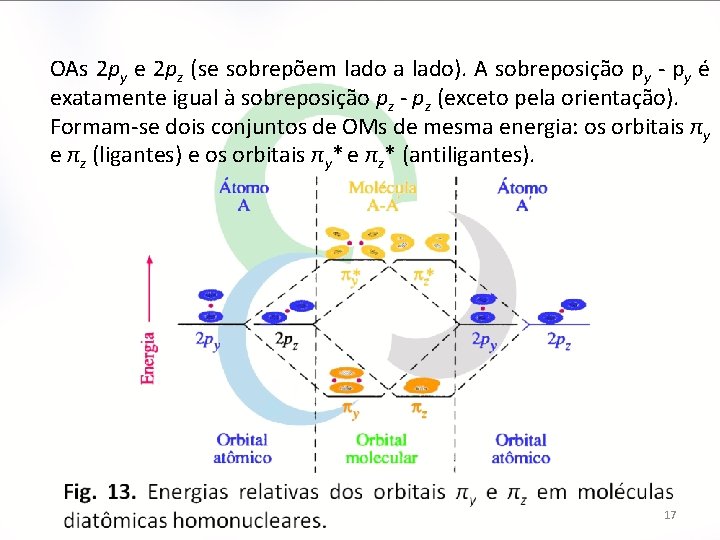
OAs 2 py e 2 pz (se sobrepõem lado a lado). A sobreposição py - py é exatamente igual à sobreposição pz - pz (exceto pela orientação). Formam-se dois conjuntos de OMs de mesma energia: os orbitais πy e πz (ligantes) e os orbitais πy* e πz* (antiligantes). 17

Preenchimento dos orbitais mole v Na distribuição eletrônica, os elétrons são adicionados a partir da base do diagrama para cima, para os orbitais de maior energia. v A molécula mais simples é a de H 2. v Os dois elétrons 1 s vão constituir um par (de spins opostos) no orbital σs (ligante) da molécula. Este par constitui uma ligação simples. A configuração eletrônica da molécula de hidrogênio pode ser escrita como (σs)2. 18
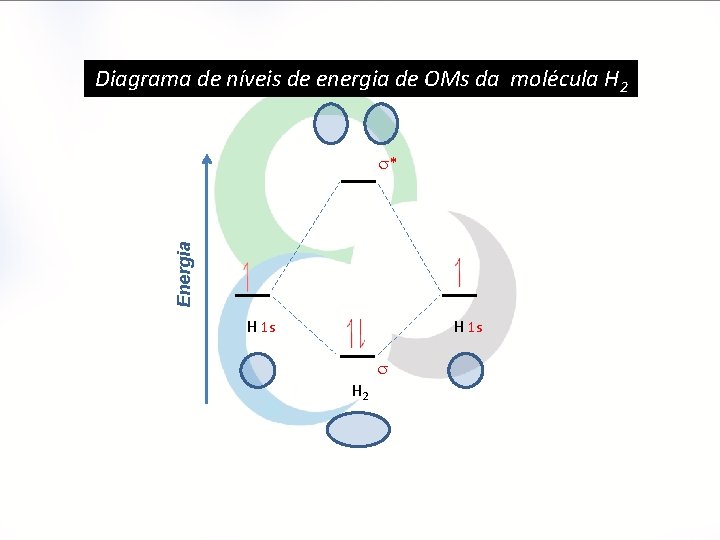
Diagrama de níveis de energia de OMs da molécula H 2 Energia * H 1 s H 2 Fig. 14. Diagrama de níveis de energia de OMs da molécula de H 2.
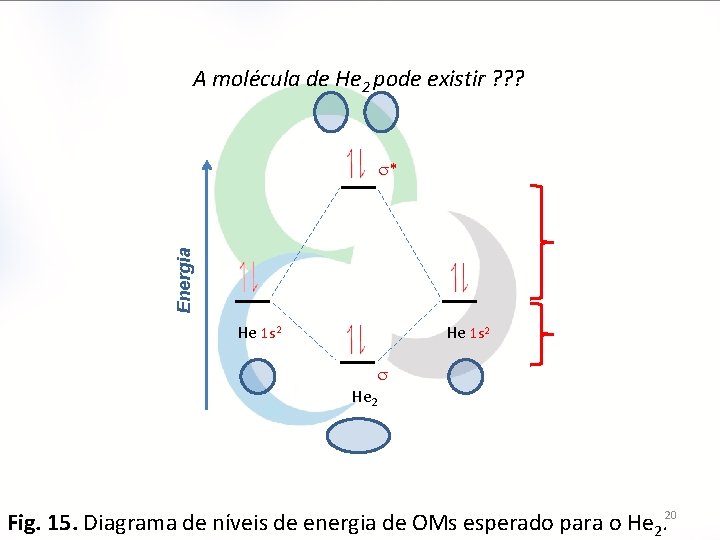
A molécula de He 2 pode existir ? ? ? Energia * He 1 s 2 He 2 Fig. 15. Diagrama de níveis de energia de OMs esperado para o He 2. 20

A molécula de He 2 pode existir ? Resposta: v A configuração eletrônica no estado fundamental na molécula de He 2 deveria ser (σs)2 (σs*)2. v Devido ao fato de que σs* (antiligante) está agora preenchido e seu efeito desestabilizador cancela o efeito estabilizador do orbital σs, não há força de atração entre os átomos de hélio devido ao número igual de elétrons ligantes e antiligantes e, assim, a molécula de He 2 não existe. 21
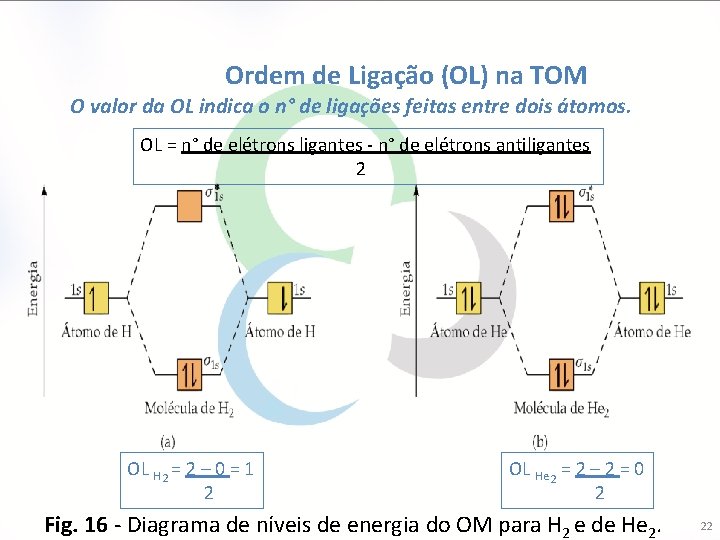
Ordem de Ligação (OL) na TOM O valor da OL indica o n° de ligações feitas entre dois átomos. OL = n° de elétrons ligantes - n° de elétrons antiligantes 2 OL H 2 = 2 – 0 = 1 2 OL He 2 = 2 – 2 = 0 2 Fig. 16 - Diagrama de níveis de energia do OM para H 2 e de He 2. 22
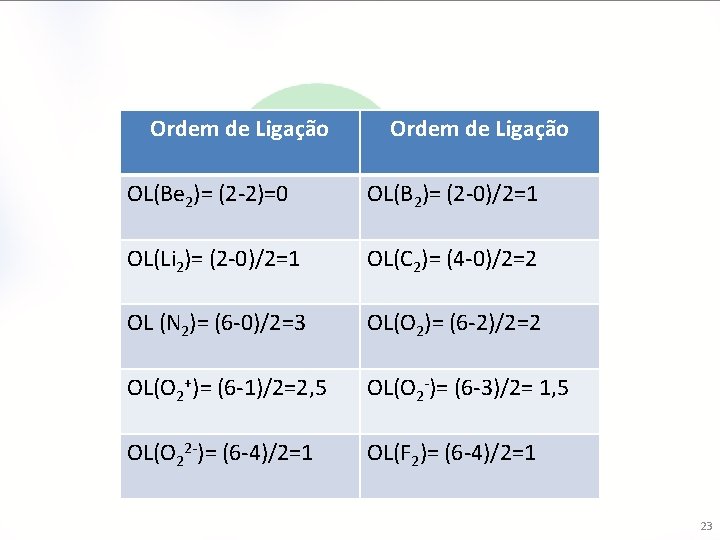
Ordem de Ligação OL(Be 2)= (2 -2)=0 OL(B 2)= (2 -0)/2=1 OL(Li 2)= (2 -0)/2=1 OL(C 2)= (4 -0)/2=2 OL (N 2)= (6 -0)/2=3 OL(O 2)= (6 -2)/2=2 OL(O 2+)= (6 -1)/2=2, 5 OL(O 2 -)= (6 -3)/2= 1, 5 OL(O 22 -)= (6 -4)/2=1 OL(F 2)= (6 -4)/2=1 23

Moléculas diatômicas do Segundo período v Moléculas diatômicas homonucleares (Li 2, Be 2, B 2, etc. ); v Após o preenchimento completo de 2 OMs s formados a partir dos orbitais 1 s, passa-se para os 2 OMs formados a partir dos orbitais 2 s. Estes são similares àqueles que já foram preenchidos. Veja outros dois exemplos: Li 2 e Be 2. 24
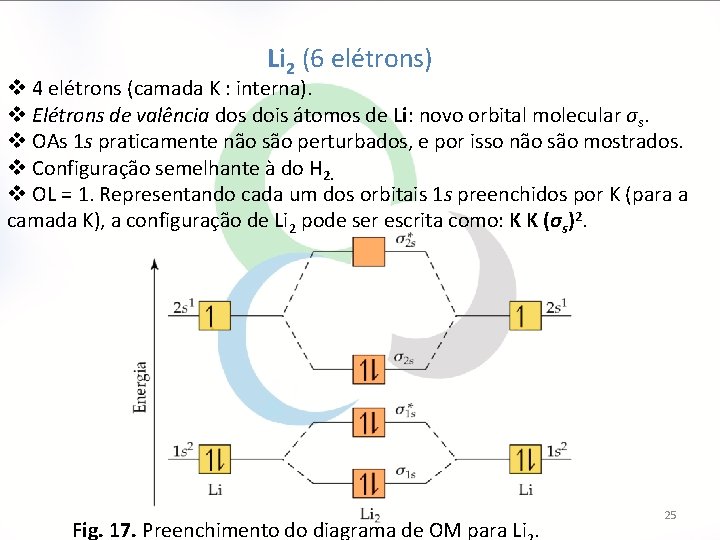
Li 2 (6 elétrons) v 4 elétrons (camada K : interna). v Elétrons de valência dos dois átomos de Li: novo orbital molecular σs. v OAs 1 s praticamente não são perturbados, e por isso não são mostrados. v Configuração semelhante à do H 2. v OL = 1. Representando cada um dos orbitais 1 s preenchidos por K (para a camada K), a configuração de Li 2 pode ser escrita como: K K (σs)2. Fig. 17. Preenchimento do diagrama de OM para Li. 25

v v 2 elétrons no 1 s; 2 elétrons no *1 s; 2 elétrons no 2 s; 2 elétrons no *2 s. Be 2 (8 elétrons) v Situação semelhante à do He 2. v O n° atômico do Be é 4 (dois destes elétrons irão preencher o orbital σs* (veja a figura do Li 2)). A desestabilização gerada pelo orbital σs* preenchido cancela o efeito de estabilização do orbital σs. v OL = zero: Be 2 não existe. Se existisse, porém, sua configuração eletrônica no estado fundamental seria K K 26 (σs)2(σs*)2.

Demais moléculas diatômicas homonucleares do segundo período. v. Sequência: B 2, C 2, N 2, O 2, F 2, Ne 2. v. OMs: orbitais σ e π (ligantes e antiligantes). Dificuldade: v. B 2 ao N 2: energia relativa dos orbitais πy e πz < σx. v. O 2 até Ne 2: energia relativa dos orbitais πy e πz > σx. v. Diferença principal: energia relativa do orbital σs comparada com as energias dos orbitais πy e πz. v Mudança na sequência de energias dos OMs entre N 2 e O 2: πy e πz têm algum caráter s. O caráter s nesses orbitais decresce à medida que a carga cresce no período. Por causa disso a energia de σs fica abaixo da energia de πy e πz no O 2. 27
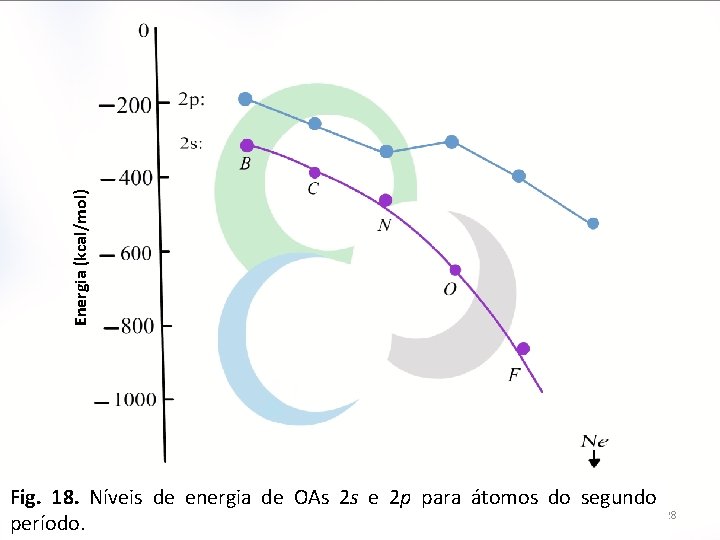
Energia (kcal/mol) Fig. 18. Níveis de energia de OAs 2 s e 2 p para átomos do segundo período. 28
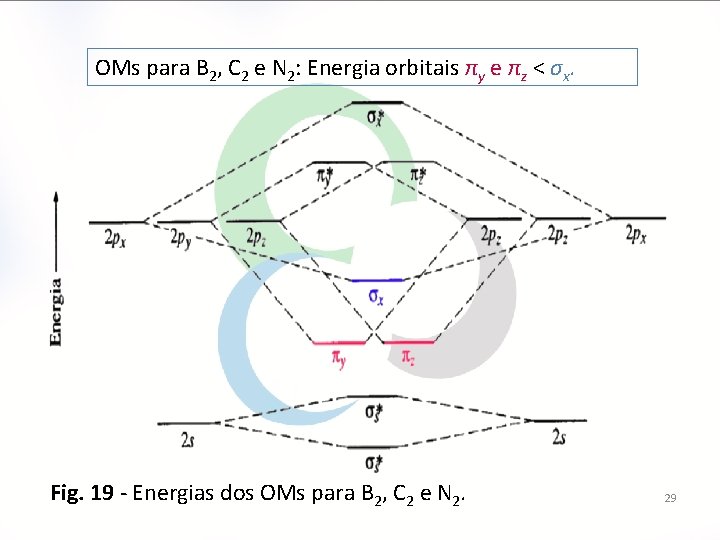
OMs para B 2, C 2 e N 2: Energia orbitais πy e πz < σx. Fig. 19 - Energias dos OMs para B 2, C 2 e N 2. 29

B 2 v 1 elétron em cada orbital πy e πz. v Os elétrons antiligantes compensam exatamente os elétrons ligantes πy e πz têm igual energia, e assim, os dois elétrons não se emparelham no mesmo orbital (menor repulsão inter-eletrônica). v Configuração eletrônica: K K (σs)2(σs*)2(πy)1(πz)1 v B 2 é paramagnético. v Como Li 2, B 2 também não é encontrado no estado sólido ou líquido. v O B elementar é encontrado como um sólido. v Sob temperaturas muito altas, pode ser detectado no estado gasoso. 30

C 2 v Adicionando-se mais dois elétrons (um para cada átomo), obtem-se a configuração para o C 2. v Esses elétrons são adicionados aos orbitais πy e πz, preenchendo-os. e, assim, v C 2 não é paramagnético (todos os elétrons estão emparelhados ). v OL = 2 (há quatro elétrons ligantes a mais na molécula). v A configuração eletrônica: K K (σs)2(σs*)2(πy)2(πz)2 v Como OL é diferente de zero, C 2 foi detectado sob altas temperaturas. 31

N 2 v Possui 6 elétrons de ligação (orbitais πy , πz e πx) que correspondem aos 6 elétrons da estrutura de Lewis. v OL = 3. v Configuração: KK(σs)2(σs*)2(πy)2(πz)2(σx)2 v Todos os elétrons estão emparelhados (N 2 não é paramagnético). v A molécula é muito estável e comum. 32
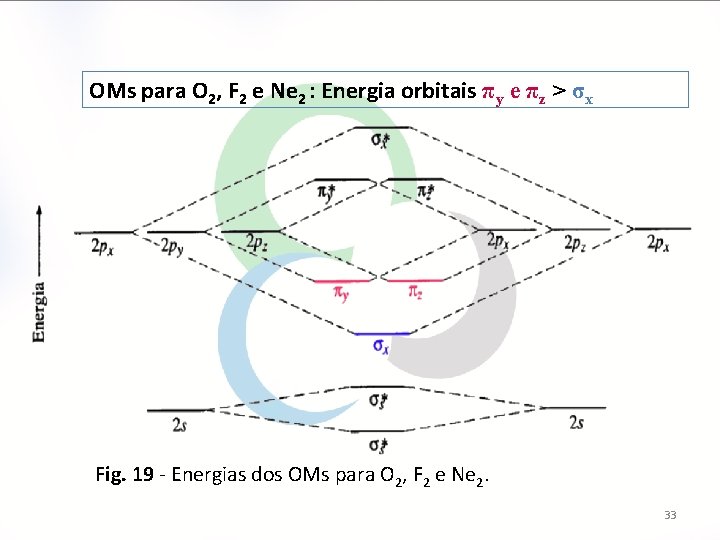
OMs para O 2, F 2 e Ne 2 : Energia orbitais πy e πz > σx Fig. 19 - Energias dos OMs para O 2, F 2 e Ne 2. 33

�A mudança na seqüência das energias OM entre N 2 e O 2 ocorre porque πy e πz, neste caso, o caráter s nesses orbitais decresce à medida que a carga cresce no período, por causa disso a energia de σx fica abaixo da energia πy e πz no O 2. 34

O 2 v A adição de mais 2 elétrons à configuração do N 2 leva ao preenchimento dos níveis do O 2. v Esses 2 elétrons devem ir para orbitais antiligantes, resultando em um decréscimo na OL (de 3, no N 2 para 2 no O 2). O valor mais baixo da ordem de ligação é consistente com o fato de o O 2 ter uma energia de ligação menor e uma distância de ligação maior que o N 2. v A configuração eletrônica é: KK(σs)2(σs*)2(σx)2(πy)2(πz)2(πy*)1(πz*)1 v É paramagnética (possui dois pares de elétrons desemparelhados). v Energia de ligação muito alta e uma distância de ligação muito curta. 35
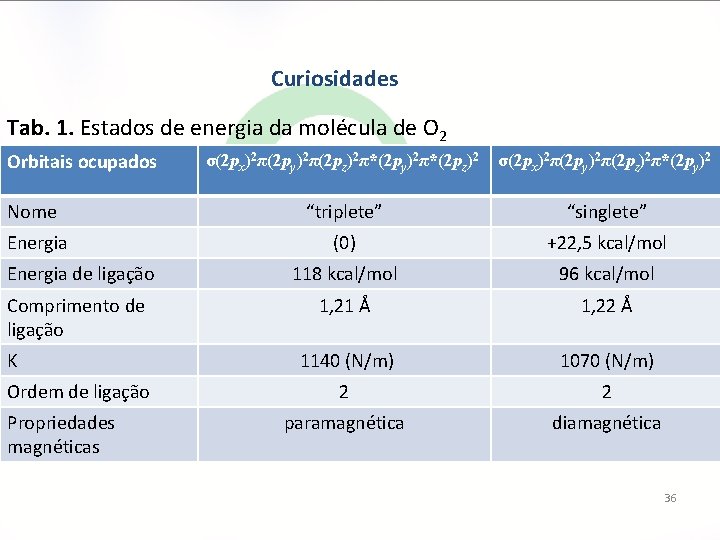
Curiosidades Tab. 1. Estados de energia da molécula de O 2 Orbitais ocupados σ(2 px)2π(2 py)2π(2 pz)2π*(2 py)2π*(2 pz)2 σ(2 px)2π(2 py)2π(2 pz)2π*(2 py)2 Nome “triplete” “singlete” Energia (0) +22, 5 kcal/mol Energia de ligação 118 kcal/mol 96 kcal/mol Comprimento de ligação 1, 21 Å 1, 22 Å 1140 (N/m) 1070 (N/m) 2 2 paramagnética diamagnética K Ordem de ligação Propriedades magnéticas 36
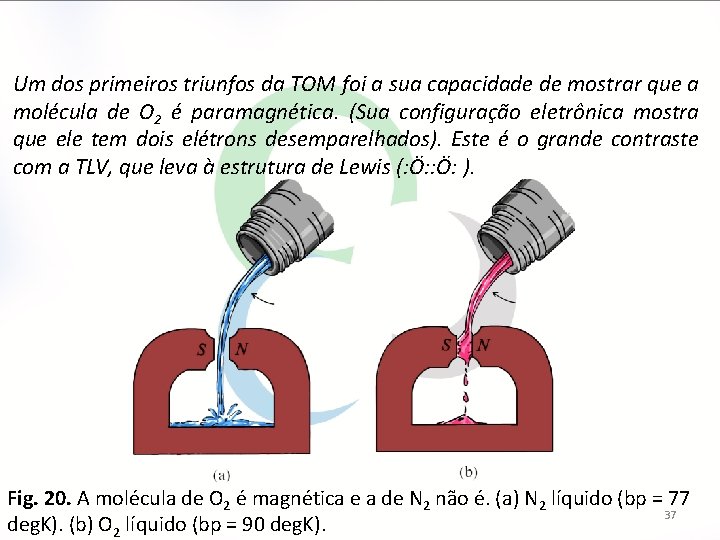
Um dos primeiros triunfos da TOM foi a sua capacidade de mostrar que a molécula de O 2 é paramagnética. (Sua configuração eletrônica mostra que ele tem dois elétrons desemparelhados). Este é o grande contraste com a TLV, que leva à estrutura de Lewis (: Ö: ). Fig. 20. A molécula de O 2 é magnética e a de N 2 não é. (a) N 2 líquido (bp = 77 37 deg. K). (b) O 2 líquido (bp = 90 deg. K).

F 2 v A adição de mais dois elétrons dá o diagrama do F 2. v Os orbitais π* estão ambos preenchidos. v OL = 1. v F 2 mostra ser diamagnético (ausência de elétrons desemparelhados). v A configuração do F 2 é: 2 KK(σs)2(σs*)2(σx)2(πy)2(πz)2(πy*)2(πz*) 38

Ne 2 v. A adição de mais dois elétrons preenche o orbital σx*. v. OL = 0. v. O estado fundamental para Ne 2 nunca foi observado. v. Se esta molécula existisse, sua configuração eletrônica seria: KK(σs)2(σs*)2(σx)2(πy)2(πz)2(πy*)2(πz*)2 (σx*)2 39
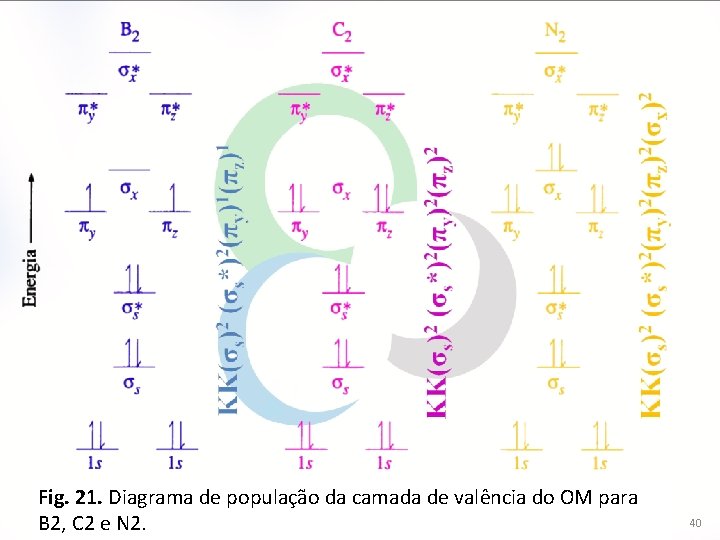
Fig. 21. Diagrama de população da camada de valência do OM para B 2, C 2 e N 2. 40
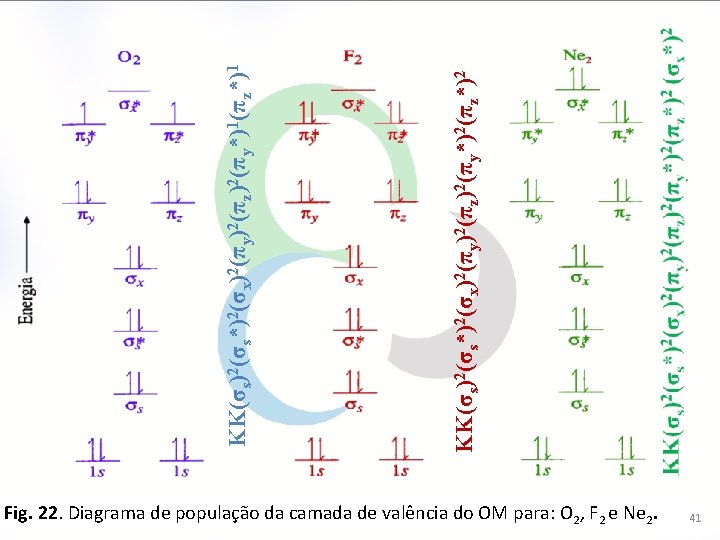
KK(σs)2(σs*)2(σx)2(πy)2(πz)2(πy*)2(πz*)2 KK(σs)2(σs*)2(σx)2(πy)2(πz)2(πy*)1(πz*)1 Fig. 22. Diagrama de população da camada de valência do OM para: O 2, F 2 e Ne 2. 41
- Slides: 41