TEORI ASAM BASA Teori Arrhenius Dasar teorinya adalah
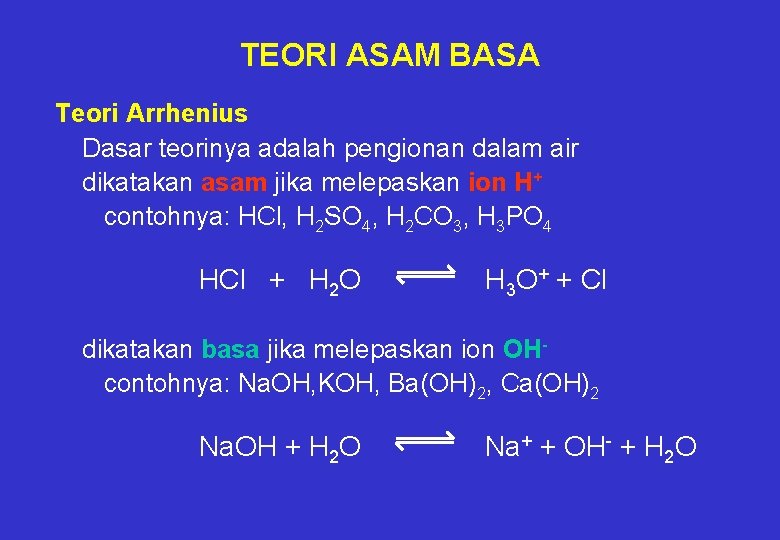
TEORI ASAM BASA Teori Arrhenius Dasar teorinya adalah pengionan dalam air dikatakan asam jika melepaskan ion H+ contohnya: HCl, H 2 SO 4, H 2 CO 3, H 3 PO 4 HCl + H 2 O H 3 O+ + Cl dikatakan basa jika melepaskan ion OHcontohnya: Na. OH, KOH, Ba(OH)2, Ca(OH)2 Na. OH + H 2 O Na+ + OH- + H 2 O
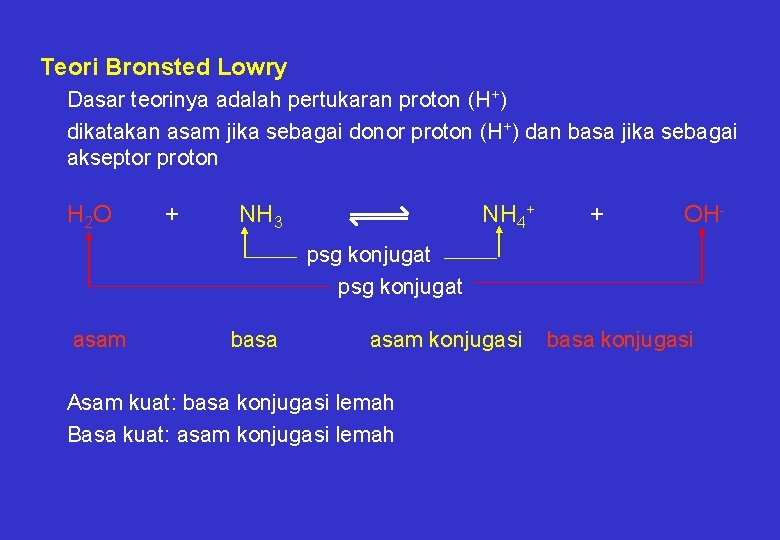
Teori Bronsted Lowry Dasar teorinya adalah pertukaran proton (H+) dikatakan asam jika sebagai donor proton (H+) dan basa jika sebagai akseptor proton H 2 O + NH 3 NH 4+ + OH- psg konjugat asam basa asam konjugasi Asam kuat: basa konjugasi lemah Basa kuat: asam konjugasi lemah basa konjugasi

Teori Lewis Dasarnya adalah pemakaian pasangan elektron bebas dikatakan asam jika menerima pasangan elektron dan basa jika memberikan pasangan elektron F. B. F asam + H. . . N H. . H basa F H. . F. B. . N. H F H senyawa koordinasi

Contoh 7. 1 Tentukanlah asam dan basa pada pasangan/reaksi: a. HCO 3 - (aq) + H 2 O (l) H 3 O+ (aq) + CO 32 - (aq) b. HCO 3 - (aq) + H 2 O (l) H 2 CO 3 (aq) + OH- (aq) Penyelesaian a. HCO 3 - sebagai asam karena melepaskan proton; H 2 O sebagai basa karena menerima proton. CO 32 - adalah basa konjugasi dari asam HCO 3 - dan H 3 O+ adalah asam konjugasi dari basa H 2 O b. HCO 3 - sebagai basa karena menerima proton; H 2 O sebagai asam karena melepaskan proton. H 2 CO 3 adalah asam konjugasi dari basa HCO 3 - dan OH- adalah basa konjugasi dari asam H 2 O

7. 3 KONSENTRASI ION H+ DAN p. H ASAM/BASA KUAT: p. H dapat ditentukan langsung dari nilai konsentrasi (M) asam dan basa tersebut p. H = - log [H+] p. OH = - log [OH-] p. H + p. OH = 14 ASAM/BASA LEMAH: Konsentrasi H+ dari asam dan OH- dari basa bergantung pada derajat ionisasi (α) dan tetapan ionisasi (Ka atau Kb) Nilai Ka menunjukkan kekuatan asam dan Kb kekuatan basa

p. H Asam/Basa lemah Reaksi HA(aq) H+(aq) + A-(aq) Awal Ca - Mengion -α. Ca Setimbang Ca – Ca. α α. Ca Ka = [H+] [A-] [HA] = [Ca. α]2 [Ca – Ca. α] = - C a. α 2 (1 – α) Bila nilai α sangat kecil maka Ca (1 - α) Ca sehingga: Ka = [H+]2/ Ca ; [H+] = Ka. Ca Analog untuk basa lemah: [OH-] = Kb. Cb

Contoh 7. 4 Hitunglah p. H larutan a. HCl 0, 1 M b. Na. OH 0, 1 M c. HCN 0, 1 M (Ka=4, 9 x 10 -10)d. C 6 H 5 COOH (Ka=6, 5 x 10 -5) e. NH 4 OH (Kb=1, 8 x 10 -5) Penyelesaian a. [H+] = [HCl] = 0, 1 M; p. H = -log [0, 1] = 1 b. [OH-] = [Na. OH] = 0, 1 M; p. H = 14 – p. OH = 14 – [-log 0, 1] = 13 c. [H+] = Ka. Ca = (4, 9 x 10 -10) x 0, 1 p. H = - log 7 x 10 -6 = 5, 16 = 7 x 10 -6 M d. [H+] = Ka. Ca = (6, 5 x 10 -5) x 0, 1 p. H = - log 2, 55 x 10 -3 = 2, 60 = 2, 55 x 10 -3 M e. [OH-] = Kb. Cb = (1, 8 x 10 -5) x 0, 1 = 1, 34 x 10 -3 M p. H = 14 – p. OH = 14 – (-log 1, 34 x 10 -3) = 11, 10

7. 4 INDIKATOR ASAM-BASA (INDIKATOR p. H) • Adalah zat (suatu asam atau basa lemah) yang akan berubah warna jika p. H berubah pada kisaran tertentu • Kisaran p. H yang menyebabkan indikator berubah warna disebut trayek p. H. • Bila p. H < trayek p. H maka indikator akan menunjukkan warna asamnya • Bila p. H > trayek p. H maka indikator akan menunjukkan warna basa • Contoh indikator: biru bromtimol (p. H 6, 0 – 7, 6), merah metil (3, 2 – 4, 4), kuning alizarin (10, 1 – 12, 0)

Beberapa indikator asam-basa yang penting: Nama Jenis Trayek p. H Jingga metil Merah metil Lakmus Biru bromtimol Fenolftalein b b 3. 1 -4. 4 4. 2 -6. 3 4. 5 -8. 3 6. 0 -7. 6 8. 0 -9. 6 a a Warna asam basa merah jingga merah kuning merah biru kuning biru Tak Merah berwarna muda

Contoh 7. 8 Suatu larutan ketika diberi indikator hijau bromkresol (trayek p. H 3, 8 – 5, 4; warna asam kuning dan warna basa biru) menunjukkan warna tepat hijau, a. Berapa kira-kira p. H larutan tersebut, b. Bila indikator merah metil (trayek p. H 3, 2 – 4, 4; warna asam merah dan warna basa kuning) dimasukkan ke dalam larutan tersebut, bagaimana warna larutannya? Penyelesaian a. Warna tepat hijau merupakan campuran dari warna kuning dan biru sehingga p. H larutan merupakan nilai tengah trayek p. H yaitu 4, 6 b. p. H 4, 6 > trayek p. H indikator merah metil, maka larutan akan berwarna merah

- Slides: 11