TEORI ASAM BASA Secara Umum Cairan berasa asam

TEORI ASAM BASA Secara Umum : Cairan berasa asam dan dapat Asam : memerahkan kertas lakmus biru Basa : Garam : Cairan berasa pahit dan dapat membirukan kertas lakmus merah Cairan yang berasa asin
TEORI ASAM BASA Teori Arrhenius : Asam adalah senyawa yang melepaskan H+ dalam air. Contoh : HCl ----- H+ + Cl. HNO 3 ----- H+ + NO 3 Basa adalah senyawa yang melepaskan OH- dalam air Contoh : Na. OH ----- Na+ + OHNH 4 OH ----- NH 4+ + OHKelemahan : hanya berlaku untuk larutan dalam air saja.
TEORI ASAM BASA Teori Bronsted - Lowry Asam : senyawa yg dapat memberikan CONTOH : proton ( H+ ) / donor proton. Basa: senyawa yg dapat menerima proton (H+) / akseptor proton. Reaksi tanpa Pelarut Air HCl(g) + NH 3(g) NH 4+ + Cl- NH 4 Cl(s) Asam Basa Reaksi dengan Pelarut Air HCl(g) + H 2 O(aq) H 3 O+(aq) + Cl-(aq) Asam Basa NH 4 OH(g) + H 2 O(aq) NH 4 OH 2+(aq) + OH-(aq) Basa Asam Air dapat bersifat asam atau basa Amfoter

TEORI ASAM BASA Pasangan Asam Basa Konjugasi HCl + H 2 O Asam 1 Basa 1 H 3 O+ + Cl- Asam 2 Basa 2 Konjugasi Pasangan asam basa konjugasi : pasangan asam 1 – basa 2 dan basa 1 – asam 2 HCl – Cl- dan H 2 O – H 3 O+ Asam konjugasi : Asam yg terbentuk dari basa yang menerima Proton H 3 O+ Basa konjugasi : Basa yg terbentuk dari asam yang melepaskan Proton Cl-

TEORI ASAM BASA Jelaskan untuk reaksi : NH 3 + H 2 O NH 4+ + OH- a. Pasangan asam basa konjugasi b. Asam konjugasi c. Basa konjugasi
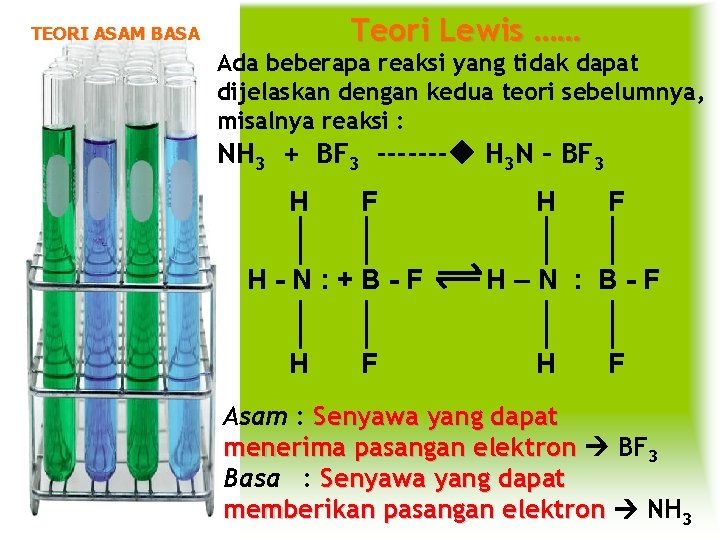
Teori Lewis …… TEORI ASAM BASA Ada beberapa reaksi yang tidak dapat dijelaskan dengan kedua teori sebelumnya, misalnya reaksi : NH 3 + BF 3 ------- H 3 N – BF 3 H F H-N: +B-F H F H–N : B-F H F Asam : Senyawa yang dapat menerima pasangan elektron BF 3 Basa : Senyawa yang dapat memberikan pasangan elektron NH 3
![KESETIMBANGAN ASAM DAN BASA Kesetimbangan Asam Monoprotik : H+ + A - HA [H+] KESETIMBANGAN ASAM DAN BASA Kesetimbangan Asam Monoprotik : H+ + A - HA [H+]](http://slidetodoc.com/presentation_image_h/d8178816a6704eed39e4f412815d7c65/image-7.jpg)
KESETIMBANGAN ASAM DAN BASA Kesetimbangan Asam Monoprotik : H+ + A - HA [H+] [A-] Ka = [HA] Asam diprotik : H 2 A Ka = Konstanta kesetimbangan asam H+ + A [H+] [A-] Ka = [H 2 A]
![KESETIMBANGAN ASAM DAN BASA HA- H+ + A 2[H+] [A 2 -] Ka 2 KESETIMBANGAN ASAM DAN BASA HA- H+ + A 2[H+] [A 2 -] Ka 2](http://slidetodoc.com/presentation_image_h/d8178816a6704eed39e4f412815d7c65/image-8.jpg)
KESETIMBANGAN ASAM DAN BASA HA- H+ + A 2[H+] [A 2 -] Ka 2 = Ka 1 x Ka 2 = ? ? ? [HA-] Konstanta kesetimbangan Asam pada 250 C Nama Rumus Ka Asam Klorida Asam Nitrat Asam Sulfat HCl HNO 3 H 2 SO 4 Asam Florida Asam Nitrit Asam Sulfita HF HNO 2 H 2 S 1, 0 x 107 sifat asam 1, 0 x 109 (Ka 1) 1, 2 x 10 -2 (Ka 2) 6, 6 x 10 -4 5, 1 x 10 -4 1, 1 x 10 -7 (Ka 1) 1, 0 x 10 -14 (Ka 2) Nilai Ka : Ka > 10 : Asam kuat Ka < 10 : Asam lemah
![Kesetimbangan Basa KESETIMBANGAN ASAM DAN BASA Basa Monohidroksi : B+ + OH- BOH [B+] Kesetimbangan Basa KESETIMBANGAN ASAM DAN BASA Basa Monohidroksi : B+ + OH- BOH [B+]](http://slidetodoc.com/presentation_image_h/d8178816a6704eed39e4f412815d7c65/image-9.jpg)
Kesetimbangan Basa KESETIMBANGAN ASAM DAN BASA Basa Monohidroksi : B+ + OH- BOH [B+] [OH-] Kb = Konstanta kesetimbangan basa Kb = [BOH] Basa dihidroksi : B(OH)2 B 2+ + 2(OH)[B 2+] [OH-]2 Kb = B[OH]2

KESETIMBANGAN ASAM DAN BASA TUGAS Carilah 20 jenis asam dan basa, beserta rumus molekul dan nilai konstanta kesetimbangannya, serta klasifikasikan berdasarkan kekuatan sifat asamnya.
- Slides: 10