Teora Atmica Teora Atmica Constitucin de la materia










- Slides: 16

Teoría Atómica

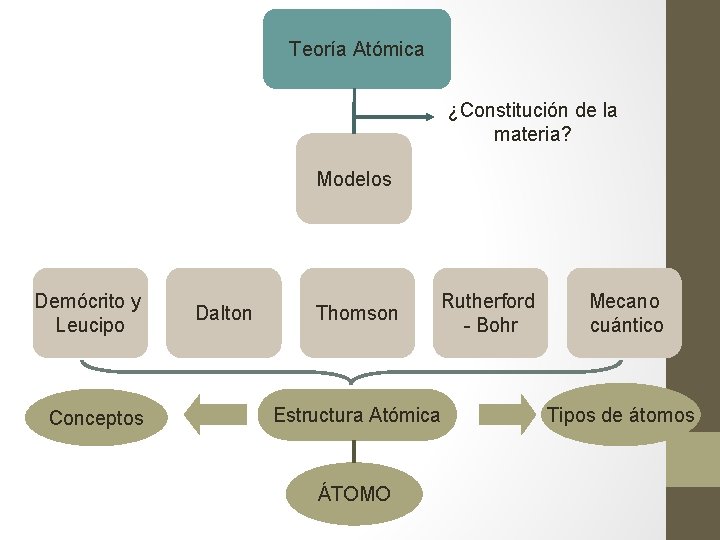
Teoría Atómica ¿Constitución de la materia? Modelos Demócrito y Leucipo Conceptos Dalton Thomson Rutherford - Bohr Estructura Atómica ÁTOMO Mecano cuántico Tipos de átomos

Demócrito y Leucipo • A través de un pensamiento filosófico, 450 AC en la Grecia antigua, fundan la escuela atomista. • Ellos sugirieron que, al dividir cualquier sustancias, se debería llegar a la unidad mínima constituyente e indivisible, el ”ÁTOMO” (del griego a= sin y tomo= división), común para toda la materia. Éste fue el primer modelo atómico propuesto. • Reconocía cuatro clases diferentes de átomos –los de piedra, los de agua , del aire y del fuego- y creía que toda la diversidad de las materias resultaba de las diferentes combinaciones de estos 4 elementos.

Modelo atómico de Dalton • Representa al átomo como un esfera compacta indivisible e indestructible.

Modelo atómico de Thomson • Átomo esfera homogénea de electricidad positiva. Los electrones partículas cargadas negativamente incrustados en ella. • Su modelo atómico es ¨estático¨ y se asemeja a un budín con pasas. Átomo estacionario

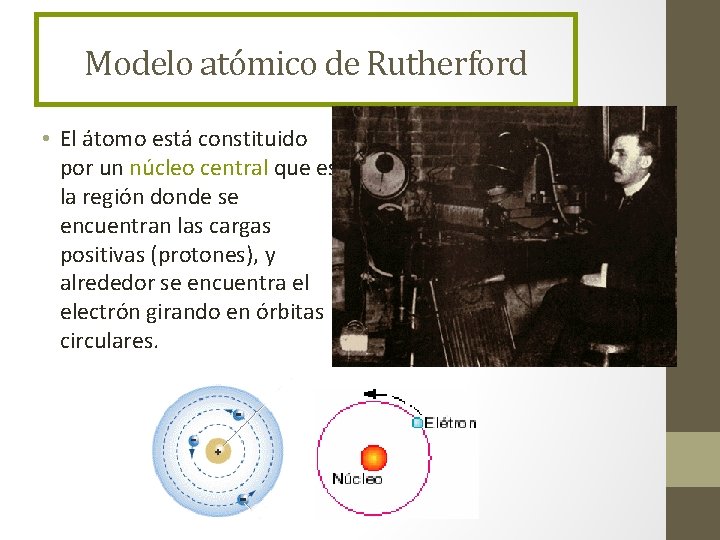
Modelo atómico de Rutherford • El átomo está constituido por un núcleo central que es la región donde se encuentran las cargas positivas (protones), y alrededor se encuentra el electrón girando en órbitas circulares.

Modelo atómico de Bohr • En 1913 Niels Bohr discípulo de Rutherford propone un nuevo modelo para el átomo de aplicando acertadamente la Teoría Cuántica de la radiación de Planck. • El modelo de Bohr recuerda al modelo planetario de Copérnico. El electrón de un átomo o ión hidrogeno que describe órbitas circulares, pero los radios de estas órbitas no pueden tener cualquier valor.

Modelo atómico de Sommerffeld • Generalizó el modelo de Bohr añadiendo a órbitas elípticas además de las circulares. • Existen ¨subniveles¨ que corresponden al mismo nivel energético.

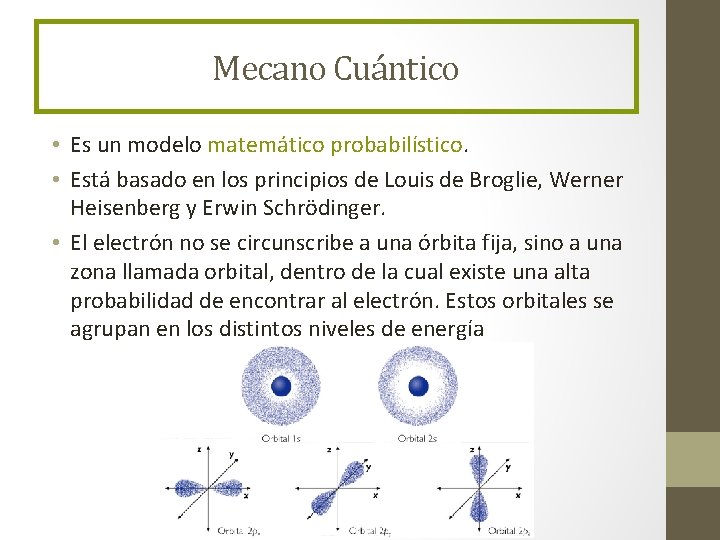
Mecano Cuántico • Es un modelo matemático probabilístico. • Está basado en los principios de Louis de Broglie, Werner Heisenberg y Erwin Schrödinger. • El electrón no se circunscribe a una órbita fija, sino a una zona llamada orbital, dentro de la cual existe una alta probabilidad de encontrar al electrón. Estos orbitales se agrupan en los distintos niveles de energía

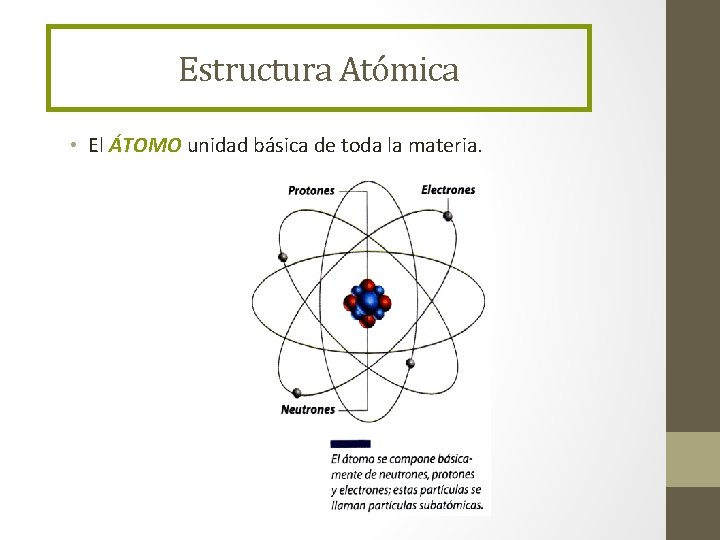
Estructura Atómica • El ÁTOMO unidad básica de toda la materia.

Partículas subatómicas Partícula Carga Protón (p+) Neutrón (n) Electrón (e-) 0 Masa

ACTIVIDAD EXPERIMENTAL 1 ACTIVIDAD 1 Frote el globo en su cabello. Frote el nylon en su cabello. Acerque ambos objetos. ACTIVIDAD 2 Frote el globo en su cabello. Intente mover la lata “acostada” sin tocarla sobre la mesa, acercando el globo a ella. ACTIVIDAD 3 Frote el globo en su cabello. Acerque el globo a pequeños trozos de papel. ¿Al acercar ambos objetos qué sucedió? ¿A qué se debe que se comporten así? ¿Cómo le llamarías a este fenómeno?

La secuencia triboeléctrica es una lista de materiales dispuestos en un orden determinado. Frotando dos materiales de la secuencia, el que esté en la posición más alta se cargará positivamente, mientras que el que se sitúe más abajo se carga negativamente.

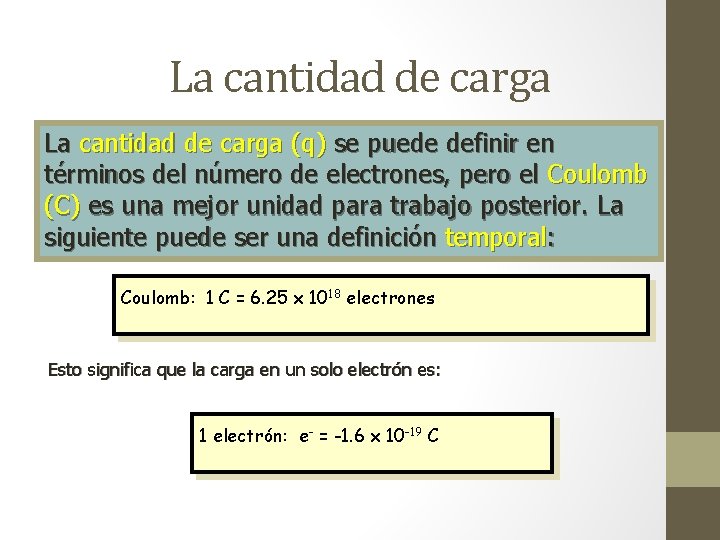
La cantidad de carga (q) se puede definir en términos del número de electrones, pero el Coulomb (C) es una mejor unidad para trabajo posterior. La siguiente puede ser una definición temporal: Coulomb: 1 C = 6. 25 x 1018 electrones Esto significa que la carga en un solo electrón es: 1 electrón: e- = -1. 6 x 10 -19 C

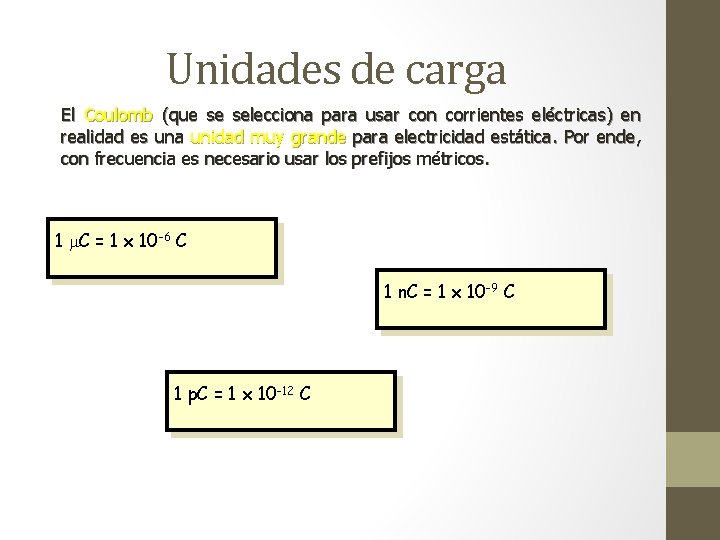
Unidades de carga El Coulomb (que se selecciona para usar con corrientes eléctricas) en realidad es una unidad muy grande para electricidad estática. Por ende, con frecuencia es necesario usar los prefijos métricos. 1 m. C = 1 x 10 -6 C 1 n. C = 1 x 10 -9 C 1 p. C = 1 x 10 -12 C

Ejemplo Si 16 millones de electrones se remueven de una esfera neutral, ¿cuál es la carga en coulombs sobre la esfera? 1 electrón: e- = -1. 6 x 10 -19 C + + + +