TEMA ACIDEZ Y BASICIDAD CARACTERISTICAS DE LOS ACIDOS

TEMA ACIDEZ Y BASICIDAD

CARACTERISTICAS DE LOS ACIDOS • 1. - Poseer un sabor agrio • 2. - Cambian el papel tornasol azul a rojo • 3. - Reacciona con los metales activos, desprendiendo hidrogeno • 4. -Neutralizan las bases formando sal y agua • 5. - Intervienen en el metabolismo de las proteínas y de otras sustancias biológicas

• 6. -Al tacto quema la piel, se irrita • 7. -Son corrosivas por lo que disuelven muchas sustancias • 8. -Forma soluciones electrolíticas • 9. -Tienen PH bajo (menor de siete) • 10. -Se enturbia con la fenolftaleina • 11. -Cambia a rojo al anaranjado de metilo • 12. -En su formula el símbolo H se escribe a la izquierda • 13. -Ceden protones o dejan en libertad iones de hidrógeno ( H )

CARACTERISTICAS DE LAS BASES • • 1. -Poseer sabor amargo 2. -Cambian el papel tornasol rojo a azul 3. -Reaccionan con las sales de amonio 4. -Neutralizan los ácidos formando sal y agua • 5. -Intervienen en el metabolismo de las proteínas y de otras sustancias biológicas • 6. -Al tacto se sienten jabonosas

• 7. -Disuelven aceites y grasas, formando jabones • 8. -Forman soluciones electrolíticas • 9. -Tienen PH alto ( mayor de siete ) • 10. -Cambia a rojo la fenolftaleina • 11. -Cambia a amarillo el anaranjado de metilo • 12. -En su fórmula el radical OH se escribe a la derecha • 13. -Ceden protones o dejan en libertad iones hidróxido
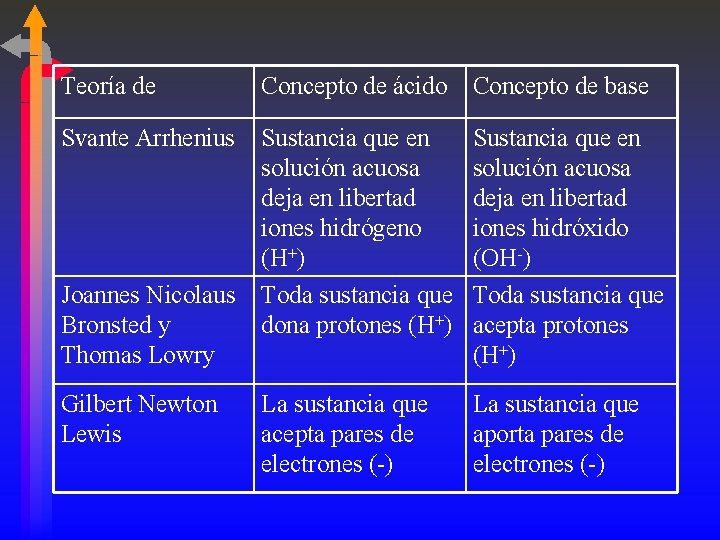
Teoría de Concepto de ácido Concepto de base Svante Arrhenius Sustancia que en solución acuosa deja en libertad iones hidrógeno (H+) Toda sustancia que dona protones (H+) Sustancia que en solución acuosa deja en libertad iones hidróxido (OH-) Toda sustancia que acepta protones (H+) La sustancia que acepta pares de electrones (-) La sustancia que aporta pares de electrones (-) Joannes Nicolaus Bronsted y Thomas Lowry Gilbert Newton Lewis

FUERZA DE LOS ACIDOS Y LAS BASES • Una de las formas en la que se clasifican las sustancias es en ácidas, básicas y neutras • Las bases también reciben el nombre de hidróxidos o alcali • Los ácidos y las bases se clasifican en fuertes y débiles

• Los ácidos y las bases fuertes; son los que se disocian completamente. • Los ácidos y las bases débiles ; son los que se disocian parcialmente. • EJEMPLOS

Ácido fuertes Ácidos débiles HCIO 4 ácido perclórico H 2 CO 3 ácido carbónico H 2 SO 4 ácido sulfúrico H 2 S ácido sulfhídrico HCI ácido clorhídrico CH 3 -COOH ácido acético (compuesto orgánico) HNO 3 ácido nítrico HBr. O ácido hipobromoso Bases fuertes Bases débiles Na. OH hidróxido de sodio o sosa cáustica NH 4 OH hidróxido de amonio KOH hidróxido de potasio o potasa NH 2 OH hidroxilamina Li. OH hidróxido de litio Ca(OH)2 hidróxido de calcio (cal apagada)
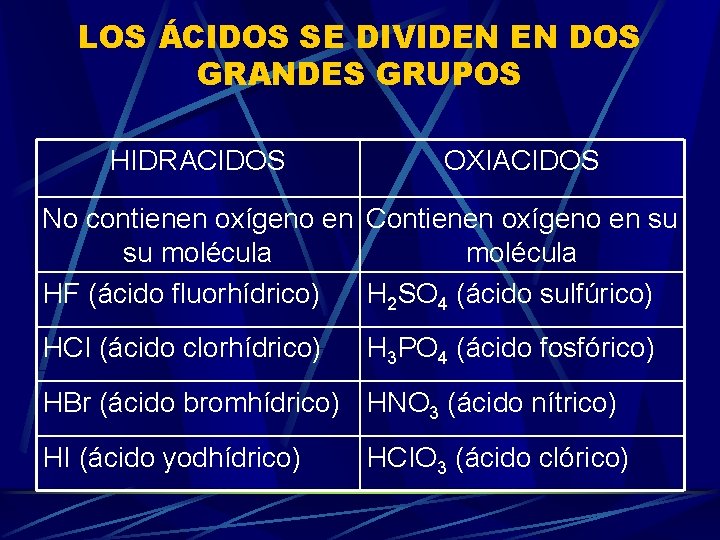
LOS ÁCIDOS SE DIVIDEN EN DOS GRANDES GRUPOS HIDRACIDOS OXIACIDOS No contienen oxígeno en Contienen oxígeno en su su molécula HF (ácido fluorhídrico) H 2 SO 4 (ácido sulfúrico) HCI (ácido clorhídrico) H 3 PO 4 (ácido fosfórico) HBr (ácido bromhídrico) HNO 3 (ácido nítrico) HI (ácido yodhídrico) HCIO 3 (ácido clórico)

p. H • Significa potencial hidrógeno y representa la concentración de hidrógeno ( H ) en una solución acuosa • El p. H indica el grado de acidez y basicidad de una sustancia

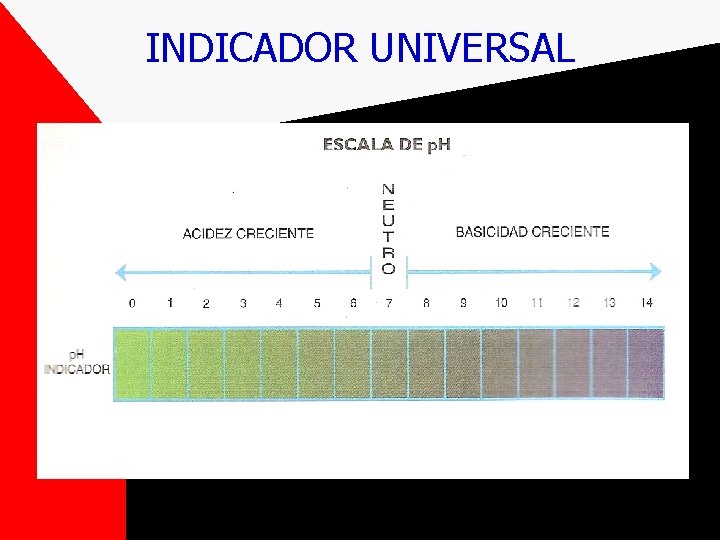
INDICADOR UNIVERSAL
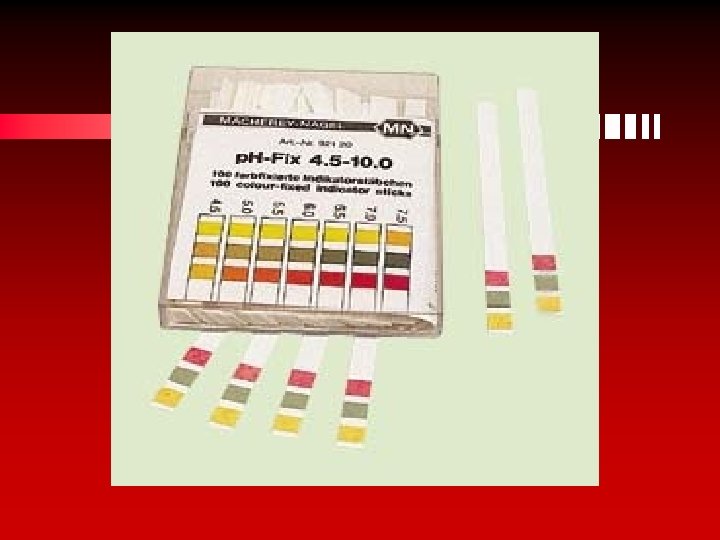

PHMETRO
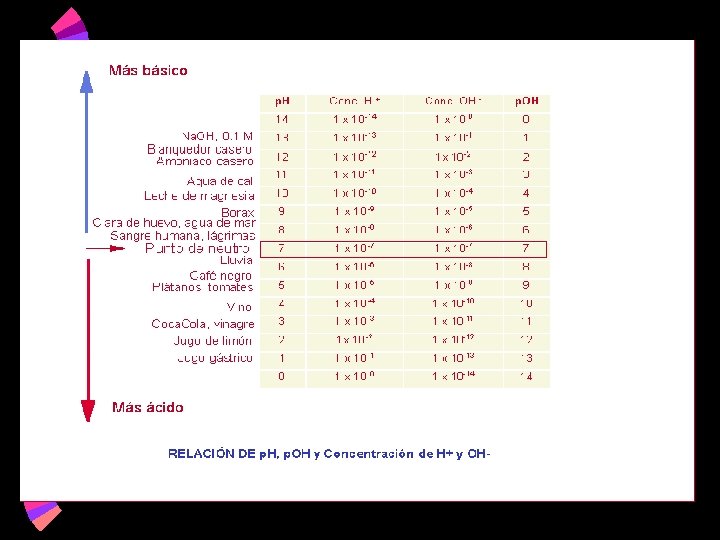

• La determinación del p. H es importante para la investigación científica, la industria y la medicina • El buen funcionamiento del cuerpo humano depende de la acidez o basicidad de las sustancias sea la adecuada. • El p. H es importante para elegir el color adecuado en el teñido de las telas • Para mejorar los cultivos se hace un análisis del suelo y el p. H nos indica su basicidad o acidez.

INDICADORES • Sustancia orgánica que cambia de color en presencia de un ácido o una base.
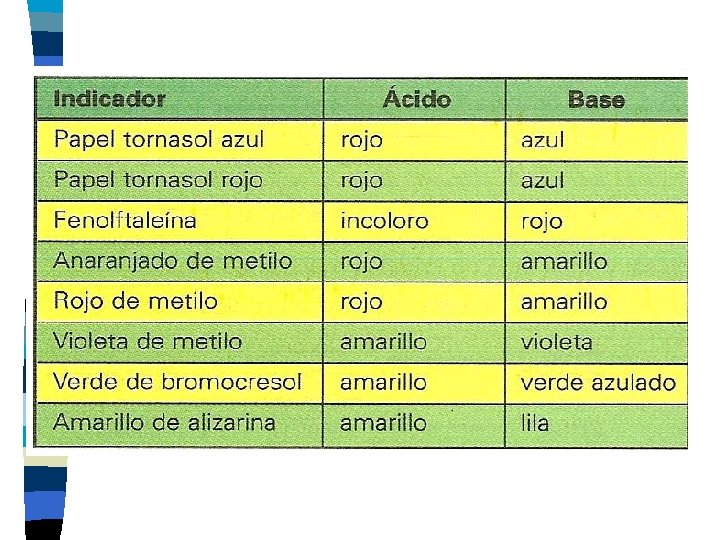

NEUTRALIZACIÓN • Es la reacción entre un ácido y una base • Los productos de la neutralización son: agua, sal y calor. • Siempre que reaccione un ácido con una base, se liberara energía en forma de calor, a este calor liberado se le llama calor de neutralización • La neutralización es un tipo de reacción exotérmica porque libera calor.

E J E M P L O • H 2 SO 4 + KOH K 2 SO 4 + H 2 O +

FORMULAS DE ACIDOS Y BASES ACIDOS: llevan el símbolo de hidrógeno ( H ) a la izquierda de la fórmula; ejemplos H 2 SO 4, HCl, HNO 3, H 2 CO 4, etc. BASES: llevan el radical hidróxido ( OH ) a la derecha de la fórmula; ejemplos. Al(OH)3, Na. OH, NH 4 OH, Ca(OH)2, etc.

ECUACIONES QUIMICAS DE NEUTRALIZACIÓN ACIDO + BASE HCl + Na. OH H 2 SO 4 + Ca(OH)2 H 2 S + Al(OH)3 HNO 3 + NH 4 OH SAL + AGUA Na. Cl + H 2 O Ca. SO 4 + H 2 O Al 2 S 3 + H 2 O NH 4 NO 3 + H 2 O

BALANCEO DE ECUACIONES QUIMICAS Balancear una ecuación química significa igualar la cantidad de átomos que hay en los reactivos, con la cantidad de átomos que hay en los productos y esto se logra colocando un coeficiente al lado izquierdo de cada compuesto.

PASOS • 1. - Conocer a los elementos que forman moléculas diatómicas; H 2 O 2, N 2, I 2, Br 2, y Cl 2. • 2. - primero se igualan los metales, en seguida los no metales, luego el hidrógeno y por ultimo el oxígeno. • 3. -Los coeficientes se pueden ir cambiando, los subíndices no • 4. - Comprobar que los átomos de los elementos sean igual tanto en el primer miembro como en el segundo miembro de la ecuación química.

EJEMPLO 2 Na. OH + H 2 SO 4 Na 2 SO 4 + 2 H 2 O 2 1 4 6 Na S H O 2 1 4 6
- Slides: 27