Tema 9 Reacciones de precipitacin Equilibrios de precipitacin

Tema 9 Reacciones de precipitación

Equilibrios de precipitación o solubilidad p. ej. : Ag. Cl (s) « Ag+ (aq) + Cl- (aq) Importancia de los equilibrios de precipitación

CONTENIDO 1. - Conceptos básicos. 2. - Producto de solubilidad. 3. - Factores que afectan a la solubilidad.

1 CONCEPTOS BÁSICOS. vdisoluc = vcristaliz Þ Equilibrio Disolución saturada: Aquélla que contiene la máxima cantidad de soluto que puede disolverse en una determinada cantidad de disolvente a una temperatura dada.

Solubilidad de un soluto en un disolvente dado: Cantidad de soluto necesaria para formar una disolución saturada en una cantidad dada de disolvente. ß Máxima cantidad de soluto que puede disolverse en una cantidad fija de disolvente. [p. ej. Na. Cl en agua a 0ºC Þ s = 35. 7 g por 100 m. L agua] Si disolvemos menos cantidad ß disolución no saturada Sólidos iónicos cristalinos s gramos soluto / 100 m. L disolvente gramos soluto / L disolución moles soluto / L disolución (Molar) • Solubles (s ³ 2× 10 -2 M) • Ligeramente solubles (10 -5 M < s < 2× 10 -2 M) • Insolubles (s £ 10 -5 M)

Pb. I 2 (s) « Pb 2+ (aq) + 2 I- (aq) • Dinámico • Heterogéneo [ • Reacción directa: disolución • Reacción inversa: precipitación [ Equilibrios de solubilidad] Equilibrios de precipitación] Reacciones de precipitación: Aquéllas que dan como resultado la formación de un producto insoluble. Precipitado: Sólido insoluble que se forma por una reacción en disolución.
![2 PRODUCTO DE SOLUBILIDAD. [Concentraciones en el equilibrio] Ag. Cl (s) « Ag+ (aq) 2 PRODUCTO DE SOLUBILIDAD. [Concentraciones en el equilibrio] Ag. Cl (s) « Ag+ (aq)](http://slidetodoc.com/presentation_image_h/88ee7682622ada6755541773b968c724/image-7.jpg)
2 PRODUCTO DE SOLUBILIDAD. [Concentraciones en el equilibrio] Ag. Cl (s) « Ag+ (aq) + Cl- (aq) Bi 2 S 3 (s) « 2 Bi 3+ (aq) + 3 S 2 - (aq) KPS = [Ag+][Cl-] Producto de solubilidad KPS = [Bi 3+]2 [S 2 -]3 KPS = (2 s)2 (3 s)3 Relación entre la solubilidad y el producto de solubilidad: Ag. Cl (s) « Ag+ (aq) + Cl- (aq) [ ]o [ ]eq s s Si KPS Þ s KPS = [Ag+][Cl-] = s 2

Mezclamos disoluciones que contienen dos iones que pueden formar una sal insoluble. ¿Cómo saber si se formará precipitado? Q = KPS Q > KPS Q < KPS Þ Þ Þ Equilibrio : disolución saturada Se desplaza hacia la izquierda : precipita No precipita : disolución no saturada.

3 FACTORES QUE AFECTAN A LA SOLUBILIDAD. 3. 1. Efecto de la temperatura. Afecta a KPS, dado que es una constante de equilibrio. ¿Cómo? Þ Ecuación de van´t Hoff AB (s) « A+ (aq) + B- (aq) [Tema 5] DHºdis = ? • Si DHºdis > 0 (endotérmica) Þ T KPS s • Si DHºdis < 0 (exotérmica) Þ T KPS ¯ s ¯


3. 2. Efecto del ión común. La solubilidad de un compuesto iónico poco soluble disminuye en presencia de un segundo soluto que proporcione un ión común. Pb. I 2 (s) « Pb 2+ (aq) + 2 I- (aq) KI (s) ® K+ (aq) + I- (aq) Ión común s (Pb. I 2 en agua) = 1. 2× 10 -3 M s (Pb. I 2 en una disolución 0. 1 M de KI) = 7. 1× 10 -7 M

3. 3. Efecto del p. H. Mg(OH)2 (s) « Mg 2+ (aq) + 2 OH- (aq) Si el p. H se hace más ácido Þ menor [OH-] Þ Þ el equilibrio se desplaza a la derecha Þ mayor solubilidad. Este efecto ocurre en todas las sales cuyo anión presente carácter básico. Ca. F 2 (s) « Ca 2+ (aq) + 2 F- (aq) + H 2 O (l) « HF (aq) + OH- (aq) La solubilidad de las sales que contienen aniones básicos aumenta conforme el p. H disminuye.

Aplicación: Formación de caries Esmalte dental: hidroxiapatita Ca 10(PO 4)6(OH)2 (s) « 10 Ca 2+ (aq) + 6 PO 43 - (aq) + 2 OH- (aq) Si añado F- se forma fluoroapatita: Ca 10(PO 4)6 F 2 (s) que resiste mejor el ataque de los ácidos. Otros fenómenos: * Lluvia ácida: disuelve Ca. CO 3 de monumentos * CO 2 de la respiración: deterioro de estalactitas y estalagmitas

3. 4. Formación de iones complejos. Los iones metálicos pueden actuar como ácidos de Lewis. La unión de un ión metálico con una (o más) bases de Lewis se conoce como ión complejo. Ag+ (aq) + 2 NH 3 (aq) « Ag(NH 3)2+ (aq) Ión complejo p. ej. : La adición de NH 3 tiene un efecto espectacular sobre la solubilidad del Ag. Cl, que aumenta mucho. Ag. Cl (s) « Ag+ (aq) + Cl- (aq)
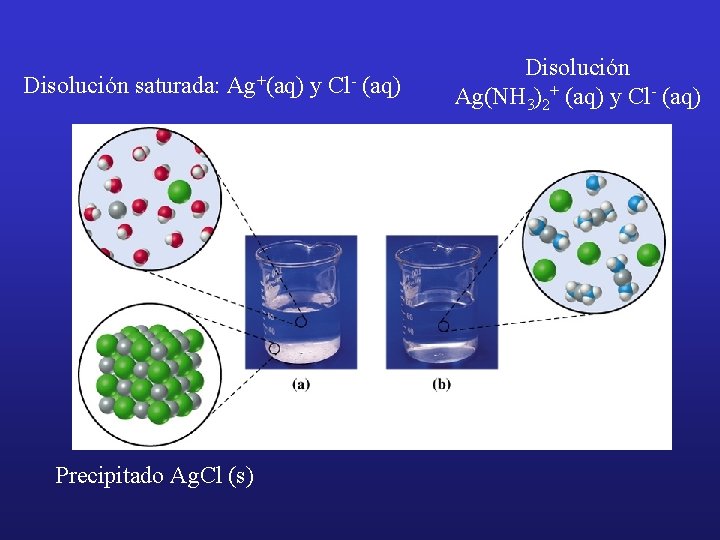
Disolución saturada: Ag+(aq) Precipitado Ag. Cl (s) y Cl- (aq) Disolución Ag(NH 3)2+ (aq) y Cl- (aq)
- Slides: 15