Tema 5 Mutacin y reparacin de DNA CA













- Slides: 19

Tema 5 Mutación y reparación de DNA CA García Sepúlveda MD Ph. D Last updated Jan 2019 Laboratorio de Genómica Viral y Humana Facultad de Medicina, Universidad Autónoma de San Luis Potosí 1

Tema 5. Mutación y reparación del DNA polimerasas procariotas Sabemos que la tasa de error en bacterias no es tan elevada, en realidad es de 1: 100 x 106 o 1: 10 x 109 Equivalente a menos de una 1 base equivocada por cada 10 generaciones bacterianas. Esto sugiere que existe un mecanismo específicamente dedicado a monitorear y corregir los errores de escritura de la polimerasa. Tipos de errores introducidos por DNA Pols • Substituciones = introducción de bases nucleotídicas equivocadas (mal apareadas con la referencia). • Corrimiento del marco de lectura = introducción o deleción (indels) de nucleótidos. 2

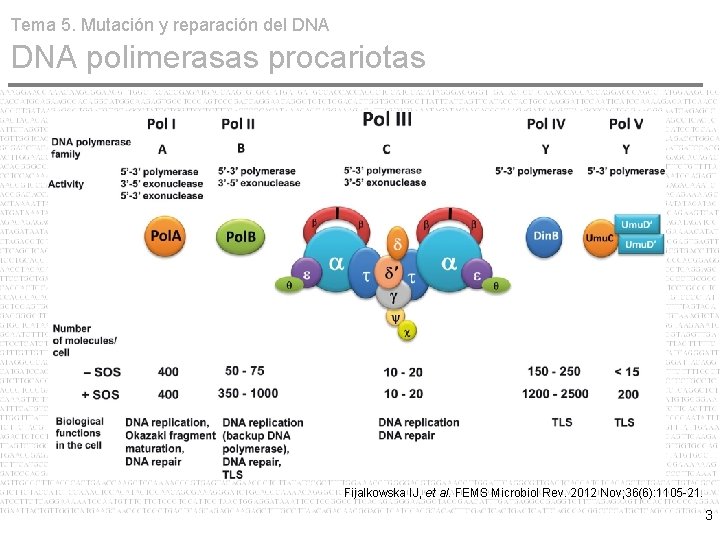
Tema 5. Mutación y reparación del DNA polimerasas procariotas Fijalkowska IJ, et al. FEMS Microbiol Rev. 2012 Nov; 36(6): 1105 -21. 3

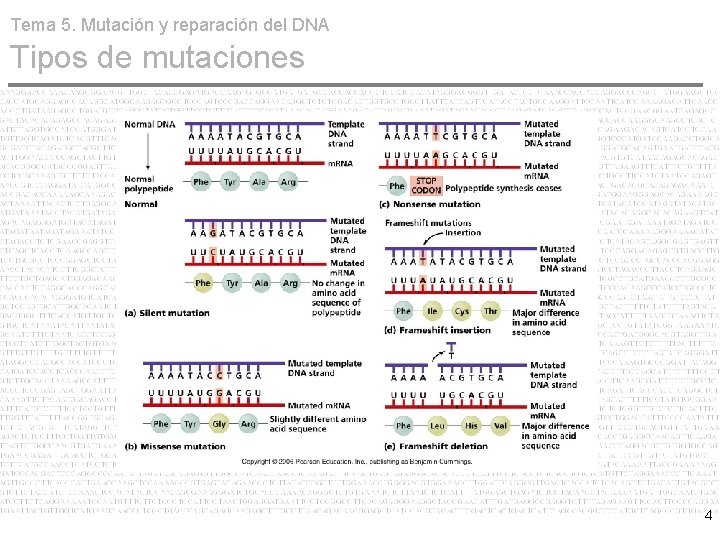
Tema 5. Mutación y reparación del DNA Tipos de mutaciones 4

Tema 5. Mutación y reparación del DNA Tipos de mutaciones 5

Tema 5. Mutación y reparación del DNA Corrección de errores (proofreading) La introducción de un nucleótido incorrecto (o de un nucleótido que no se aparee correctamente) lleva a la enzima a retroceder una base y quitar el nucleótido en sentido 3' 5'. Posteriormente, la enzima continua avanzando. La actividad de exonucleasa puede residir en la misma subunidad involucrada en la síntesis de DNA o en una diferente. Las diferentes DNA polimerasas conocidas poseen diferentes grados de fidelidad (lo cual depende de su capacidad de “proofreading”. En general la capacidad de “proofreading” incrementa la fidelidad de las enzimas 100, 000 a 10’ 000, 000 X (lo que explica la disminución de la tasa de error sintética de 1 en 1, 000 a 1 en 100'000, 000 a 10, 000'000, 000. 6

Tema 5. Mutación y reparación del DNA polimerasas procariotas Cinco enzimas bien conocidas. DNA Pol I • Implicada en la reparación de DNA dañado. • Exonucleasa tanto 5' 3' (Nick-translation) • Exonucleasa 3' 5' (proofreading). Primera en ser descubierta DNA Pol II • Involucrada en la replicación de DNA dañado TLS (trans-lesional synthesis). • Polimerasa 5' 3'. • Exonucleasa 3' 5'. DNA Pol III • Principal replicasa procariota con actividad de exonucleasa. DNA Pol IV y V • Miembros de familia Y (Polimerasas de Síntesis Translesional). 7

Tema 5. Mutación y reparación del DNA polimerasas ecuariotas Existen por lo menos 15 distintas. DNA Pol a = Primasa y DNA pol por primeras 20 bases. DNA Pol b = Reparación de DNA dañado, escisión de bases o llenados de gaps. DNA Pol g = Replicación y reparación de DNA mitocondrial. DNA Pol d = Replicasa de cadena retardada con capacidad de exonucleasa. DNA Pol e = Replicasa de cadena lider, alta procesividad y capacidad de exonucleasa. DNA Pol , i, k y Rev 1 = TLS pol de la familia Y (Xeroderma pigmentosum variante XPV) DNA Pol z = miembro de la familia B, replicasa de alta fidelidad sin actividad exonucleasa. Otras DNA pol no muy bien caracterizadas (q, l, f, s y m). ¡Ninguna DNA pol eucariota posee capacidad de exonucleasa 5' 3' por lo que para retirar los oligos cebadores de RNA hace falta reclutar a otras enzimas! 8

Tema 5. Mutación y reparación del DNA polimerasas ecuariotas Familia Y Incluye a DNA pol , , y Rev 1 (Desoxicitidil-Transferasa Terminal) eucariota y la Pol IV (DINB) y Pol. V (UMUC) de E coli. Baja fidelidad en DNA integro pero eficientes para replicar el DNA dañado = TLS Pol = Polimerasas de Síntesis Translesional Los pacientes con Xeroderma pigmentosum variante XPV poseen una mutación de DNA pol que evita que reparen exitosamente el daño a la piel inducido por luz UV. Familia RT Tanto eucariotas como retrovirales. Implicadas en la síntesis de DNA a partir de RNA DNA polimerasa RNA dependiente (Rd. Dp). Las eucariotas restringidas a los telómeros. 9

Tema 5. Mutación y reparación del DNA Patologías de la reparación de DNA También conocidos como “Desordenes por reparación deficiente del DNA”. La deleción total (knock-out) de genes involucrados en la reparación del DNA son embrionarios letales. La mayor parte de los DRDD muestran grados variables de envejecimiento acelardo o predisposición a cancer, en ocasiones ambos. Se observan defectos en la reparación del DNA en casi todas las “enfermedades de evenjecimiento acelerado” en las cuales los tejidos, órganos o sistemas envejecen prematuramente. También conocidas com progerias segmentales. • Ataxia telangiectasia • Síndrome de Bloom • Síndrome de Cockayne • Anemia Fanconi • Progeria (Síndrome de Hutchinson-Gilford) • Síndrome de Rothmund-Thomson • Tricotiodistrofia • Síndrome de Werner • Xeroderma pigmentosum 10

Tema 5. Mutación y reparación del DNA Ataxia telangiectasia Síndrome neurodegenerativo raro discapacitante caracterizado por trastornos motores y dilatación de vasos pequeños. 1: 40, 000 a 1: 100, 000 nacimiento vivos. Defecto del gen ATM responsable de identificar rupturas de doble cadena, de reclutar a DNA reparasas translesionales al sitio y de evitar nuevos ciclos replicativos. Afecta a cerebelo causando dificultades de movimiento y coordinación. Condiciona inmunocompromiso que predispone a infecciones (sinusitis, bronquitis y penumonía). Incrementa riesgo a cancer. Síntomas evidentes en infancia temprana de (de 4 a 5 años), empeorando hacia la infancia tardia. Postura flácida de infantes al estar sentados (postura de borracho). Evoluciona hacia apraxia oculomotora (dificultad para mover ojos de un lado a otro). Problemas de deglución, habla distorsionada y arrastrada. Expectativa de vida variable (ca 25 años), muerte por EPOC y Cancer. 11

Tema 5. Mutación y reparación del DNA Síndrome de Bloom También síndrome de Bloom–Torre–Machacek (descrito en 1954). Trastorno autosómico recesivo raro con alta inestabilidad genómica y excesivamente elevada recombinación homóloga (ver imagen inferior denotando intercambios de cromátides hermanas). 1: 50, 000 nacimientos. Mutación en gen BLM, miembro de la familia de las helicasas Rec. Q involucrado en la desnaturalización del DNA durante transcripción, replicación y reparación. Corta estatura, hombros caidos, voz de alto tono, cara delgada y larga, micrognatia y orejas/nariz prominentes. Rash cutáneo en forma de mariposa eritematoso, telangiectático y escamoso sobre cachetes y nariz. Inmunodeficiencias moderadas particularmente de ciertas clases de Igs (pneumonía, otitis y EPOC). Hipogonadismo e infertilidad. Afecta a varones y mujeres por igual. Muerte por EPOC o cancer alrededor de los 25 años de edad. 12

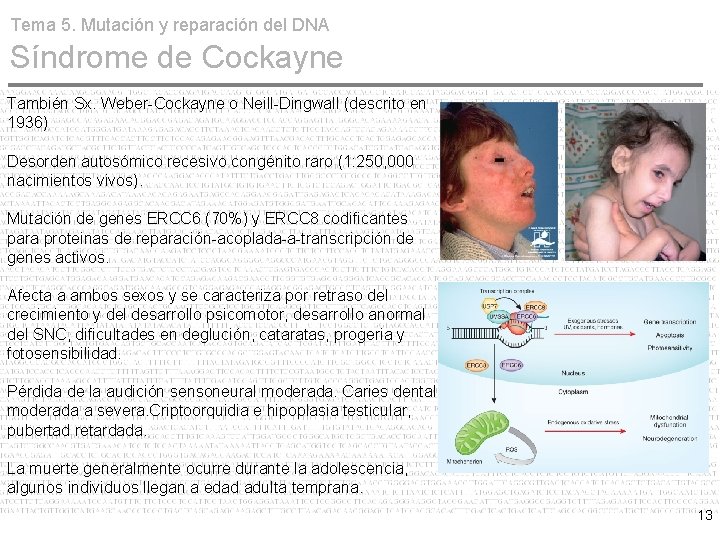
Tema 5. Mutación y reparación del DNA Síndrome de Cockayne También Sx. Weber-Cockayne o Neill-Dingwall (descrito en 1936) Desorden autosómico recesivo congénito raro (1: 250, 000 nacimientos vivos). Mutación de genes ERCC 6 (70%) y ERCC 8 codificantes para proteinas de reparación-acoplada-a-transcripción de genes activos. Afecta a ambos sexos y se caracteriza por retraso del crecimiento y del desarrollo psicomotor, desarrollo anormal del SNC, dificultades en deglución, cataratas, progeria y fotosensibilidad. Pérdida de la audición sensoneural moderada. Caries dental moderada a severa. Criptoorquidia e hipoplasia testicular, pubertad retardada. La muerte generalmente ocurre durante la adolescencia, algunos individuos llegan a edad adulta temprana. 13

Tema 5. Mutación y reparación del DNA Anemia de Fanconi Enfermedad autosómica recesiva rara (1: 350, 000 nacimientos) más frecuente en comunidades endogámicas Afrikaners y Judios Ashkenazi. Defecto de uno más genes de un cluster de reparación, 15 genes asociados a FA: FANCA, FANCB, FANCC, FANCD 1 (BRCA 2), FANCD 2, FANCE, FANCF, FANCG, FANCI, FANCJ, FANCL, FANCM, FANCN, FANCP y RAD 51 C. Caracterizada por predisposición a cancer (Leucemia mieloide aguda) y falla medular (90% antes de los 40 años de edad). Manchas café au lait 60 a 75% presentan otros defectos como estatura corta, dermopatías, anormalidades en brazos, ojos, cabeza, riñones, oidos, retraso del crecimiento y anormalidades esqueléticas. 75% poseen endocrinopatías. Sobrevida promedio de 30 años. 14

Tema 5. Mutación y reparación del DNA Síndrome de Hutchinson-Gilford (progeria) Enfermedad genética extremadamente rara (1: 4 a 8 x 106 nacimientos). Descrita en 1886 Hutchinson y 1897 por Gilford. Causada por mutación de novo puntual en posición 1824 de gen LMNA rara vez heredada. LMNA codifica para laminina nuclear que organiza a la cromatina y dá soporte al núcleo. Mutación ocurre durante desarrollo embrionario. Caracterizada por envejicimiento precoz acelerado a etapas muy tempranas de la infancia. Presentan tempranamente esclerodermia, retraso del crecimiento, alopecia, fascies característica. En etapas tardías presentan piel arrugada, aterosclerosis, falla renal, presbiacusia, pérdida de la visión y problemas cardiovasculares. Pocos sobreviven a los 13 años de edad. 15

Tema 5. Mutación y reparación del DNA Síndrome de Rothmund-Thomson Enfermedad genética autosómica recesiva rara descrita en 1868 (solo 300 casos descritos). Mutación en gen codificante para helicasa RECQL 4 se ha visto implicada. Fotosensibilidad, poiquiloderma (adelgazamiento, increm/decrem. pigmentación, telangiectasias) y cataratas a exposición solar. Nariz en silla de montar. Defectos congénitos en huesos, estatura corta y anormalidades de dedos como ausencia de pulgar. Alopecia o trastornos del crecimiento de vello/cabello. Hipoodntia Alta incidencia de osteosarcomas. En ausencia de malignidades la sobrevida es normal. 16

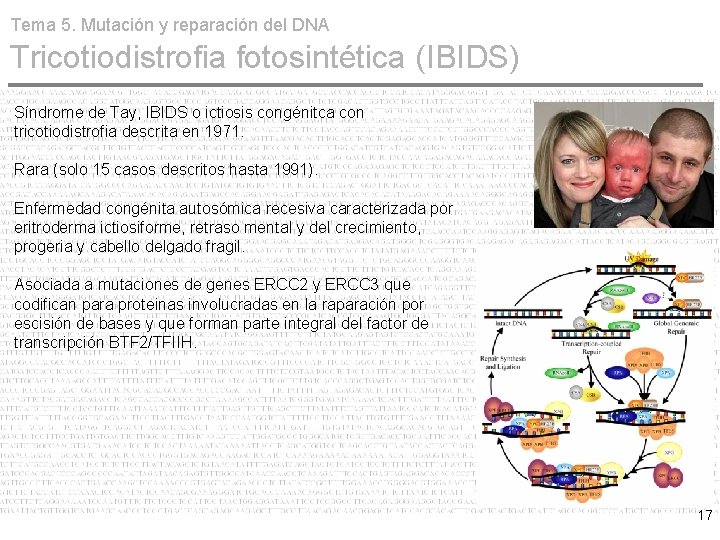
Tema 5. Mutación y reparación del DNA Tricotiodistrofia fotosintética (IBIDS) Síndrome de Tay, IBIDS o ictiosis congénitca con tricotiodistrofia descrita en 1971. Rara (solo 15 casos descritos hasta 1991). Enfermedad congénita autosómica recesiva caracterizada por eritroderma ictiosiforme, retraso mental y del crecimiento, progeria y cabello delgado fragil. Asociada a mutaciones de genes ERCC 2 y ERCC 3 que codifican para proteinas involucradas en la raparación por escisión de bases y que forman parte integral del factor de transcripción BTF 2/TFIIH. 17

Tema 5. Mutación y reparación del DNA Síndrome de Werner También conocido como progeria adulta, enfermedad autosómica recesiva muy rara caracterizada por envejecimiento prematuro descrito en 1904. Asociado a mutaciones del gen WRN (chromosoma 8) también conocido como Rec. QL 2 codificante para una helicasa 3´-5´que también ejerce la función de escisión de bases en la misma dirección. Síntomas normalmente se observan tras los 10 años de edad, acelerándose tras la pubertad y siendo extremos a los 40 años de edad. Ausencia de crecimiento acelerado pubertal, adelgazamiento y decoloración del cabello, cambios de voz, engrosamiento de la piel, diabetes mellitus, cataratas, hipogonadismo, cancer y aterosclerosis. Caracterizado por acortamiento telomérico acelerado e inestabilidad genómica. Muerte usualmente por infartos al miocardio ocancer ca 50 años. 18

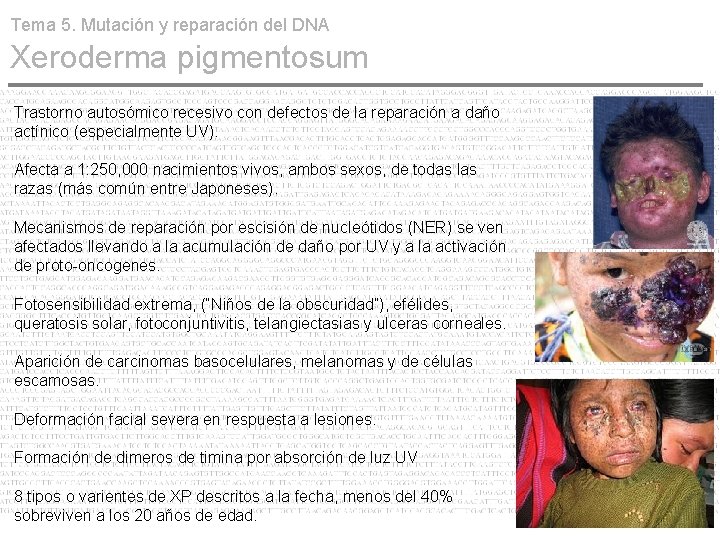
Tema 5. Mutación y reparación del DNA Xeroderma pigmentosum Trastorno autosómico recesivo con defectos de la reparación a daño actínico (especialmente UV). Afecta a 1: 250, 000 nacimientos vivos, ambos sexos, de todas las razas (más común entre Japoneses). Mecanismos de reparación por escisión de nucleótidos (NER) se ven afectados llevando a la acumulación de daño por UV y a la activación de proto-oncogenes. Fotosensibilidad extrema, (“Niños de la obscuridad”), efélides, queratosis solar, fotoconjuntivitis, telangiectasias y ulceras corneales. Aparición de carcinomas basocelulares, melanomas y de células escamosas. Deformación facial severa en respuesta a lesiones. Formación de dimeros de timina por absorción de luz UV 8 tipos o varientes de XP descritos a la fecha, menos del 40% sobreviven a los 20 años de edad. 19