Tema 5 Las PROTENAS BIOLOGA 2 BACHILLERATO IES

Tema 5. Las PROTEÍNAS BIOLOGÍA 2º BACHILLERATO IES "La Gándara", Toreno (León) Prof. Rubén Rodríguez Fernández Esta obra está bajo una licencia Creative Commons Reconocimiento – Compartir igual 4. 0
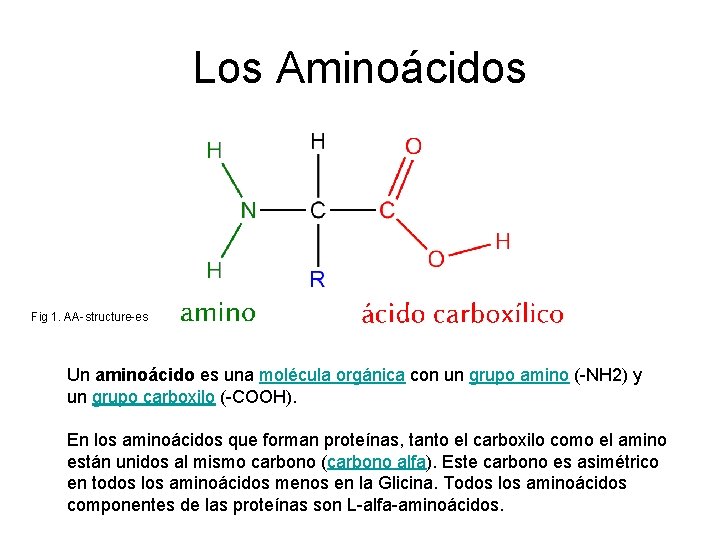
Los Aminoácidos Fig 1. AA-structure-es Un aminoácido es una molécula orgánica con un grupo amino (-NH 2) y un grupo carboxilo (-COOH). En los aminoácidos que forman proteínas, tanto el carboxilo como el amino están unidos al mismo carbono (carbono alfa). Este carbono es asimétrico en todos los aminoácidos menos en la Glicina. Todos los aminoácidos componentes de las proteínas son L-alfa-aminoácidos.
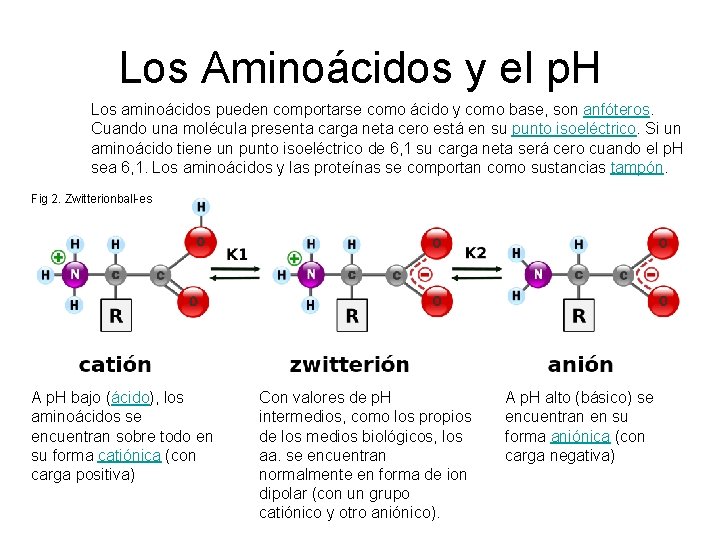
Los Aminoácidos y el p. H Los aminoácidos pueden comportarse como ácido y como base, son anfóteros. Cuando una molécula presenta carga neta cero está en su punto isoeléctrico. Si un aminoácido tiene un punto isoeléctrico de 6, 1 su carga neta será cero cuando el p. H sea 6, 1. Los aminoácidos y las proteínas se comportan como sustancias tampón. Fig 2. Zwitterionball-es A p. H bajo (ácido), los aminoácidos se encuentran sobre todo en su forma catiónica (con carga positiva) Con valores de p. H intermedios, como los propios de los medios biológicos, los aa. se encuentran normalmente en forma de ion dipolar (con un grupo catiónico y otro aniónico). A p. H alto (básico) se encuentran en su forma aniónica (con carga negativa)
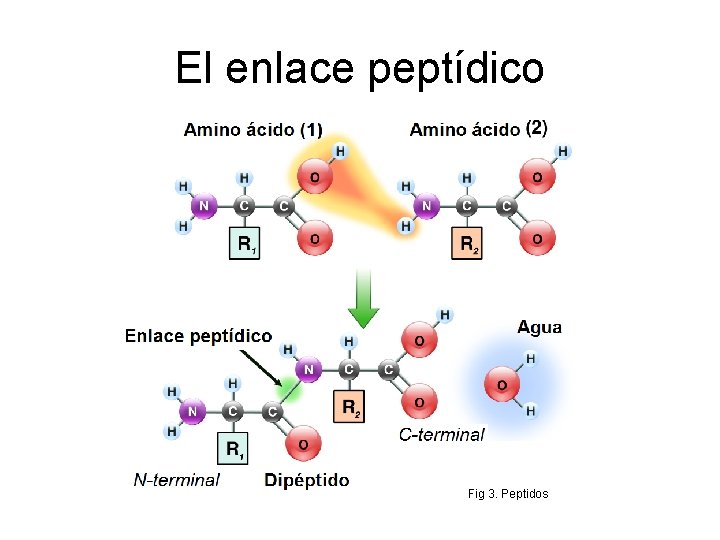
El enlace peptídico Fig 3. Peptidos
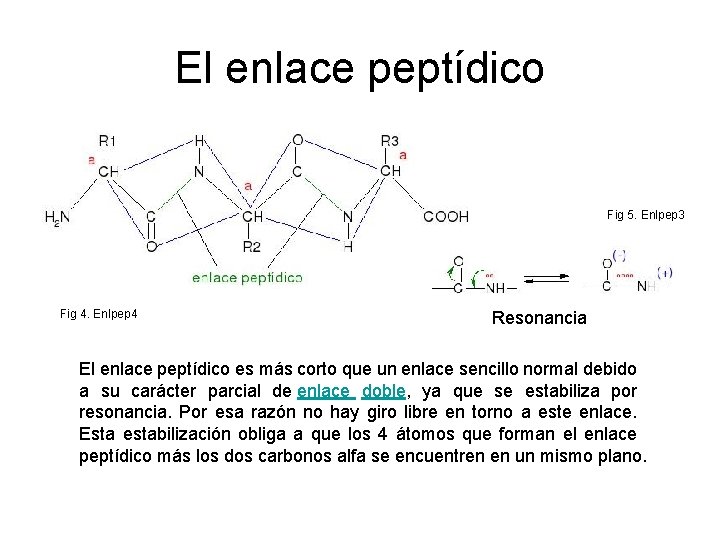
El enlace peptídico Fig 5. Enlpep 3 Fig 4. Enlpep 4 Resonancia El enlace peptídico es más corto que un enlace sencillo normal debido a su carácter parcial de enlace doble, ya que se estabiliza por resonancia. Por esa razón no hay giro libre en torno a este enlace. Esta estabilización obliga a que los 4 átomos que forman el enlace peptídico más los dos carbonos alfa se encuentren en un mismo plano.
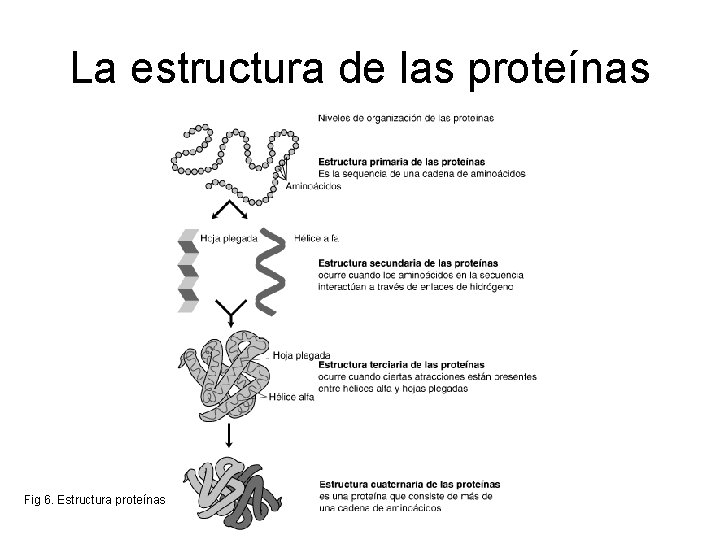
La estructura de las proteínas Fig 6. Estructura proteínas
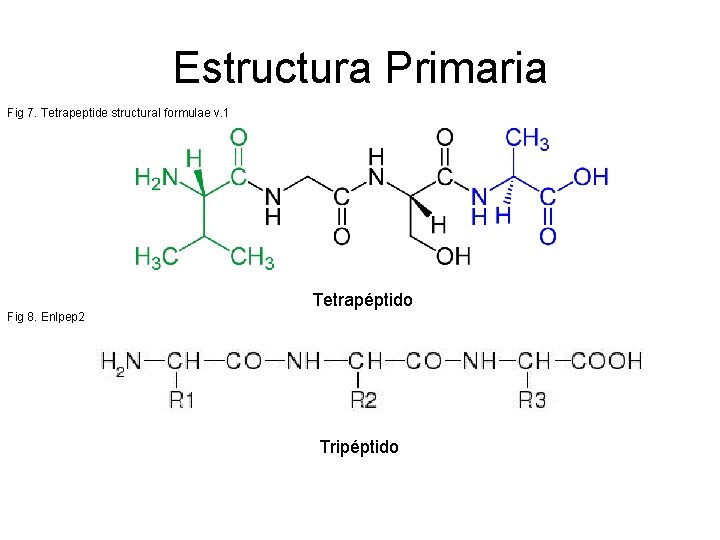
Estructura Primaria Fig 7. Tetrapeptide structural formulae v. 1 Tetrapéptido Fig 8. Enlpep 2 Tripéptido
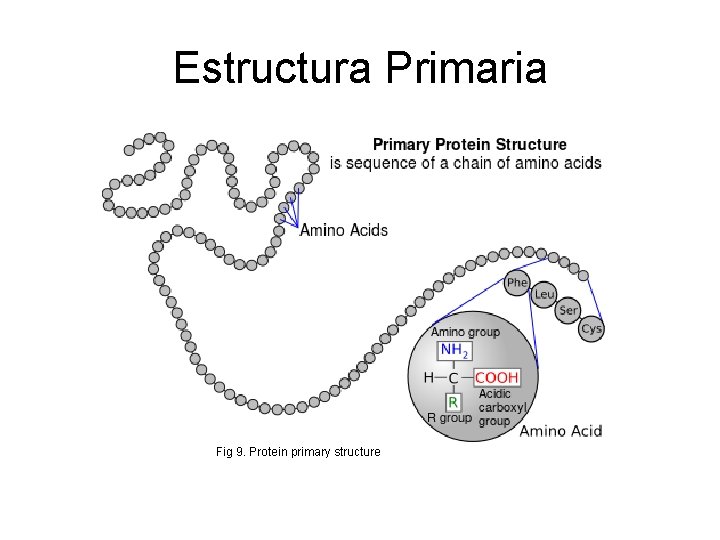
Estructura Primaria Fig 9. Protein primary structure
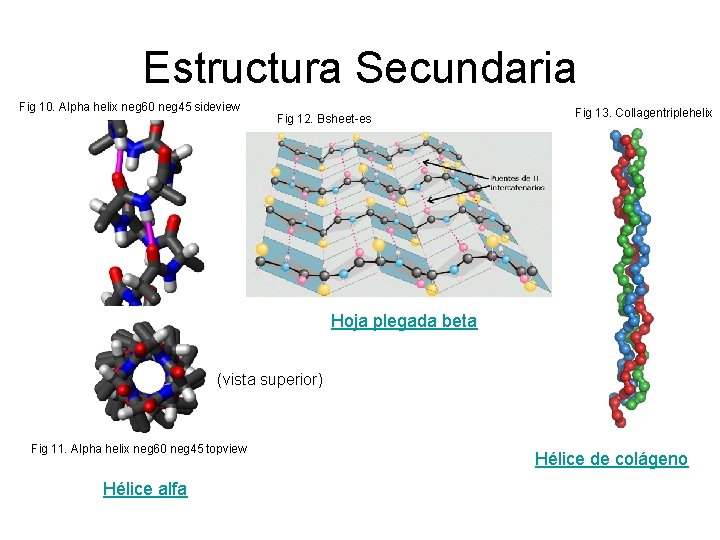
Estructura Secundaria Fig 10. Alpha helix neg 60 neg 45 sideview Fig 12. Bsheet-es Fig 13. Collagentriplehelix Hoja plegada beta (vista superior) Fig 11. Alpha helix neg 60 neg 45 topview Hélice alfa Hélice de colágeno

Estructura Terciaria La mioglobina fue la primera proteína cuya estructura tridimensional se determinó experimentalmente. En 1958, John Kendrew y sus colegas determinaron la estructura de la mioglobina empleando cristalografía de rayos X de alta resolución. Por este descubrimiento, John Kendrew obtuvo en 1962 el Premio Nobel de Química, compartido con Max Perutz Alrededor del 78% de la estructura secundaria tiene una conformación de hélice alfa Fig 14. Myoglobin

Estructura Terciaria Fig 15. Concanavalin_A Estructura terciaria de un protómero de Concanavalina A, una Lectina. Pueden observarse varias regiones conformación en lámina beta. Cada fragmento (flecha) va en sentido contrario a los contiguos.
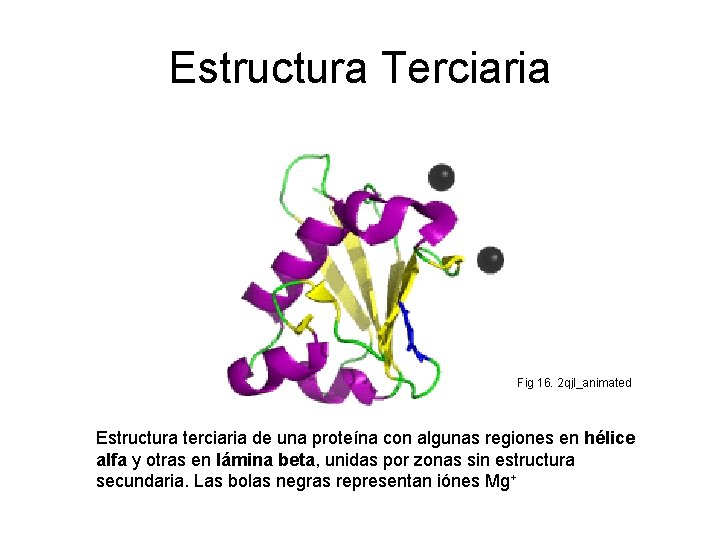
Estructura Terciaria Fig 16. 2 qjl_animated Estructura terciaria de una proteína con algunas regiones en hélice alfa y otras en lámina beta, unidas por zonas sin estructura secundaria. Las bolas negras representan iónes Mg+
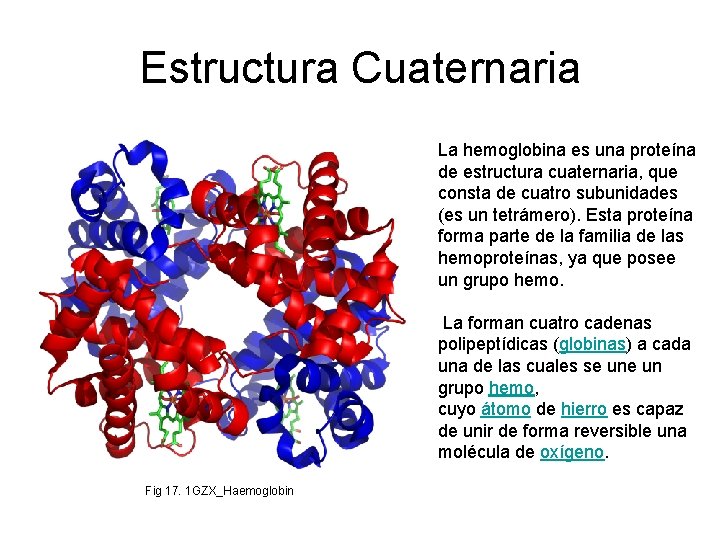
Estructura Cuaternaria La hemoglobina es una proteína de estructura cuaternaria, que consta de cuatro subunidades (es un tetrámero). Esta proteína forma parte de la familia de las hemoproteínas, ya que posee un grupo hemo. La forman cuatro cadenas polipeptídicas (globinas) a cada una de las cuales se un grupo hemo, cuyo átomo de hierro es capaz de unir de forma reversible una molécula de oxígeno. Fig 17. 1 GZX_Haemoglobin

Estructura Cuaternaria Tetrámero: 4 protómeros Fig 18. Inmunoglobulina Molécula de inmunoglobulina con su típica forma de Y. En azul se observan las cadenas pesadas con cuatro dominios Ig, mientras que en verde se muestran las cadenas ligeras

Estructura Cuaternaria Fig 19. Catalase-1 DGF Catalasa
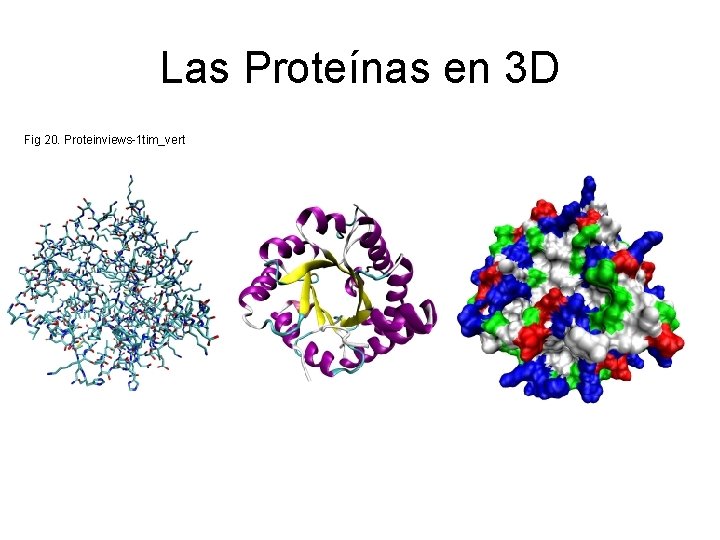
Las Proteínas en 3 D Fig 20. Proteinviews-1 tim_vert
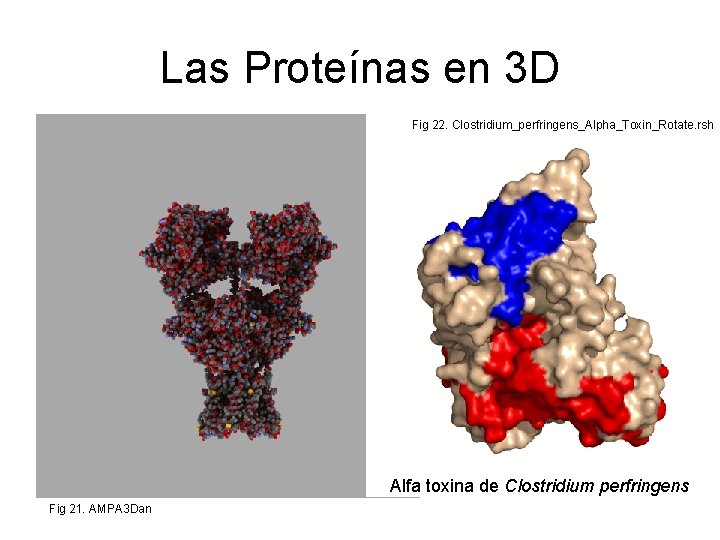
Las Proteínas en 3 D Fig 22. Clostridium_perfringens_Alpha_Toxin_Rotate. rsh Alfa toxina de Clostridium perfringens Fig 21. AMPA 3 Dan
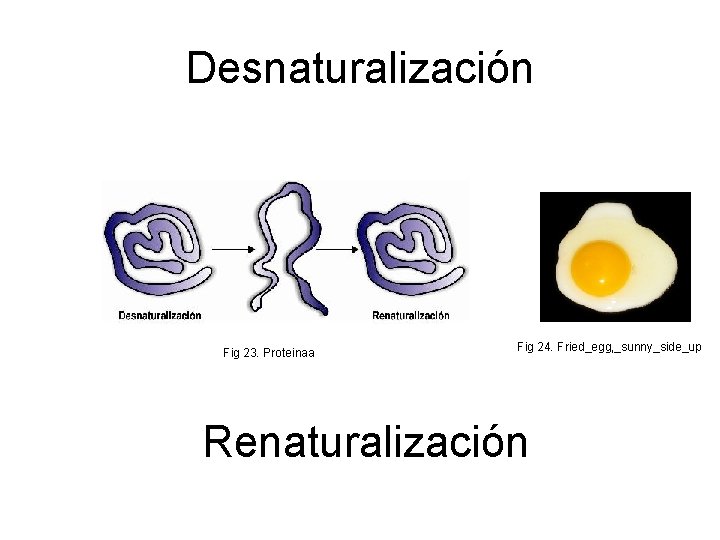
Desnaturalización Fig 23. Proteinaa Fig 24. Fried_egg, _sunny_side_up Renaturalización

Protein Data Bank El Protein Data Bank (PDB) (Banco de Datos de Proteínas) es una base de datos de la estructura tridimensional de las proteínas y ácidos nucleicos. Estos datos, generalmente obtenidos mediante cristalografía de rayos X o resonancia magnética nuclear, son enviados por biólogos y bioquímicos de todo el mundo. Están bajo el dominio público y pueden ser usados libremente. Cuando se fundó, el PDB contenía tan sólo 7 estructuras de proteínas. Desde entonces ha experimentado un crecimiento aproximadamente exponencial en el número de estructuras y nada parece indicar que el ritmo vaya a decaer. El ritmo de crecimiento del PDB ha sido analizado en profundidad en diversos estudios. Fuente: Wikipedia

Proteómica es el estudio a gran escala de las proteínas, en particular de su estructura y función. Las proteínas son partes vitales de los organismos vivos, ya que son los componentes principales de las rutas metabólicas de las células. El término proteómica fue acuñado en 1997 como una analogía con genómica, el estudio de los genes. La palabra "proteoma" es la fusión de "proteína" y "genoma", y fue acuñada por Marc Wilkins en 1994, mientras trabajaba en ese concepto como estudiante de doctorado. El proteoma es la dotación completa de proteínas, incluyendo las modificaciones hechas a un conjunto particular de proteínas, producidas por un organismo o sistema. Esto varía con el tiempo y con requisitos diferentes, o debido al estrés, que sufre una célula o un organismo. La descripción del proteoma permite tener una imagen dinámica de todas las proteínas expresadas, en un momento dado y bajo determinadas condiciones concretas de tiempo y ambiente. Fuente: Wikipedia

Créditos de las Imágenes Todas las imágenes que aparecen en esta presentación han sido obtenidas de Wikipedia y están bajo licencia Creative Commons Autores: 1, 2. Basquetteur, 3. Pozitron, 4. ? ? , 5. Netkk, 6 y 9. National Human Genome Research Institute, 7. Jü, 8. ? ? , 10 y 11. Willow. W, 12. Preston Manor School + JFL, 13. ? ? , 14. Aza. Toth, 15. Lijealso, 16. Hsp 90, 17. Zephyris, 18. ? ? , 19. Dominio Público, 20. Opabinia regalis -Retama, 21. Fuse 809, 22. Ramin Herati, 23. Llkmc 105, 24. Esta obra está bajo una licencia Creative Commons Reconocimiento – Compartir igual 4. 0
- Slides: 21