Tema 5 GASES GASES Disposicin y distancia entre












- Slides: 28

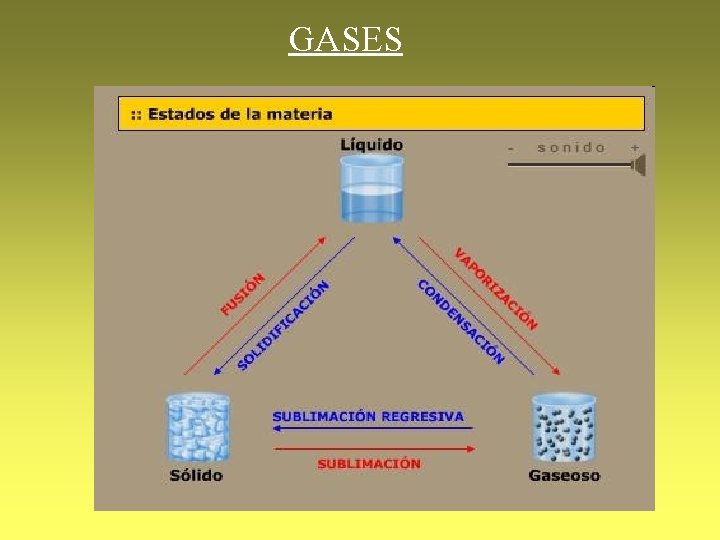
Tema 5 GASES

GASES

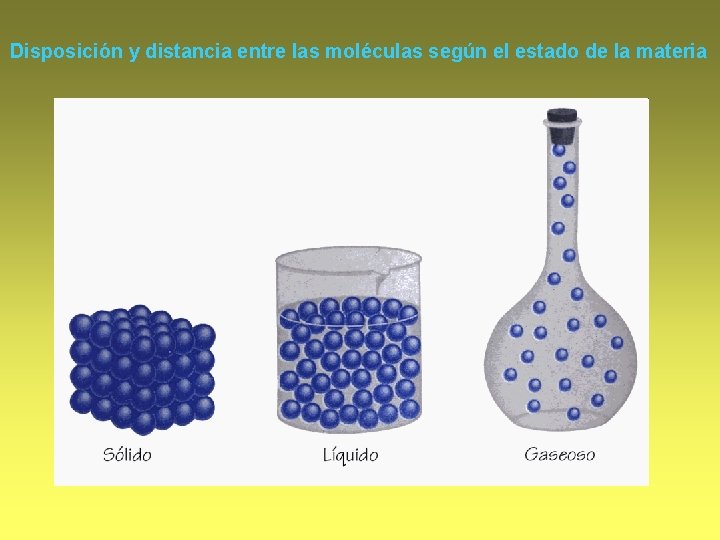
Disposición y distancia entre las moléculas según el estado de la materia

Características de los Gases • Los gases adoptan la forma del recipiente que los contiene. • Pueden ser comprimidos a menores volúmenes. • Cuando en un recipiente hay 2 o mas gases, difunden mezclándose homogéneamente y uniformemente. • Sus densidades son mucho menores que la de los líquidos y sólidos. • Ejercen presión sobre su entorno. Por lo tanto hay que ejercer presión para contenerlos.

Presión Se define como fuerza por unidad de área. Unidad en SI: PASCAL (Pa) Pa = Fuerza x área = N/m 2 = kg/m seg 2 N = kg m/seg 2

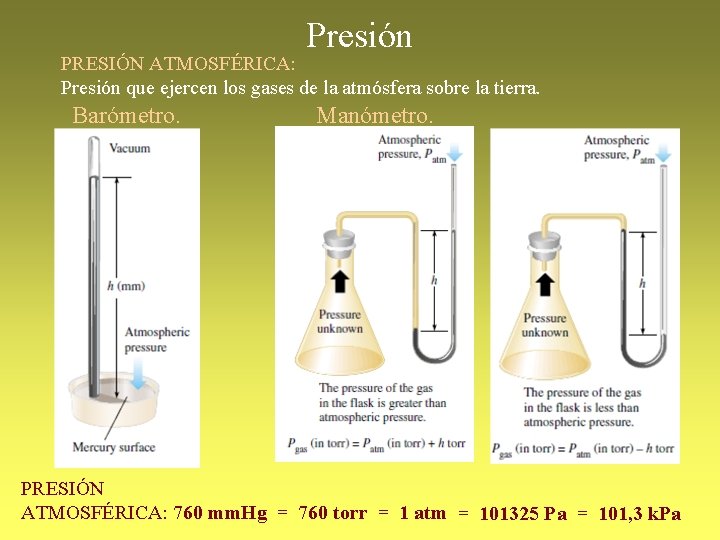
Presión PRESIÓN ATMOSFÉRICA: Presión que ejercen los gases de la atmósfera sobre la tierra. Barómetro. Manómetro. PRESIÓN ATMOSFÉRICA: 760 mm. Hg = 760 torr = 1 atm = 101325 Pa = 101, 3 k. Pa

Teoría Cinética de los Gases • Los gases están constituidos por partículas que se mueven en línea recta y al azar. • Las colisiones entre si y con las paredes del recipiente son perfectamente elásticas: transferencia de energía completa y esta permanece constante en el sistema. • La Presión es fruto de estos choques y depende de la frecuencia y de la fuerza. • Distancia de separación entre moléculas es mucho mayor que sus propias dimensiones: tamaño y volumen despreciable. • No hay fuerzas de atracción entre las moléculas que conforman el gas. • Energía cinética promedio es proporcional a la temperatura del sistema: Dos gases diferentes a la misma temperatura tendrán la misma Energía Cinética promedio. Gases Ideales

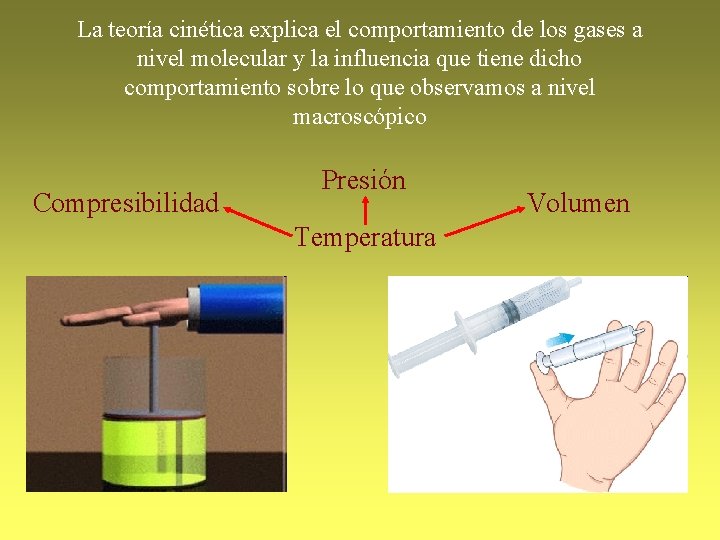
La teoría cinética explica el comportamiento de los gases a nivel molecular y la influencia que tiene dicho comportamiento sobre lo que observamos a nivel macroscópico Compresibilidad Presión Temperatura Volumen

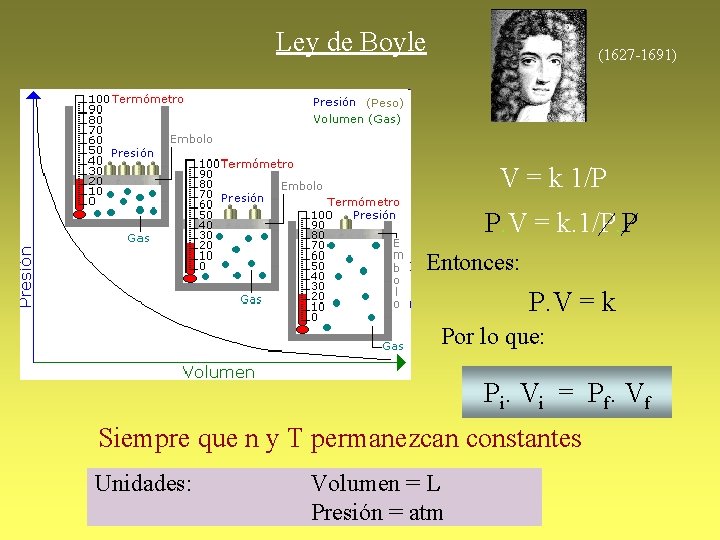
Ley de Boyle (1627 -1691) V = k 1/P P. V = k. 1/P. P Entonces: P. V = k Por lo que: P i. V i = P f. V f Siempre que n y T permanezcan constantes Unidades: Volumen = L Presión = atm

Veamos un ejemplo Una muestra de He ocupa 500 cm 3 a 2, 00 atm. Suponiendo que la Temperatura permanece constante: ¿Qué Volumen ocupará dicho gas a 4 atm? Datos: Vi = 0, 5 L Pi = 2 atm Pf = 4 atm Vf = ? Utilizando la Ley de Boyle P i. V i = P f. V f » Vf = (Pi. Vi) / Pf Reemplazando: Vf = (2 atm. 0, 5 L) / 4 atm Vf = 0, 25 L Rta: Vf = 0, 25 L

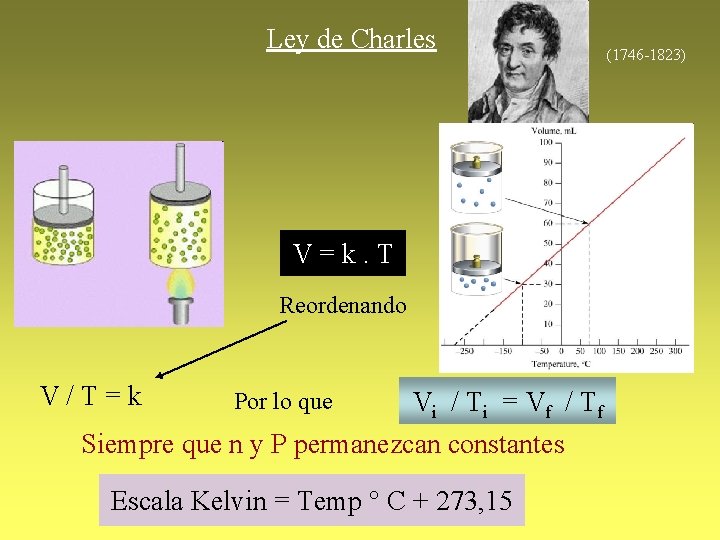
Ley de Charles V=k. T Reordenando V/T=k Por lo que Vi / T i = V f / T f Siempre que n y P permanezcan constantes Escala Kelvin = Temp ° C + 273, 15 (1746 -1823)

Veamos un ejemplo 250 m. L de Cl 2 medidos a 273 K son calentados a presión constante hasta alcanzar una temperatura de 373 K. ¿Cuál es el Volumen final que ocupa el gas? Datos: Vi = 0, 25 L Ti = 273 K Tf = 373 K Vf = ? Aplicando la Ley de Charles Vi / T i = V f / T f Reordenando y Reemplazando Vf = (0, 25 L. 373 °K) / 273 °K Vf = 0, 341 L Rta: Vf = 0, 341 L

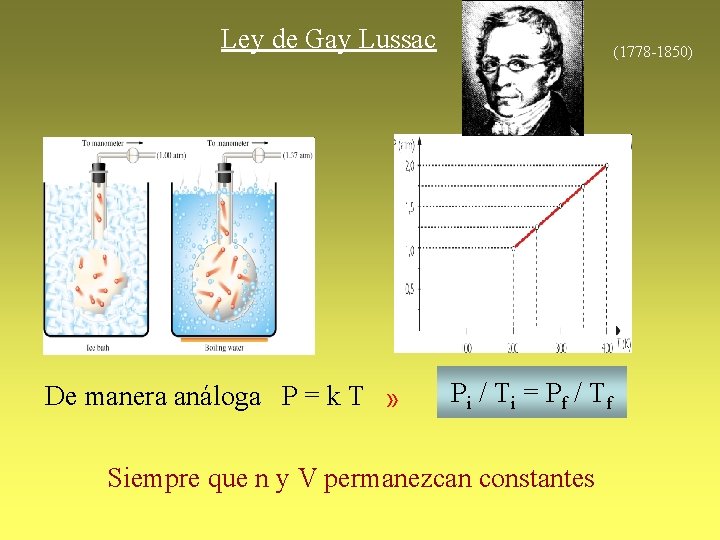
Ley de Gay Lussac De manera análoga P = k T » (1778 -1850) Pi / T i = P f / T f Siempre que n y V permanezcan constantes

Veamos un ejemplo 250 m. L de Cl 2 medidos a 273 K a una Presión de 1 atm son calentados a volumen constante hasta alcanzar una temperatura de 373 K. ¿Cuál será la Presión final del gas? Aplicando la Ley de Gay Lussac Datos: Pi = 1 atm Ti = 273 ° K Tf = 373 ° K Pf = ? Pi / T i = P f / T f Reordenando y Reemplazando Pf = (1 atm. 373 K) / 273 K Pf = 1, 37 atm Rta: Pf = 1, 37 atm

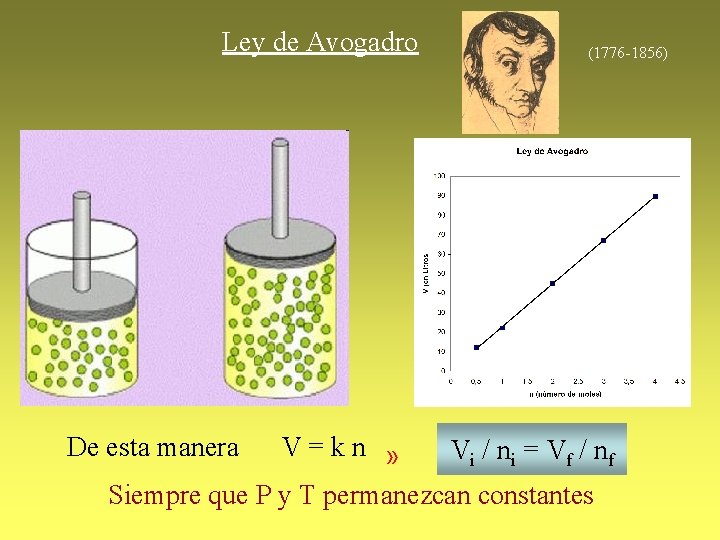
Ley de Avogadro De esta manera (1776 -1856) V=kn » Vi / ni = Vf / nf Siempre que P y T permanezcan constantes

Veamos un ejemplo Inicialmente se tiene 0, 5 moles de Cl 2 que ocupan un volumen de 11, 2 L. Si luego de cierto experimento a presión y temperatura constante se tienen 10 moles de Cl 2. ¿Cuál será el volumen final del gas? Aplicando la Ley de Avogadro Datos: Vi = 11, 2 L ni = 0, 5 moles nf = 10 moles Vf = ? Vi / ni = Vf / nf Reordenando y Reemplazando Vf = (11, 2 L. 10 moles) / 0, 5 moles Vf = 224 L Rta: Vf = 224 L

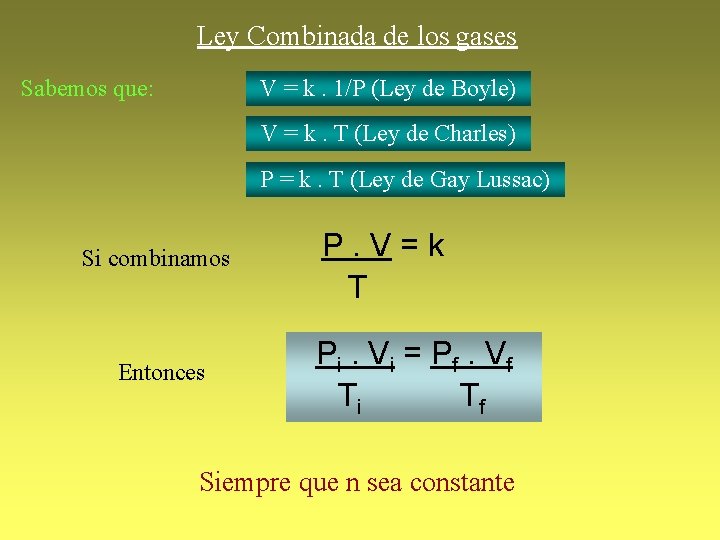
Ley Combinada de los gases V = k. 1/P (Ley de Boyle) Sabemos que: V = k. T (Ley de Charles) P = k. T (Ley de Gay Lussac) Si combinamos Entonces P. V=k T Pi. V i = Pf. V f Ti Tf Siempre que n sea constante

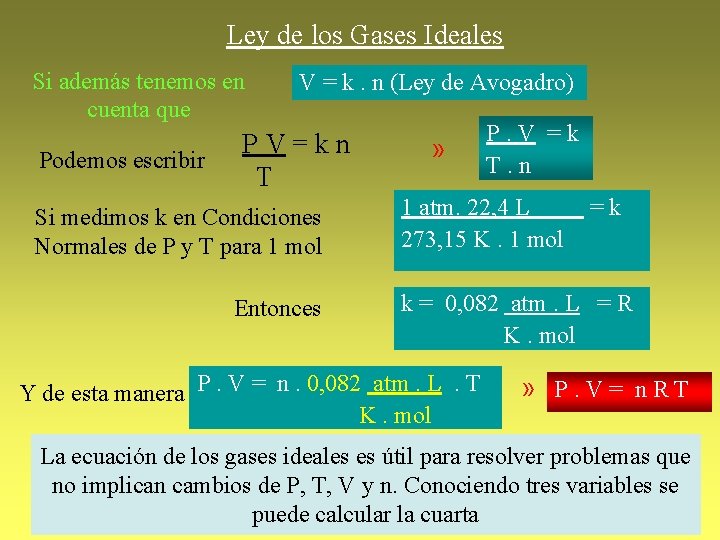
Ley de los Gases Ideales Si además tenemos en cuenta que Podemos escribir V = k. n (Ley de Avogadro) PV=kn T Si medimos k en Condiciones Normales de P y T para 1 mol Entonces » P. V =k T. n 1 atm. 22, 4 L 273, 15 K. 1 mol =k k = 0, 082 atm. L = R K. mol Y de esta manera P. V = n. 0, 082 atm. L. T K. mol » P. V= n. RT La ecuación de los gases ideales es útil para resolver problemas que no implican cambios de P, T, V y n. Conociendo tres variables se puede calcular la cuarta

Veamos un ejemplo El hexafluoruro de azufre es un gas incoloro e inodoro muy poco reactivo. Calcule la presión (en atm) ejercida por 1, 82 moles de dicho gas contenido en un recipiente de acero de 5, 43 L de volumen a 69, 5 °C. Datos n = 1, 82 moles V = 5, 43 L T = 69, 5°C = 342, 5 K Aplicando la ecuación P. V= n. RT P = n. RT V P = (1, 82 moles. 0, 082 atm L. 342, 5 K ) / 5, 43 L K. mol P = 9, 41 atm Rta: P = 9, 41 atm

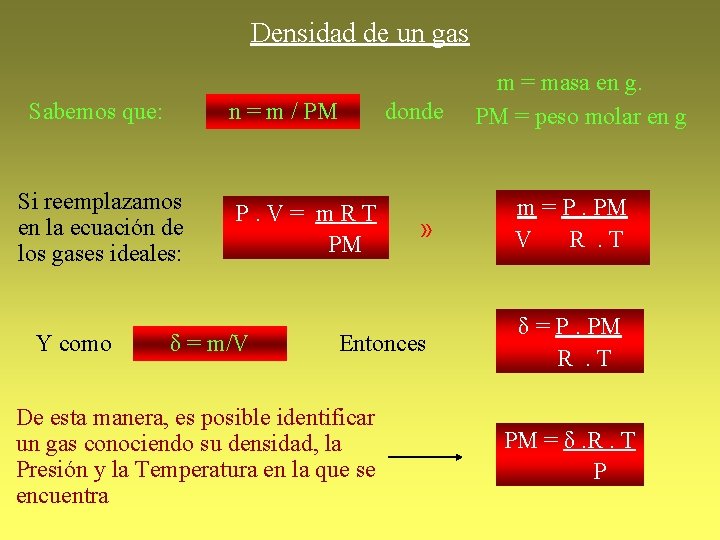
Densidad de un gas n = m / PM Sabemos que: Si reemplazamos en la ecuación de los gases ideales: Y como donde P. V= m. RT PM δ = m/V » Entonces De esta manera, es posible identificar un gas conociendo su densidad, la Presión y la Temperatura en la que se encuentra m = masa en g. PM = peso molar en g m = P. PM V R. T δ = P. PM R. T PM = δ. R. T P

Veamos un ejemplo Un químico ha sintetizado un compuesto gaseoso amarillo verdoso a partir de cloro y oxigeno, y encuentra que su densidad es 7, 71 gr / L a 36 °C y 2, 895 atm. Calcule el PM del compuesto y determine su formula molecular. Datos δ = 7, 71 gr/ L P = 2, 895 atm T = 36 °C = 309 K Aplicando PM = δ. R. T P PM = (7, 71 gr/L. 0, 082 atm L. 309 K) 2, 895 atm K. mol PM = 67, 48 g / mol Entonces 1 mol de Cl + 2 moles de O = 67, 45 gr / mol Rta: Cl. O 2

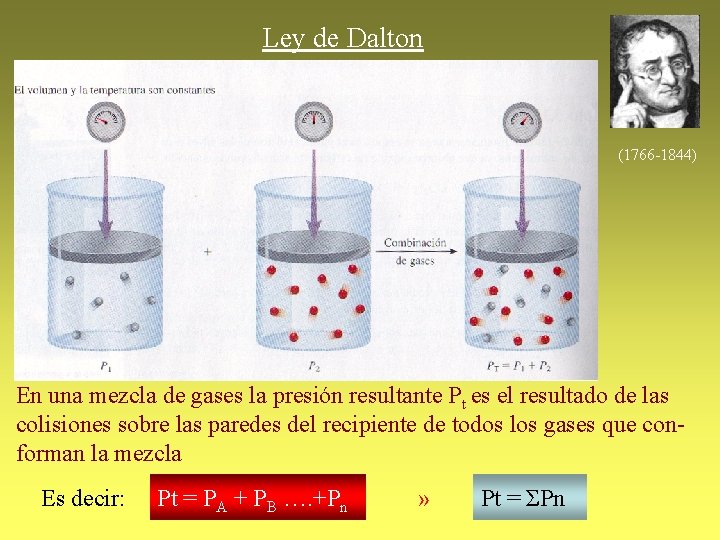
Ley de Dalton (1766 -1844) En una mezcla de gases la presión resultante Pt es el resultado de las colisiones sobre las paredes del recipiente de todos los gases que conforman la mezcla Es decir: Pt = PA + PB …. +Pn » Pt = ΣPn

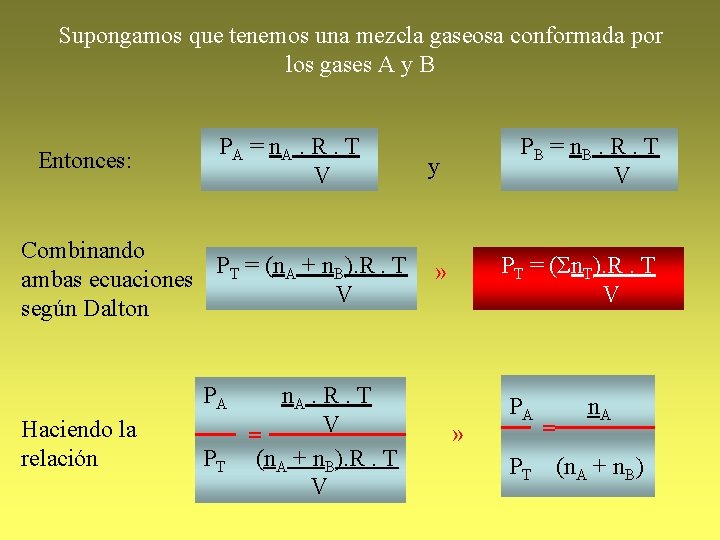
Supongamos que tenemos una mezcla gaseosa conformada por los gases A y B Entonces: P A = n. A. R. T V Combinando PT = (n. A + n. B). R. T ambas ecuaciones V según Dalton PA Haciendo la relación PT n. A. R. T V = (n. A + n. B). R. T V P B = n. B. R. T V y PT = (Σn. T). R. T V » » PA PT = n. A (n. A + n. B)

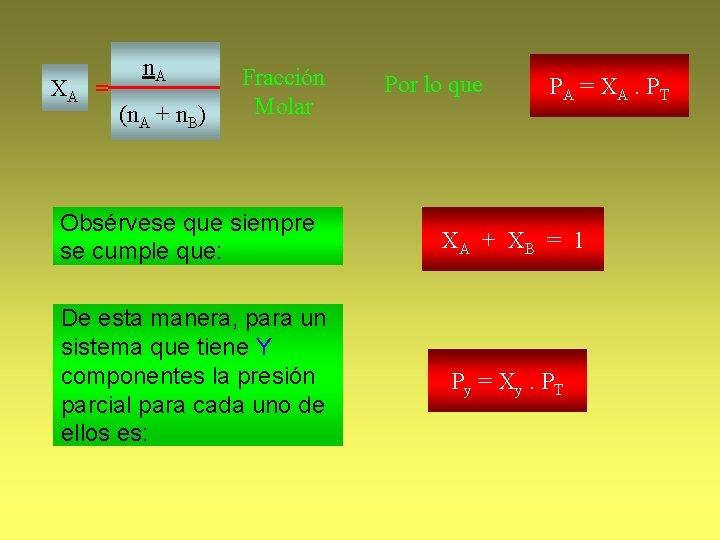
XA = n. A (n. A + n. B) Fracción Molar Por lo que PA = X A. PT Obsérvese que siempre se cumple que: XA + X B = 1 De esta manera, para un sistema que tiene Y componentes la presión parcial para cada uno de ellos es: Py = Xy. PT

Veamos un ejemplo Una mezcla gaseosa contiene 4. 46 moles de Ne, 0, 74 moles de Ar y 2, 15 moles de Xe. Calcule las presiones parciales de cada gas en la mezcla si la presión total del sistema es de 2, 00 atm a una dada temperatura n. A Datos XA = Utilizando n Ne = 4, 46 (n. A + n. B) n Ar = 0, 74 n Xe = 2, 14 n totales = 7, 34 XNe = 0, 6076 XAr = 0, 1008 XXe = 0, 2916 Pt = 2, 00 atm Pp. Ne = 1, 2152 atm Y aplicando Px = Xx. PT Se tiene que Pp. Ar = 0, 2016 atm Pp. Xe = 0, 5832 atm

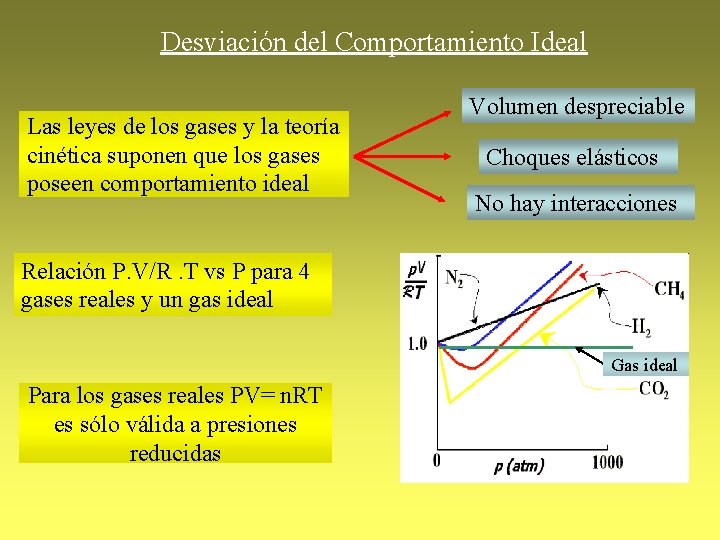
Desviación del Comportamiento Ideal Las leyes de los gases y la teoría cinética suponen que los gases poseen comportamiento ideal Volumen despreciable Choques elásticos No hay interacciones Relación P. V/R. T vs P para 4 gases reales y un gas ideal Gas ideal Para los gases reales PV= n. RT es sólo válida a presiones reducidas

Para estudiar el comportamiento de los gases reales con mayor exactitud hay que tener en cuenta las fuerzas intermoleculares y los volúmenes moleculares J. P. Van der Waals Propone una ecuación de estado modificada (P real + a n 2/V 2) (V – n b) = n R T (1837 -1923) Presión corregida Volumen corregido a y b = ctes de proporcionalidad y dependen de cada gas a α a la fuerza de atracción b α al volumen molecular a n 2/V 2 -nb Frecuencia de encuentros entre las moléculas del gas Volumen ocupado por las moléculas del gas

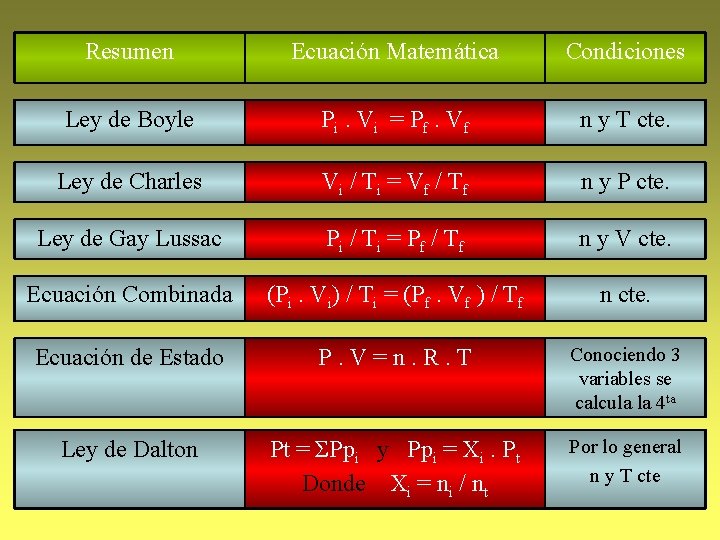
Resumen Ecuación Matemática Condiciones Ley de Boyle Pi. Vi = P f. Vf n y T cte. Ley de Charles Vi / T i = V f / T f n y P cte. Ley de Gay Lussac Pi / T i = P f / T f n y V cte. Ecuación Combinada (Pi. Vi) / Ti = (Pf. Vf ) / Tf n cte. Ecuación de Estado P. V=n. R. T Conociendo 3 variables se calcula la 4 ta Ley de Dalton Pt = ΣPpi y Ppi = Xi. Pt Donde Xi = ni / nt Por lo general n y T cte