TEMA 5 ESPECTROSCOPA ORIGEN DEL PROBLEMA Durante el

TEMA 5 ESPECTROSCOPÍA
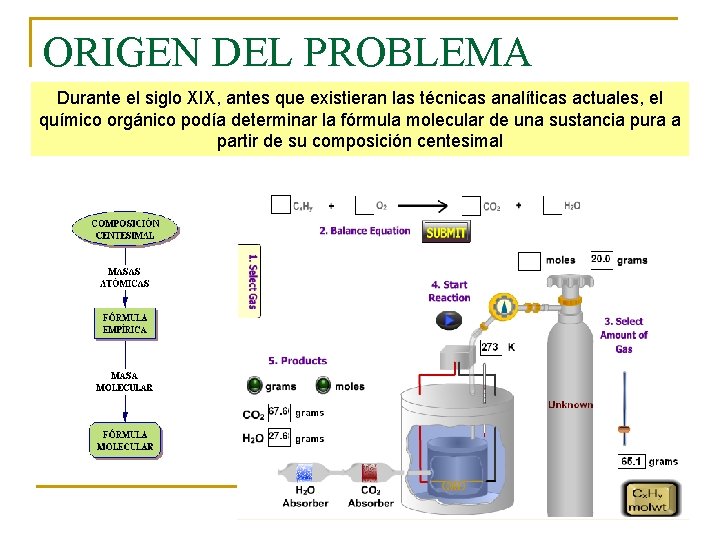
ORIGEN DEL PROBLEMA Durante el siglo XIX, antes que existieran las técnicas analíticas actuales, el químico orgánico podía determinar la fórmula molecular de una sustancia pura a partir de su composición centesimal
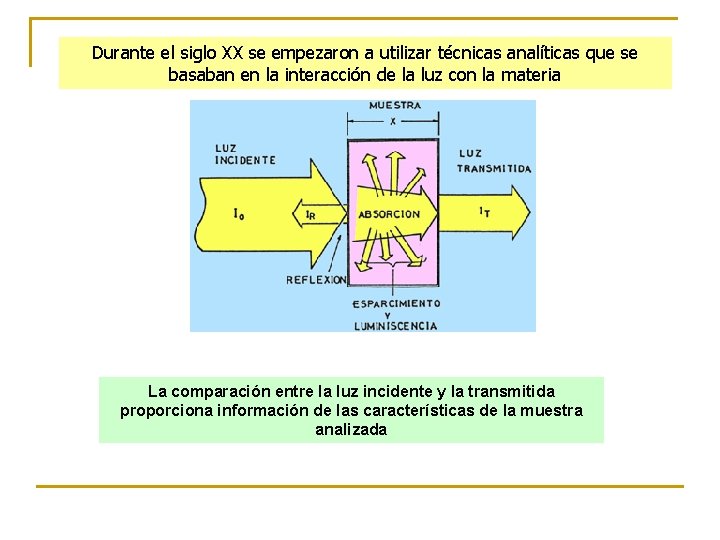
Durante el siglo XX se empezaron a utilizar técnicas analíticas que se basaban en la interacción de la luz con la materia La comparación entre la luz incidente y la transmitida proporciona información de las características de la muestra analizada
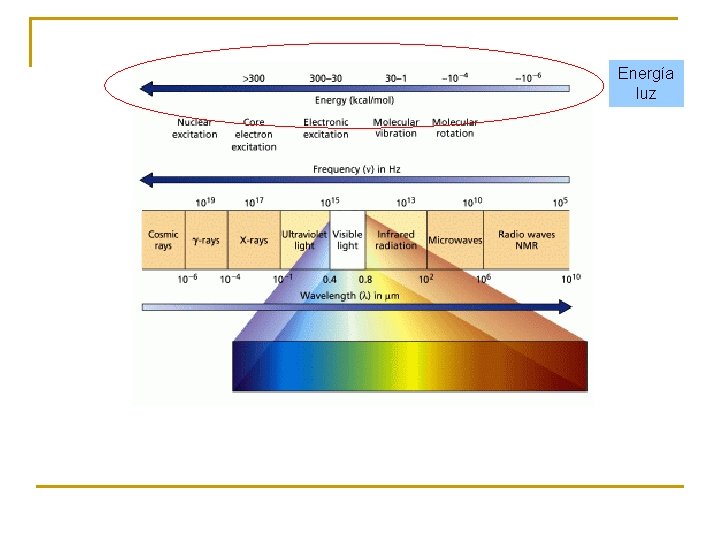
Energía luz
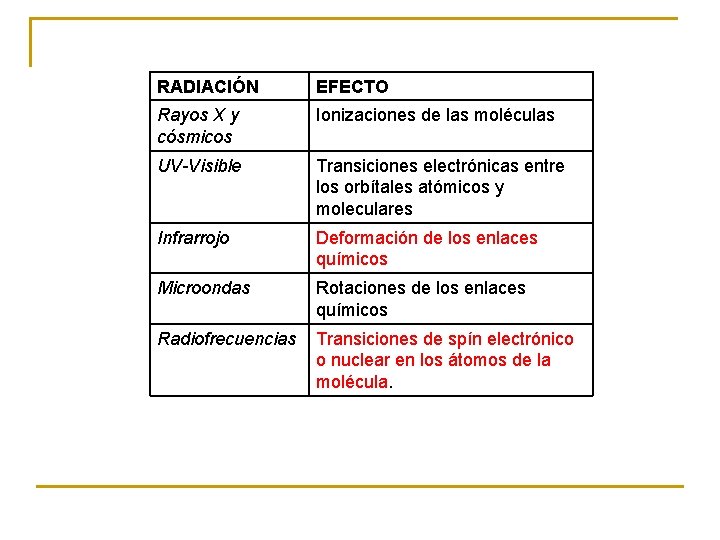
RADIACIÓN EFECTO Rayos X y cósmicos Ionizaciones de las moléculas UV-Visible Transiciones electrónicas entre los orbítales atómicos y moleculares Infrarrojo Deformación de los enlaces químicos Microondas Rotaciones de los enlaces químicos Radiofrecuencias Transiciones de spín electrónico o nuclear en los átomos de la molécula.
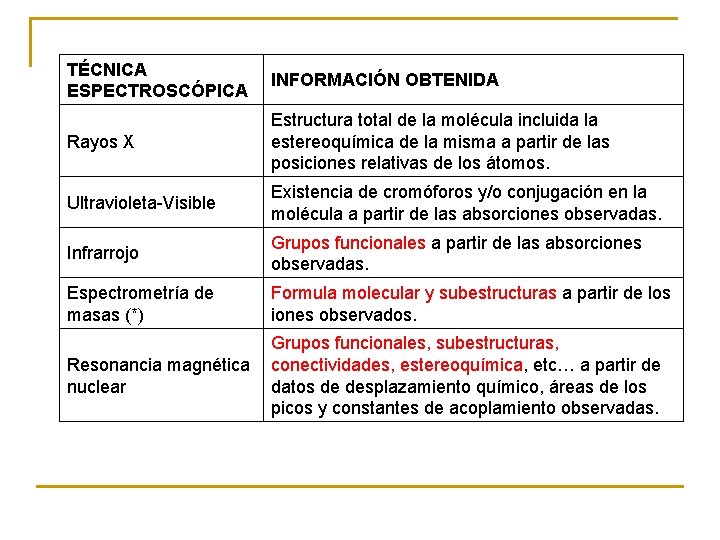
TÉCNICA ESPECTROSCÓPICA INFORMACIÓN OBTENIDA Rayos X Estructura total de la molécula incluida la estereoquímica de la misma a partir de las posiciones relativas de los átomos. Ultravioleta-Visible Existencia de cromóforos y/o conjugación en la molécula a partir de las absorciones observadas. Infrarrojo Grupos funcionales a partir de las absorciones observadas. Espectrometría de masas (*) Formula molecular y subestructuras a partir de los iones observados. Grupos funcionales, subestructuras, Resonancia magnética conectividades, estereoquímica, etc… a partir de datos de desplazamiento químico, áreas de los nuclear picos y constantes de acoplamiento observadas.
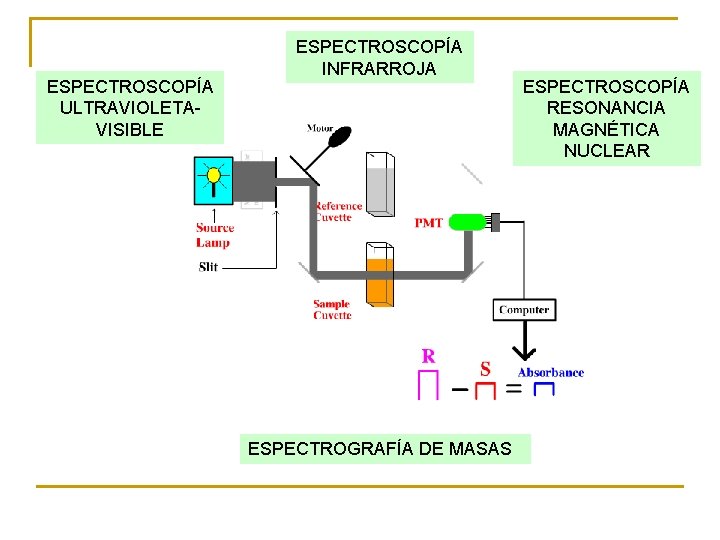
ESPECTROSCOPÍA ULTRAVIOLETAVISIBLE ESPECTROSCOPÍA INFRARROJA ESPECTROGRAFÍA DE MASAS ESPECTROSCOPÍA RESONANCIA MAGNÉTICA NUCLEAR

ESPECTRO DE MASAS
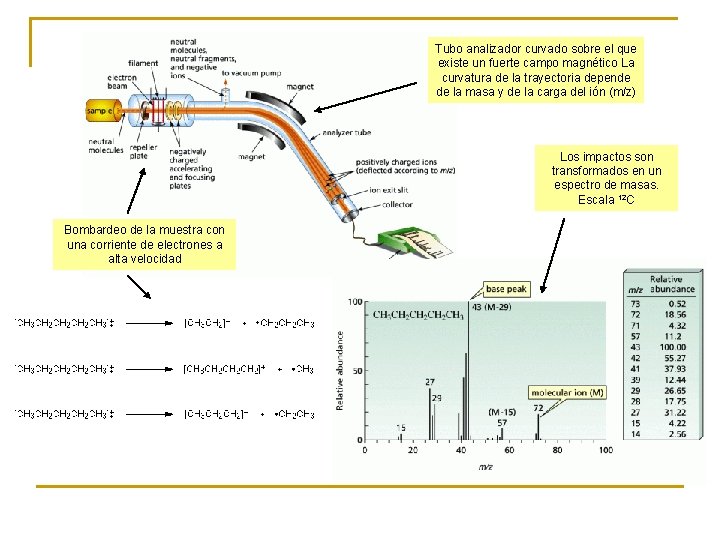
Tubo analizador curvado sobre el que existe un fuerte campo magnético La curvatura de la trayectoria depende de la masa y de la carga del ión (m/z) Los impactos son transformados en un espectro de masas. Escala 12 C Bombardeo de la muestra con una corriente de electrones a alta velocidad
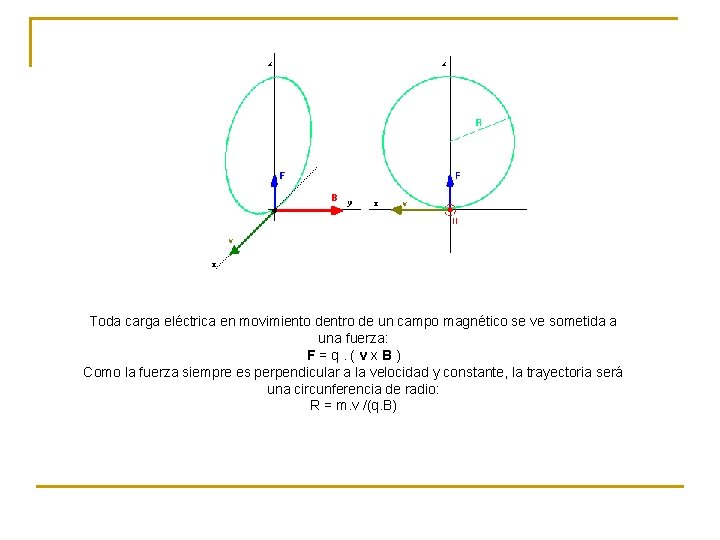
Toda carga eléctrica en movimiento dentro de un campo magnético se ve sometida a una fuerza: F = q. ( v x B ) Como la fuerza siempre es perpendicular a la velocidad y constante, la trayectoria será una circunferencia de radio: R = m. v /(q. B)
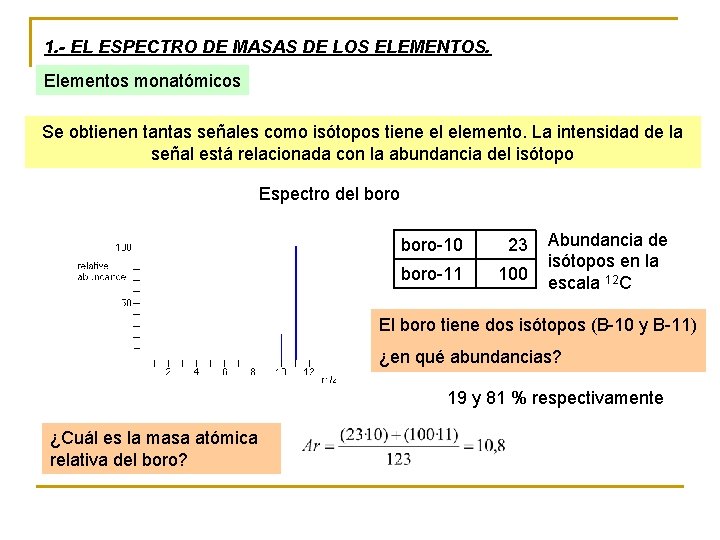
1. - EL ESPECTRO DE MASAS DE LOS ELEMENTOS. Elementos monatómicos Se obtienen tantas señales como isótopos tiene el elemento. La intensidad de la señal está relacionada con la abundancia del isótopo Espectro del boro-10 23 boro-11 100 Abundancia de isótopos en la escala 12 C El boro tiene dos isótopos (B-10 y B-11) ¿en qué abundancias? 19 y 81 % respectivamente ¿Cuál es la masa atómica relativa del boro?
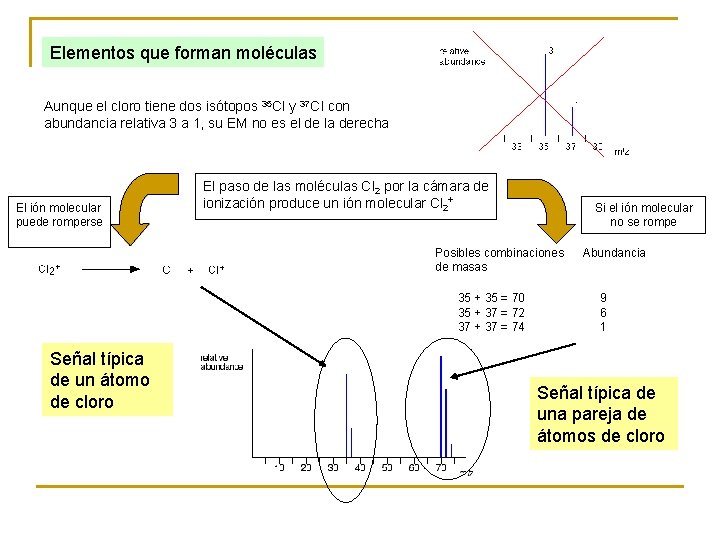
Elementos que forman moléculas Aunque el cloro tiene dos isótopos 35 Cl y 37 Cl con abundancia relativa 3 a 1, su EM no es el de la derecha El ión molecular puede romperse El paso de las moléculas Cl 2 por la cámara de ionización produce un ión molecular Cl 2+ Si el ión molecular no se rompe Posibles combinaciones de masas 35 + 35 = 70 35 + 37 = 72 37 + 37 = 74 Señal típica de un átomo de cloro Abundancia 9 6 1 Señal típica de una pareja de átomos de cloro
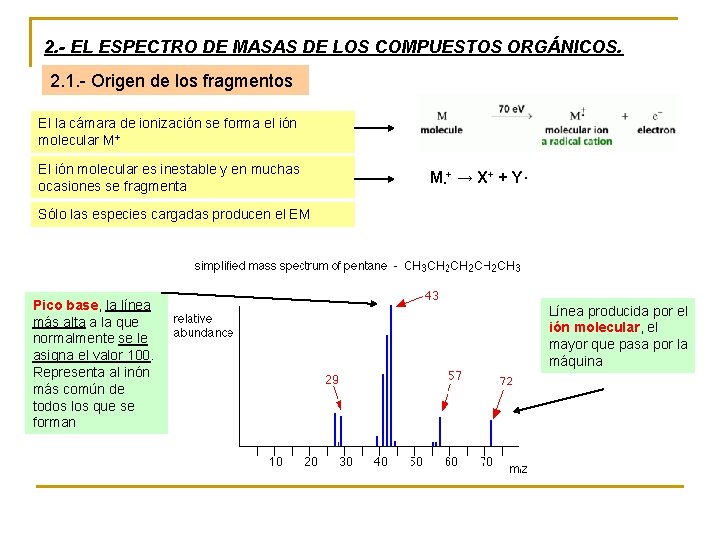
2. - EL ESPECTRO DE MASAS DE LOS COMPUESTOS ORGÁNICOS. 2. 1. - Origen de los fragmentos El la cámara de ionización se forma el ión molecular M+ El ión molecular es inestable y en muchas ocasiones se fragmenta M·+ → X+ + Y· Sólo las especies cargadas producen el EM Pico base, la línea más alta a la que normalmente se le asigna el valor 100. Representa al inón más común de todos los que se forman Línea producida por el ión molecular, el mayor que pasa por la máquina
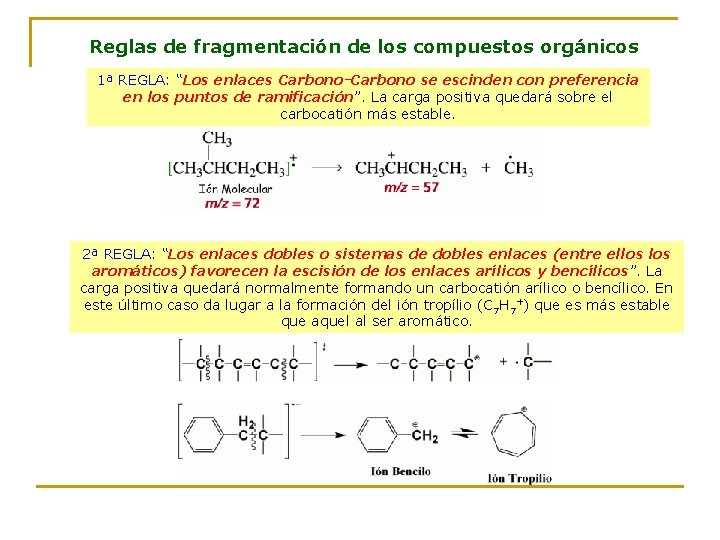
Reglas de fragmentación de los compuestos orgánicos 1ª REGLA: “Los enlaces Carbono-Carbono se escinden con preferencia en los puntos de ramificación”. La carga positiva quedará sobre el carbocatión más estable. 2ª REGLA: “Los enlaces dobles o sistemas de dobles enlaces (entre ellos aromáticos) favorecen la escisión de los enlaces arílicos y bencílicos”. La carga positiva quedará normalmente formando un carbocatión arílico o bencílico. En este último caso da lugar a la formación del ión tropílio (C 7 H 7+) que es más estable que aquel al ser aromático.
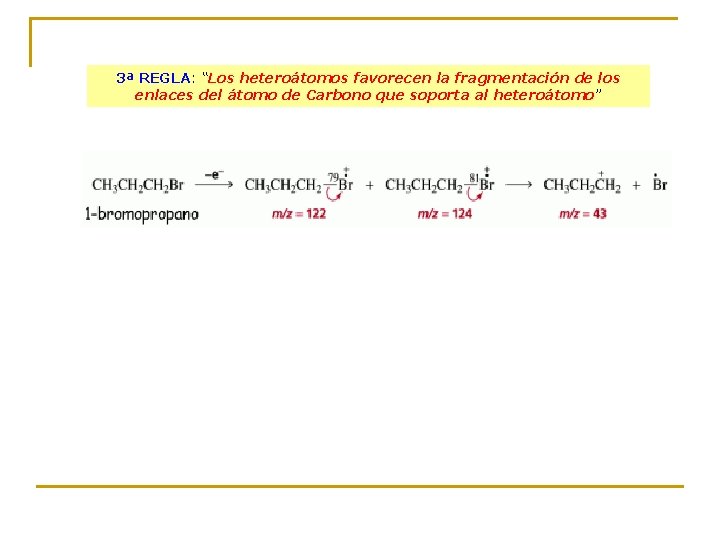
3ª REGLA: “Los heteroátomos favorecen la fragmentación de los enlaces del átomo de Carbono que soporta al heteroátomo”
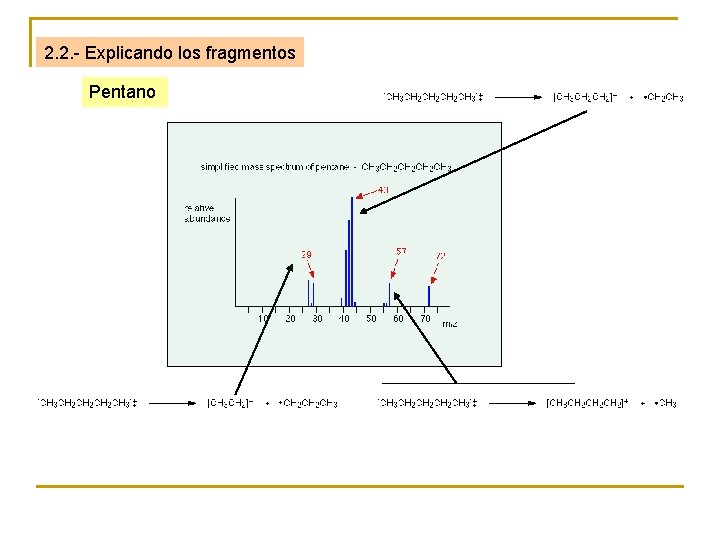
2. 2. - Explicando los fragmentos Pentano
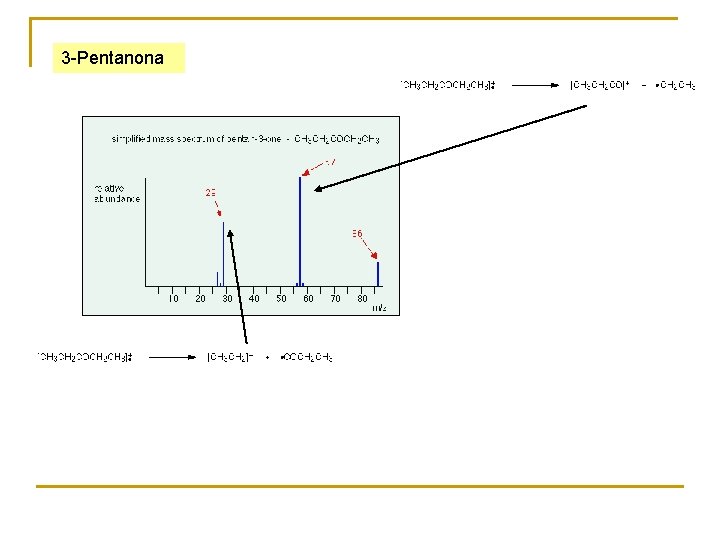
3 -Pentanona
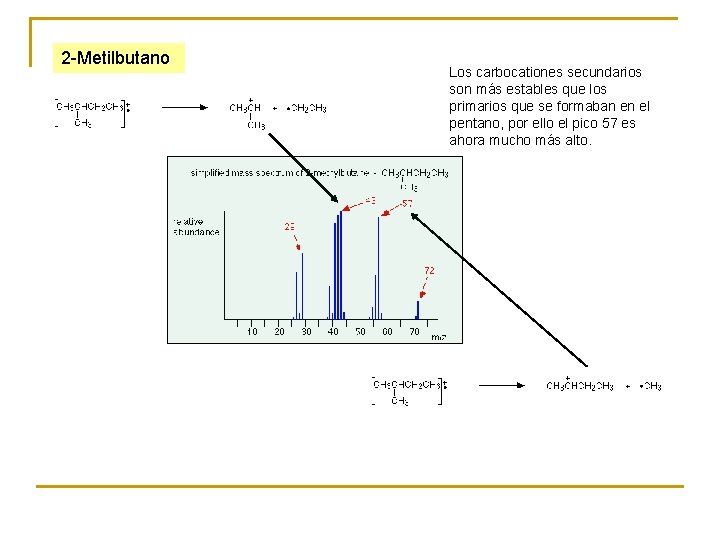
2 -Metilbutano Los carbocationes secundarios son más estables que los primarios que se formaban en el pentano, por ello el pico 57 es ahora mucho más alto.
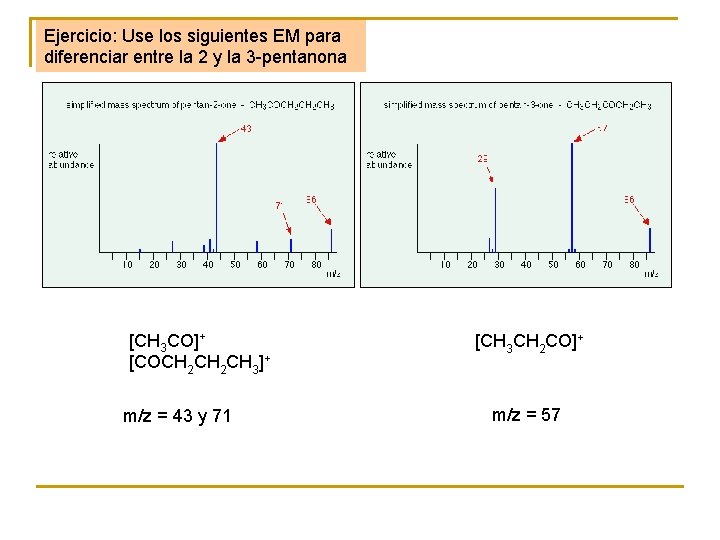
Ejercicio: Use los siguientes EM para diferenciar entre la 2 y la 3 -pentanona [CH 3 CO]+ [COCH 2 CH 3]+ m/z = 43 y 71 [CH 3 CH 2 CO]+ m/z = 57
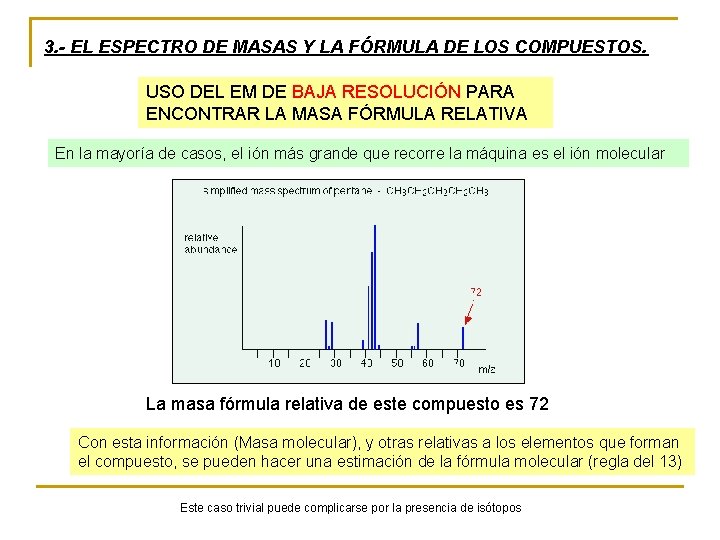
3. - EL ESPECTRO DE MASAS Y LA FÓRMULA DE LOS COMPUESTOS. USO DEL EM DE BAJA RESOLUCIÓN PARA ENCONTRAR LA MASA FÓRMULA RELATIVA En la mayoría de casos, el ión más grande que recorre la máquina es el ión molecular La masa fórmula relativa de este compuesto es 72 Con esta información (Masa molecular), y otras relativas a los elementos que forman el compuesto, se pueden hacer una estimación de la fórmula molecular (regla del 13) Este caso trivial puede complicarse por la presencia de isótopos
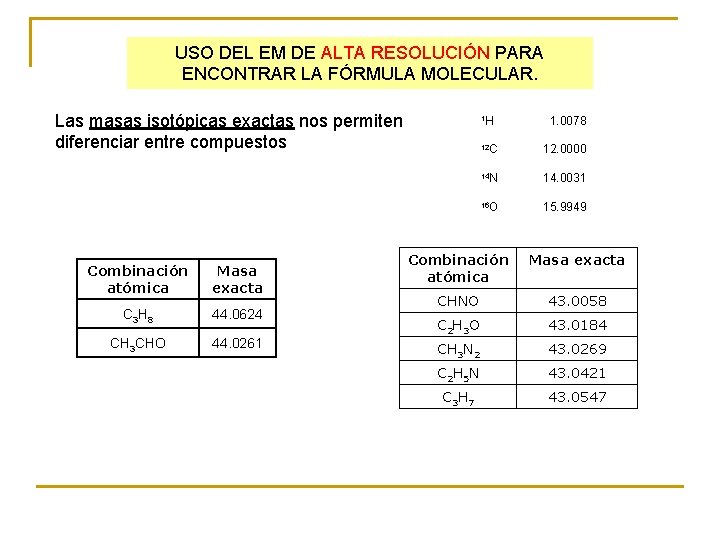
USO DEL EM DE ALTA RESOLUCIÓN PARA ENCONTRAR LA FÓRMULA MOLECULAR. Las masas isotópicas exactas nos permiten diferenciar entre compuestos Combinación atómica Masa exacta C 3 H 8 44. 0624 CH 3 CHO 44. 0261 1 H 1. 0078 12 C 12. 0000 14 N 14. 0031 16 O 15. 9949 Combinación atómica Masa exacta CHNO 43. 0058 C 2 H 3 O 43. 0184 CH 3 N 2 43. 0269 C 2 H 5 N 43. 0421 C 3 H 7 43. 0547
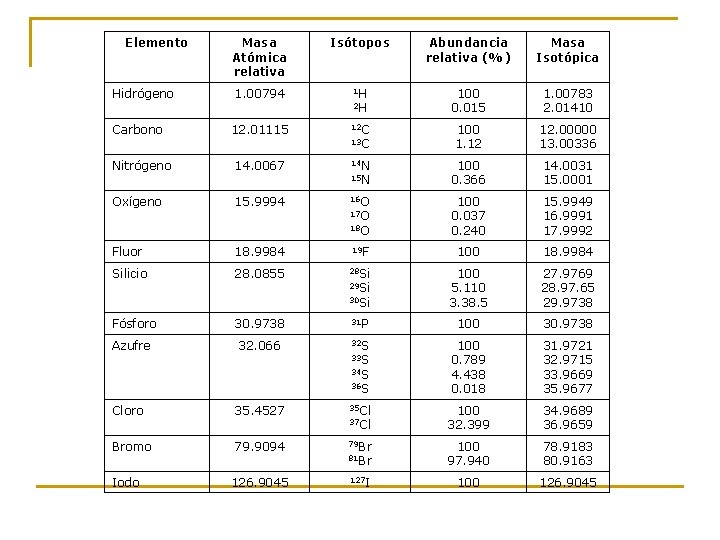
Elemento Masa Atómica relativa Isótopos Abundancia relativa (%) Masa Isotópica 1. 00794 1 H 100 0. 015 1. 00783 2. 01410 12. 01115 12 C 100 1. 12 12. 00000 13. 00336 Nitrógeno 14. 0067 14 N 100 0. 366 14. 0031 15. 0001 Oxígeno 15. 9994 16 O 17 O 18 O 100 0. 037 0. 240 15. 9949 16. 9991 17. 9992 Hidrógeno Carbono 2 H 13 C 15 N Fluor 18. 9984 19 F 100 18. 9984 Silicio 28. 0855 28 Si 29 Si 30 Si 100 5. 110 3. 38. 5 27. 9769 28. 97. 65 29. 9738 Fósforo 30. 9738 31 P 100 30. 9738 Azufre 32. 066 32 S 100 0. 789 4. 438 0. 018 31. 9721 32. 9715 33. 9669 35. 9677 33 S 34 S 36 S Cloro 35. 4527 35 Cl 100 32. 399 34. 9689 36. 9659 Bromo 79. 9094 79 Br 81 Br 100 97. 940 78. 9183 80. 9163 126. 9045 127 I 100 126. 9045 Iodo 37 Cl
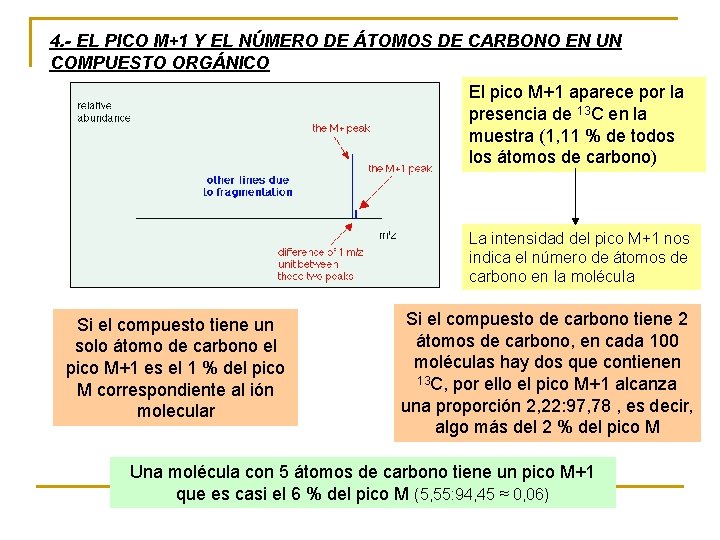
4. - EL PICO M+1 Y EL NÚMERO DE ÁTOMOS DE CARBONO EN UN COMPUESTO ORGÁNICO El pico M+1 aparece por la presencia de 13 C en la muestra (1, 11 % de todos los átomos de carbono) La intensidad del pico M+1 nos indica el número de átomos de carbono en la molécula Si el compuesto tiene un solo átomo de carbono el pico M+1 es el 1 % del pico M correspondiente al ión molecular Si el compuesto de carbono tiene 2 átomos de carbono, en cada 100 moléculas hay dos que contienen 13 C, por ello el pico M+1 alcanza una proporción 2, 22: 97, 78 , es decir, algo más del 2 % del pico M Una molécula con 5 átomos de carbono tiene un pico M+1 que es casi el 6 % del pico M (5, 55: 94, 45 ≈ 0, 06)
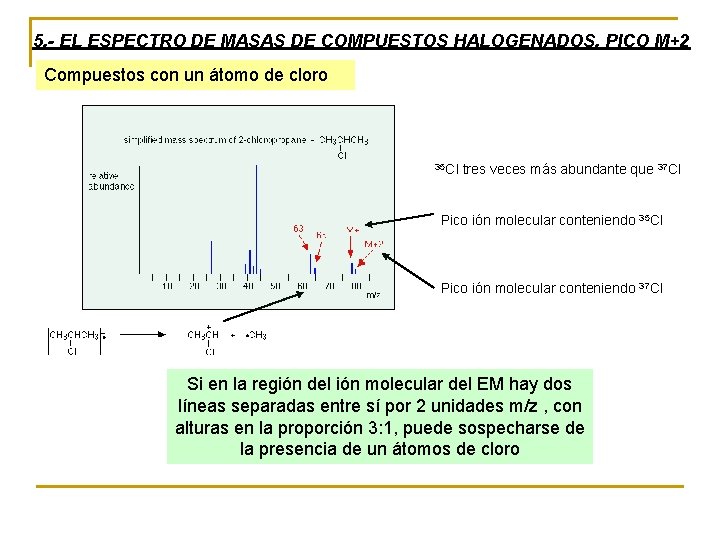
5. - EL ESPECTRO DE MASAS DE COMPUESTOS HALOGENADOS. PICO M+2 Compuestos con un átomo de cloro 35 Cl tres veces más abundante que 37 Cl Pico ión molecular conteniendo 35 Cl Pico ión molecular conteniendo 37 Cl Si en la región del ión molecular del EM hay dos líneas separadas entre sí por 2 unidades m/z , con alturas en la proporción 3: 1, puede sospecharse de la presencia de un átomos de cloro
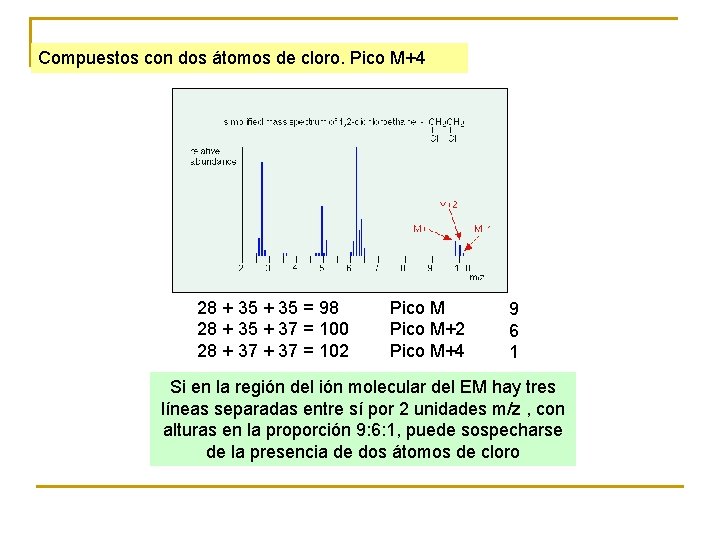
Compuestos con dos átomos de cloro. Pico M+4 28 + 35 = 98 28 + 35 + 37 = 100 28 + 37 = 102 Pico M+2 Pico M+4 9 6 1 Si en la región del ión molecular del EM hay tres líneas separadas entre sí por 2 unidades m/z , con alturas en la proporción 9: 6: 1, puede sospecharse de la presencia de dos átomos de cloro
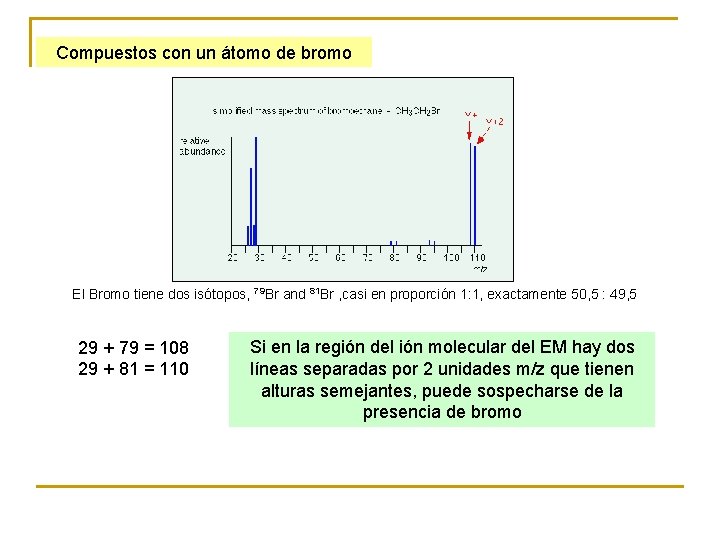
Compuestos con un átomo de bromo El Bromo tiene dos isótopos, 79 Br and 81 Br , casi en proporción 1: 1, exactamente 50, 5 : 49, 5 29 + 79 = 108 29 + 81 = 110 Si en la región del ión molecular del EM hay dos líneas separadas por 2 unidades m/z que tienen alturas semejantes, puede sospecharse de la presencia de bromo
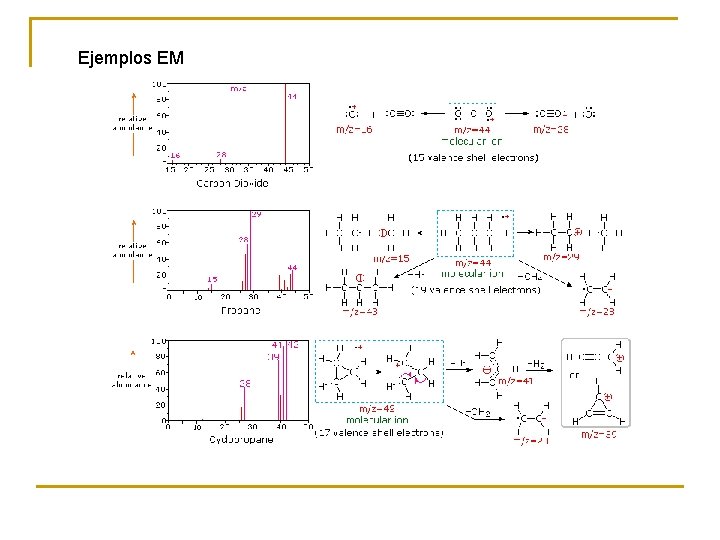
Ejemplos EM
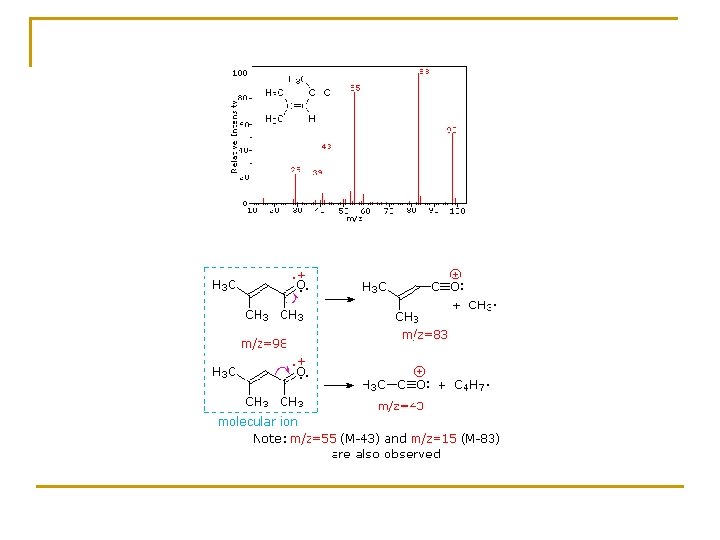
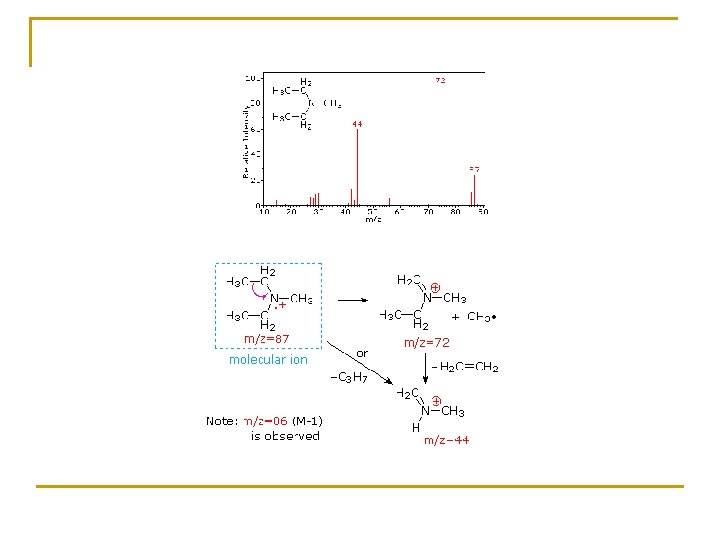
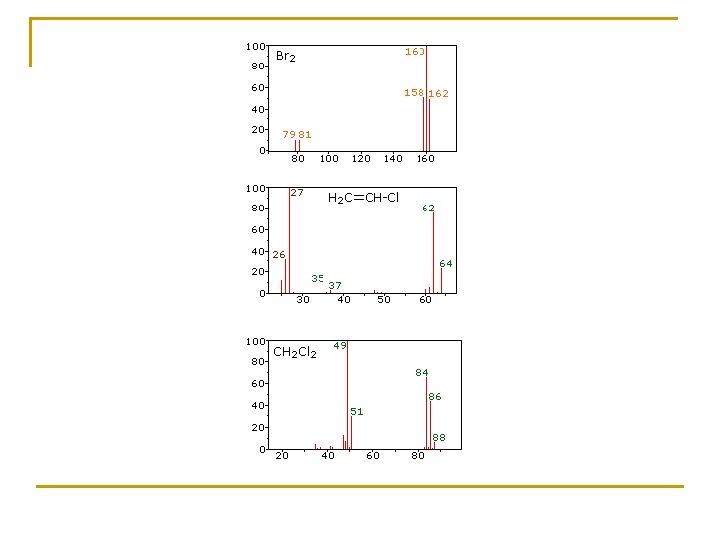

INFRARROJO
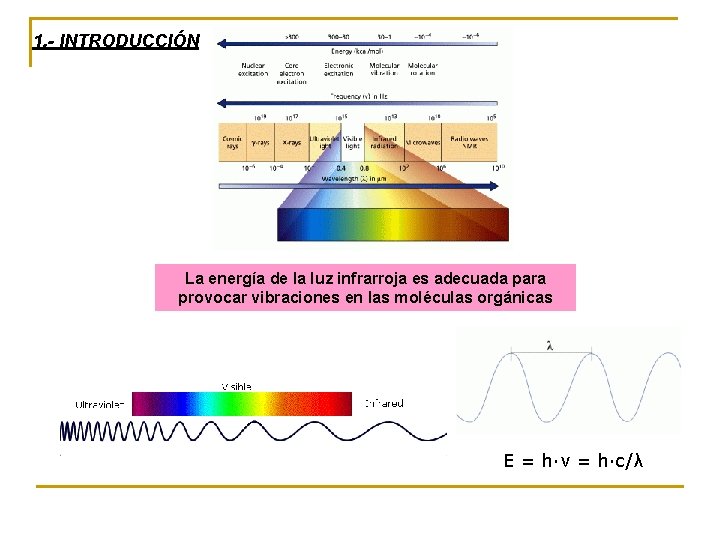
1. - INTRODUCCIÓN La energía de la luz infrarroja es adecuada para provocar vibraciones en las moléculas orgánicas E = h·ν = h·c/λ
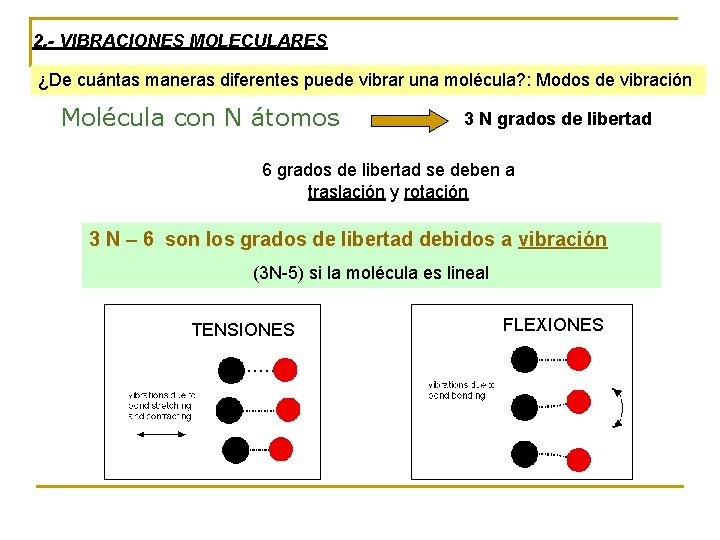
2. - VIBRACIONES MOLECULARES ¿De cuántas maneras diferentes puede vibrar una molécula? : Modos de vibración Molécula con N átomos 3 N grados de libertad 6 grados de libertad se deben a traslación y rotación 3 N – 6 son los grados de libertad debidos a vibración (3 N-5) si la molécula es lineal TENSIONES FLEXIONES
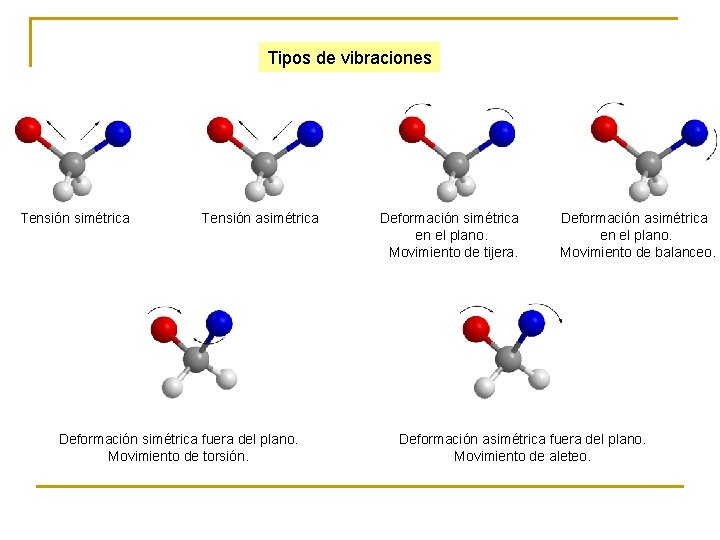
Tipos de vibraciones Tensión simétrica Tensión asimétrica Deformación simétrica fuera del plano. Movimiento de torsión. Deformación simétrica en el plano. Movimiento de tijera. Deformación asimétrica en el plano. Movimiento de balanceo. Deformación asimétrica fuera del plano. Movimiento de aleteo.
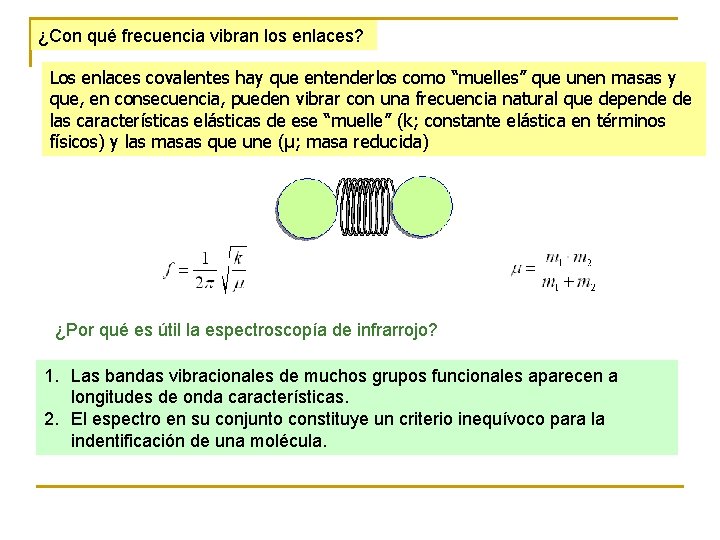
¿Con qué frecuencia vibran los enlaces? Los enlaces covalentes hay que entenderlos como “muelles” que unen masas y que, en consecuencia, pueden vibrar con una frecuencia natural que depende de las características elásticas de ese “muelle” (k; constante elástica en términos físicos) y las masas que une (μ; masa reducida) ¿Por qué es útil la espectroscopía de infrarrojo? 1. Las bandas vibracionales de muchos grupos funcionales aparecen a longitudes de onda características. 2. El espectro en su conjunto constituye un criterio inequívoco para la indentificación de una molécula.
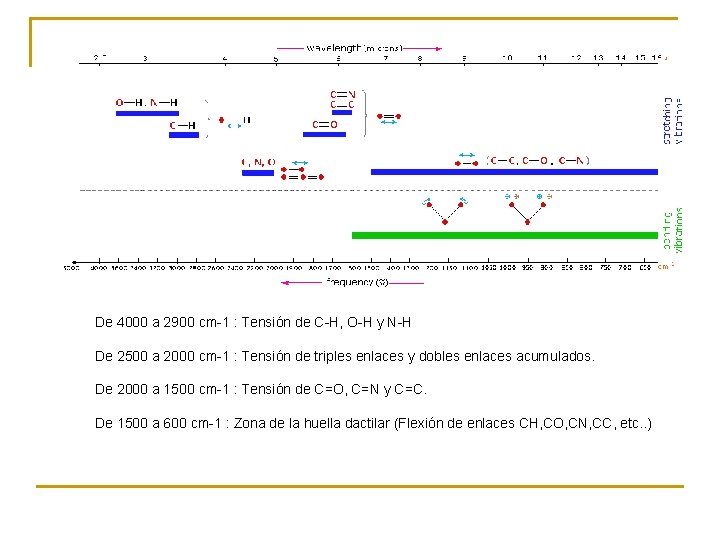
De 4000 a 2900 cm-1 : Tensión de C-H, O-H y N-H De 2500 a 2000 cm-1 : Tensión de triples enlaces y dobles enlaces acumulados. De 2000 a 1500 cm-1 : Tensión de C=O, C=N y C=C. De 1500 a 600 cm-1 : Zona de la huella dactilar (Flexión de enlaces CH, CO, CN, CC, etc. . )
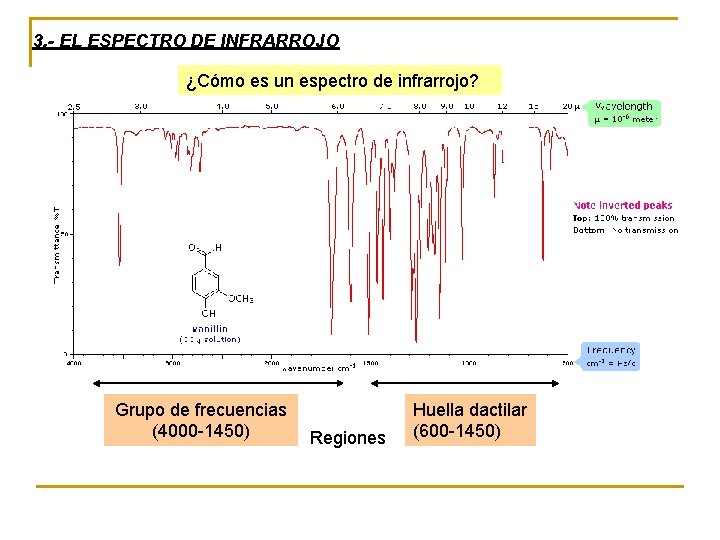
3. - EL ESPECTRO DE INFRARROJO ¿Cómo es un espectro de infrarrojo? Grupo de frecuencias (4000 -1450) Regiones Huella dactilar (600 -1450)
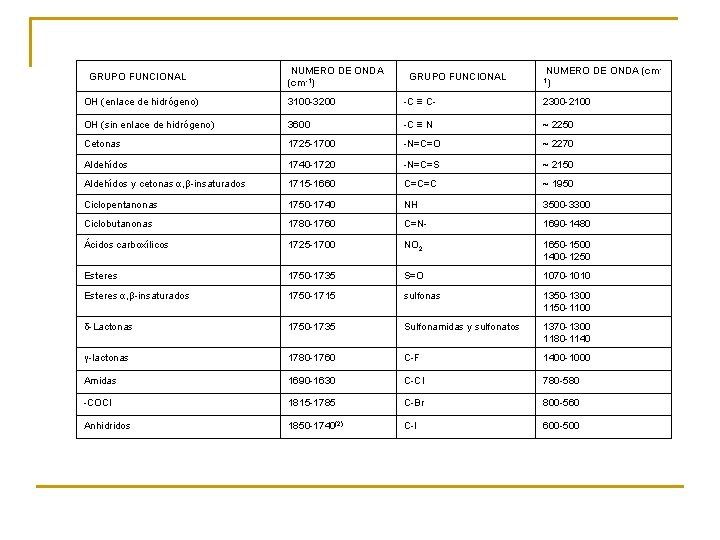
GRUPO FUNCIONAL NUMERO DE ONDA (cm-1) GRUPO FUNCIONAL NUMERO DE ONDA (cm 1) OH (enlace de hidrógeno) 3100 -3200 -C ≡ C- 2300 -2100 OH (sin enlace de hidrógeno) 3600 -C ≡ N ~ 2250 Cetonas 1725 -1700 -N=C=O ~ 2270 Aldehídos 1740 -1720 -N=C=S ~ 2150 Aldehídos y cetonas α, β-insaturados 1715 -1660 C=C=C ~ 1950 Ciclopentanonas 1750 -1740 NH 3500 -3300 Ciclobutanonas 1780 -1760 C=N- 1690 -1480 Ácidos carboxílicos 1725 -1700 NO 2 1650 -1500 1400 -1250 Esteres 1750 -1735 S=O 1070 -1010 Esteres α, β-insaturados 1750 -1715 sulfonas 1350 -1300 1150 -1100 δ-Lactonas 1750 -1735 Sulfonamidas y sulfonatos 1370 -1300 1180 -1140 γ-lactonas 1780 -1760 C-F 1400 -1000 Amidas 1690 -1630 C-Cl 780 -580 -COCl 1815 -1785 C-Br 800 -560 Anhidridos 1850 -1740(2) C-I 600 -500
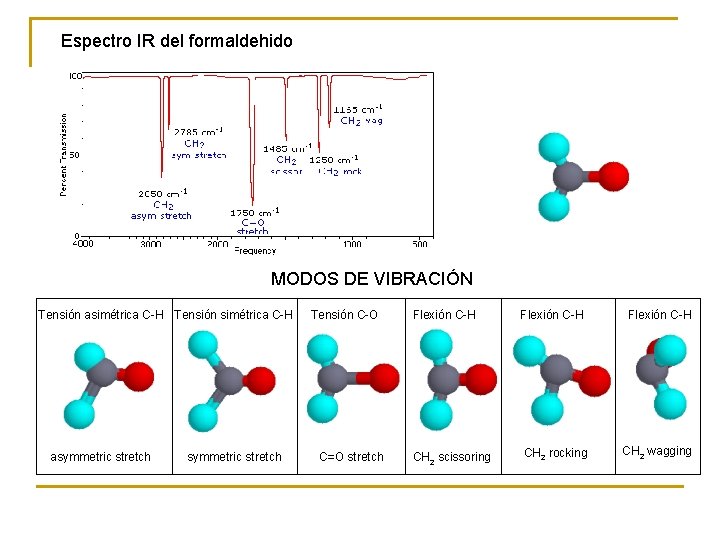
Espectro IR del formaldehido MODOS DE VIBRACIÓN Tensión asimétrica C-H Tensión simétrica C-H asymmetric stretch Tensión C-O C=O stretch Flexión C-H CH 2 scissoring CH 2 rocking Flexión C-H CH 2 wagging
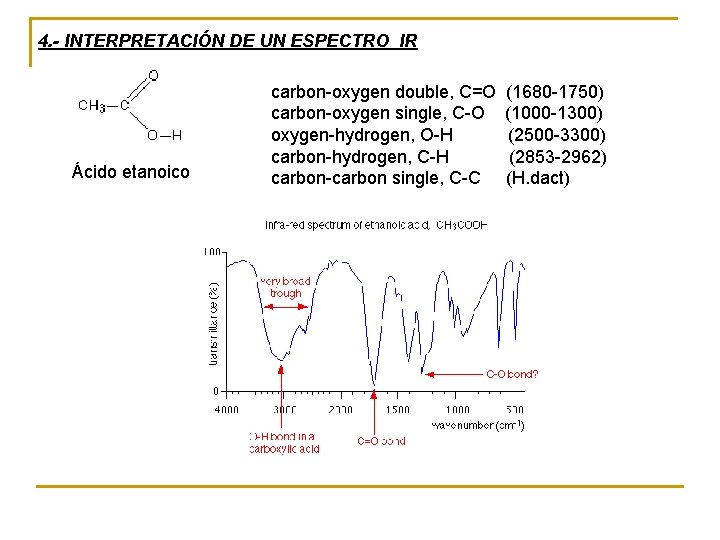
4. - INTERPRETACIÓN DE UN ESPECTRO IR Ácido etanoico carbon-oxygen double, C=O (1680 -1750) carbon-oxygen single, C-O (1000 -1300) oxygen-hydrogen, O-H (2500 -3300) carbon-hydrogen, C-H (2853 -2962) carbon-carbon single, C-C (H. dact)
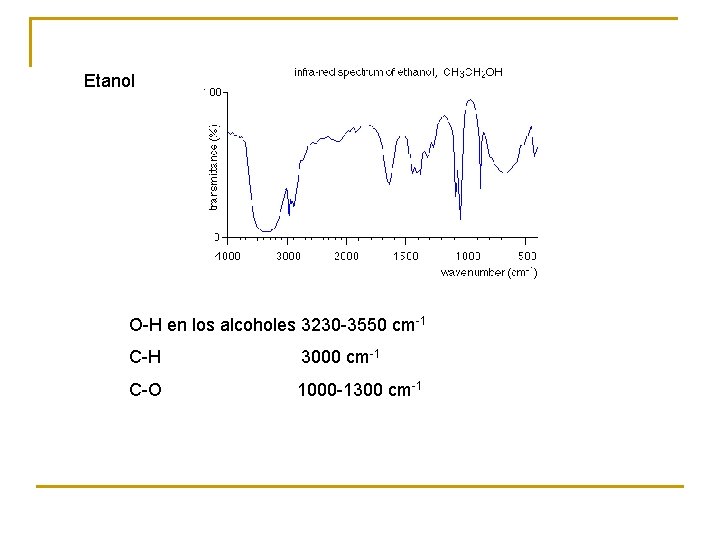
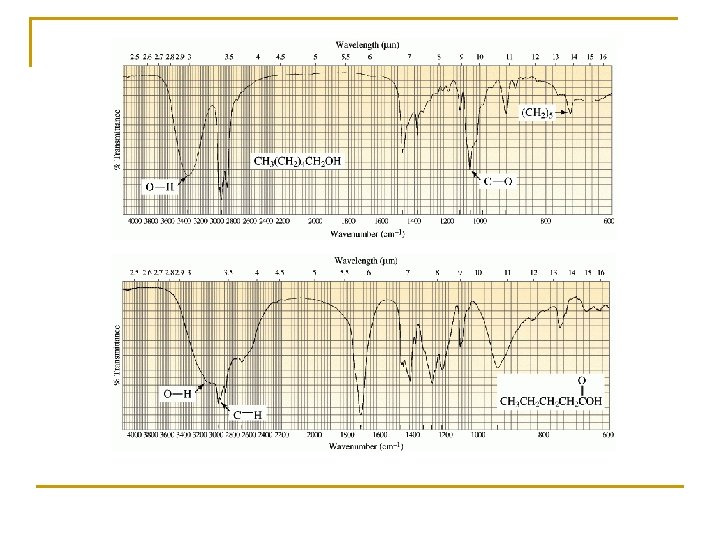
Etanol O-H en los alcoholes 3230 -3550 cm-1 C-H 3000 cm-1 C-O 1000 -1300 cm-1
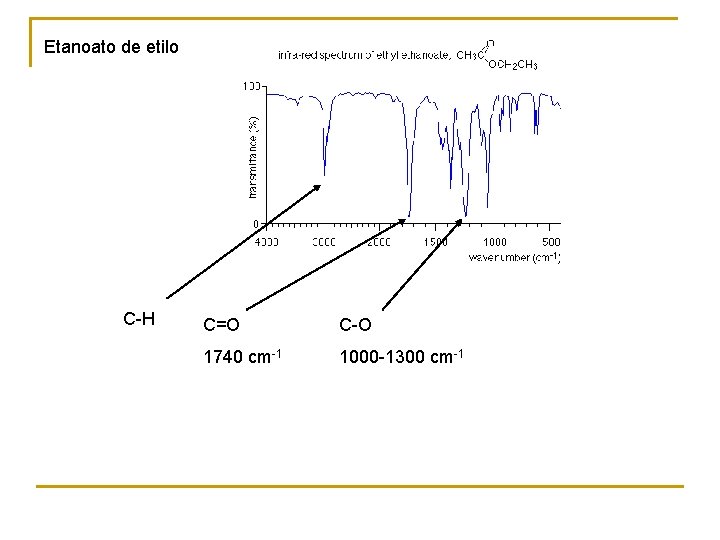
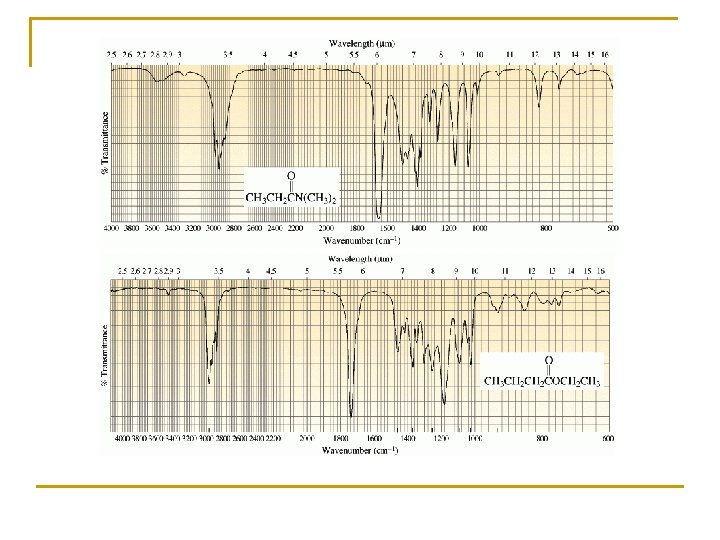
Etanoato de etilo C-H C=O C-O 1740 cm-1 1000 -1300 cm-1
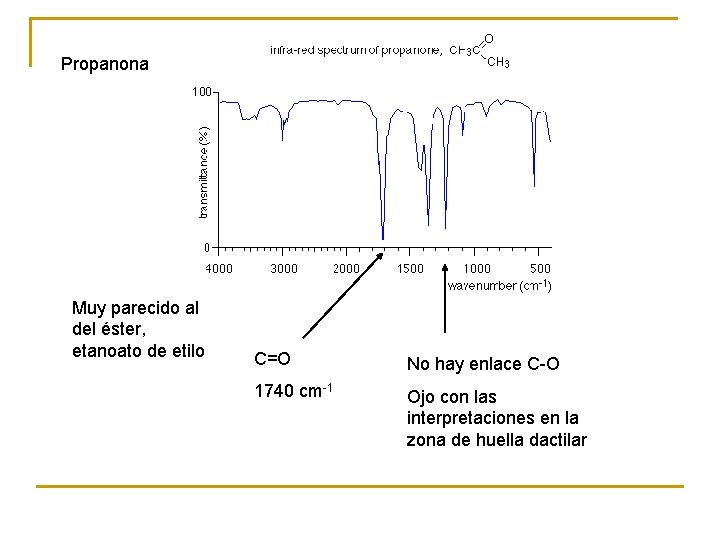
Propanona Muy parecido al del éster, etanoato de etilo C=O No hay enlace C-O 1740 cm-1 Ojo con las interpretaciones en la zona de huella dactilar
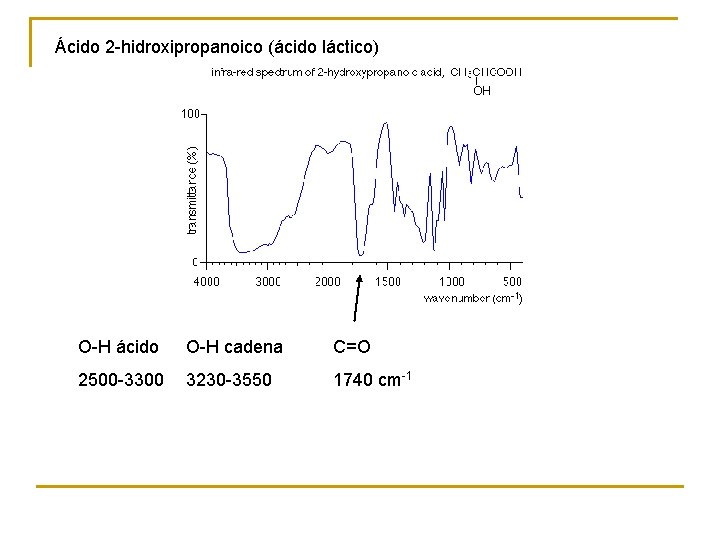
Ácido 2 -hidroxipropanoico (ácido láctico) O-H ácido O-H cadena C=O 2500 -3300 3230 -3550 1740 cm-1
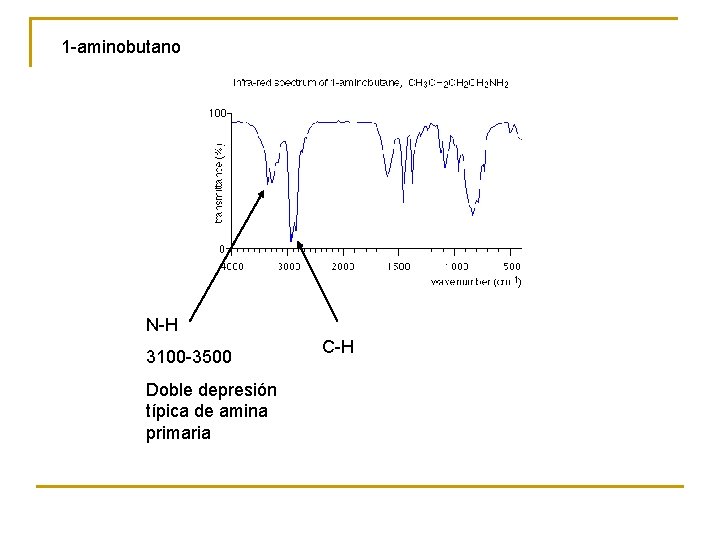
1 -aminobutano N-H 3100 -3500 Doble depresión típica de amina primaria C-H
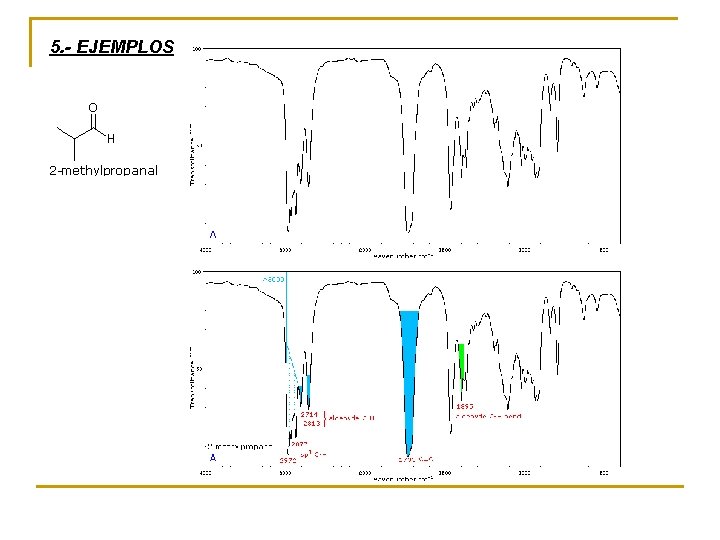
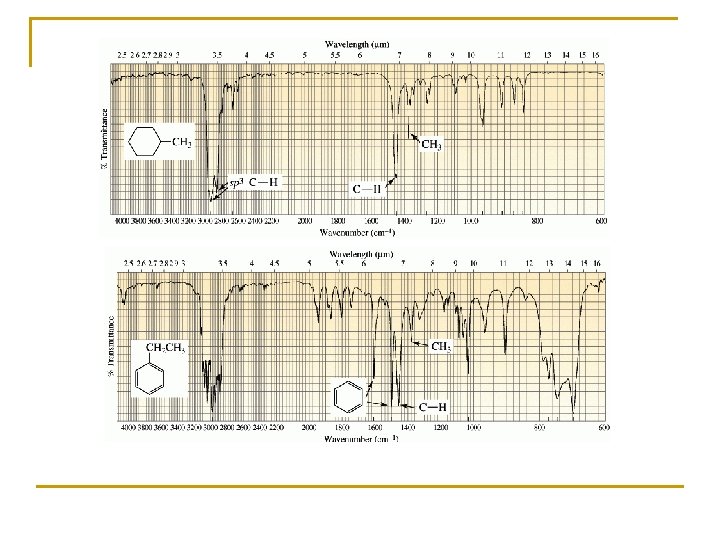
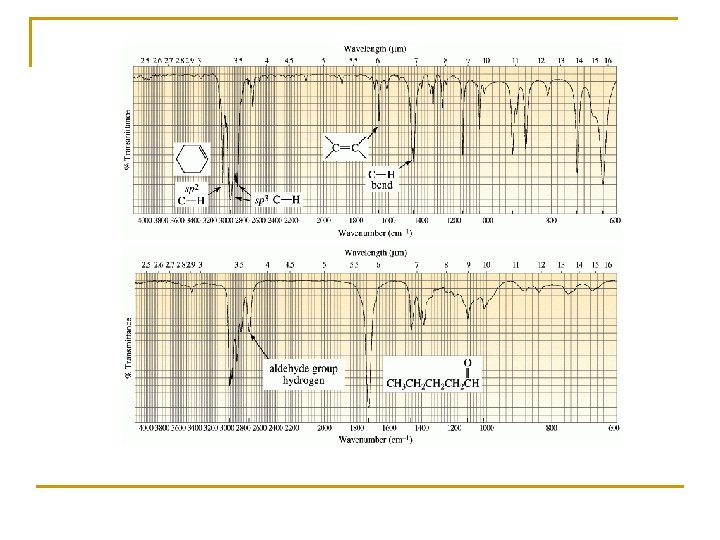
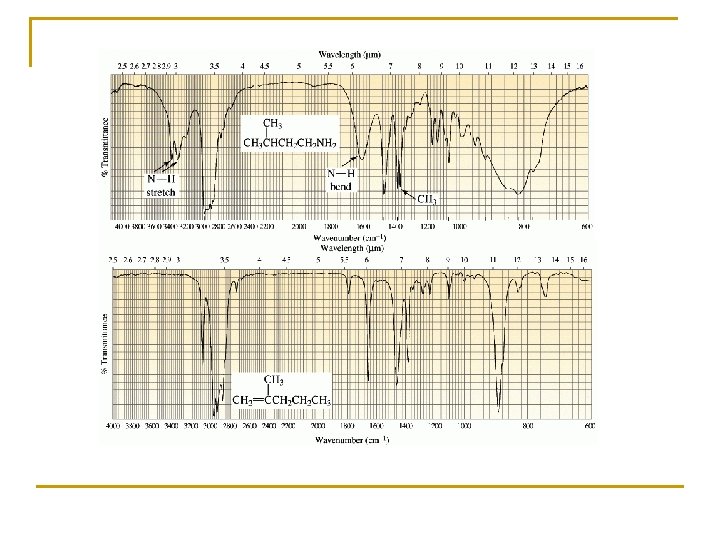
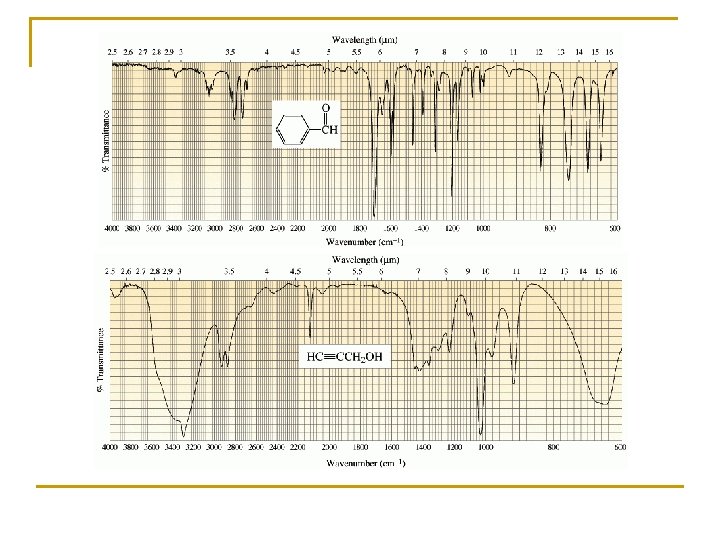
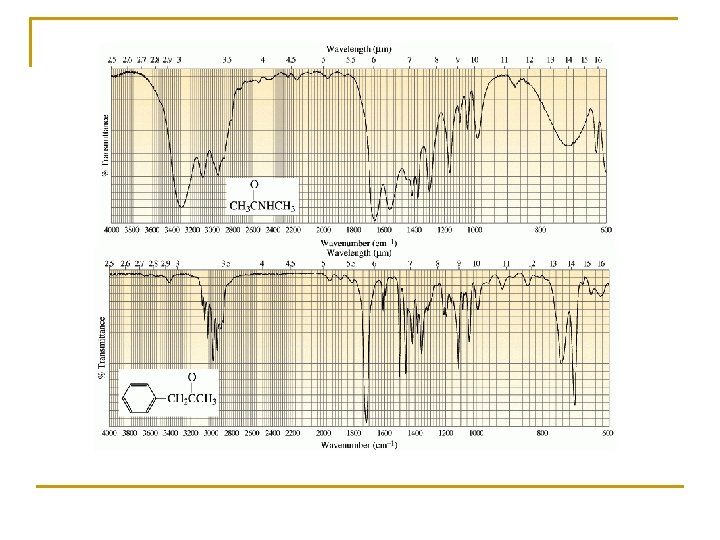
5. - EJEMPLOS
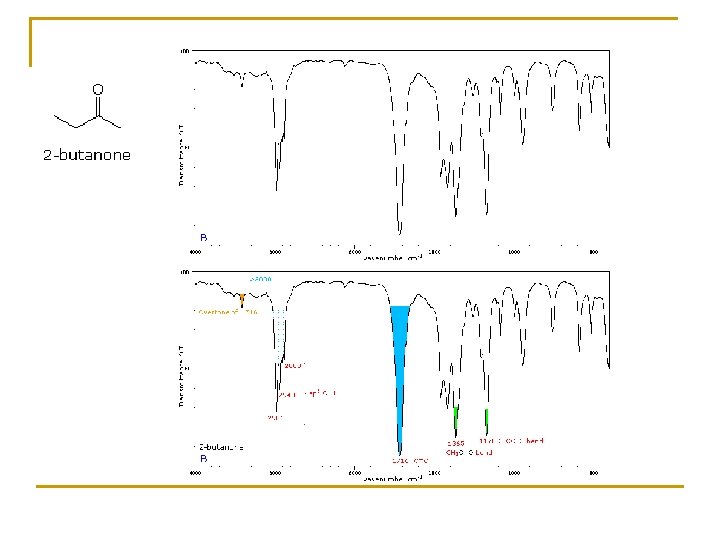
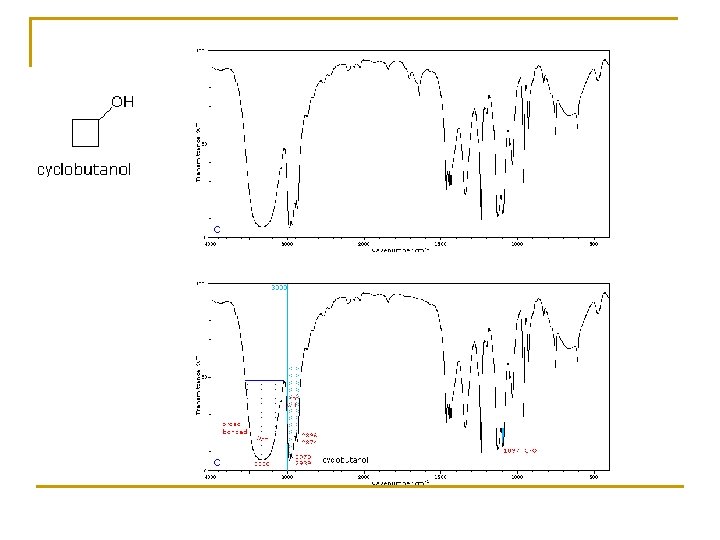
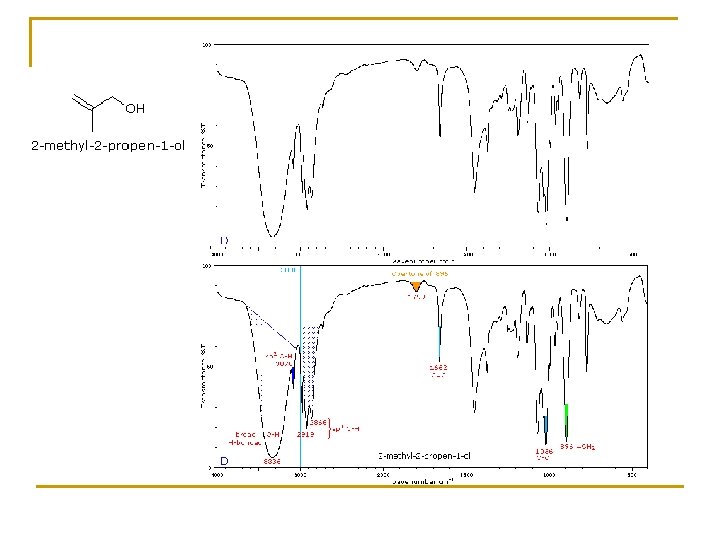
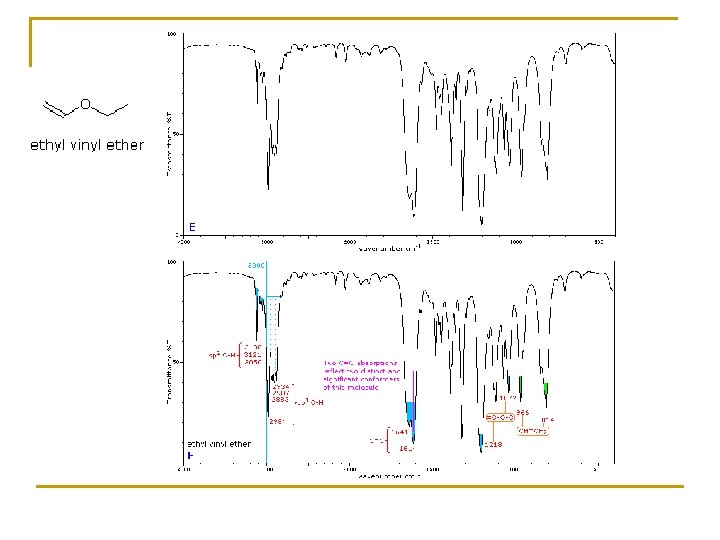
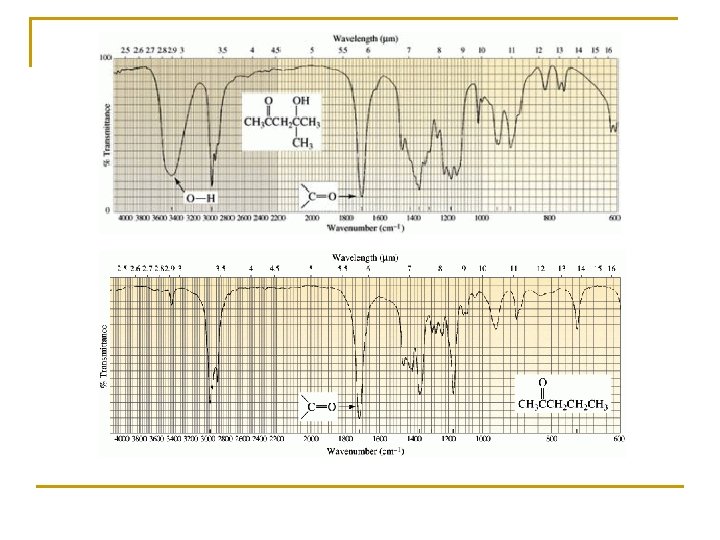

RESONANCIA MAGNÉTICA NUCLEAR
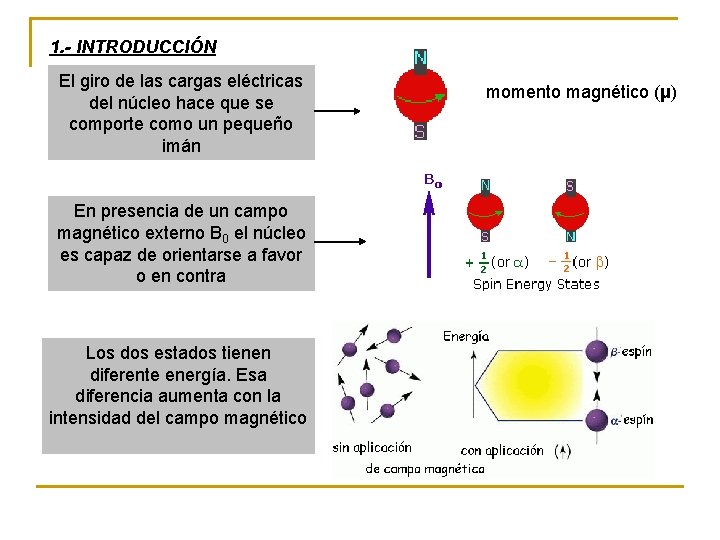
1. - INTRODUCCIÓN El giro de las cargas eléctricas del núcleo hace que se comporte como un pequeño imán En presencia de un campo magnético externo B 0 el núcleo es capaz de orientarse a favor o en contra Los dos estados tienen diferente energía. Esa diferencia aumenta con la intensidad del campo magnético momento magnético (μ)
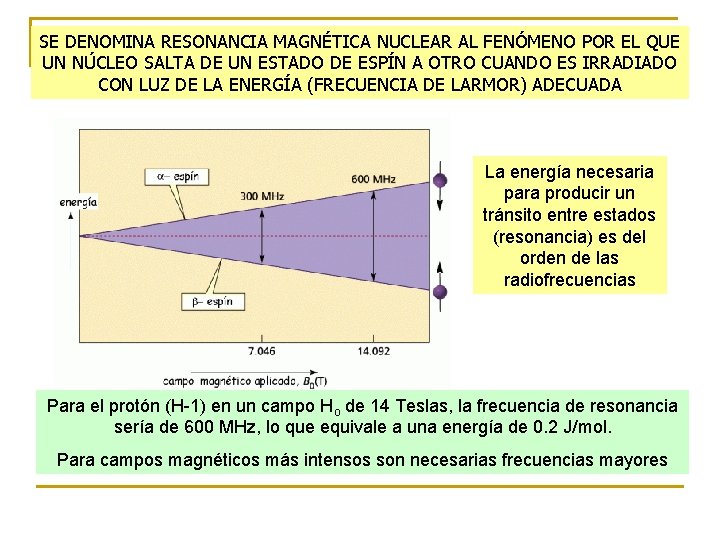
SE DENOMINA RESONANCIA MAGNÉTICA NUCLEAR AL FENÓMENO POR EL QUE UN NÚCLEO SALTA DE UN ESTADO DE ESPÍN A OTRO CUANDO ES IRRADIADO CON LUZ DE LA ENERGÍA (FRECUENCIA DE LARMOR) ADECUADA La energía necesaria para producir un tránsito entre estados (resonancia) es del orden de las radiofrecuencias Para el protón (H-1) en un campo Ho de 14 Teslas, la frecuencia de resonancia sería de 600 MHz, lo que equivale a una energía de 0. 2 J/mol. Para campos magnéticos más intensos son necesarias frecuencias mayores
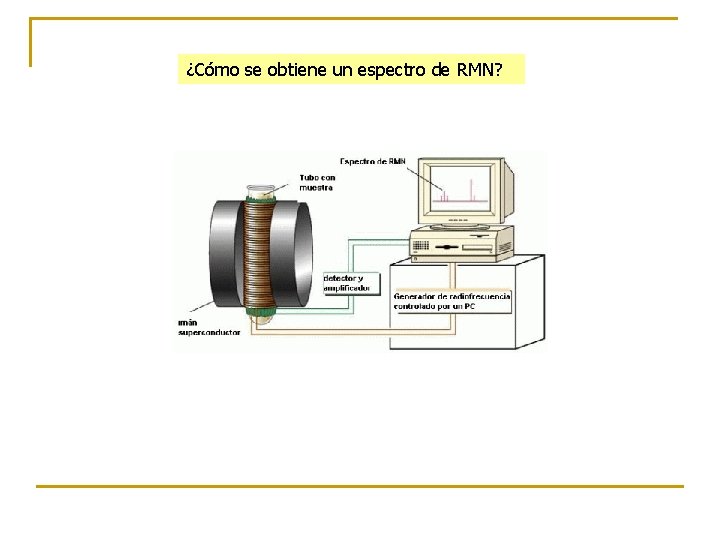
¿Cómo se obtiene un espectro de RMN?
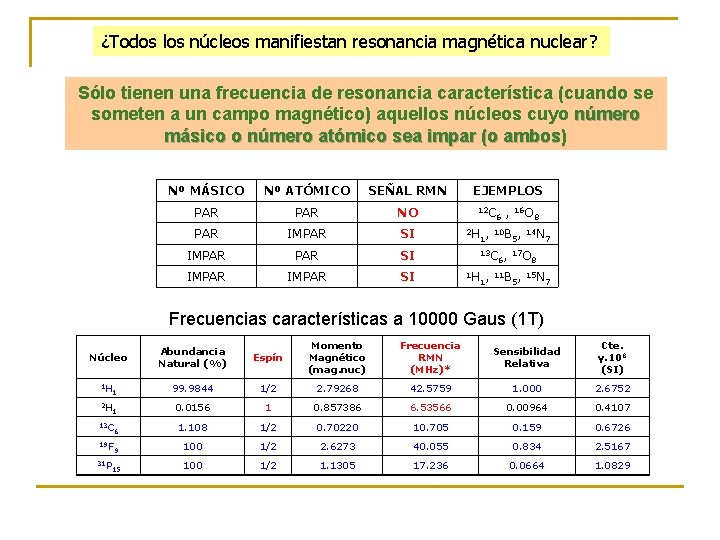
¿Todos los núcleos manifiestan resonancia magnética nuclear? Sólo tienen una frecuencia de resonancia característica (cuando se someten a un campo magnético) aquellos núcleos cuyo número másico o número atómico sea impar (o ambos) Nº MÁSICO Nº ATÓMICO SEÑAL RMN PAR NO EJEMPLOS 12 C 6 , 16 O 8 PAR IMPAR SI 2 H , 10 B , 14 N 1 5 7 IMPAR SI 13 C , 17 O 6 8 IMPAR SI 1 H , 11 B , 15 N 1 5 7 Frecuencias características a 10000 Gaus (1 T) Núcleo Abundancia Natural (%) Espín Momento Magnético (mag. nuc) Frecuencia RMN (MHz)* Sensibilidad Relativa Cte. γ. 108 (SI) 1 H 1 99. 9844 1/2 2. 79268 42. 5759 1. 000 2. 6752 2 H 1 0. 0156 1 0. 857386 6. 53566 0. 00964 0. 4107 6 1. 108 1/2 0. 70220 10. 705 0. 159 0. 6726 9 100 1/2 2. 6273 40. 055 0. 834 2. 5167 100 1/2 1. 1305 17. 236 0. 0664 1. 0829 13 C 19 F 31 P 15
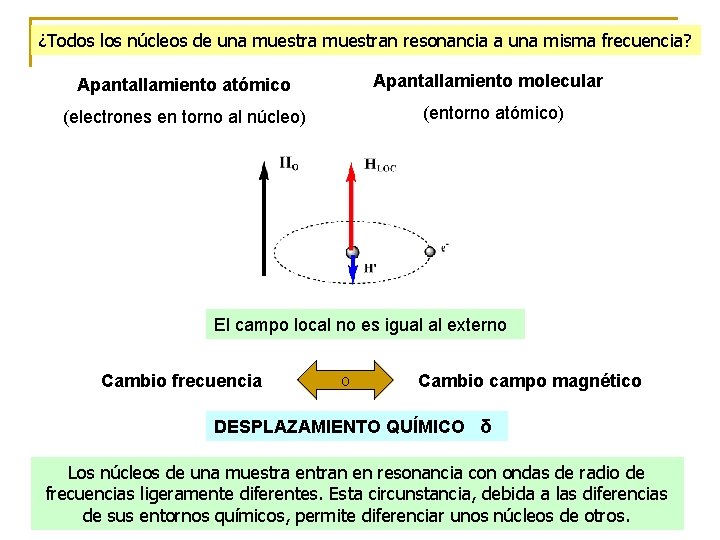
¿Todos los núcleos de una muestran resonancia a una misma frecuencia? Apantallamiento molecular Apantallamiento atómico (entorno atómico) (electrones en torno al núcleo) El campo local no es igual al externo Cambio frecuencia o Cambio campo magnético DESPLAZAMIENTO QUÍMICO δ Los núcleos de una muestra entran en resonancia con ondas de radio de frecuencias ligeramente diferentes. Esta circunstancia, debida a las diferencias de sus entornos químicos, permite diferenciar unos núcleos de otros.
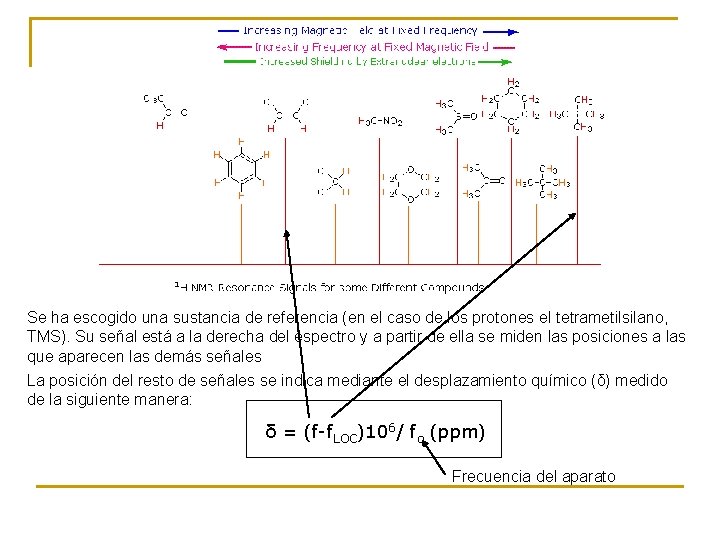
Se ha escogido una sustancia de referencia (en el caso de los protones el tetrametilsilano, TMS). Su señal está a la derecha del espectro y a partir de ella se miden las posiciones a las que aparecen las demás señales La posición del resto de señales se indica mediante el desplazamiento químico (δ) medido de la siguiente manera: δ = (f-f. LOC)106/ fo (ppm) Frecuencia del aparato
DESPLAZAMIENTO QUÍMICO δ Variación de la frecuencia de resonancia de un determinado núcleo respecto a la frecuencia del estándar en las condiciones del aparato de medida Unidad Medido en ppm Origen δ = 0, tetrametilsilano, Si. Me 4 Partes por millón Por ejemplo, si nuestra señal aparece a 60 Hz del TMS en un aparato de 60 Mhz , el desplazamiento químico sería δ = 1 ppm, es decir, una parte por millón de la frecuencia del aparato empleado
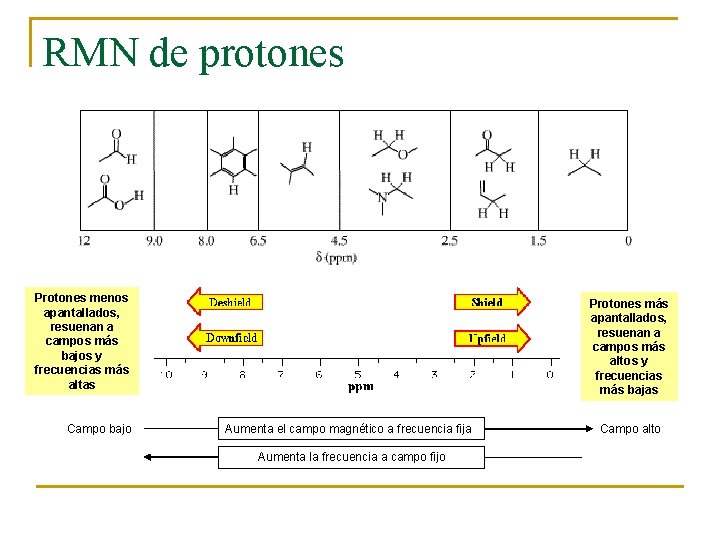
RMN de protones Protones menos apantallados, resuenan a campos más bajos y frecuencias más altas Campo bajo Protones más apantallados, resuenan a campos más altos y frecuencias más bajas Aumenta el campo magnético a frecuencia fija Aumenta la frecuencia a campo fijo Campo alto
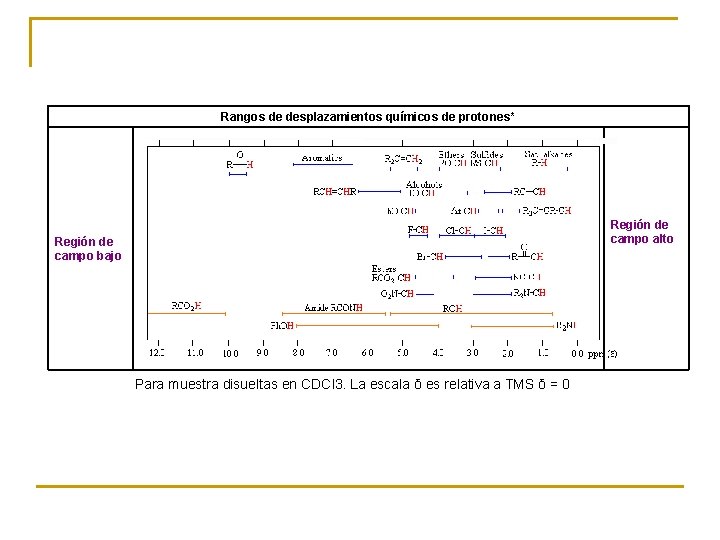
Rangos de desplazamientos químicos de protones* Región de campo bajo Para muestra disueltas en CDCl 3. La escala δ es relativa a TMS δ = 0 Región de campo alto
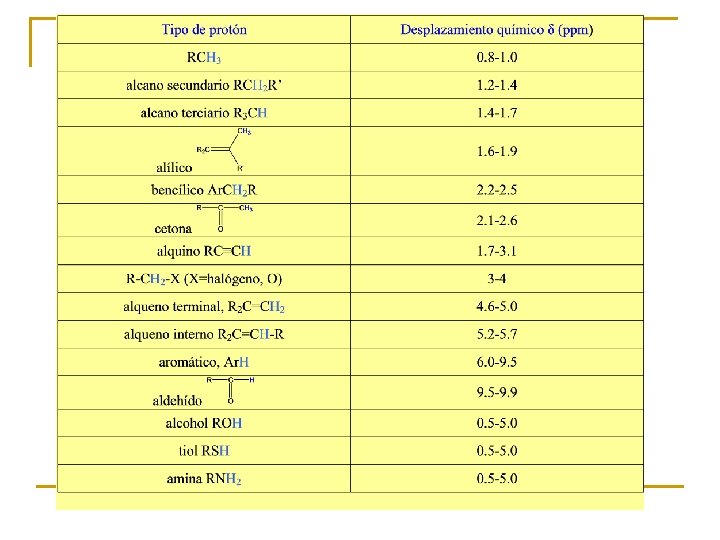
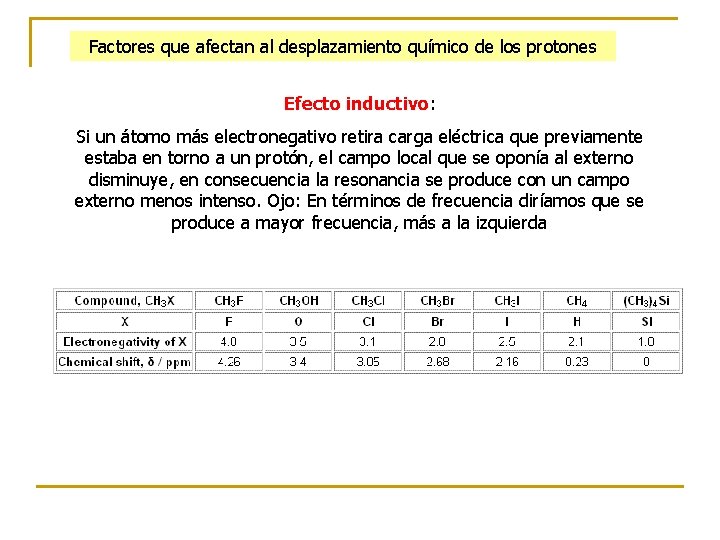
Factores que afectan al desplazamiento químico de los protones Efecto inductivo: Si un átomo más electronegativo retira carga eléctrica que previamente estaba en torno a un protón, el campo local que se oponía al externo disminuye, en consecuencia la resonancia se produce con un campo externo menos intenso. Ojo: En términos de frecuencia diríamos que se produce a mayor frecuencia, más a la izquierda
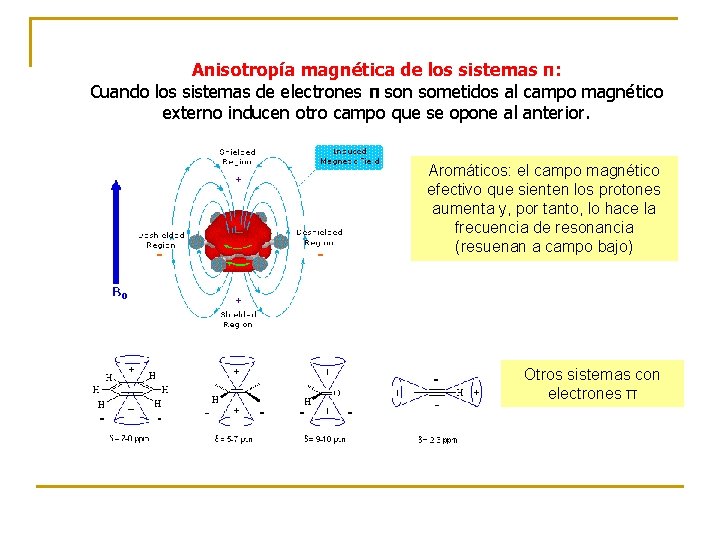
Anisotropía magnética de los sistemas π: Cuando los sistemas de electrones π son sometidos al campo magnético externo inducen otro campo que se opone al anterior. Aromáticos: el campo magnético efectivo que sienten los protones aumenta y, por tanto, lo hace la frecuencia de resonancia (resuenan a campo bajo) Otros sistemas con electrones π
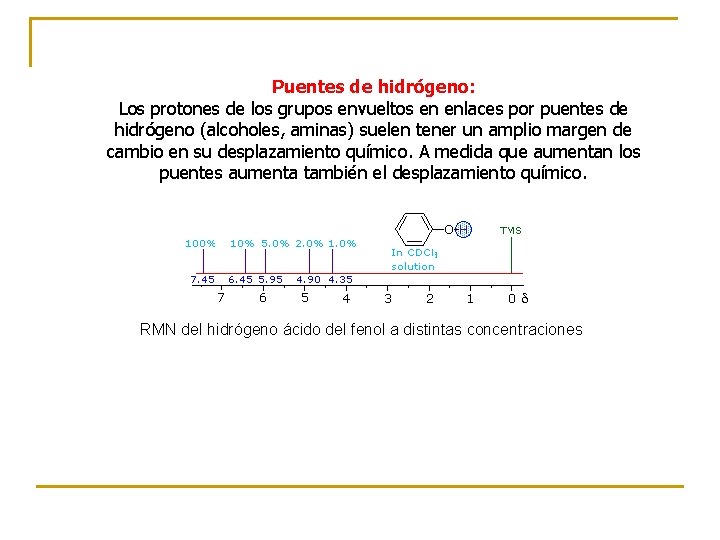
Puentes de hidrógeno: Los protones de los grupos envueltos en enlaces por puentes de hidrógeno (alcoholes, aminas) suelen tener un amplio margen de cambio en su desplazamiento químico. A medida que aumentan los puentes aumenta también el desplazamiento químico. RMN del hidrógeno ácido del fenol a distintas concentraciones

INTERPRETACIÓN DE UN ESPECTRO RMN DE PROTONES Para interpretar un HRMN hay que tener en cuenta tres fuentes de información: a) DESPLAZAMIENTO QUÍMICO - Indica el número de tipos de protones diferentes que hay en la molécula - Indica los tipos de protones que hay en la molécula b) INTEGRAL c) ACOPLAMIENTO DE ESPÍN Indica el número de protones que contribuyen a una determinada señal del espectro Indica las interacciones que se establecen entre los diferentes protones de la molécula
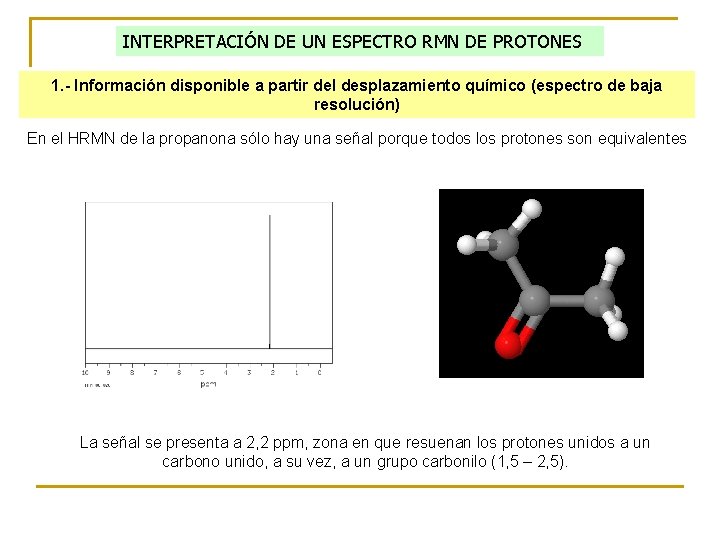
INTERPRETACIÓN DE UN ESPECTRO RMN DE PROTONES 1. - Información disponible a partir del desplazamiento químico (espectro de baja resolución) En el HRMN de la propanona sólo hay una señal porque todos los protones son equivalentes La señal se presenta a 2, 2 ppm, zona en que resuenan los protones unidos a un carbono unido, a su vez, a un grupo carbonilo (1, 5 – 2, 5).
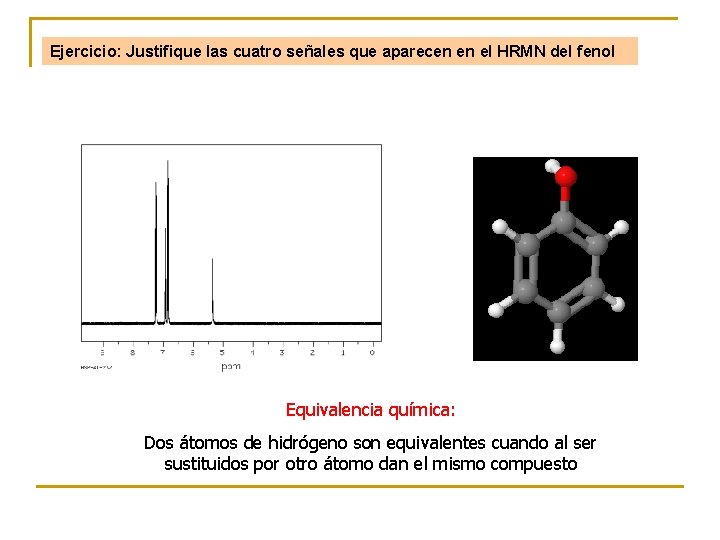
Ejercicio: Justifique las cuatro señales que aparecen en el HRMN del fenol Equivalencia química: Dos átomos de hidrógeno son equivalentes cuando al ser sustituidos por otro átomo dan el mismo compuesto
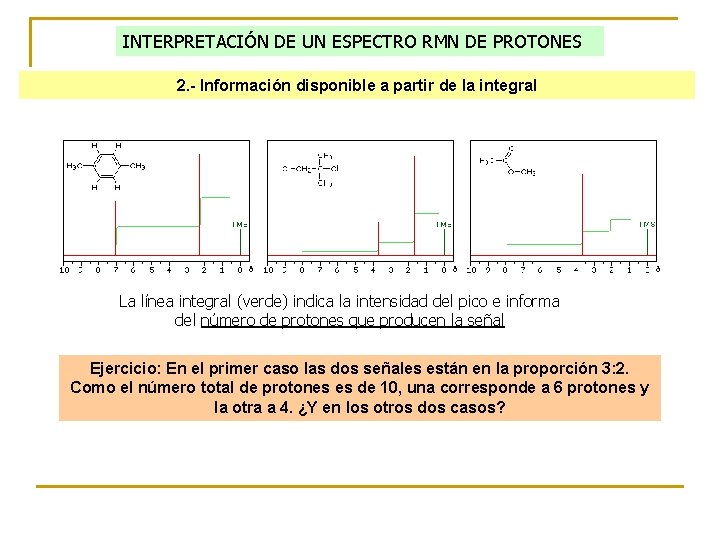
INTERPRETACIÓN DE UN ESPECTRO RMN DE PROTONES 2. - Información disponible a partir de la integral La línea integral (verde) indica la intensidad del pico e informa del número de protones que producen la señal Ejercicio: En el primer caso las dos señales están en la proporción 3: 2. Como el número total de protones es de 10, una corresponde a 6 protones y la otra a 4. ¿Y en los otros dos casos?
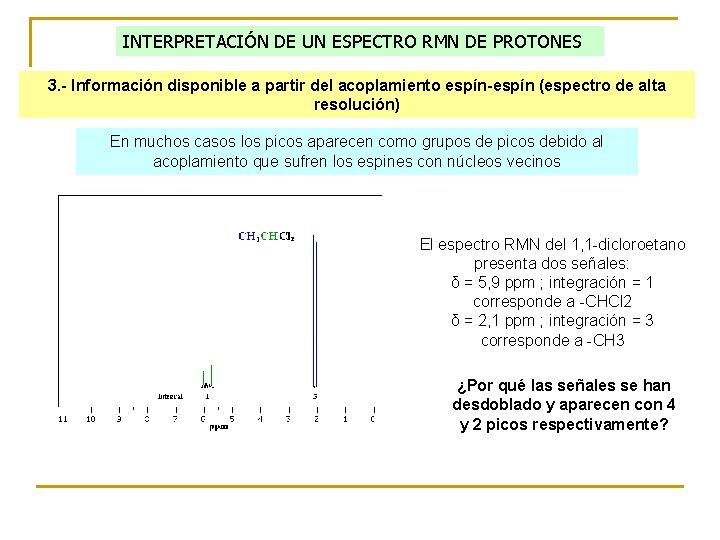
INTERPRETACIÓN DE UN ESPECTRO RMN DE PROTONES 3. - Información disponible a partir del acoplamiento espín-espín (espectro de alta resolución) En muchos casos los picos aparecen como grupos de picos debido al acoplamiento que sufren los espines con núcleos vecinos El espectro RMN del 1, 1 -dicloroetano presenta dos señales: δ = 5, 9 ppm ; integración = 1 corresponde a -CHCl 2 δ = 2, 1 ppm ; integración = 3 corresponde a -CH 3 ¿Por qué las señales se han desdoblado y aparecen con 4 y 2 picos respectivamente?
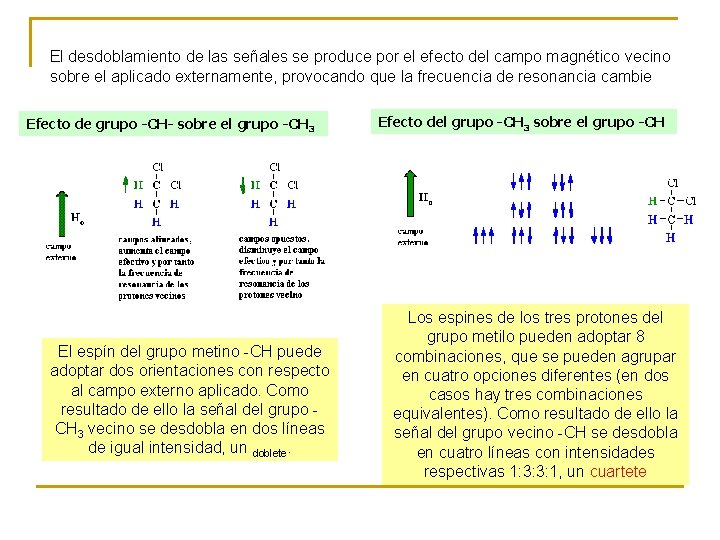
El desdoblamiento de las señales se produce por el efecto del campo magnético vecino sobre el aplicado externamente, provocando que la frecuencia de resonancia cambie Efecto de grupo -CH- sobre el grupo -CH 3 El espín del grupo metino -CH puede adoptar dos orientaciones con respecto al campo externo aplicado. Como resultado de ello la señal del grupo CH 3 vecino se desdobla en dos líneas de igual intensidad, un doblete. Efecto del grupo -CH 3 sobre el grupo -CH Los espines de los tres protones del grupo metilo pueden adoptar 8 combinaciones, que se pueden agrupar en cuatro opciones diferentes (en dos casos hay tres combinaciones equivalentes). Como resultado de ello la señal del grupo vecino -CH se desdobla en cuatro líneas con intensidades respectivas 1: 3: 3: 1, un cuartete
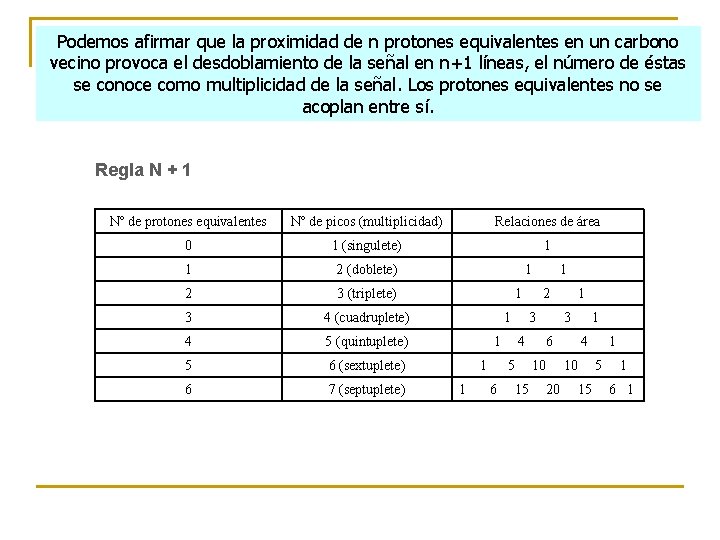
Podemos afirmar que la proximidad de n protones equivalentes en un carbono vecino provoca el desdoblamiento de la señal en n+1 líneas, el número de éstas se conoce como multiplicidad de la señal. Los protones equivalentes no se acoplan entre sí. Regla N + 1 Nº de protones equivalentes Nº de picos (multiplicidad) Relaciones de área 0 1 (singulete) 1 1 2 (doblete) 2 3 (triplete) 3 4 (cuadruplete) 4 5 (quintuplete) 5 6 (sextuplete) 6 7 (septuplete) 1 1 2 1 3 1 1 6 3 4 5 1 6 10 15 1 4 10 20 1 5 15 1 6 1
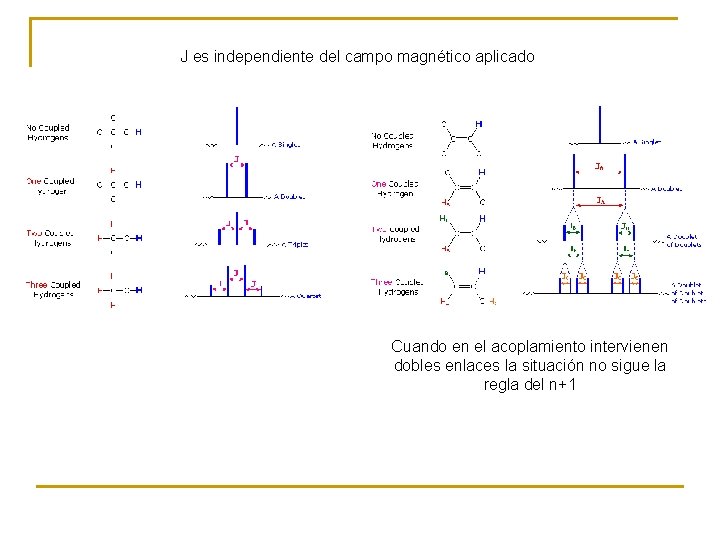
J es independiente del campo magnético aplicado Cuando en el acoplamiento intervienen dobles enlaces la situación no sigue la regla del n+1
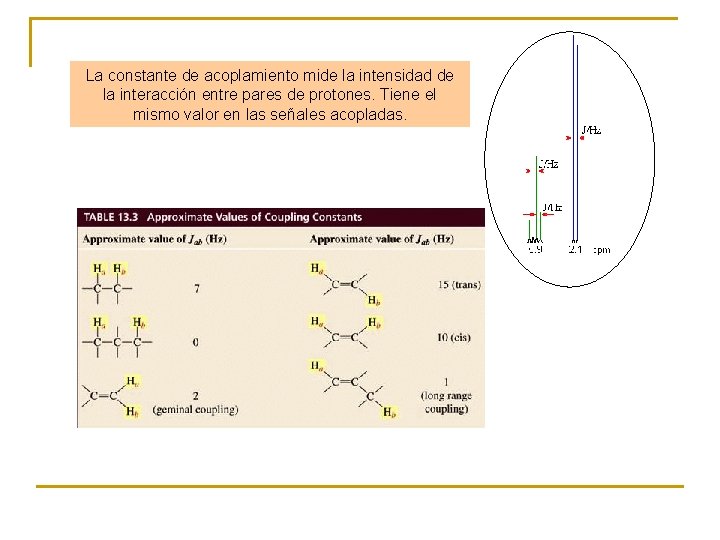
La constante de acoplamiento mide la intensidad de la interacción entre pares de protones. Tiene el mismo valor en las señales acopladas.
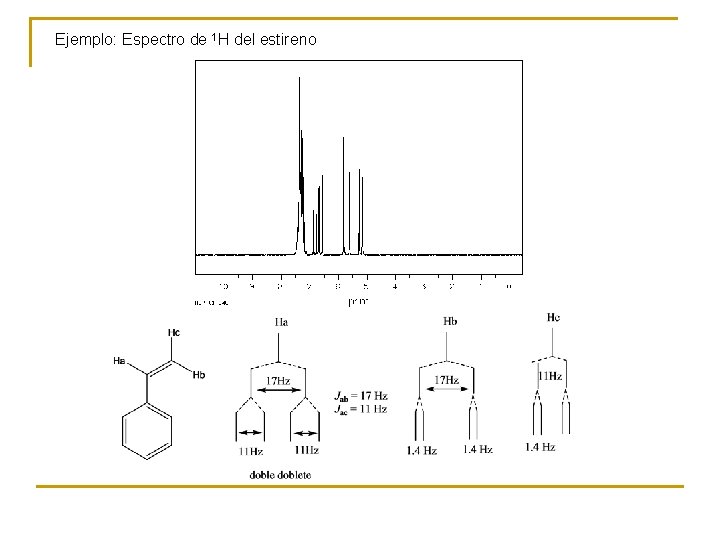
Ejemplo: Espectro de 1 H del estireno
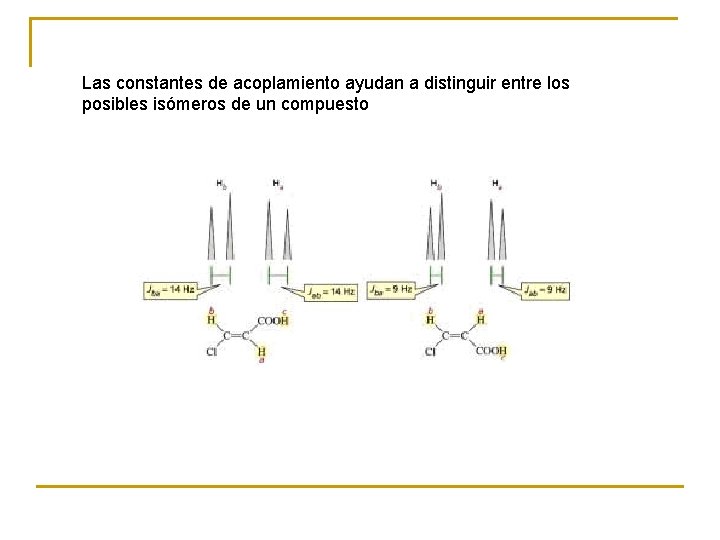
Las constantes de acoplamiento ayudan a distinguir entre los posibles isómeros de un compuesto
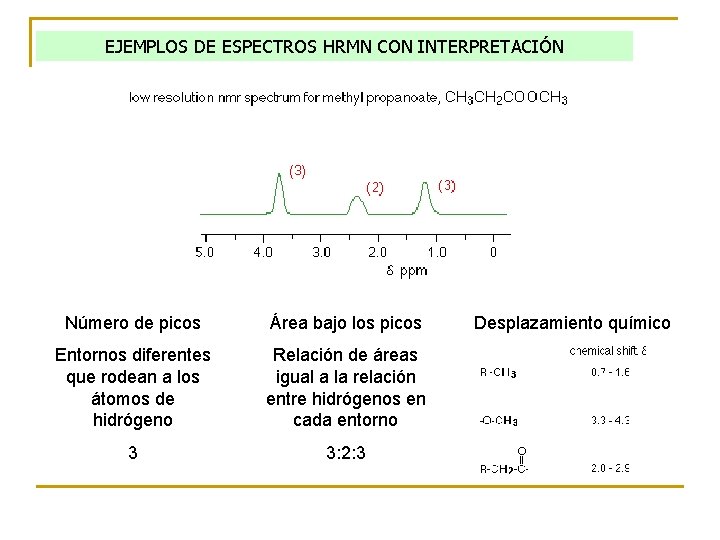
EJEMPLOS DE ESPECTROS HRMN CON INTERPRETACIÓN Número de picos Área bajo los picos Entornos diferentes que rodean a los átomos de hidrógeno Relación de áreas igual a la relación entre hidrógenos en cada entorno 3 3: 2: 3 Desplazamiento químico
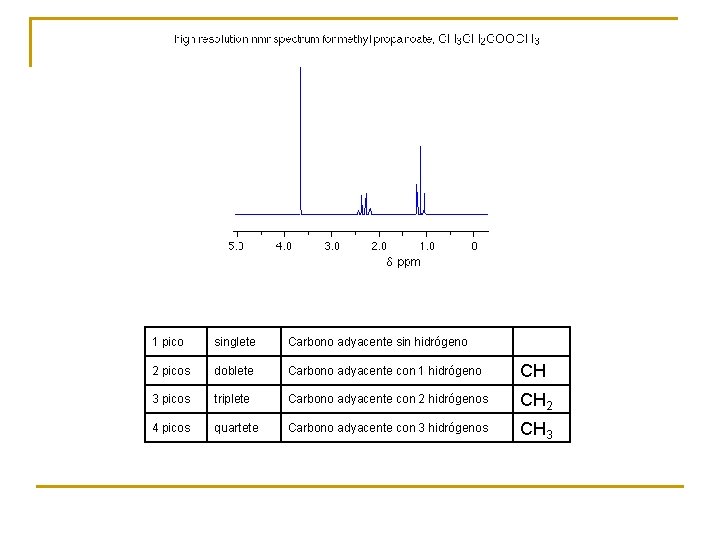
1 pico singlete Carbono adyacente sin hidrógeno 2 picos doblete Carbono adyacente con 1 hidrógeno CH 3 picos triplete Carbono adyacente con 2 hidrógenos CH 2 4 picos quartete Carbono adyacente con 3 hidrógenos CH 3
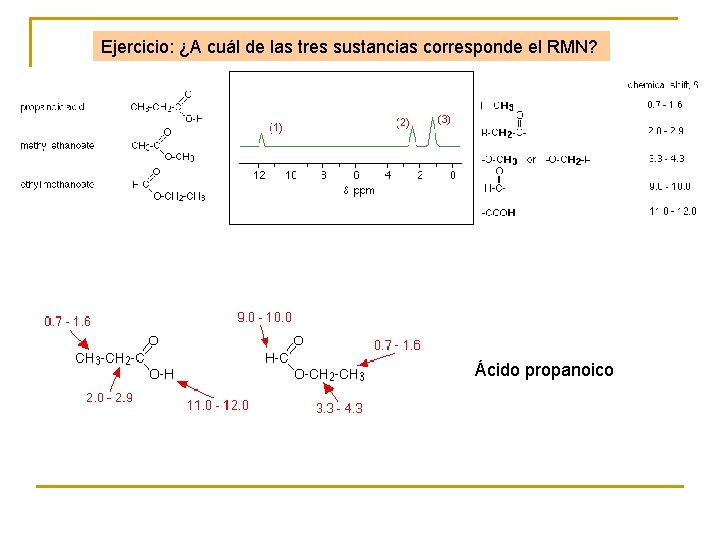
Ejercicio: ¿A cuál de las tres sustancias corresponde el RMN? Ácido propanoico
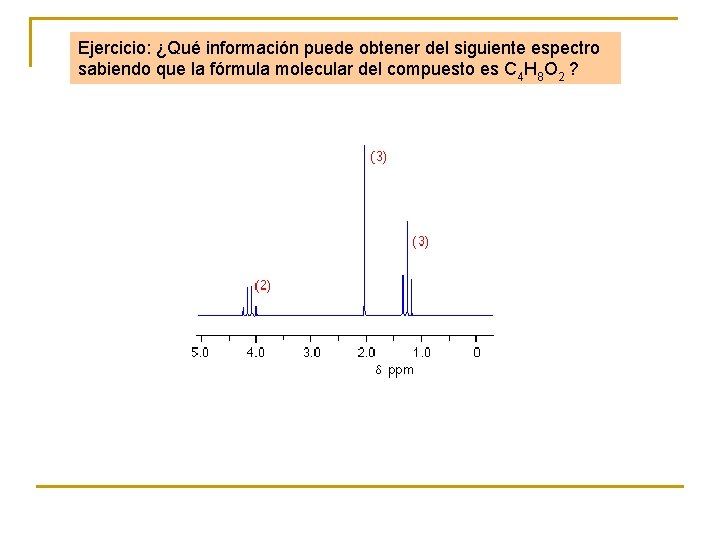
Ejercicio: ¿Qué información puede obtener del siguiente espectro sabiendo que la fórmula molecular del compuesto es C 4 H 8 O 2 ?

3 entornos diferentes para los átomos de hidrógeno Los átomos de hidrógeno en estos tres ambientes están en una relación 2: 3: 3 Como son 8 hidrógenos, hay un grupo CH 2 y dos grupos CH 3 El grupo CH 2 de 4. 1 ppm tiene junto a él un grupo CH 3 El grupo CH 3 de 1. 3 ppm tiene junto a él un grupo CH 2 El grupo CH 3 de 2. 0 ppm tiene junto a él un carbono sin hidrógeno
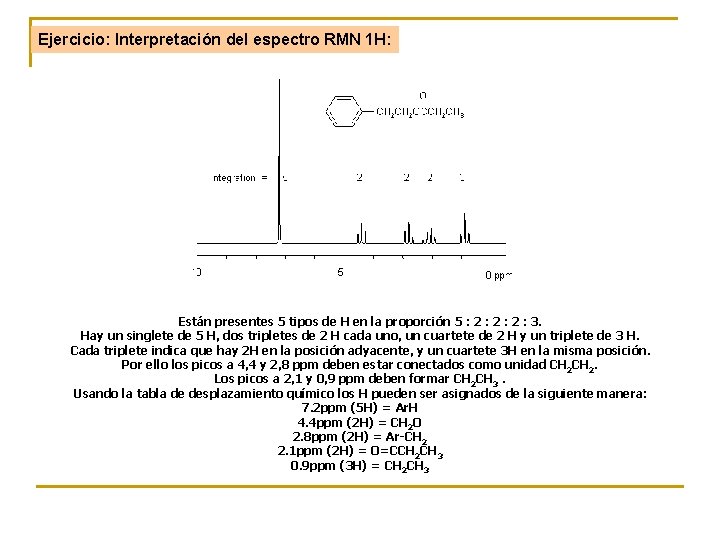
Ejercicio: Interpretación del espectro RMN 1 H: Están presentes 5 tipos de H en la proporción 5 : 2 : 2 : 3. Hay un singlete de 5 H, dos tripletes de 2 H cada uno, un cuartete de 2 H y un triplete de 3 H. Cada triplete indica que hay 2 H en la posición adyacente, y un cuartete 3 H en la misma posición. Por ello los picos a 4, 4 y 2, 8 ppm deben estar conectados como unidad CH 2. Los picos a 2, 1 y 0, 9 ppm deben formar CH 2 CH 3. Usando la tabla de desplazamiento químico los H pueden ser asignados de la siguiente manera: 7. 2 ppm (5 H) = Ar. H 4. 4 ppm (2 H) = CH 2 O 2. 8 ppm (2 H) = Ar-CH 2 2. 1 ppm (2 H) = O=CCH 2 CH 3 0. 9 ppm (3 H) = CH 2 CH 3
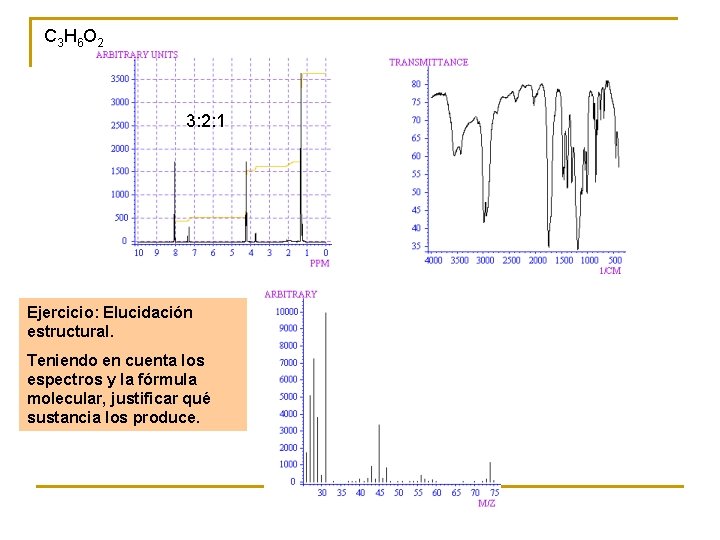
C 3 H 6 O 2 3: 2: 1 Ejercicio: Elucidación estructural. Teniendo en cuenta los espectros y la fórmula molecular, justificar qué sustancia los produce.
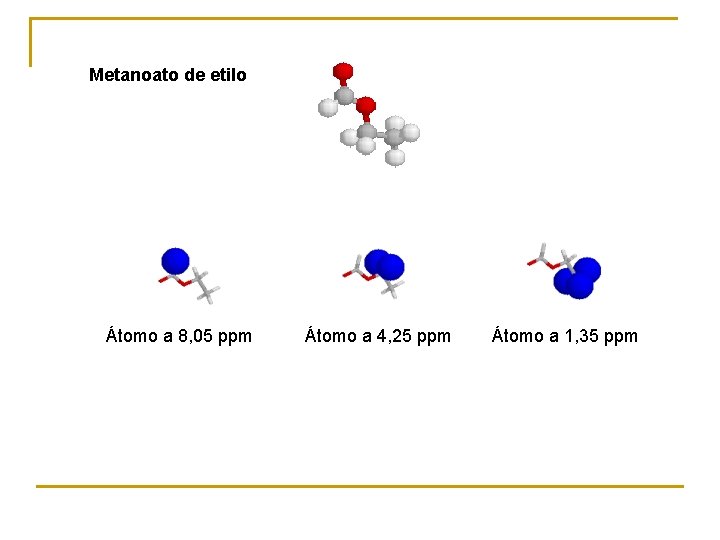
Metanoato de etilo Átomo a 8, 05 ppm Átomo a 4, 25 ppm Átomo a 1, 35 ppm
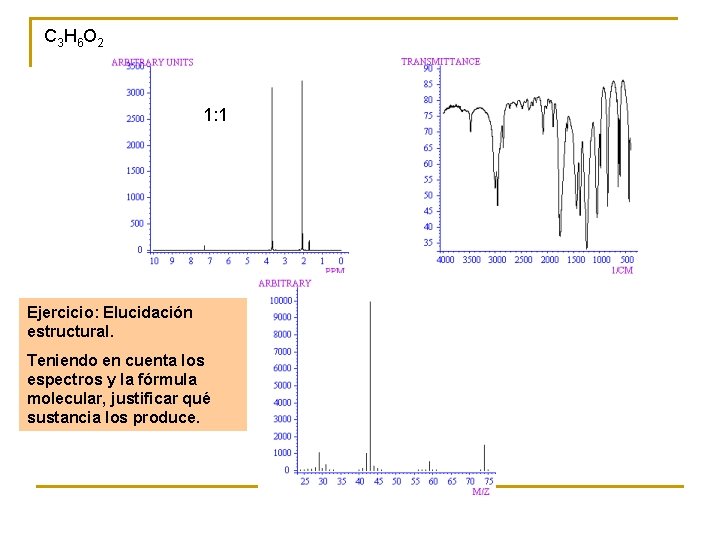
C 3 H 6 O 2 1: 1 Ejercicio: Elucidación estructural. Teniendo en cuenta los espectros y la fórmula molecular, justificar qué sustancia los produce.
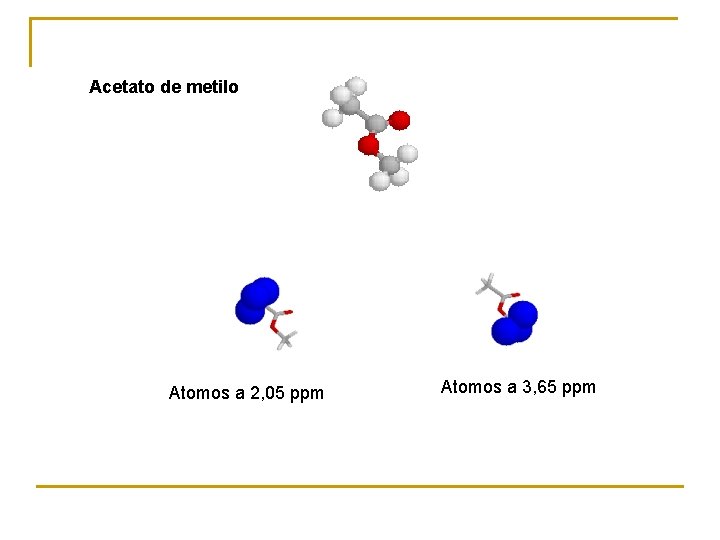
Acetato de metilo Atomos a 2, 05 ppm Atomos a 3, 65 ppm
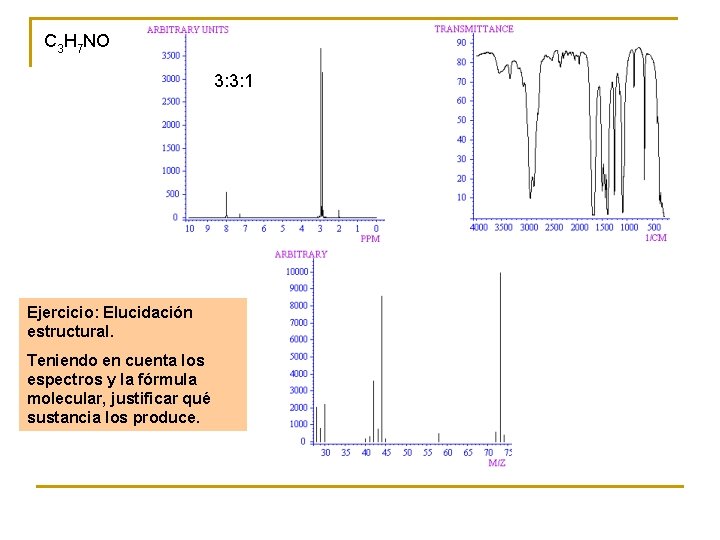
C 3 H 7 NO 3: 3: 1 Ejercicio: Elucidación estructural. Teniendo en cuenta los espectros y la fórmula molecular, justificar qué sustancia los produce.
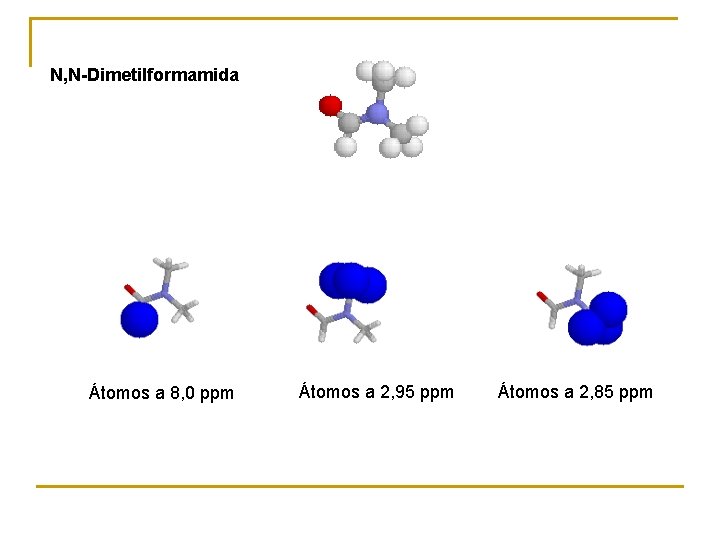
N, N-Dimetilformamida Átomos a 8, 0 ppm Átomos a 2, 95 ppm Átomos a 2, 85 ppm
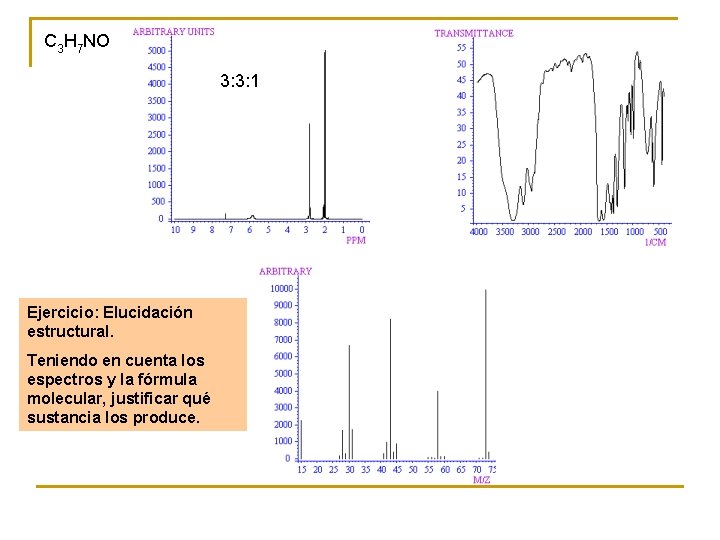
C 3 H 7 NO 3: 3: 1 Ejercicio: Elucidación estructural. Teniendo en cuenta los espectros y la fórmula molecular, justificar qué sustancia los produce.
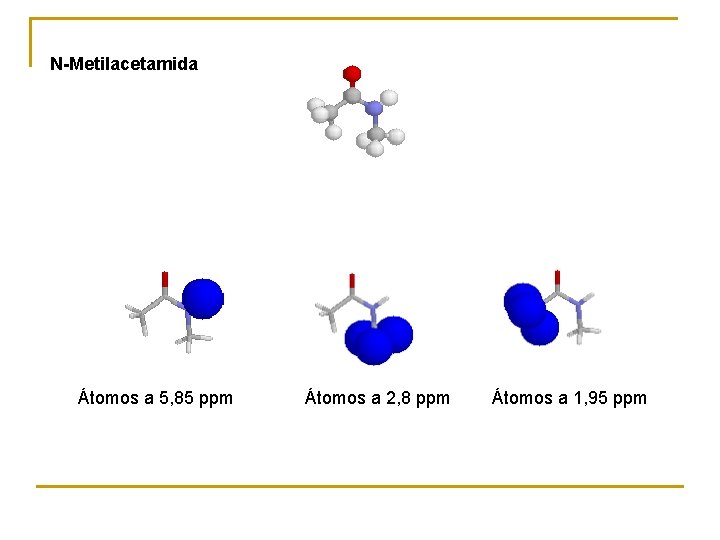
N-Metilacetamida Átomos a 5, 85 ppm Átomos a 2, 8 ppm Átomos a 1, 95 ppm
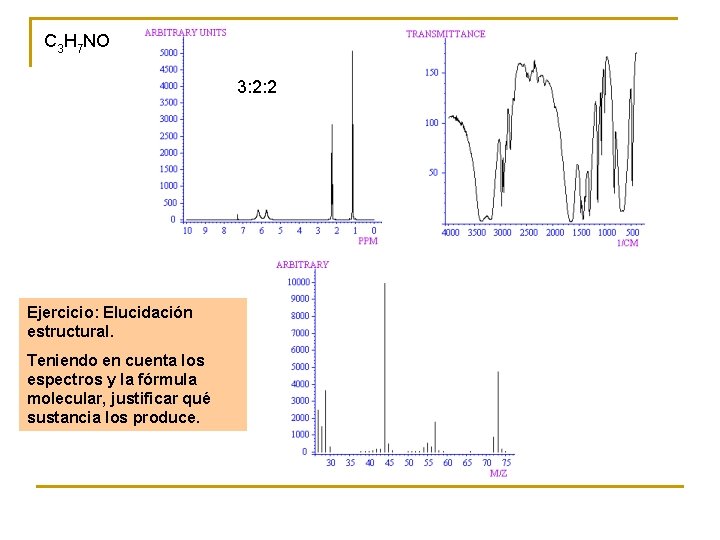
C 3 H 7 NO 3: 2: 2 Ejercicio: Elucidación estructural. Teniendo en cuenta los espectros y la fórmula molecular, justificar qué sustancia los produce.
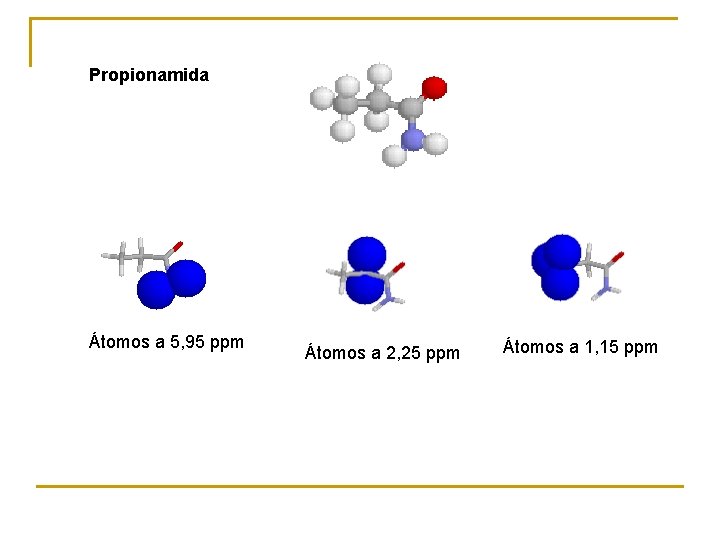
Propionamida Átomos a 5, 95 ppm Átomos a 2, 25 ppm Átomos a 1, 15 ppm
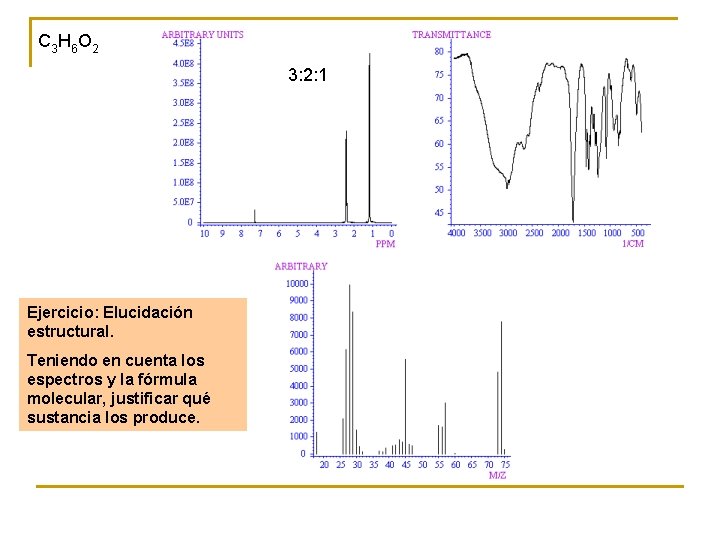
C 3 H 6 O 2 3: 2: 1 Ejercicio: Elucidación estructural. Teniendo en cuenta los espectros y la fórmula molecular, justificar qué sustancia los produce.
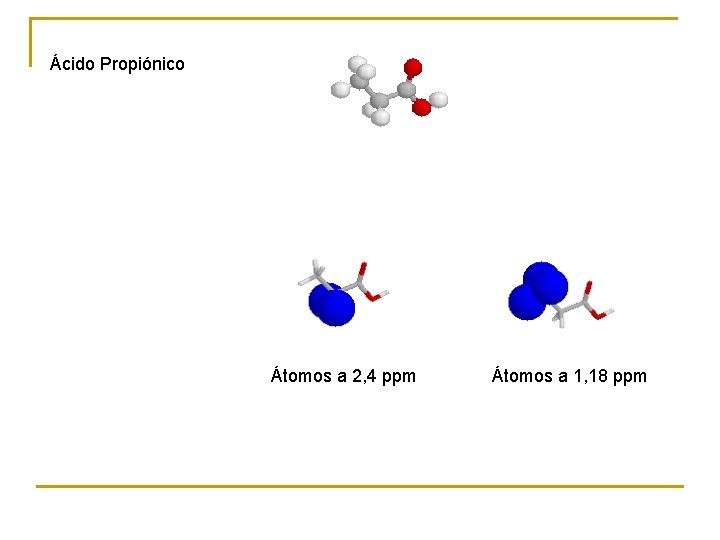
Ácido Propiónico Átomos a 2, 4 ppm Átomos a 1, 18 ppm

RMN de 13 C
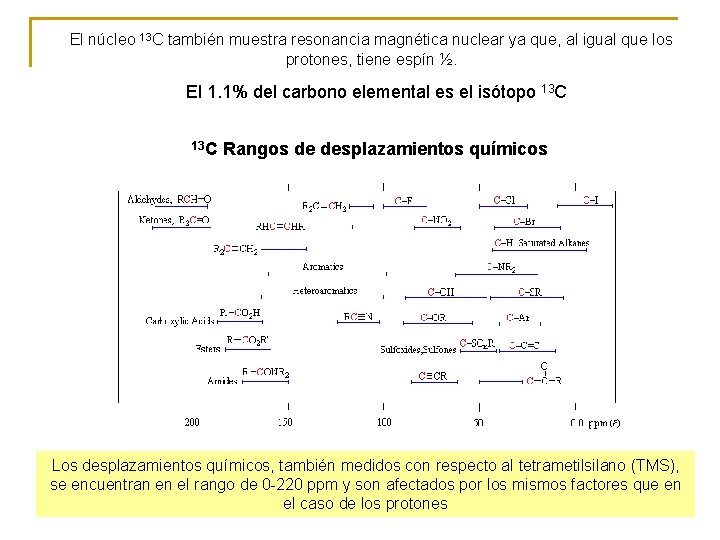
El núcleo 13 C también muestra resonancia magnética nuclear ya que, al igual que los protones, tiene espín ½. El 1. 1% del carbono elemental es el isótopo 13 C Rangos de desplazamientos químicos Los desplazamientos químicos, también medidos con respecto al tetrametilsilano (TMS), se encuentran en el rango de 0 -220 ppm y son afectados por los mismos factores que en el caso de los protones
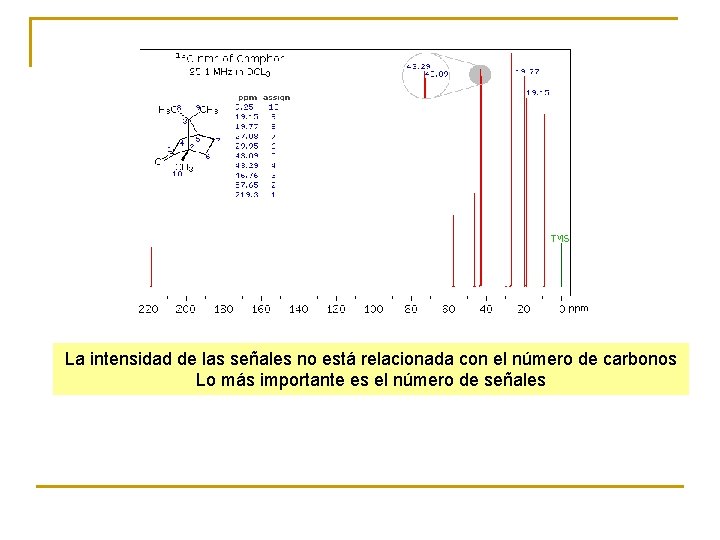
La intensidad de las señales no está relacionada con el número de carbonos Lo más importante es el número de señales
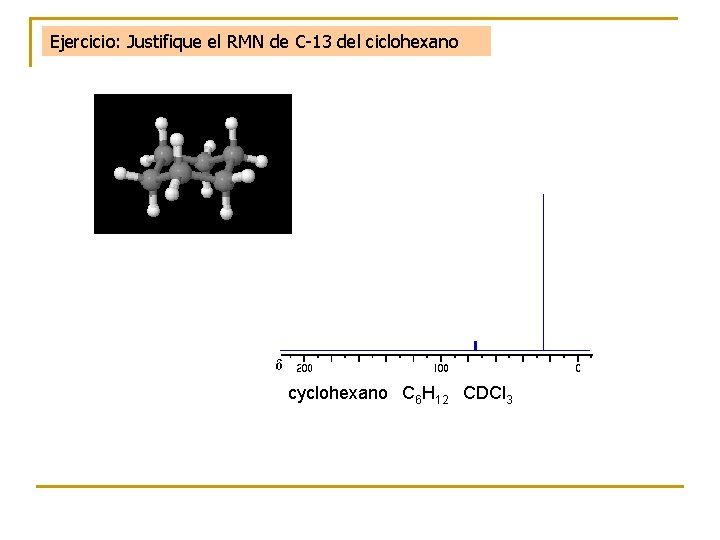
Ejercicio: Justifique el RMN de C-13 del ciclohexano cyclohexano C 6 H 12 CDCl 3
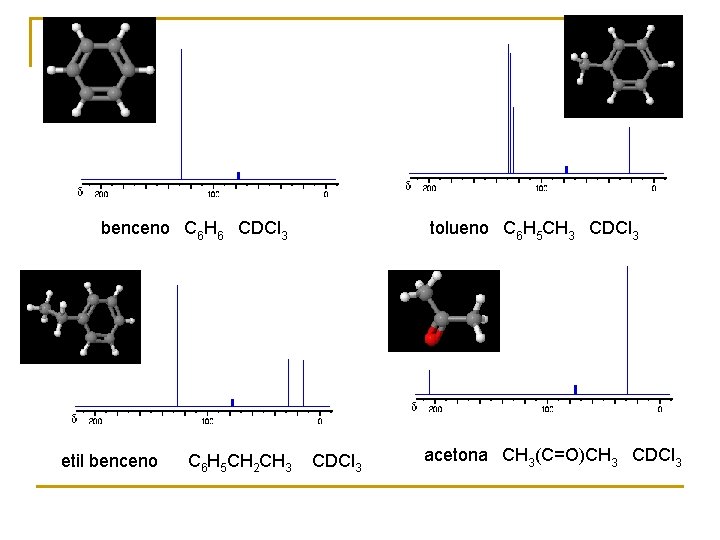
benceno C 6 H 6 CDCl 3 etil benceno C 6 H 5 CH 2 CH 3 CDCl 3 tolueno C 6 H 5 CH 3 CDCl 3 acetona CH 3(C=O)CH 3 CDCl 3
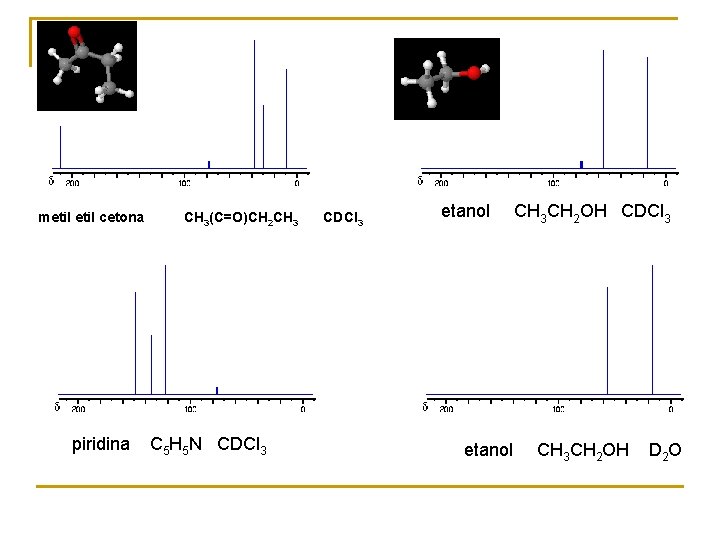
metil cetona piridina CH 3(C=O)CH 2 CH 3 C 5 H 5 N CDCl 3 etanol CH 3 CH 2 OH CDCl 3 CH 3 CH 2 OH D 2 O
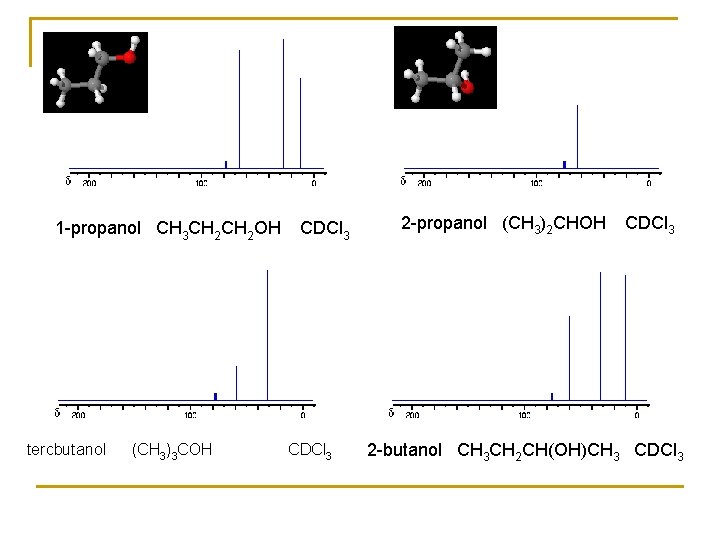
1 -propanol CH 3 CH 2 OH CDCl 3 tercbutanol (CH 3)3 COH CDCl 3 2 -propanol (CH 3)2 CHOH CDCl 3 2 -butanol CH 3 CH 2 CH(OH)CH 3 CDCl 3
- Slides: 108